血液透析時間的延長對老年維持性血液透析患者超聲心動圖的影響及臨床分析
穆春華,鄒金華
(連云港市第四人民醫院,江蘇 連云港 222002)
隨著醫學的發展和血液透析技術的進步,維持性血液透析(MHD)患者的生存率得到了很大的提高,但是血液透析的患者病死率仍居高不下[1]。隨著透析次數的增加以及病情的進展,尤其是老年MHD患者中,心血管疾病(CVD)仍然是其主要的死亡原因,透析患者CVD所致病死率大約為普通人群的30倍,所以終末期腎臟病(ESRD)最近被稱為“血管疾病狀態”[2],ESRD患者在血液動力學負荷方面,如心臟壓力負荷、容量負荷增加導致的高動力循環是引起心肌受損的重要因素[3-4]。本研究觀察延長透析時間對老年MHD患者左心室結構、功能及心肌變化的影響,對臨床設置合適的透析時間、減少心血管疾病發生具有一定的意義。
1 資料與方法
1.1 一般資料
選擇2019年7月—2019年12月收治的老年尿毒癥維持性血液透析患者57 例,采用雙盲隨機法分為延長透析組(29 例)和正常透析組(28 例)。兩組患者接受規律血液透析治療的時間均≥12 個月。兩組患者的年齡、性別及透析齡等一般資料比較,差異無統計學意義(P>0.05),具有可比性(見表1)。

表1 兩組患者的一般資料比較
1.2 納入和排除標準
1.2.1 納入標準
規律血液透析患者且年齡大于60 周歲,透析頻率每周3 次,透析間隔為1 d,并具備以下條件:近6 個月無活動性感染、外傷、手術等狀況;無嚴重心律失常、風濕性心臟病、心臟瓣膜疾病、大面積心梗及胃腸道癥狀等;無肝臟疾病及肝功能受損、腦血管病變及精神障礙病史;原發病非糖尿病、甲狀腺功能亢進病史等;殘余尿均≤400 mL/d;血壓穩定在正常值內,且未服用影響心臟結構的藥物;患者自愿參加本研究,入選前簽署知情同意書。
1.2.2 排除標準
近6 個月內發生急性心腦血管意外者;血壓波動范圍大者;使用各類激素及抗腫瘤藥物者;嚴重感染者;患自身免疫性疾病者;出現惡性腫瘤及腎移植、預期壽命少于2年者[5]。
1.3 方法
1.3.1 透析相關參數
采用德國貝朗透析機,型號DIALOG+,采用1.3~1.5 m2尼普洛聚砜膜透析器,透析液流量500 mL/min,血流量200~250 mL/min,常規碳酸氫鹽透析液,普通肝素常規肝素化、低分子肝素抗凝。常規透析組每次透析4 h,延長透析組則將透析時間延長至>6 h,所有患者每周透析3 次,每次超濾量為0.5~5.0 L。
1.3.2 儀器
超聲心動圖檢查使用德國西門子ACUSON S2000彩色多普勒超聲診斷儀,4v1C探頭(頻率范圍1.5~3.5 MHz)。
1.4 觀察指標
1.4.1 超聲心動圖檢測指標
左心室后壁厚度(LVPW)、室間隔厚度(IVS)、左房收縮末期內徑(LADS)、左心室舒張末期內徑(LVEDD)、左室心肌重量指數(LVMI)、二尖瓣前向血流頻譜舒張早期左室充盈峰速度(E)與心房收縮期左室充盈峰速度(A)比值(E/A)、射血分數(EF)、心率(HR)等;根據Devereux公式計算左室心肌重量(LVM):LVM(g)=1.04×[(LVEDD+IVS+LVPW)3-LVEDD3]-13.6[5];LVMI(g/m2)=LVM/BSA(體表面積)[6]。
1.4.2 超聲診斷標準及評價指標
目前國內超聲心動圖的心臟測量標準問題還沒有達成共識[7]。本研究中采用成人超聲心動圖正常值,并結合本院彩超室正常值標準:LADS為20~37 mm,LVEDD為35~50 mm,LVPW為 7~11 mm;IVS為5.5~11.5 mm,心輸出量(CO)為3.5~5.5 L/min,每搏量(SV)為60~130 mL;男性LVMI≥(130±5) g/m2,女性LVMI≥(126±4) g/m2診斷為左心室肥厚[7];E/A 延長透析6 個月后,LVPW,LADS,LVEDD減小,LVM減輕,IVS,LVMI,E/A,CO和SV均有明顯改善,差異均有統計學意義(P<0.05)(見表2)。 表2 延長透析組入選時與延長透析時間后左心室結構及功能的比較 6 個月后,延長透析組LVPW,LADS,LVEDD較正常透析組減小,LVM減輕;IVS,LVMI,LVEF(%),E/A,SV,CO和HR明顯改善,差異有統計學意義(P<0.05)(見表3)。 表3 6 個月后正常透析組與延長透析組心臟結構及功能情況的比較 國外文獻近期發表的一項研究中[8],學者們從不同的國家和地區醫院中選擇維持血液透析患者,按照相同的比例隨機分為正常透析組和延長透析組,隨訪1 年,評估兩組患者的生活質量及臨床獲益。結果提示,延長透析組患者整體生活質量沒有顯著改善,但是對改善高血壓和營養狀況、提高血鈣吸收、降低心血管并發癥等方面有著顯著成效,一定程度上降低了患者的病死率[9]。在FHN試驗機構的前瞻性隨機研究中[10]指出,提高透析頻率、時間能有效控制左室容積、高血壓及高血磷的變化。 在老年MHD患者中,CVD逐年增高,此類疾病仍然是老年MHD患者主要死亡原因,占老年MHD患者病死率的45%[11]。臨床上,高血壓在老年MHD患者中最常見(占80%~90%),一般情況下,患者血壓即使在允許范圍內,其病死率也與血壓數值相關,高血壓不僅可以增加老年MHD患者心臟后負荷,使其室壁肥厚更加明顯、心室擴大,同時也影響心臟收縮功能,進一步加速心力衰竭發生;貧血、動靜脈瘺的發生也可以導致外周循環壓力升高,加重心臟負擔;各類代謝性產物如兒茶酚胺、尿毒癥毒素及腎素-血管緊張素-醛固酮系統等因素均能影響心肌功能,尤其是對左心室的影響,造成心肌嚴重損傷。而營養不良的發生、甲狀旁腺激素的升高會使原有心肌損傷進一步加重,導致心肌出現不可逆的改變。老年MHD患者常表現為心臟結構損害,以左心室肥厚為多見,隨著病情發展,左心室肥厚會進一步加重,心律失常、心力衰竭、猝死的概率明顯增加,由此可見,左心擴大、心肌肥厚與老年MHD患者的病死率也呈正相關[1]。本研究發現,延長透析時間對老年MHD患者的左心室大小及結構均有不同程度的改善,以左心室心肌及室間隔改善最為明顯,左心室后壁厚度、左房內徑、左室舒張末期內徑也有顯著改善,兩組比較差異有統計學意義(P<0.05)。綜合以上因素,延長透析時間可在一定程度上降低患者病死率。 心臟的功能性障礙是MHD患者最常見的心血管并發癥之一,許多MHD患者左心室舒張功能異常往往發生在左心室結構改變之前[12],而老年性MDH患者臨床表現更明顯。尿毒癥患者因水鈉長期潴留,心臟容量負荷過大,心臟擴張,引起心肌功能損傷,部分心肌細胞出現壞死或者凋亡。研究表明[13],在尿毒癥環境下,盡管患者沒有出現心肌缺血,一定程度上也會引起心肌細胞壞死,而老年MHD患者心肌對缺血性損傷更加敏感,一旦出現,可迅速引起心肌收縮功能下降以及泵功能損傷。尿毒癥心肌病的病理基礎為心肌間質纖維化,在心肌細胞壞死的過程中,心肌間質發生結構重建,心肌間質原有膠原增粗,新膠原的沉積導致膠原體積增加,破壞正常心肌間質結構,引起心肌間質纖維化,導致心室舒張期硬度增加,順應性減退[14]。而左心室順應性下降會使心房后負荷進一步增加,導致左心房的壓力增高,首先表現為心房舒張功能減退,影響左心房收縮功能。機體為了維持正常的心輸出量,勢必加強心房收縮期代償能力,使心房收縮期形成的A峰進一步增高,導致E/A比值降低、EF斜率減慢。左心房由于長期處于高壓力、高負荷的狀態下,進一步導致左心房容積擴張[15]。隨著病情進展,左心室壓力進一步增高,左房收縮期阻力也隨之升高,出現一系列左室舒張功能減退的臨床表現,如左房擴大、左心室順應性降低、每搏輸出量減少等;而老年MHD患者的高血壓、水鈉潴留、營養不良、生化指標等因素會使心臟受累進一步加重,導致心肌纖維化進程加快、心臟擴大、左心室肥厚、左室收縮和舒張功能下降,EF值降低[16]。本研究發現,延長透析時間組的老年MHD患者心臟功能明顯得到改善,心率、每搏輸出量、心輸出量明顯增加,而左心室射血分數、E/A比值顯著減小(P<0.05)。 綜上所述,盡管維持性血液透析是老年MHD患者的重要腎臟替代療法,但是老年性MHD患者心臟結構及功能改變是由于各種內因、外因共同作用下引起的,常規透析時間無法阻止心臟病變發生,不能降低心血管疾病發病率和死亡風險[17]。本研究發現,延長透析時間有許多優點,是一種最接近生理性的透析方法,不僅能有效控制血壓、血鈣、血紅蛋白的水平,并可明顯改善老年MHD患者左心系統的結構和功能。1.5 統計學方法
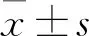
2 結 果
2.1 延長透析組透析前后左心室結構及功能比較

2.2 兩組左心室結構及功能比較

3 討 論
3.1 左心室大小改變及原因分析
3.2 左心室功能性改變及原因分析

