分析保護劑對煙草香味成分的基質效應補償
史天彩,潘立寧,王曉瑜,秦亞瓊,郭 瓊,謝 飛,謝復煒,劉惠民
中國煙草總公司鄭州煙草研究院,鄭州高新技術產業開發區楓楊街2 號 450001
GC-MS 法用于痕量分析時常存在基質效應[1-2],即樣品中除待測物以外的其他基質成分對待測物測定的影響。由于GC 進樣口和色譜柱內存在金屬離子和硅醇基活性位點,敏感性待測物在活性位點發生吸附作用或降解,導致待測物損失或色譜峰拖尾[3]。測定實際樣品時,樣品基質中的其他活性成分填充了GC 活性位點,減少了待測物與活性位點的相互作用,改善了色譜峰形和峰高,導致相同質量分數待測物在實際樣品中的響應值高于純溶劑中,這種現象被稱為“基質增強效應”[1]。目前,對基質效應的補償方法主要有基質匹配標準溶液校正法[4-6]、同位素內標法[7]、多種內標校正法[8]、進樣技術改進法[9-10]、樣品多次凈化法[11-12]、加入分析保護劑法[13-22]等。其中,最常用的是基質匹配標準溶液校正法,即利用不含待測物的空白基質匹配標準溶液對樣品溶液進行校準,從而補償基質效應。然而,在實際分析檢測中,采用基質匹配校正法主要存在以下3 點不足:一是不含待測物的空白基質不易獲得,二是不同類型樣品基質之間有差異,三是基質匹配標準溶液可使用的時間期限一般很短,需要現用現配,而基質匹配標準溶液的配制復雜且耗時。
在標準溶液中加入分析保護劑(Analyte protectant,AP),使AP 代替基質占據GC 活性位點,從而改善溶劑標準溶液中待測物的響應及峰形,達到基質效應補償的效果。Anastassiades 等[2]在2003 年選擇93 種不同化合物作為AP,評估了其對提高30 種農藥殘留分析質量的影響,結果表明,AP 的氫鍵能力和揮發性是影響基質效應補償效果的重要因素,其中L-古洛糖酸γ-內酯的整體補償效果最好,然而,單一的AP 并不能使30 種農藥殘留的響應和峰形均達到最優。Cajka 等[13]在2005 年評價了十幾種AP 組合,所選擇的最佳組合為3-乙氧基-1,2-丙二醇、L-古洛糖酸γ-內酯和D-山梨醇,三者的揮發性由高到低,組合后可以滿足揮發性差異較大的不同農殘組分的分析。但是,L-古洛糖酸γ-內酯和D-山梨醇極性較大,配制溶液過程中一般需引入水,這樣會影響GC 系統的長期穩定性;同時受溶解性的影響,不適用于極性較弱的溶劑體系中待測物的測定。另外,目前關于AP 補償基質效應的研究主要針對農殘化合物[13-18],對于香味成分在煙草中的基質效應研究尚未見報道。因此,本研究中選擇V乙腈∶V二氯甲烷=2∶1體系作為弱極性溶劑體系,開展了AP 對煙草中香味成分的基質效應補償研究,旨在為AP 適用范圍的擴展以及煙草香味成分分析中基質效應的補償提供技術支撐。
1 材料與方法
1.1 材料、試劑和儀器
2019 年云南產C3F 中部煙葉樣品。
QuEChERS 萃取試劑盒(4 g 硫酸鎂+1 g 氯化鈉,美國Agilent 公司);46 種香味成分標準品及內標己酸甲酯(>98%,美國Sigma 公司、東京化成工業株式會社、加拿大TRC 公司或北京百靈威科技有限公司等);23 種分析保護劑(>95%,上海阿拉丁試劑有限公司、東京化成工業株式會社和北京百靈威科技有限公司等);磷酸(AR,天津市科密歐化學試劑有限公司);磷酸二氫鈉(AR,國藥集團化學試劑有限公司);乙腈和甲醇(色譜純,美國J T Baker 公司);二氯乙烷(色譜純,美國Omni Chem 公司);二氯甲烷(色譜純,德國Merck 公司);超純水(自制,電阻率18.2 MΩ·cm)。
7890N 氣相色譜-5975C 質譜聯用儀(美國Agilent 公司);Multi Reax 試管震蕩器(德國Heidolph 公司);Sigma 3-30KS 高速冷凍離心機、CPA225D 電子分析天平(感量0.000 1 g)(德國Sartorius 公司);Milli-Q 超純水儀(美國Millipore公司);Sigmole-NYL1111A 有機相濾膜(尼龍,13 mm×0.22 μm,上海科醚化學科技有限公司)。
1.2 方法
1.2.1 溶液配制
內標工作溶液:準確稱取100 mg 己酸甲酯(精確至±0.1 mg),用二氯乙烷溶解并定容至10 mL,配制成濃度為10 000 mg/L 的內標儲備液,于4 ℃下儲存;準確移取0.1 mL 內標儲備液于10 mL 容量瓶中,用V乙腈∶V二氯甲烷=2∶1 的溶劑定容,配制成濃度為100 mg/L 的內標工作溶液。
混合標準工作溶液:準確稱取各香味成分標準品100 mg(精確至±0.1 mg),用二氯乙烷溶解并定容至10 mL,配制成質量濃度為10 000 mg/L 的單標儲備液。準確移取0.1 mL 各單標儲備液于同一個50 mL 容量瓶中,用V乙腈∶V二氯甲烷=2∶1 的溶劑定容,配制成各香味成分的濃度均為20 mg/L 的混合標準工作溶液。
單一分析保護劑溶液:準確稱取200 mg 各分析保護劑(精確至±0.1 mg),選用合適的溶劑溶解并定容至10 mL,配制成質量濃度均為20 000 mg/L的單一分析保護劑溶液。
3 種溶劑體系下的香味成分標準溶液:
①溶劑標準溶液:采用V乙腈∶V二氯甲烷=2∶1 的混合溶劑,配制一定濃度的香味成分標準溶液;移取1 mL 該標準溶液,加入50 μL 如前的混合溶劑。
②“溶劑+AP”標準溶液:采用V乙腈∶V二氯甲烷=2∶1的溶劑配制一定濃度的香味成分標準溶液;移取1 mL 該標準溶液后,加入50 μL AP 溶液(20 000 mg/L)。
③煙草基質匹配標準溶液:采用煙草基質提取液為溶劑,配制一定濃度的香味成分標準溶液;移取1 mL 該標準溶液后,加入50 μL 如①中的混合溶劑。
磷酸鹽緩沖溶液:準確稱取2.80 g 磷酸以及10.00 g 磷酸二氫鈉,加入100 mL 超純水,超聲、攪拌至溶解,常溫放置。
色譜、質譜條件:
色譜柱:DB-5MS UI 彈性石英毛細管色譜柱(60 m×0.25 mm i.d.×0.25 μm d.f.);進樣口溫度:290 ℃;程序升溫:40 ℃(3 min);進樣模式:不分流進樣;不分流時間:1 min;隔墊吹掃流速:3 mL/min;載氣:氦氣(99.999%);恒流流速:1.5 mL/min;進樣量:0.5 μL。電離模式:電子轟擊(EI);電離能量:70 eV;燈絲電流:35 μA;離子源溫度:230 ℃;四極桿溫度:150 ℃;傳輸線溫度:280 ℃;檢測方式:選擇離子監測(SIM)模式。31 種香味成分及內標的保留時間(RT)和SIM 掃描離子見表1,選擇離子流圖見圖1。
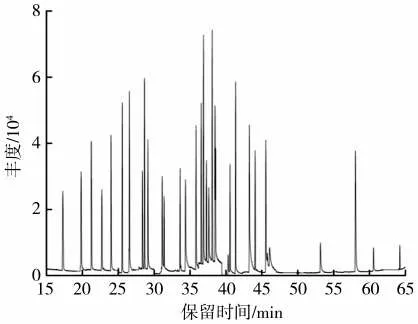
圖1 31 種香味成分及內標的選擇離子流圖Fig.1 Selective ion chromatogram of 31 aroma components and internal standard
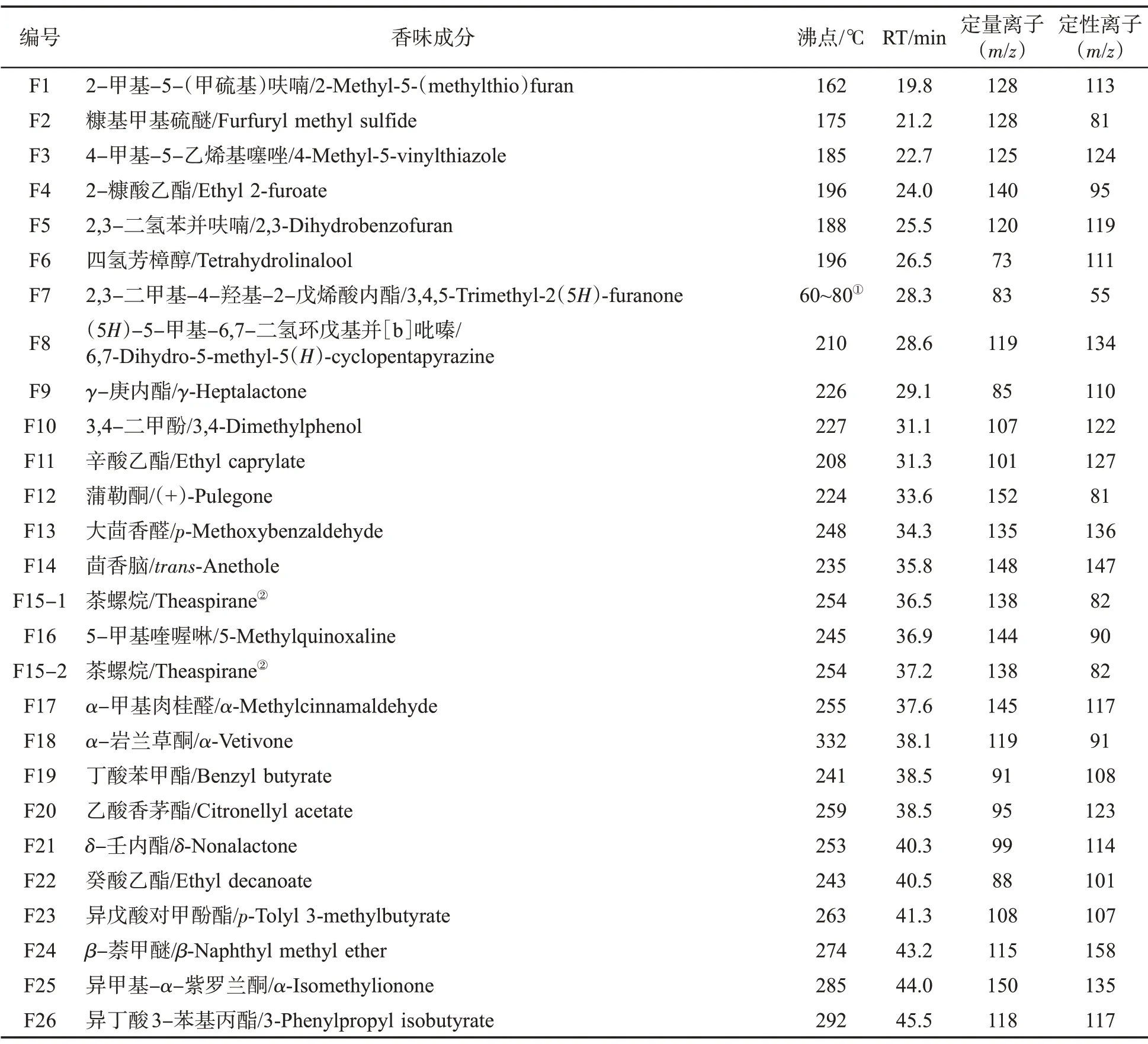
表1 31 種香味成分的保留時間和SIM 掃描離子Tab.1 Retention time and SIM ions of 31 aroma components

表1(續)
1.2.2 煙草基質制備
將實驗所用煙葉研磨成粉,過0.38 mm(40目)篩。準確稱取1.00 g 樣品于50 mL 具塞離心管中,加入10 mL 磷酸鹽緩沖溶液使其完全浸潤樣品,靜置20 min;加入10 mL 乙腈,以2 500 r/min渦旋萃取10 min,-18 ℃冷凍30 min;取出后加入4.00 g 無水硫酸鎂、1.00 g 氯化鈉并迅速劇烈搖晃,然后加入5 mL 二氯甲烷,再依次以2 500 r/min 渦旋10 min,8 000 r/min 離心3 min,取上清液過有機相濾膜后轉移至儲液瓶中。
2 結果與討論
2.1 分析保護劑的選擇
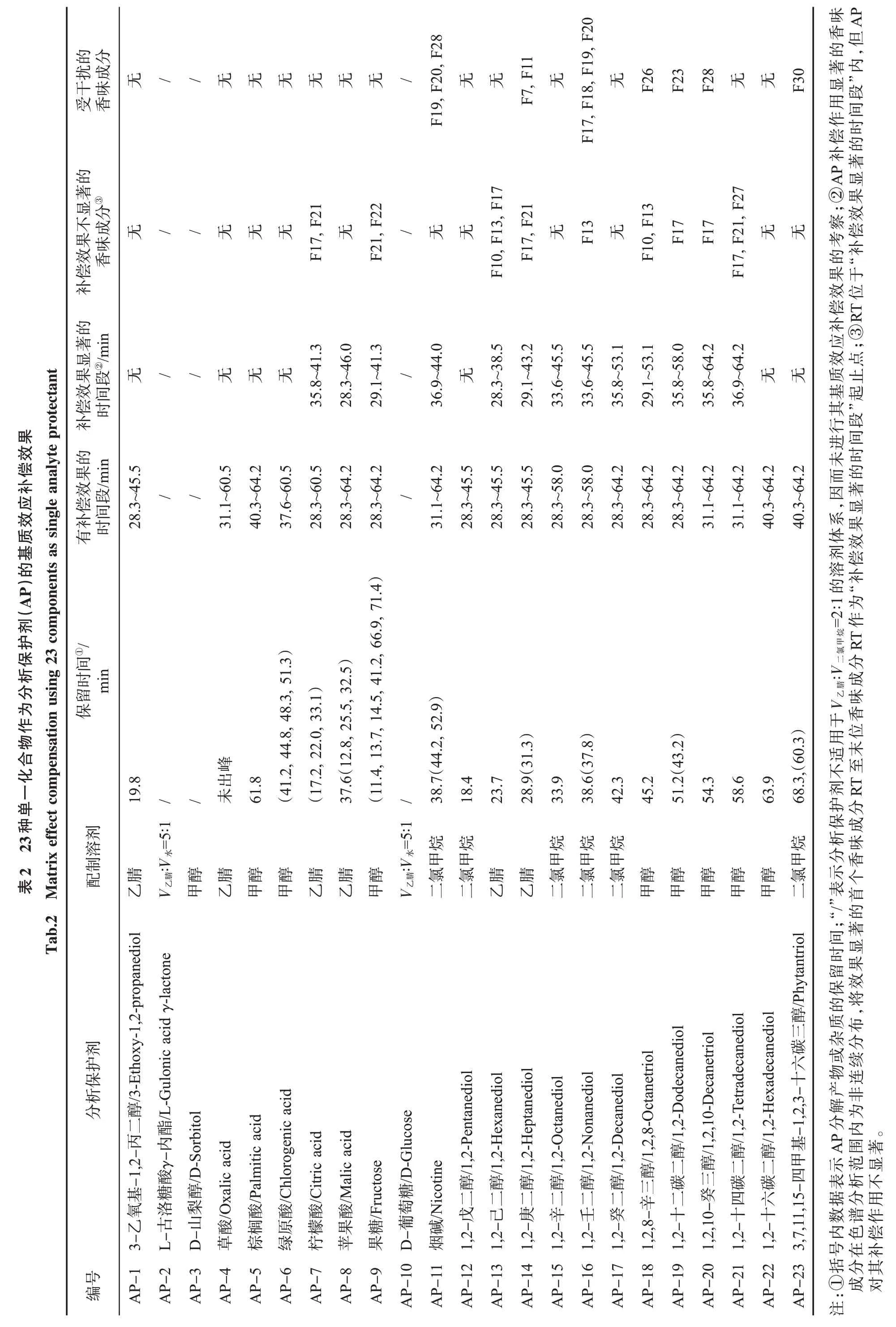
通常,一種理想的分析保護劑(或組合)的選擇需要考慮的主要因素有:①在溶液中和GC 系統中與待測物不發生反應;②不干擾待測物的檢測;③不影響GC 系統和檢測器的性能;④無毒、廉價且實用性高。本研究中初選了23 種分析保護劑(表2),主要包括3 類:①文獻中常用的對敏感性化合物色譜峰有良好保護效果的3 種化合物(3-乙氧基-1,2-丙二醇、L-古洛糖酸γ-內酯和D-山梨醇);②在煙葉中質量分數較高的部分化合物(果糖、葡萄糖、綠原酸、煙堿、草酸、蘋果酸、檸檬酸、棕櫚酸);③含不同碳原子數的二元及三元碳醇類化合物(1,2-戊二醇、1,2-己二醇、1,2-庚二醇、1,2-辛二醇、1,2-壬二醇、1,2-癸二醇、1,2,8-辛三醇、1,2-十二碳二醇、1,2,10-癸三醇、1,2-十四碳二醇、1,2-十六碳二醇、3,7,11,15-四甲基-1,2,3-十六碳三醇)。
根據分析保護劑的溶解性,選擇合適的有機溶劑配制成濃度為20 000 mg/L 的單一分析保護劑溶液(配制溶劑見表2)。由于L-古洛糖酸γ-內酯和葡萄糖的極性較強,采用乙腈配制的同時引入了一定量水進行助溶。
2.2 分析保護劑對香味成分色譜峰的影響
2.2.1 香味成分基質效應考察
選擇31 種香味成分(表1),種類包括醇、酚、醚、醛、酮、酯/內酯、烷烴和含氮化合物等,沸點為162~360 ℃,覆蓋了GC 可測化合物的揮發性范圍。為了便于基質效應考察以及分析保護劑效果評價,這31 種香味成分在所選煙草樣品中為未檢出。
對比了0.2 mg/L各香味成分在V乙腈∶V二氯甲烷=2∶1溶劑與煙草基質中的色譜峰,以峰高[23](己酸甲酯為內標進行校正,己酸甲酯基本不受基質效應影響)和對稱因子為評價指標,考察其受基質效應的影響。結果見表3,31 種香味成分基質與溶劑峰高的比值范圍為0.99~8.27,在溶劑和煙草基質中的對稱因子范圍分別為0.96~6.52 和0.90~1.52。其中,10 種香味成分基本不受基質效應影響,基質與溶劑峰高的比值小于1.20;21 種香味成分受基質效應影響,基質與溶劑峰高的比值大于1.20。尤其是有10種香味成分受基質效應影響比較明顯,在溶劑中色譜峰較低,拖尾較嚴重;而在基質中峰形較好(基質與溶劑峰高的比值大于2,溶劑中對稱因子大于1.9,基質中對稱因子趨于1),分別為3,4-二甲酚、大茴香醛、α-甲基肉桂醛、δ-壬內酯、β-萘甲醚、異丁酸3-苯基丙酯、丙烯基乙基愈創木酚、δ-十二內酯、苯乙酸對甲苯酯和δ-十四內酯。
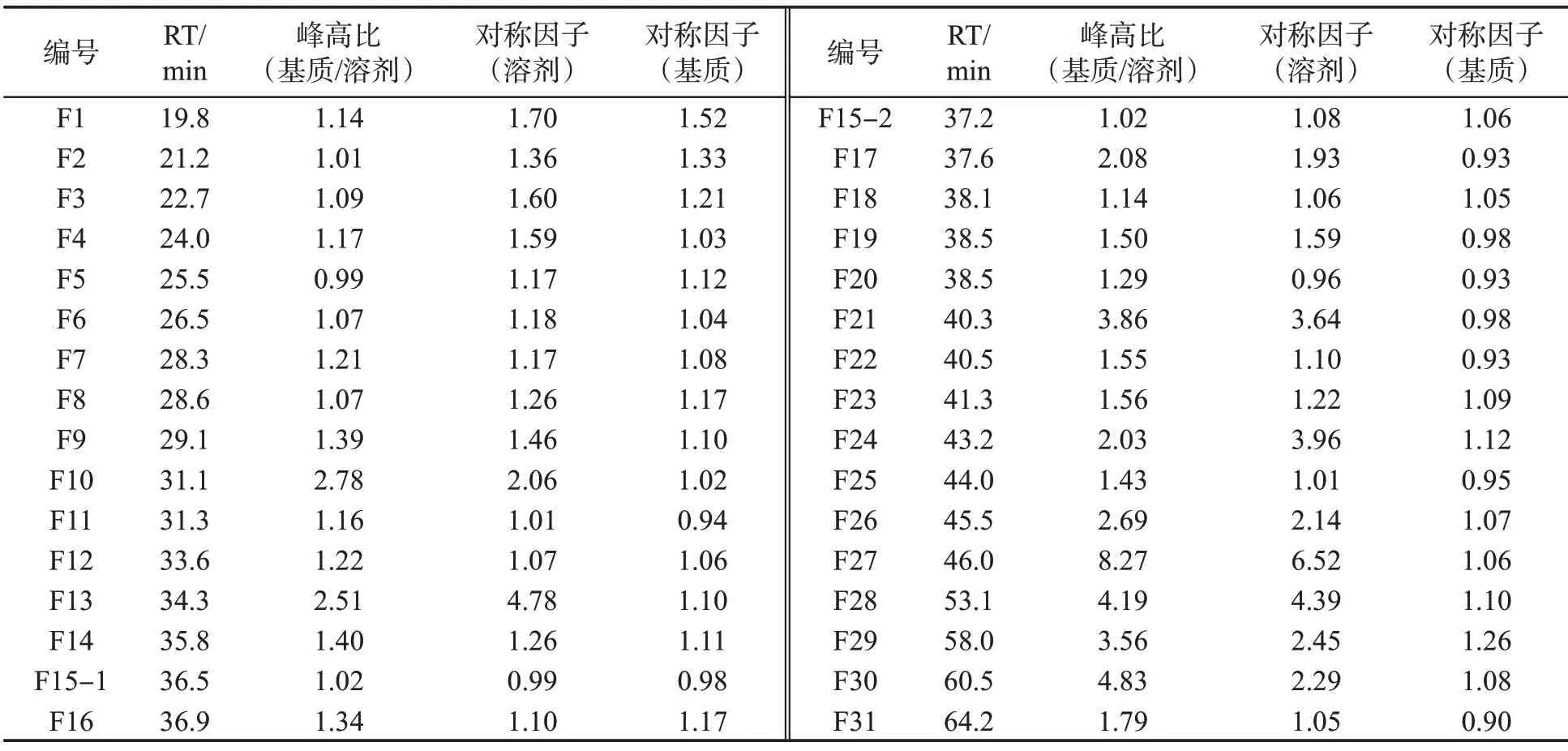
表3 31 種香味成分在溶劑和煙草基質中的色譜峰對比Tab.3 Chromatographic peaks of 31 aroma components in solvent and tobacco matrix
2.2.2 單一分析保護劑對香味成分色譜峰的影響
以上述受基質效應影響(基質與溶劑峰高的比值大于1.20)的21 種香味成分為分析對象,采用峰高為評價指標[23],考察在0.2 mg/L 香味成分標準溶液中加入1 000 mg/L 單一AP 溶液后色譜峰的變化,并與煙草基質匹配標準溶液中的色譜峰進行對比。通常當待測物在基質中的響應與在溶劑中的響應相比超過定量方法要求的回收率上限時,認為有基質效應存在[23]。GB/T 27404—2008[24]中對于待測物回收率范圍要求:當待測組分質量分數為0.1~1.0 mg/kg 時,回收率范圍為80%~110%;當待測組分質量分數小于0.1 mg/kg時,回收率范圍為60%~120%。綜合考慮,本研究中以±20%作為判斷基質效應補償效果的標準,即當“溶劑+AP”標準溶液中香味成分色譜峰高大于溶劑標準溶液中峰高的20%及以上,認為AP 對香味成分有一定的基質效應補償效果;而達到基質中峰高的80%及以上,認為有比較顯著的基質效應補償效果。23 種單一化合物作為分析保護劑的基質效應補償效果見表2。
3-乙氧基-1,2-丙二醇、L-古洛糖酸γ-內酯和D-山梨醇為文獻中常見的對敏感性化合物色譜峰有良好基質效應補償效果的分析保護劑[2-3]。本研究結果顯示,3-乙氧基-1,2-丙二醇的保留時間為19.8 min,對保留時間范圍為28.3~45.5 min 的16 種香味成分具有一定的基質效應補償作用(受到基質效應影響的21 種香味成分的保留時間范圍為28.3~64.2 min),但并未顯示出顯著的補償效果,3-乙氧基-1,2-丙二醇的加入不會干擾香味成分的測定。于1 mL 0.2 mg/L 香味成分標準溶液中加入50 μL L-古洛糖酸γ-內酯或D-山梨醇溶液后,溶液出現分層現象,L-古洛糖酸γ-內酯和D-山梨醇極性較強,不適用于當前V乙腈∶V二氯甲烷=2∶1的弱極性溶劑體系。
選用煙葉中質量分數較高的成分作為AP 時,蘋果酸、果糖對受到基質效應影響的21 種香味成分均有一定的基質效應補償作用。蘋果酸對保留時間范圍為28.3~46.0 min 的17 種香味成分補償效果顯著,可以達到基質匹配標準溶液中相應色譜峰峰高的80%及以上,并且不干擾待測香味成分的定量。果糖對保留時間范圍為29.1~41.3 min(除δ-壬內酯和癸酸乙酯外)的10 種香味成分補償效果顯著。圖2 中給出了蘋果酸對其基質效應補償效果顯著的部分香味成分,可以看出,3,4-二甲酚、大茴香醛、α-甲基肉桂醛、β-萘甲醚、δ-壬內酯和丙烯基乙基愈創木酚6 種香味成分在溶劑標準溶液中的色譜峰響應較低,且存在不同程度的拖尾,加入蘋果酸后,其響應值明顯增大,峰形變高、變窄,3,4-二甲酚、大茴香醛、α-甲基肉桂醛、β-萘甲醚4 種香味成分在“溶劑+AP”標準溶液中的色譜峰與在基質匹配標準溶液中的色譜峰基本一致,δ-壬內酯和丙烯基乙基愈創木酚2 種香味成分在“溶劑+AP”標準溶液中的色譜峰峰高達到了基質匹配標準溶液的80%以上,與溶劑標準溶液相比色譜峰峰高均增加了約3.5 倍。
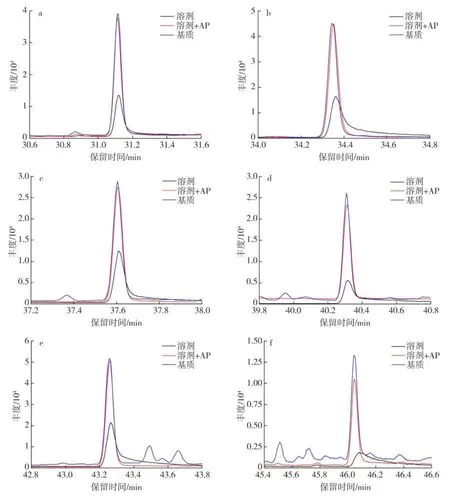
圖2 蘋果酸基質效應補償效果顯著的6 種代表性香味成分Fig.2 Six representative aroma components with remarkable matrix effect compensation by malic acid
綠原酸、草酸、棕櫚酸、檸檬酸和煙堿分別對不同保留時間段內出峰的香味成分有一定的基質效應補償效果。綠原酸、草酸和棕櫚酸無顯著的補償效果,檸檬酸對35.8~41.3 min 出峰(除α-甲基肉桂醛和δ-壬內酯外)的6 種香味成分補償效果較為顯著,煙堿對36.9~44.0 min 出峰(除α-甲基肉桂醛和δ-壬內酯外)的5 種香味成分基質效應補償效果較為顯著。煙堿干擾丁酸苯甲酯、乙酸香茅酯和δ-十二內酯3 種香味成分的定量。D-葡萄糖與香味成分標準溶液不混溶,不適用于V乙腈∶V二氯甲烷=2∶1 的弱極性溶劑體系。
考察了12 種二元及三元醇類化合物作為AP對香味成分的基質效應補償效果。含有相同羥基數量的多元醇類化合物,隨分子中碳原子數增加,其保留時間遞增。1,2-戊二醇出峰較早,保留時間為18.4 min,對保留時間范圍為28.3~45.5 min的16 種香味成分具有一定的基質效應補償作用,但未顯示出顯著的補償效果。1,2-己二醇和1,2-庚二醇分別對保留時間范圍為28.3~45.5 min 的部分香味成分具有一定的基質效應補償作用,1,2-辛二醇和1,2-壬二醇分別對保留時間范圍為28.3~58.0 min 的香味成分具有一定的基質效應補償作用,并且補償效果顯著的時間段隨保留時間的增加而向后移動。1,2-癸二醇、1,2,8-辛三醇和1,2-十二碳二醇對受到基質效應影響的香味成分分別表現出不同程度的基質效應補償作用,1,2-癸二醇對35.8~53.1 min 的13 種香味成分補償效果顯著,1,2,8-辛三醇對29.1~53.1 min(除3,4-二甲酚和大茴香醛外)的14 種香味成分補償效果顯著,1,2-十二碳二醇對35.8~58.0 min(除α-甲基肉桂醛外)的12 種香味成分補償效果顯著。1,2,10-癸三醇、1,2-十四碳二醇、1,2-十六碳二醇和3,7,11,15-四甲基-1,2,3-十六碳三醇出峰時間較晚,隨保留時間的增加,有一定基質效應補償作用的時間段起點向后移動,時間段范圍縮短,1,2,10-癸三醇對35.8~64.2 min(除α-甲基肉桂醛外)的14 種香味成分基質效應補償效果顯著,1,2-十四碳二醇對36.9~64.2 min(除α-甲基肉桂醛、δ-壬內酯和丙烯基乙基愈創木酚外)的12 種香味成分基質效應補償效果顯著,1,2-十六碳二醇和3,7,11,15-四甲基-1,2,3-十六碳三醇無顯著的基質效應補償效果。對香味成分具有顯著補償效果的二元及三元醇類AP 中,除1,2-己二醇、1,2-辛二醇、1,2-癸二醇和1,2-十四碳二醇外,其他對待測香味成分的定性定量檢測均有不同程度的干擾。圖3 為1,2-十四碳二醇對其基質效應補償效果顯著的部分香味成分。

圖3 1,2-十四碳二醇基質效應補償效果顯著的6 種代表性香味成分Fig.3 Six representative aroma components with remarkable matrix effect compensation by 1,2-tetradecanediol
綜上所述,在溶劑標準溶液中加入分析保護劑后,各香味成分的響應不同程度地增大,色譜峰形得到一定改善。這主要是由于襯管玻璃表面存在游離硅醇基和金屬離子活性位點,當樣品溶液在襯管中氣化時,含有活性基團的分析保護劑在氣化過程中迅速占據活性位點,一方面減少了香味成分在襯管中的不可逆吸附和降解,使到達檢測器的香味成分增多,響應值增大;另一方面,減少了香味成分與活性位點的相互作用,抑制了色譜峰拖尾和展寬,峰形得到改善。
2.2.3 組合分析保護劑的考察
綜上可以看出,單一AP 并不能對所有香味成分均具有顯著的基質效應補償效果,因此需要對不同的AP 進行組合。對比單一AP 基質效應補償作用顯著的時間段,組合后保證能完全覆蓋待測香味成分,并且不干擾其定性定量檢測。
由上述分析可知,在21 種受基質效應影響的香味成分中,蘋果酸對其中17 種香味成分有顯著的基質效應補償作用,對δ-十二內酯、苯乙酸對甲苯酯、δ-十四內酯和香紫蘇內酯4 種香味成分有一定的基質效應補償作用,但未達到煙草基質匹配標準溶液中色譜峰峰高的80%,而1,2-十四碳二醇對這4 種香味成分呈現顯著的基質效應補償作用,同時二者均不干擾待測香味成分的檢測。因此,選擇蘋果酸+1,2-十四碳二醇作為組合AP。
進一步考察了不同濃度的蘋果酸+1,2-十四碳二醇(各為200、500、1 000 mg/L)組合AP 對香味成分的基質效應補償作用。如圖4 所示,隨蘋果酸+1,2-十四碳二醇濃度的增加,其基質效應補償效果越顯著。當蘋果酸和1,2-十四碳二醇的濃度均為1 000 mg/L 時,21 種香味成分的色譜峰峰高均達到煙草基質匹配標準溶液中對應色譜峰峰高的80%及以上。
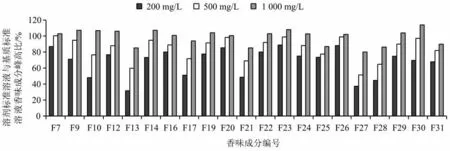
圖4 加入不同濃度AP 組合的溶劑標準溶液與基質標準溶液中21 種香味成分峰高百分比Fig.4 The percentages of peak height of 21 aroma components in solvent standard added different concentrations of AP combination versus matrix standard
2.3 校正曲線的比較
分別配制了31 種香味成分的溶劑、“溶劑+AP組合”和煙草基質匹配標準溶液,3 種溶劑體系下標準溶液濃度均為5.00、2.00、1.00、0.50、0.20、0.10、0.05 mg/L,AP 組合為蘋果酸和1,2-十四碳二醇(各1 000 mg/L)的組合。以各香味成分與內標的峰面積比對每種香味成分濃度作線性回歸,得到31 種香味成分在3 種溶劑體系下的標準工作曲線,線性相關系數(r2)見表4。結果表明,在溶劑配制的混合標準溶液中添加蘋果酸和1,2-十四碳二醇(各1 000 mg/L)后,標準工作曲線的線性得到了較大改善,31 種香味成分的r2均大于0.99,其中29 種香味成分的r2大于0.999。圖5 以香味成分濃度為橫軸,以其與內標峰面積的比值為縱軸,比較了β-萘甲醚、異丁酸3-苯基丙酯和苯乙酸對甲苯酯在3 種溶劑體系下的標準曲線。可以看出,這3 種香味成分的溶劑標準曲線的r2均小于0.99,線性較差;加入蘋果酸和1,2-十四碳二醇(各1 000 mg/L)組合后,r2大于0.999,標準曲線與基質匹配標準曲線基本一致。
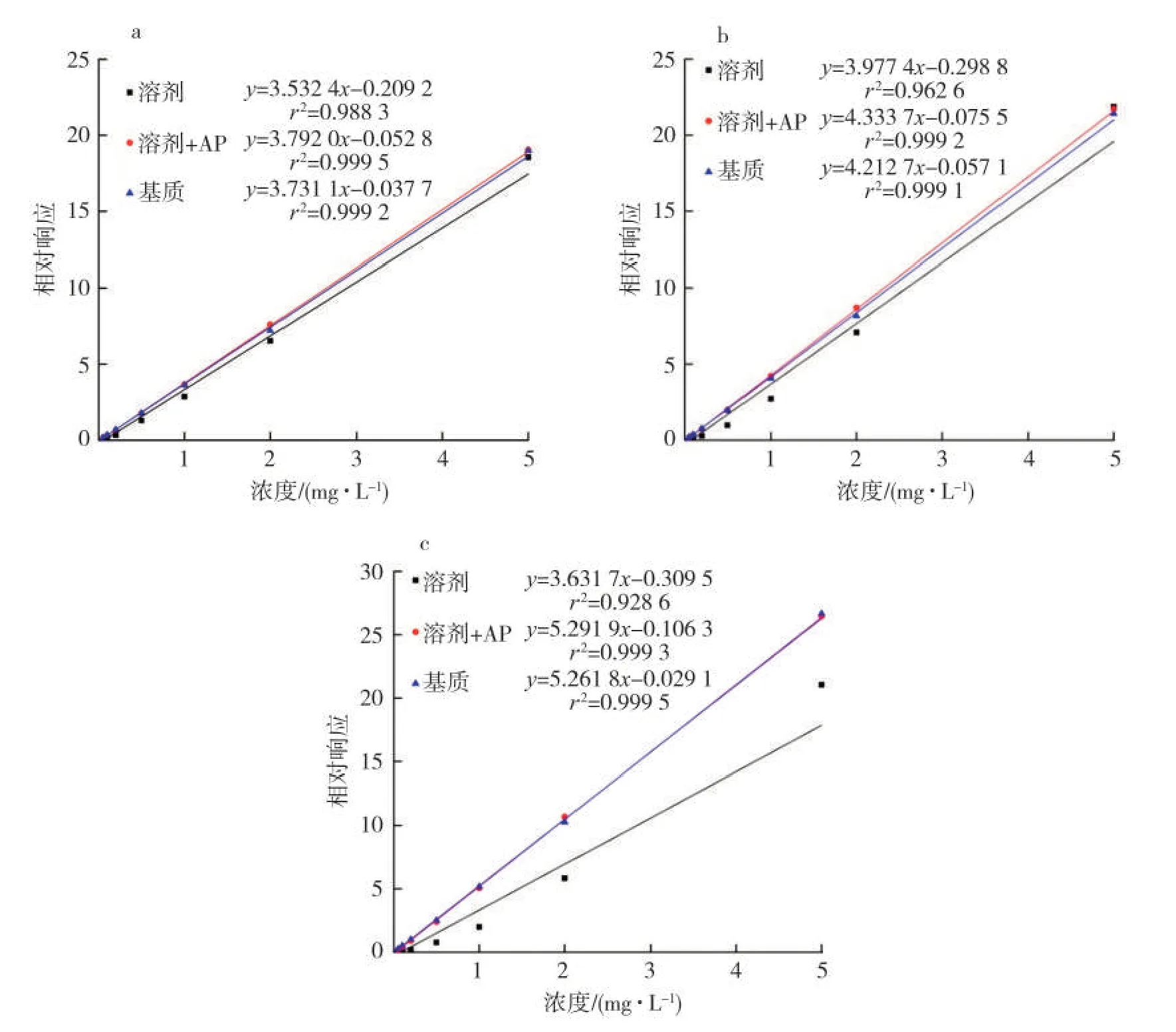
圖5 β-萘甲醚(a)、異丁酸3-苯基丙酯(b)和苯乙酸對甲苯酯(c)標準曲線的比較Fig.5 Calibration curves of β-naphthyl methyl ether(a),3-phenylpropyl isobutyrate(b)and p-tolyl phenylacetate(c)
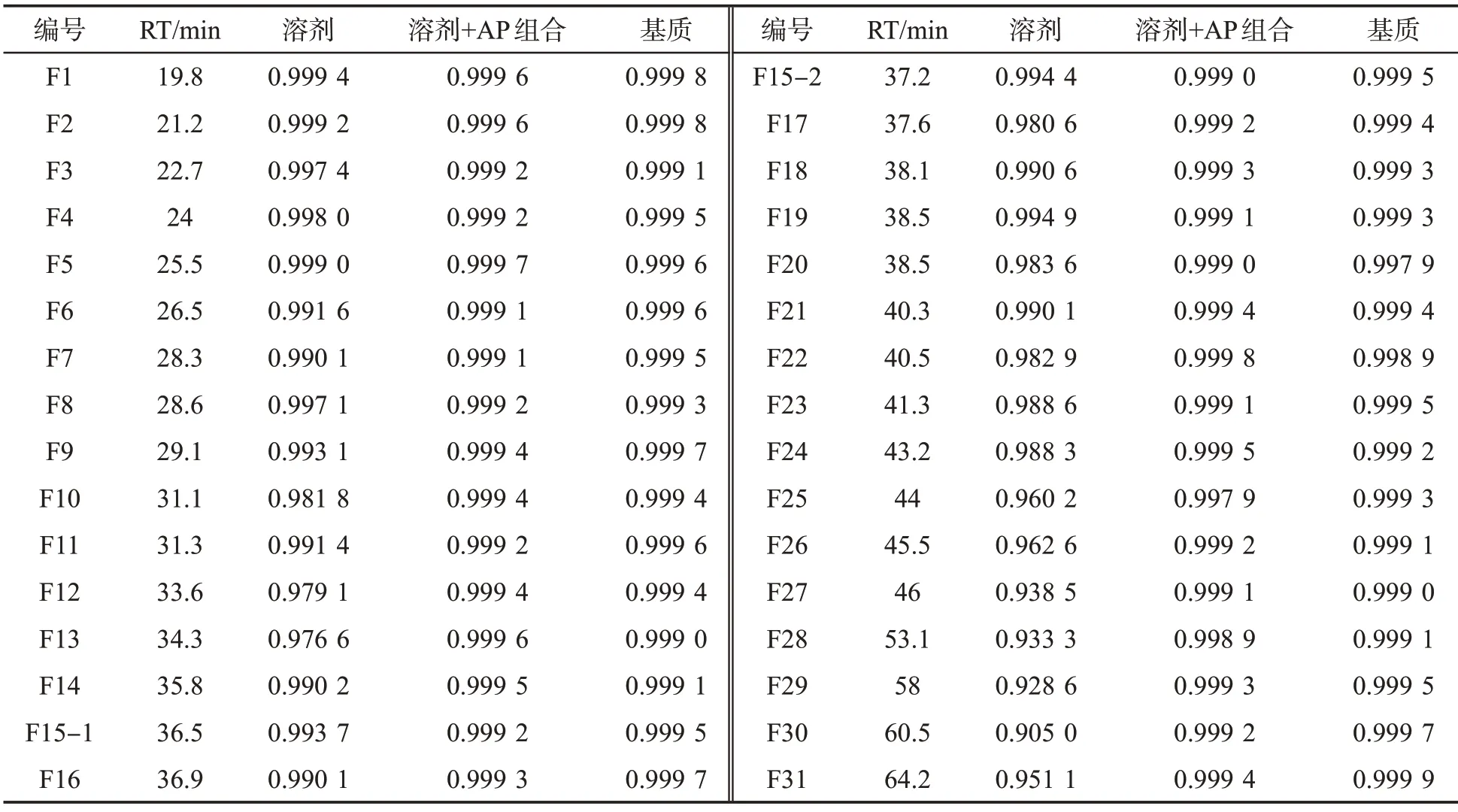
表4 31 種香味成分的溶劑、“溶劑+AP 組合”和基質匹配標準曲線的線性相關系數(r2)Tab.4 Linear correlation coefficient(r2)for calibration curves of 31 aroma components in solvent,“solvent+AP combination”and matrix
為進一步驗證蘋果酸和1,2-十四碳二醇(各1 000 mg/L)組合的基質效應補償效果,選擇了15種所選煙草樣品中含有的香味成分(表5),比較了其在溶劑、“溶劑+AP 組合”和煙草基質匹配3種溶劑體系下的標準曲線(標準溶液濃度均為10.00、5.00、2.00、1.00、0.50、0.20、0.10、0.05 mg/L)。結果表明,加入AP 組合使煙葉中含有的15 種香味成分標準曲線的線性有了較大改善,r2均大于等于0.999,且標準曲線與基質匹配標準曲線的斜率比在0.9~1.1 之間。紫丁香醇、香蘭素和棕櫚酸乙酯在3 種溶劑體系下的標準曲線見圖6,相比于溶劑匹配標準曲線,在3 種溶劑體系下的標準曲線的線性得到了較大改善,且斜率與基質匹配標準曲線基本一致。
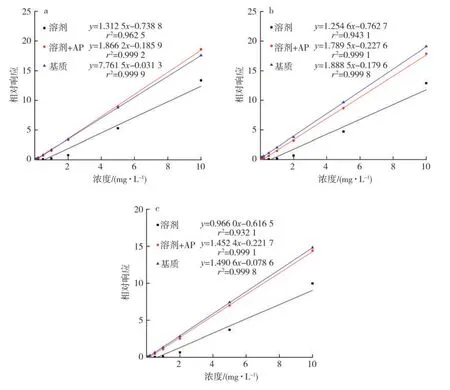
圖6 紫丁香醇(a)、香蘭素(b)和棕櫚酸乙酯(c)標準曲線的比較Fig.6 Calibration curves of 2,6-dimethoxyphenol(a),vanillin(b)and ethyl palmitate(c)

表5 15 種煙草香味成分的溶劑、“溶劑+AP 組合”和基質匹配標準曲線的對比Tab.5 Comparison of calibration curves of 15 tobacco aroma components in solvent,“solvent+AP combination”and matrix
3 結論
①在V乙腈∶V二氯甲烷=2∶1 的弱極性溶劑體系下,在溶劑標準溶液中加入分析保護劑,改善了敏感性香味成分的色譜峰形,提高了峰強度。②通過優化分析保護劑種類、組合及組合濃度,找到了補償煙草香味成分基質效應的分析保護劑組合:蘋果酸+1,2-十四碳二醇(濃度均為1 000 mg/L)。③驗證結果顯示,加入所選分析保護劑組合后,各煙草香味成分標準曲線的線性得到了較大改善,其斜率及線性相關系數(r2)與煙草基質匹配標準曲線基本一致,基質效應補償效果良好。

