超臨界氨水改性活性炭及其對CO2的吸附性能
陳藝蘭,鐘琴華,曾煒鵬,劉亞敏,劉敏毅,林小英
(福建工程學院 生態環境與城市建設學院,福建 福州 350118)
氣候變化是全球關注的問題,控制溫室氣體排放特別是CO2的排放尤為迫切。CO2減排技術中,活性炭(AC)吸附因其具有應用條件寬泛、耗能少、操作簡單等特點,具有很好的應用前景[1-23]。影響AC吸附性能的主要因素有材料孔隙結構、表面官能團數量和種類等。研究表明,將含氮官能團引入AC表面能夠提高AC對CO2的吸附性能[4]。使吸附劑與含氮試劑發生反應是引入含氮基團的常用方法。超臨界流體具有特殊的溶解性,能迅速地深入到溶質的微小結構中,且兼具氣體和液體的性質,具有良好的傳遞性質[5]。
本研究采用超臨界氨水改性AC,表征了改性前后AC的表面結構和化學性質,探討了改性AC對CO2的吸附性能。
1 實驗部分
1.1 試劑和儀器
柱形AC,河南綠都炭業有限公司提供;氨水:分析純;CO2、N2:體積分數99.999%。
SOWO-Ⅱ型機械力超臨界反應釜:南通市華安超臨界萃取有限公司。
1.2 實驗方法
1.2.1 AC的改性
用蒸餾水淋洗AC表面以去除雜質,出水清澈后在100 ℃下烘干24 h,備用。
取氨水180 mL置于200 mL的超臨界反應釜中,加入5 g AC,分別在150,220,250,280 ℃下反應2 h,冷卻至室溫,過濾后在100 ℃下烘干24 h,冷卻。樣品分別記為AC-150、AC-220、AC-250和AC-280。
1.2.2 表征方法
采用美國Quantachrome公司的Autosorb IQ型全自動比表面積與孔隙度分析儀測定樣品的N2吸附-脫附等溫線和比表面積(BET法);采用美國Thermo Fisher公司的Nicolet iS5型傅里葉紅外光譜儀分析測定樣品官能團,掃描波數在400~4 000 cm-1;采用美國 FEI 公司的Nova NanoSEM450型場發射掃描電子顯微鏡觀測樣品的表面形貌。
1.2.3 吸附-脫附實驗
采用德國Netzsch公司的TG209-F3型熱重分析儀進行CO2吸附-脫附實驗。將改性后樣品(m0,g)在高純N2流(100 cm3/min)中以10 ℃/min的升溫速率升溫至100 ℃,保持恒溫30 min脫氣至恒重,然后降溫至30 ℃,持續通入高純CO2(流量為20 cm3/min)1 h,記錄樣品質量(m1,g)。再通入高純N2流(流量為100 cm3/min),同時快速升溫至100 ℃脫附1 h,脫附過程結束,繼續下一個吸附過程。吸附量(q,mmol/g)按式(1)計算。44為CO2分子量。

2 結果與討論
2.1 表面基團分析
改性前后AC的FTIR譜圖見圖1。由圖1可知:改性前后AC在3 650~3 200 cm-1之間均出現了較強的寬吸收峰,主要歸因于O—H鍵的伸縮振動[6],AC-150在該處的吸收峰高度比AC略有增強。該處峰值加強的原因包含兩個方面:一方面是表面—OH含量有所增加,另一方面是N—H伸縮振動疊加增強了此處的峰強度;1 560 cm-1附近和1 396 cm-1附近出現的吸收峰分別歸屬于—COOH和C=O的伸縮振動[7],改性后樣品在此處的峰強度明顯減弱,歸因于樣品表面酸性官能團與氨水發生了中和反應,酸性官能團的減少促進了AC對CO2等非極性分子的親和力,從而增加了吸附量[8];1 070 cm-1附近的吸收峰可能歸屬于AC表面的C—O伸縮振動[9]。
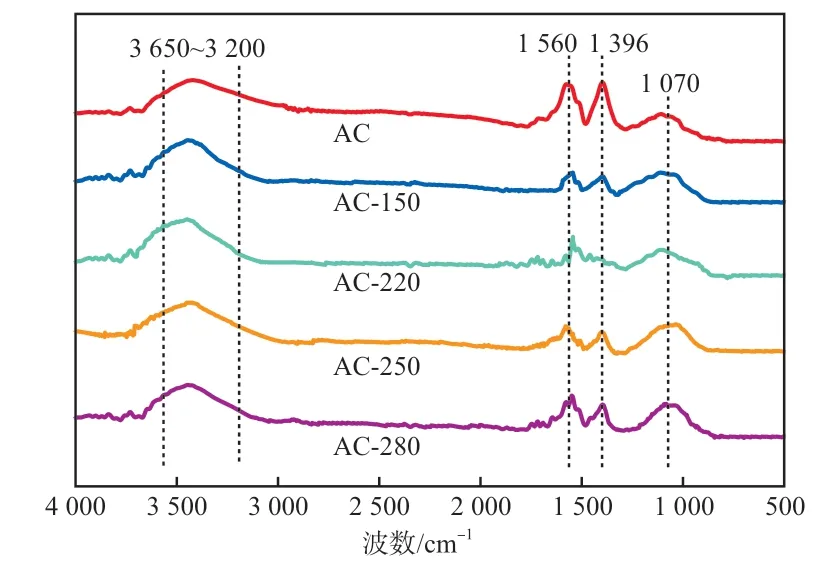
圖1 改性前后AC的FTIR譜圖
2.2 吸附-脫附等溫線及比表面積
改性前后AC的N2吸附-脫附等溫線見圖2,結構參數見表1。由圖2可知:相對壓力較低處(p/p0<0.5),吸附-脫附曲線基本重合;隨著相對壓力增大,N2吸附量緩慢增加,說明AC具有微孔結構;p/p0>0.5處,吸附-脫附曲線出現滯回環,這是由于毛細凝聚現象造成吸附和脫附曲線不重合[10]。改性前后AC的吸附等溫線屬于Ⅳ型,表明樣品具有中孔特征[11]。改性后樣品的N2吸附量降低,結合表1的結構參數可知,改性后AC的BET比表面積減小,且隨著改性溫度的升高,比表面積減小量增大,N2吸附為物理吸附,因此吸附量隨著比表面積的降低而減小。
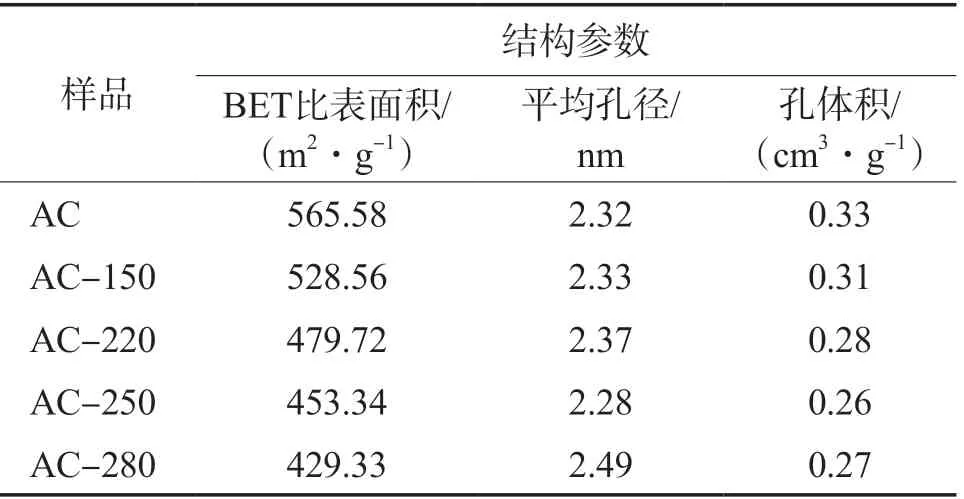
表1 改性前后AC的結構參數
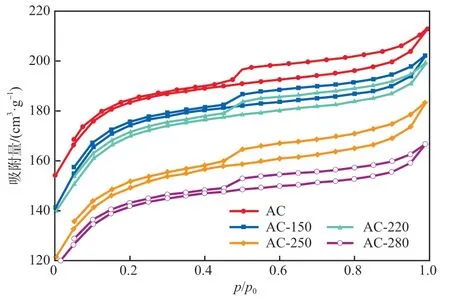
圖2 改性前后AC的N2吸附-脫附等溫線
2.3 元素分析結果
AC和AC-150的元素分析結果見表2。由表2可見:AC中未發現N元素,經過改性后的AC-150樣品中N元素質量分數增至2.73%,與其他學者研究報道的結果大致相同[12],表明改性后樣品孔道內含有一定量的含氮基團,說明氨基負載到了AC表面。

表2 AC和AC-150的元素分析結果
2.4 SEM表征結果
AC和AC-150的SEM照片見圖3。由圖3可知:AC表面平滑,含有少量雜質;AC-150表面無雜質,與其他學者所報道的相類似[13-14],超臨界氨水流經AC表面時帶走了雜質;AC-150表面有明顯的細小孔洞,是由于超臨界氨水在高溫下腐蝕炭表面造成的,部分微孔結構塌陷,這也是改性后樣品BET比表面積降低的一個重要原因。

圖3 AC和AC-150的SEM照片
2.5 吸附等溫線
25 ℃條件下,改性前后AC的CO2吸附曲線見圖4。由圖4可知,改性后AC的CO2吸附量顯著增加,AC-150的吸附量最高,從改性前的0.979 mmol/g增至1.291 mmol/g,增加了約30%。
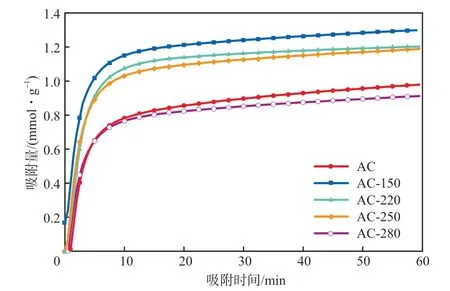
圖4 改性前后AC的CO2吸附曲線
AC對CO2的吸附性能不僅取決于其比表面積大小,還與樣品表面的基團相關[15]。改性后AC表面負載有—OH和含氮基團,增加了化學吸附量且增強了樣品對CO2的親和力[16]。圖4的吸附過程呈現兩個階段:在0~10 min以內,CO2被快速吸附;隨后,吸附速率變緩并逐漸趨于吸附平衡。AC表面具有充裕的親和位點,快速吸附了CO2分子,隨著吸附位點被占據,反應速率下降直至平衡。AC-280較AC吸附量減少,其原因是AC-280的BET比表面積較AC降低了136 m2/g,增加的化學吸附量未能彌補減少的物理吸附量。
2.6 吸附動力學
采用Lagergren準一級吸附動力學模型、Ho準二級動力模型和Avrami分數階動力學模型探究吸附機理。Lagergren一級吸附動力學模型也稱線性驅動力(LDF)模型,主要用于解釋基于吸附容量的吸附過程,其表達式見式(2)。

式中,qt為t時刻的吸附量,mmol/g;qe為平衡吸附量,mmol/g;k1為準一級吸附速率常數,mmol/(g·s)。
Ho準二級吸附動力學模型假設吸附量與吸附劑表面占據的活性位點數量成正比。其表達式見式(3)。

式中,k2為準二級吸附速率常數,mmol/(g·s)。
Avrami模型最初是應用于粒子成核的分數階動力學模型,近年來被用于描述不同類型吸附劑對CO2、N2等的吸附行為[17-18],其表達式見式(4)。

式中,ka為Avrami模型的動力學常數,min-1;n為Avrami指數,無量綱。
實驗數據模擬結果見圖5,動力學模型模擬參數見表3。由表3可見:準一級動力學模型的R2隨著溫度升高逐漸減小,說明低溫適于一階模型,主要以物理吸附為主[19];溫度越高,準二級動力學模型的R2越大,說明隨著溫度升高,CO2在AC表面發生化學反應,即CO2與負載于AC表面的氨基發生反應;Avrami模型的R2均大于0.98,說明Avrami模型適用于描述改性后AC對CO2的吸附機理,即改性后AC在吸附CO2時物理吸附和化學吸附同時進行。
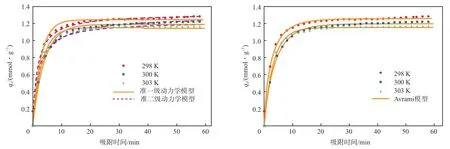
圖5 AC-150的吸附模擬曲線
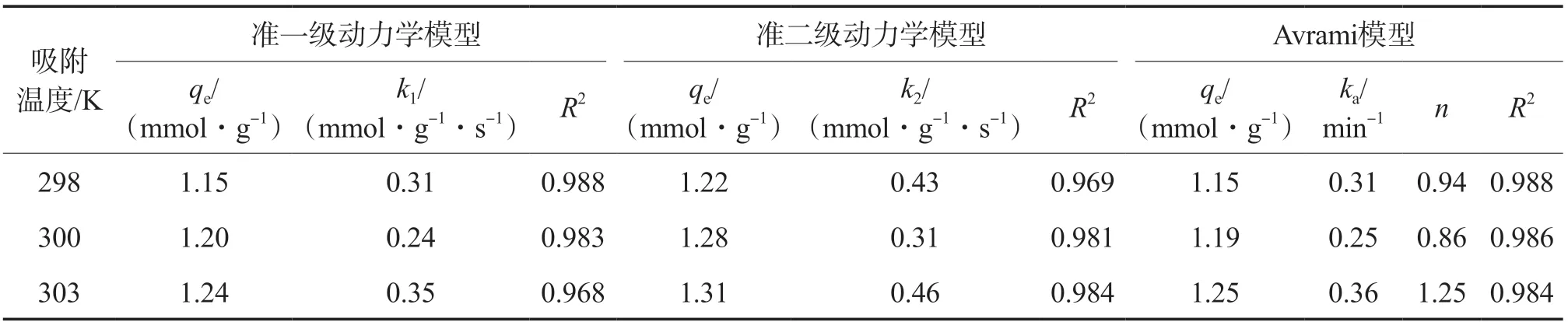
表3 動力學模型模擬參數
3 結論
a)采用超臨界氨水改性AC,改性溫度為150 ℃下制備的改性AC具有最高的CO2吸附量,25 ℃時吸附量從改性前的0.979 mmol/g增至1.291 mmol/g,增加了約30%。
b)改性后AC表面成功負載了含氮基團,改性后AC的BET比表面積減小,且隨著改性溫度的升高,比表面積減小量增大。
c)改性后AC吸附CO2的過程兼有物理吸附和化學吸附,吸附過程符合Avrami模型。

