全球腫瘤疫苗臨床轉化現狀分析*
盧 巖,范云滿,楊瀟逸,張 婷,歐陽昭連
(中國醫學科學院醫學信息研究所,北京 100020)
世界衛生組織(WHO)《疾病和有關健康問題的國際統計分類》第10次修訂本(ICD-10)中將腫瘤分為良性腫瘤、原位腫瘤、惡性腫瘤和不確定或未知腫瘤四大類[1]。癌癥泛指所有類型的惡性腫瘤,是全球各國的主要死亡原因,也是延長人類預期壽命的重要障礙。全球癌癥負擔迅速增長,預計到2040年,全球新發癌癥病例將達2840萬例,比2020年的1930萬例增長47%[2]。針對癌癥的有效防治措施的研究應納入國家層面的衛生計劃,以減少全球罹患癌癥人數,減輕疾病負擔[2-4]。
目前,腫瘤治療方式包括手術、化學治療(簡稱化療)、放射治療(簡稱放療)等傳統治療手段,以及免疫治療、靶向治療、激素治療等生物療法。生物療法在腫瘤的綜合治療中越來越重要,腫瘤疫苗作為生物療法的重要手段,是近年來研究的熱點,進展迅速[5]。臨床應用方面,腫瘤疫苗主要作為手術、放療和化療后的輔助治療,幫助預防癌癥的復發與轉移,另外,已有作用較好的預防性腫瘤疫苗投入了大規模使用,如人乳頭瘤狀病毒(HPV)疫苗[6]。臨床研究方面,已開展大量關于腫瘤疫苗單用或與其他生物療法聯用的臨床試驗,臨床試驗數據庫ClinicalTrials.gov中與疫苗相關的臨床試驗約1/3與腫瘤疫苗相關[5]。臨床試驗是旨在發現或驗證某種試驗藥物療效與安全性的系統性試驗,是藥品獲得藥監部門批準進入臨床使用的必要條件,可在一定程度上體現基礎研究向臨床轉化的活躍程度[7-8]。本研究中基于Clinical Trials.gov中注冊的腫瘤疫苗臨床試驗數據,從臨床試驗注冊概況和注冊內容兩方面分析全球腫瘤疫苗的臨床轉化現狀,為我國加速腫瘤疫苗的臨床轉化、布局腫瘤疫苗技術路線和實現疫苗產業創新提供參考。
1 資料與方法
1.1 數據來源
臨床試驗數據庫:ClinicalTrials.gov是由美國國立衛生研究院(NIH)和美國食品和藥物管理局(FDA)共同開發的臨床試驗注冊和結果數據庫,涵蓋美國50個州及其他220個國家/地區的約38萬項臨床試驗數據,注冊、查詢免費,信息更新及時,是目前全球最大、國際認同度最高、使用最普遍的臨床試驗數據庫[9-11]。
檢索策略:以“Cancer OR Tumor OR Tumour OR Neoplasm OR Oncolog OR Carcinoma”和“Vaccine”為檢索詞,在ClinicalTrials.gov的“Condition or disease”和“Intervention/treatment”字段中檢索,納入所有國家/地區的數據,檢索日期為2021年1月28日。
納入標準:受試者為腫瘤患者,疫苗起治療腫瘤作用;受試者為健康人群,疫苗起預防腫瘤作用。
排除標準:受試者為腫瘤患者,但接種疫苗并非治療腫瘤;受試者為健康人群,但臨床試驗目的并非評估疫苗的有效性、安全性或免疫原性,而是評估提高疫苗接種率的某項措施等;其他不符合納入標準的臨床試驗。
1.2 方法
采用文獻計量學方法,從臨床試驗數量與時間變化趨勢、國家分布、申辦者分布及構成、臨床試驗機構分布、研究類型與方法、臨床試驗分期、適應證等角度,分析全球腫瘤疫苗領域的臨床轉化現狀。
2 結果
2.1 檢索結果
按臨床試驗檢索策略,初始獲得腫瘤疫苗相關臨床試驗2080項,最終納入1772項。
2.2 臨床試驗注冊概況
數量與時間變化趨勢:隨著腫瘤疫苗領域科學研究不斷取得進展,全球腫瘤疫苗相關臨床試驗呈增長趨勢,詳見圖1(受制于檢索時間且數據庫收錄存在延遲,圖中展示的為近30年數據;“中國腫瘤疫苗領域臨床試驗”是指在中國開展,即有中國醫療機構參與的腫瘤疫苗臨床試驗)。全球腫瘤疫苗領域臨床試驗共1772項,第1項(試驗號NCT00002454)開展于1971年,近50%(846項,47.74%)開展于近10年;1995年前,臨床試驗注冊數量一直為個位數;1996年(15項)后總體逐漸增多,至2020年增至87項。中國腫瘤疫苗領域臨床試驗共102項,占全球的5.76%,第1項(試驗號NCT00122681)開展于2004年,大多數(84項,82.35%)開展于近10年;臨床試驗數量一直較少,年均臨床試驗注冊數量僅5.94項,近3年臨床試驗數量超過10項。
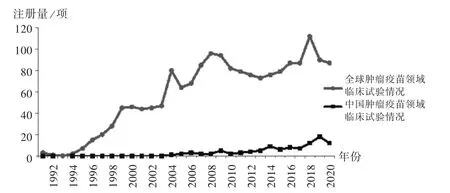
圖1 全球和中國腫瘤疫苗領域臨床試驗注冊數量年度分布Fig.1 Distribution of the annual number of clinical trial registrations of tumor vaccines in the worldwide and China
國家分布:全球共72個國家開展了腫瘤疫苗相關臨床試驗,按注冊數量排名前10的國家依次為美國、德國、中國、英國、加拿大、荷蘭、法國、比利時、日本和西班牙,詳見圖2(圖中“國家”指臨床試驗開展地)。其中,美國引領全球,有1102項;德國、中國處于第二梯隊,分別有109項、102項;排名前10位國家中后9位數量總和剛過美國臨床試驗數量的50%(608項比1102項)。
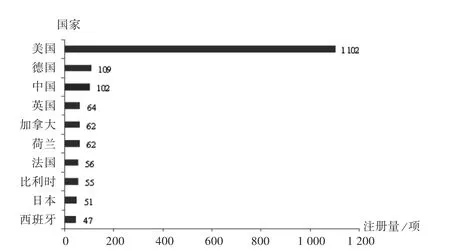
圖2 全球腫瘤疫苗領域臨床試驗注冊數量排名前10的國家Fig.2 Top 10 countries in the worldwide in terms of the number of clinical trial registrations of tumor vaccines
申辦者分布及構成:申辦者是指負責臨床試驗的發起、管理和提供臨床試驗經費的個人、組織或機構[8]。腫瘤疫苗領域臨床試驗申辦者數量排名前5的國家分別為美國、中國、德國、英國和日本,詳見圖3。全球申辦者類型以企業最多見,詳見圖4A。中國申辦者類型以醫療機構最多見,詳見圖4 B。在全球腫瘤疫苗領域,美國國立癌癥研究所、美國國立衛生研究院臨床中心、默沙東公司、紀念斯隆-凱特琳癌癥中心、葛蘭素史克公司和約翰斯·霍普金斯大學Sidney Kimmel綜合癌癥中心表現突出,申辦臨床試驗的數量均不少于40項(見表1)。此外,在此次新冠疫苗開發中表現突出的BioNTech公司(11項)、輝瑞公司(3項)和Moderna公司(2項)均有申辦腫瘤疫苗相關臨床試驗。在中國腫瘤疫苗領域,表現突出的申辦者為廣州復大腫瘤醫院、廈門大學、軍事醫學科學院附屬醫院(307醫院)和上海澤潤生物科技有限公司(見表2)。
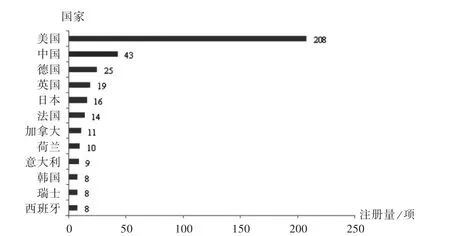
圖3 全球腫瘤疫苗臨床試驗申辦者主要國家分布Fig.3 Distribution of main sponsor′s countries applying for clinical trials of tumor vaccines
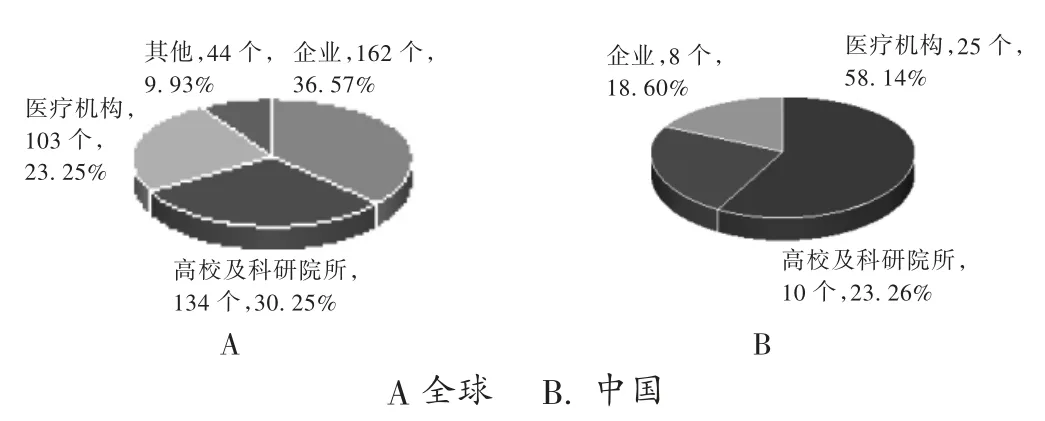
圖4 全球和中國腫瘤疫苗臨床試驗申辦者類型構成A.The whole world B.ChinaFig.4 Types and composition of the sponsors applying for clinical trials of tumor vaccines in the worldwide and China
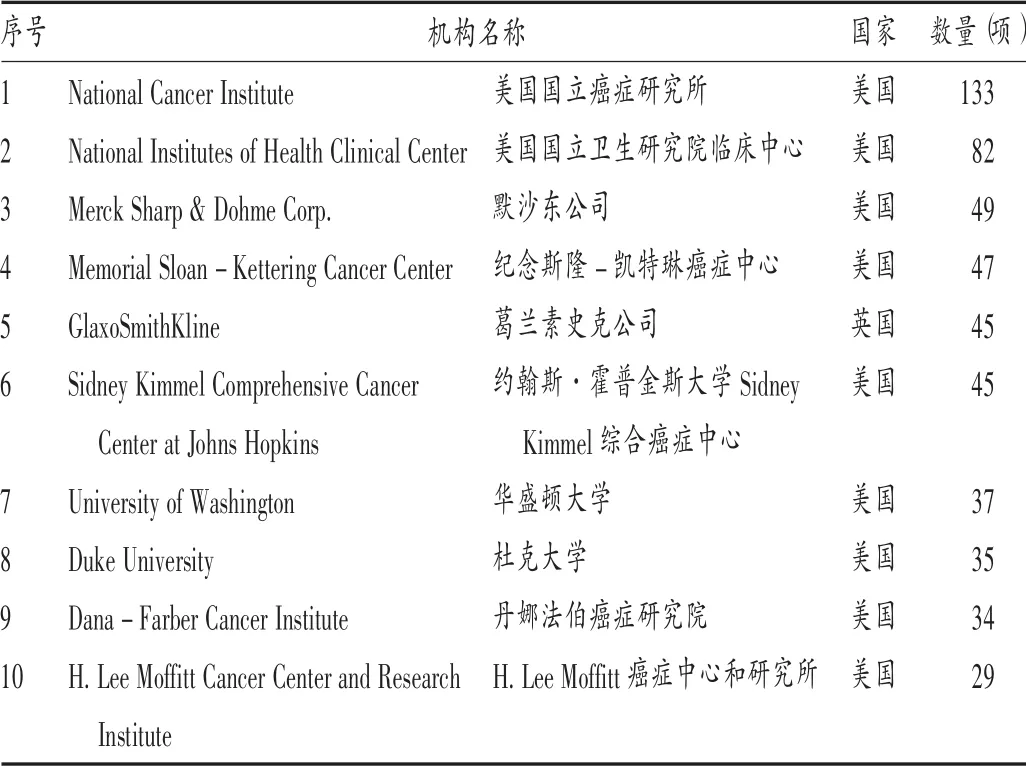
表1 全球腫瘤疫苗領域臨床試驗注冊數量排名前10的申辦者Tab.1 Top 10 sponsors in the worldwide in terms of the number of clinical trial registrations of tumor vaccines

表2 中國腫瘤疫苗領域臨床試驗的主要申辦者(注冊量≥3項)Tab.2 Main sponsors applying for clinical trials of tumor vaccines in China(number of registrations≥three items)
臨床試驗機構分布:臨床試驗機構是新藥各期臨床試驗的實施主體[12]。腫瘤疫苗領域臨床試驗機構數量排名前10的國家分別為美國、德國、法國、英國、西班牙、意大利、波蘭、加拿大、中國和俄羅斯,詳見圖5。其中,美國醫療機構2294個,中國醫療機構97個(包括中國臺灣的14個,中國香港的5個)。在全球腫瘤疫苗領域,臨床試驗注冊數量排名前10的臨床試驗機構均為美國的醫療機構,這些醫療機構不僅參與了相關臨床試驗的開展,在多中心臨床試驗中常為組長單位(牽頭單位)。其中,排名前5的分別為丹娜法伯癌癥研究院、紀念斯隆-凱特琳癌癥中心、MD安德森癌癥中心、美國國立衛生研究院臨床中心和梅奧醫學中心(見表3)。在中國腫瘤疫苗領域,表現突出的臨床試驗機構為廣州復大腫瘤醫院、江蘇省疾病預防控制中心、中國醫藥大學附設醫院(中國臺灣)、成功大學醫學院附設醫院(中國臺灣),詳見表4。
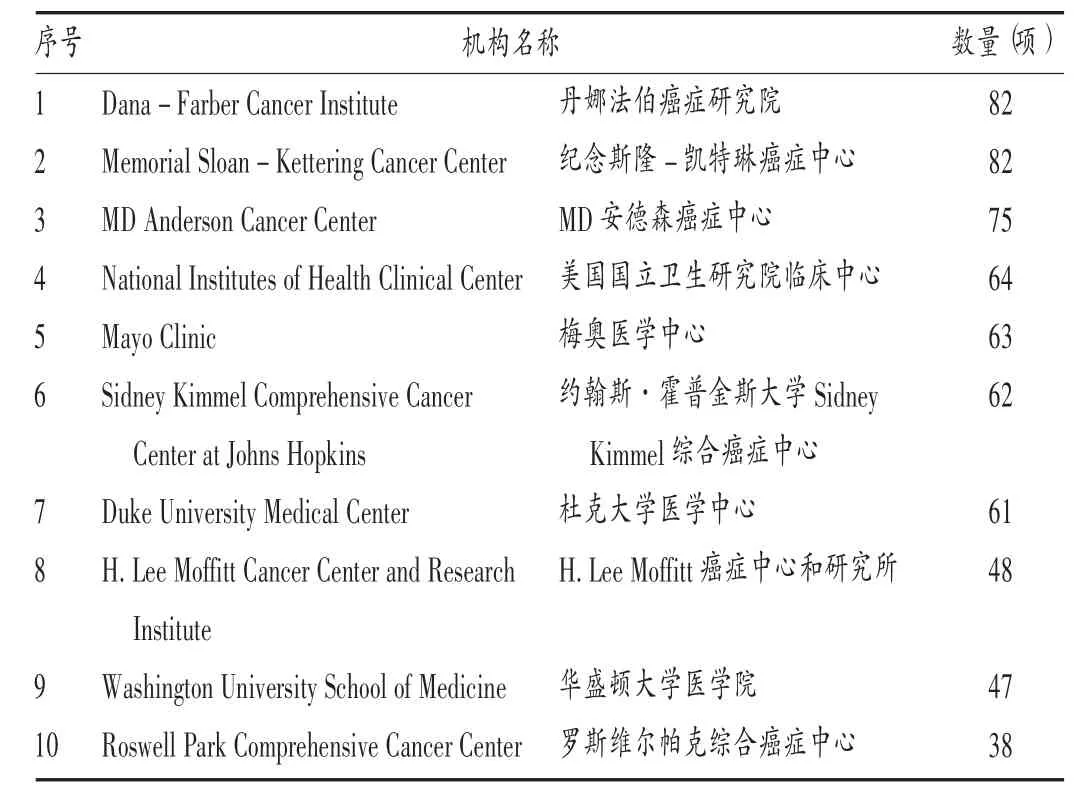
表3 全球腫瘤疫苗領域數量排名前10的臨床試驗機構Tab.3 Top 10 clinical trial institutions in the worldwide in the term of the number of tumor vaccines
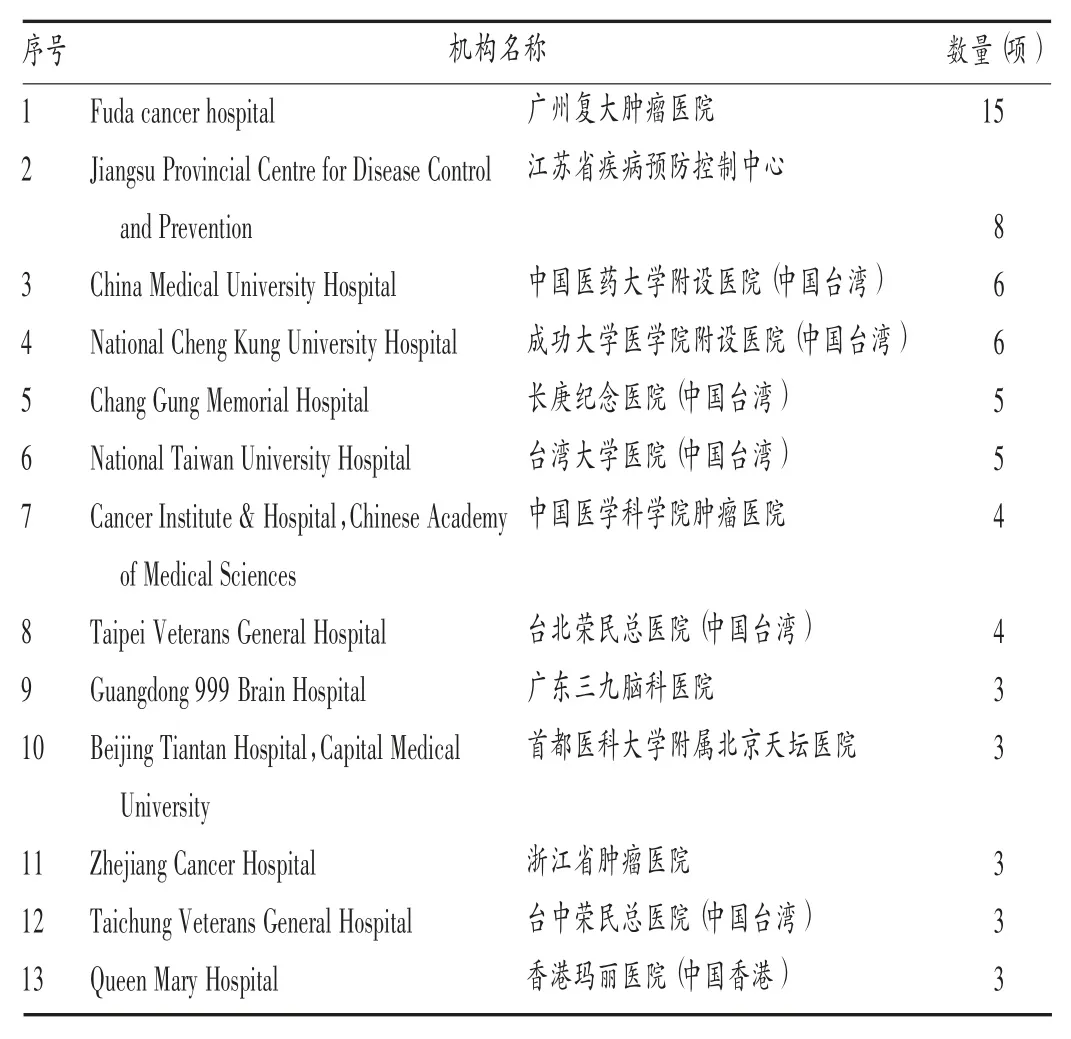
表4 中國腫瘤疫苗領域主要臨床試驗機構(注冊量≥3項)Tab.4 Main clinical trial institutions of tumor vaccines in China(number of registrations≥three items)
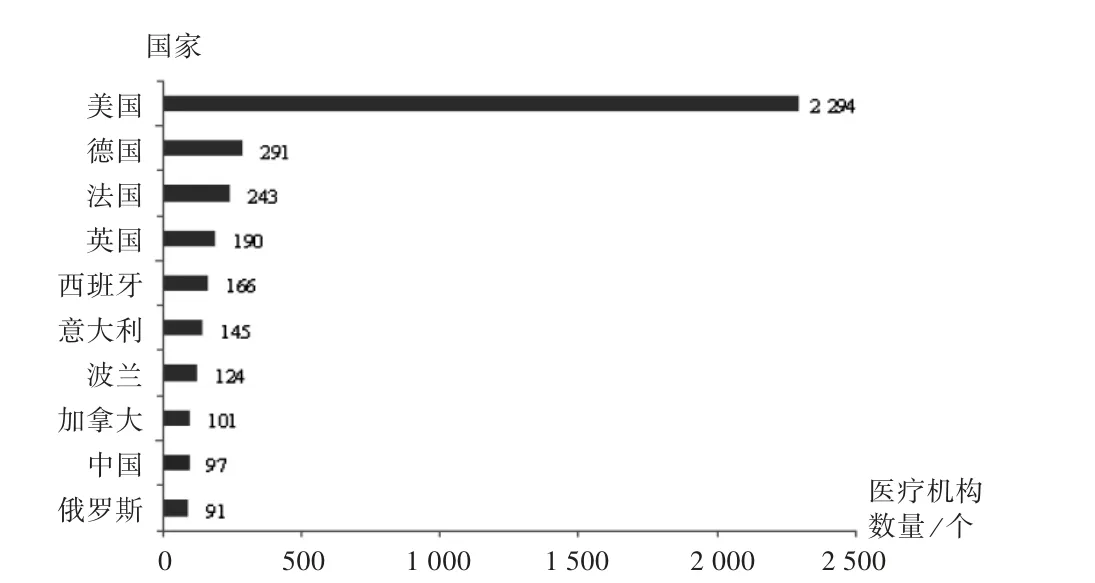
圖5 全球腫瘤疫苗領域臨床試驗醫療機構國家分布Fig.5 Distribution of countries of clinical trial institutions researching the tumor vaccines in the worldwide
2.3 臨床試驗注冊內容
研究類型與方法:按干預措施是否由研究者決定和分配,臨床研究可分為試驗性研究和觀察性研究[13]。全球腫瘤疫苗領域臨床試驗中,絕大多數為試驗性研究(1740項,98.19%);剩余32項臨床試驗中,30項為觀察性研究,2項為擴展訪問試驗,其具體研究類型及方法見表5。依據醫學研究證據分級,隨機對照研究(RCT)證據級別高[13-14],有552項;其次為隊列研究(cohort study)、病例對照研究(case control study),分別有20項和4項。與全球情況基本一致,中國腫瘤疫苗領域臨床試驗也以試驗性研究為主(98項,96.08%),余4項為觀察性研究(見表5)。其中,證據級別較高的RCT、隊列研究和病例對照研究分別有53,3,1項。
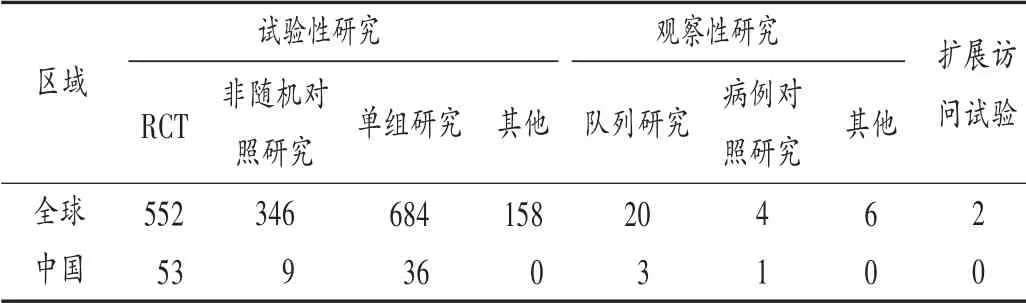
表5 全球和中國腫瘤疫苗臨床試驗研究類型及方法(項)Tab.5 Types and methods of clinical trials of tumor vaccines in the worldwide and China(item)
臨床試驗分期:全球腫瘤疫苗領域臨床試驗中,處于0期的有37項(2.09%),均與治療性腫瘤疫苗相關;處于Ⅰ期的有588項(33.18%),處于Ⅰ期/Ⅱ期或Ⅱ期的有877項(49.49%),以上兩部分臨床試驗大多數與治療性腫瘤疫苗相關,僅少部分與預防性腫瘤疫苗相關;進入Ⅱ期/Ⅲ期或Ⅲ期的有171項(9.65%),超過50%的與治療性腫瘤疫苗相關;進入Ⅳ期的有35項(1.98%),約90%與預防性腫瘤疫苗相關,詳見圖6。中國腫瘤疫苗領域臨床試驗中,處于0期的有1項,處于Ⅰ期的有27項(26.47%),處于Ⅰ期/Ⅱ期或Ⅱ期的有42項(41.18%);進入Ⅲ期的有24項(23.53%),進入Ⅳ期的有1項。以上臨床試驗中,有18項與預防性腫瘤疫苗相關,均處于Ⅲ期,評估不同廠家HPV疫苗的功效、免疫原性、安全性和免疫持久性;其余與治療性腫瘤疫苗相關。
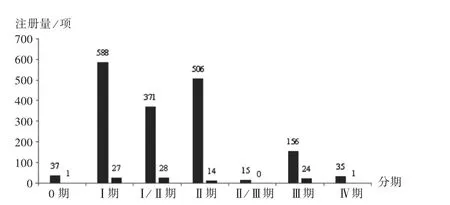
圖6 全球及中國腫瘤疫苗領域臨床試驗分期Fig.6 The phase of clinical trials of tumor vaccines in the worldwide and China
適應證:在全球腫瘤疫苗領域,臨床試驗注冊數量排名前10的腫瘤見圖7(由于有些臨床試驗有多個適應證,因此圖中數據存在重疊,圖8同),黑色素瘤有448項,淋巴瘤/白血病和乳腺癌/腫瘤均有347項。因疾病譜存在差異,中國腫瘤疫苗臨床試驗適應證與全球情況有所不同,中國腫瘤疫苗臨床試驗常見于宮頸上皮內瘤變(22項)、宮頸癌/腫瘤(18項)和膠質母細胞瘤/膠質瘤(15項),詳見圖8。
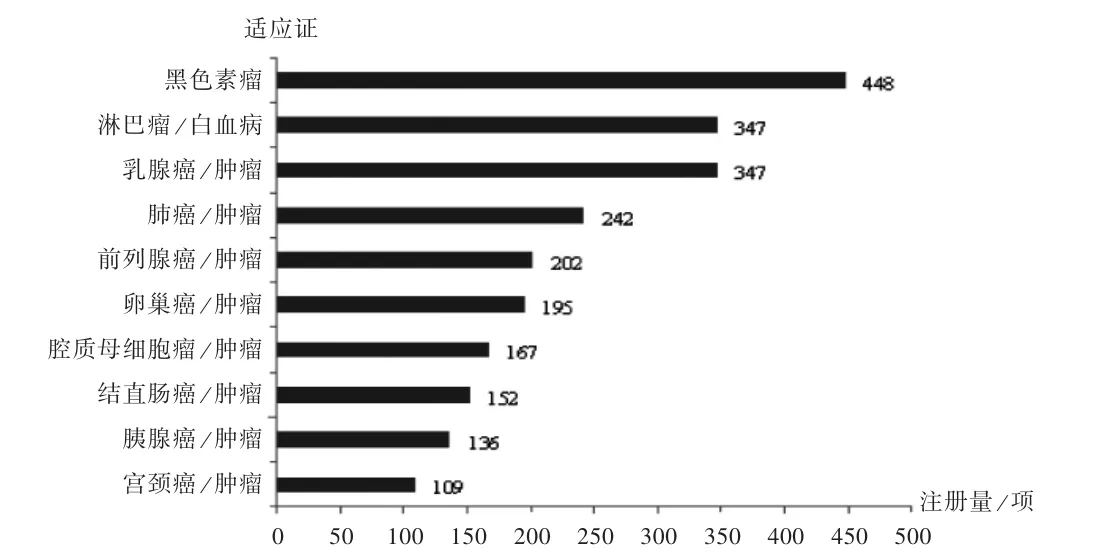
圖7 全球腫瘤疫苗領域臨床試驗注冊數量排名前10的適應證Fig.7 Top 10 indications of tumor vaccines in the terms of the number of clinical trial registrations in the worldwide
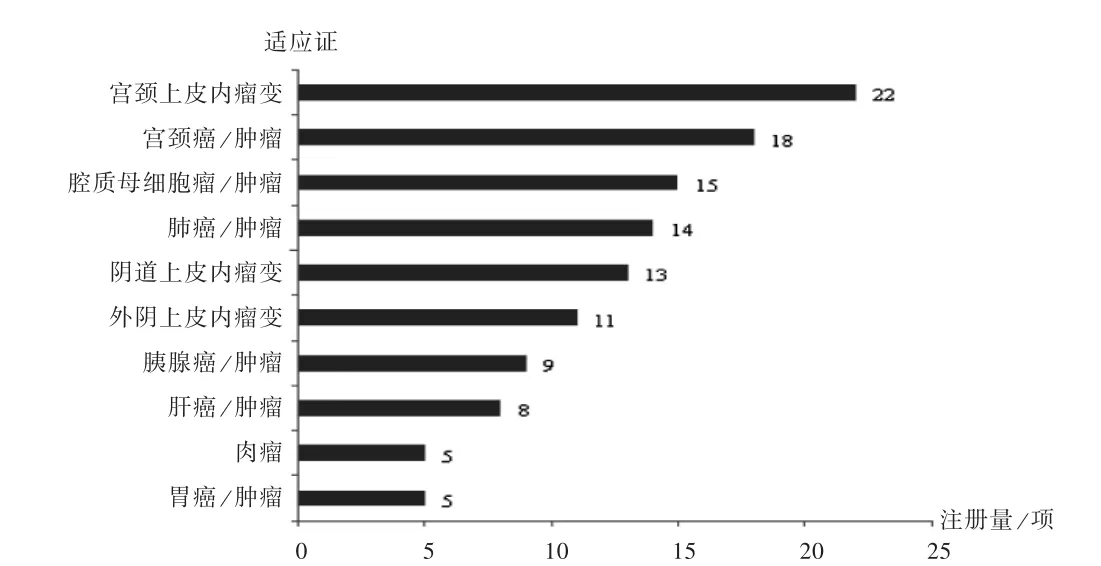
圖8 中國腫瘤疫苗領域臨床試驗注冊數量排名前10的適應證Fig.8 Top 10 indications of tumor vaccines in the terms of the number of clinical trial registrations in China
3 討論
1991年,Threrry Boon實驗室發現首個人類腫瘤特異性抗原(TSA)MAGE-1,被認為是腫瘤免疫學和腫瘤免疫治療學的“里程碑”[5]。經過20余年的積累,基礎研究不斷取得突破,推動腫瘤疫苗技術逐漸成熟。2010年4月,FDA批準Provenge(Sipuleucel-T)用于治療晚期前列腺癌,標志著該技術正式進入臨床應用[15]。本研究結果表明,基于新的技術路線或針對新適應證的腫瘤疫苗不斷進入臨床階段,相關臨床試驗集中開展于近10年。
臨床試驗注冊概況:1)國家分布。美國境內腫瘤疫苗領域臨床試驗最活躍,德國和中國較活躍。2)申辦者分布和構成。全球臨床試驗申辦者以企業、高校及科研院所為主,美國申辦者數量最多;中國臨床試驗申辦者超過50%為醫療機構。3)臨床試驗機構分布。全球腫瘤疫苗領域美國臨床試驗機構數量最多,臨床試驗注冊數量排名前20位的臨床試驗機構均為美國醫療機構,丹娜法伯癌癥研究所、紀念斯隆-凱特琳癌癥中心和MD安德森癌癥中心處于領先地位;中國開展腫瘤疫苗相關臨床試驗的醫療機構中,廣州復大腫瘤醫院、江蘇省疾病預防控制中心處于領先地位。
臨床試驗注冊內容:1)研究類型與方法。全球腫瘤疫苗領域臨床試驗幾乎全為實驗性研究,證據級別較高的RCT占31.15%;與全球情況相同,中國該領域臨床試驗也以實驗性研究為主,RCT占51.96%。2)臨床試驗分期。全球腫瘤疫苗領域臨床試驗大多處于臨床試驗Ⅰ期和Ⅱ期,離正式上市尚早,中國情況相同。3)適應證。全球腫瘤疫苗領域臨床試驗最常見的適應證為黑色素瘤、淋巴瘤/白血病、乳腺癌/腫瘤、肺癌/腫瘤、前列腺癌/腫瘤;因疾病譜存在差異,中國該領域臨床試驗適應證與全球情況有所不同,主要包括宮頸上皮內瘤變、宮頸癌/腫瘤、膠質母細胞瘤/膠質瘤。
腫瘤疫苗作為近年新興的一種免疫療法,臨床應用頻率落后于其他幾類免疫治療方法,同時在技術層面也面臨著挑戰。但總體而言,目前已有的絕大多數腫瘤疫苗的安全性和反應原性良好,隨著臨床標準的不斷完善和技術層面的突破,有望在未來成為腫瘤精準醫療大趨勢下的一類重要的腫瘤治療方式[16]。
本研究的局限性是所依據的臨床試驗數據集未能包含實際開展的所有腫瘤疫苗相關臨床試驗,原因為ClinicalTrials.gov僅為全球臨床試驗注冊數據平臺之一,且企業開展以產品上市為目的的臨床試驗可能未注冊,因此其注冊登記的臨床試驗數量少于實際開展的數量。但本研究對腫瘤疫苗領域的臨床轉化現狀進行了全面分析,對研究腫瘤疫苗的臨床應用、調整腫瘤疫苗的技術儲備及實現產業創新具有一定參考價值。

