小劑量帕利哌酮聯合經顱電刺激治療頑固性幻聽臨床觀察*
孫玉濤,盧秀春,劉彥彬
(河北省唐山市第五醫院,河北 唐山 063000)
精神分裂癥多伴認知功能損害[1-2],幻聽為其常見癥狀[3]。部分慢性精神分裂癥患者經治療后大部分癥狀可緩解,但殘留幻聽癥狀,對于頑固性幻聽需積極治療[4]。既往臨床常用經顱電刺激治療,該法屬無創性物理治療,通過對大腦相應功能區域的電信號刺激,產生大腦功能的興奮或抑制效應,從而發揮治療作用,但單用效果欠佳,難以根治,且易復發[5-6]。帕利哌酮對精神分裂癥有良好的治療作用[7]。本研究中探討了小劑量帕利哌酮聯合經顱電刺激治療頑固性幻聽的臨床療效,現報道如下。
1 資料與方法
1.1 一般資料
納入標準:符合《中國精神障礙分類與診斷標準(第三版)》(CCMD-3)中的診斷標準并確診[8];均伴有頑固性幻聽;年齡30~70歲;對經顱電刺激治療耐受;對帕利哌酮無禁忌證。本研究方案經醫院醫學倫理委員會批準,患者及其家屬簽署知情同意書。
排除標準:合并其他精神障礙性疾病;病歷資料不全;未嚴格執行本方案;妊娠期或哺乳期;肝腎功能不全;入組前已使用其他藥物治療。
病例選擇與分組:選取醫院2017年12月至2020年12月收治的頑固性幻聽患者120例,按治療方法的不同分為觀察組和對照組,各60例。兩組患者一般資料比較,差異無統計學意義(P>0.05),具有可比性。詳見表1。
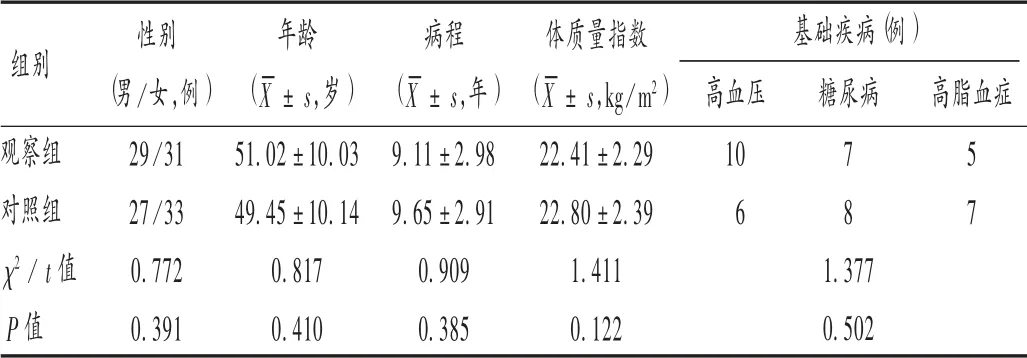
表1 兩組患者一般資料比較(n=60)Tab.1 Comparison of the patients′general data between the two groups(n=60)
1.2 方法
兩組患者均予YRD-10型經顱電刺激治療儀(北京依瑞德科技有限公司)行電刺激治療,選用8字型線圈,刺激患者左側前額葉外側皮質投射區域;治療參數設置:刺激頻率10 Hz、刺激強度80%~120%運動閾值,治療序列共30組,每個序列電刺激時間為5 s,間隔30 s,每日1次,每周治療5 d后休息2 d,觀察患者的耐受情況。觀察組患者每日晨加服帕利哌酮緩釋片(江蘇豪森藥業集團有限公司,國藥準字H20203265,規格為每片3 mg),每次1片。兩組均以4周為1個療程,連續治療3個療程。
1.3 觀察指標與療效判定標準
癥狀評分:以陽性癥狀和陰性癥狀量表(PANSS)、聽幻覺量表(AHRS)、社會功能缺陷量表(SDSS)評分評估癥狀改善情況。PANSS量表滿分為100分,分值越高表明精神癥狀越嚴重;AHRS量表滿分為30分,分值越高表明幻聽癥狀越嚴重;SDSS量表滿分為30分,分值越高表明社會功能缺陷越嚴重。
神經遞質水平:采集患者空腹靜脈血各約3 mL,抗凝,3000 r/min離心15 min,分離,得血清。采用imark 20型多功能酶標儀(美國BioTek公司),以酶聯免疫吸附法檢測患者血清的N-甲基天冬氨酸(NMDA)、5-羥色胺(5-HT)、多巴胺(DA)水平,檢測試劑盒均購自廣州達瑞生物科技公司,嚴格按試劑盒說明書操作。
神經電生理指標:采用DB1020型聽覺腦干誘發電位儀(丹麥Radiometer公司)檢測患者的P300,N2-P3,ERN水平。
療效判定[9]:顯效,幻聽癥狀消退,聽力恢復正常水平,AHRS評分降幅>80%;有效,幻聽癥狀、聽力水平均有顯著改善,AHRS評分降幅≥30%且≤80%;無效,幻聽癥狀、聽力水平和AHRS評分均無改善。總有效=顯效+有效。
安全性:觀察患者治療期間惡心嘔吐、腹瀉腹痛、肝功能異常、血壓異常等不良反應發生情況。
1.4 統計學處理
2 結果
結果見表2至表6。
表2 兩組患者各項癥狀評分比較(±s,分,n=60)Tab.2 Comparison of symptom scores between the two groups(±s,point,n=60)
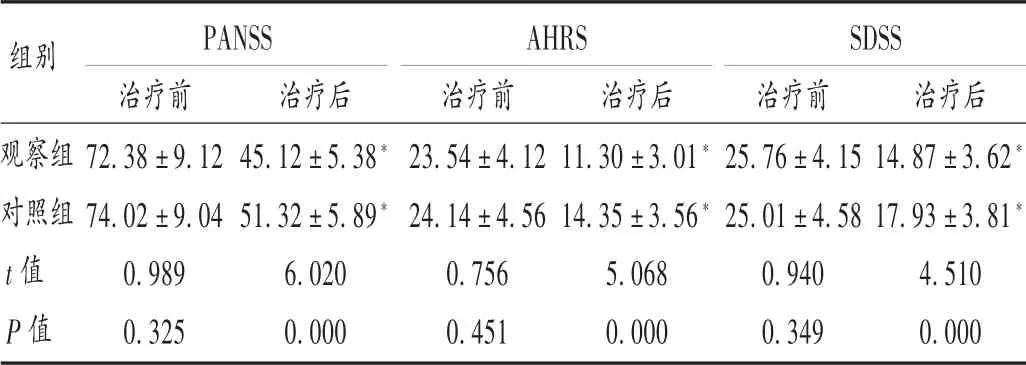
表2 兩組患者各項癥狀評分比較(±s,分,n=60)Tab.2 Comparison of symptom scores between the two groups(±s,point,n=60)
注:與本組治療前比較,*P<0.05。表3和表4同。Note:Compared with those before treatment,*P<0.05,as well as Tab.3 and Tab.4.
組別PANSS AHRS SDSS觀察組對照組t值 P值治療前72.38±9.1274.02±9.040.9890.325治療后45.12±5.38*51.32±5.89*6.0200.000治療前23.54±4.1224.14±4.560.7560.451治療后11.30±3.01*14.35±3.56*5.0680.000治療前25.76±4.1525.01±4.580.9400.349治療后14.87±3.62*17.93±3.81*4.5100.000
表3 兩組患者神經遞質水平比較(±s,n=60)Tab.3 Comparison of neurotransmitter levels between the two groups(±s,n=60)
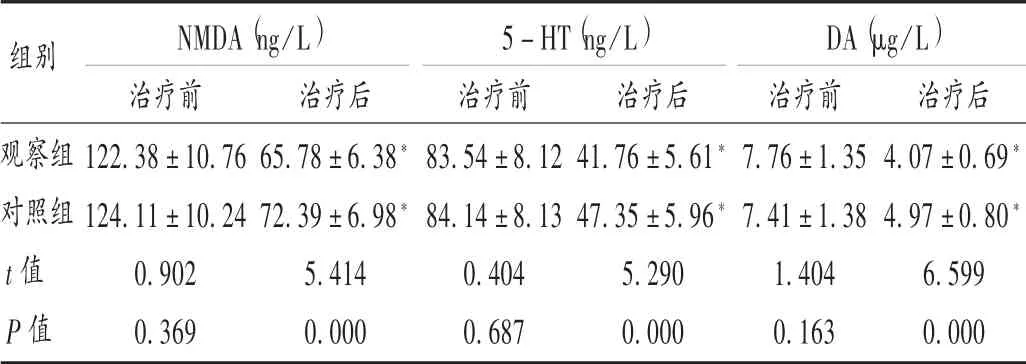
表3 兩組患者神經遞質水平比較(±s,n=60)Tab.3 Comparison of neurotransmitter levels between the two groups(±s,n=60)
組別NMDA(ng/L) 5-HT(ng/L) DA(μg/L)觀察組對照組t值 P值治療前122.38±10.76124.11±10.240.9020.369治療后65.78±6.38*72.39±6.98*5.4140.000治療前83.54±8.1284.14±8.130.4040.687治療后41.76±5.61*47.35±5.96*5.2900.000治療前7.76±1.357.41±1.381.4040.163治療后4.07±0.69*4.97±0.80*6.5990.000
表4 兩組患者神經電生理指標水平比較(±s,mV,n=60)Tab.4 Comparison of neuro electrophysiological indexes between the two groups(±s,mV,n=60)
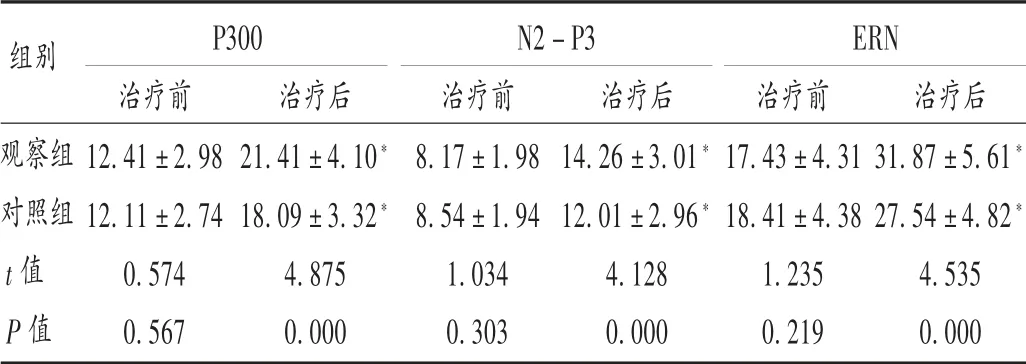
表4 兩組患者神經電生理指標水平比較(±s,mV,n=60)Tab.4 Comparison of neuro electrophysiological indexes between the two groups(±s,mV,n=60)
組別P300 N2-P3 ERN觀察組對照組t值 P值治療前12.41±2.9812.11±2.740.5740.567治療后21.41±4.10*18.09±3.32*4.8750.000治療前8.17±1.988.54±1.941.0340.303治療后14.26±3.01*12.01±2.96*4.1280.000治療前17.43±4.3118.41±4.381.2350.219治療后31.87±5.61*27.54±4.82*4.5350.000
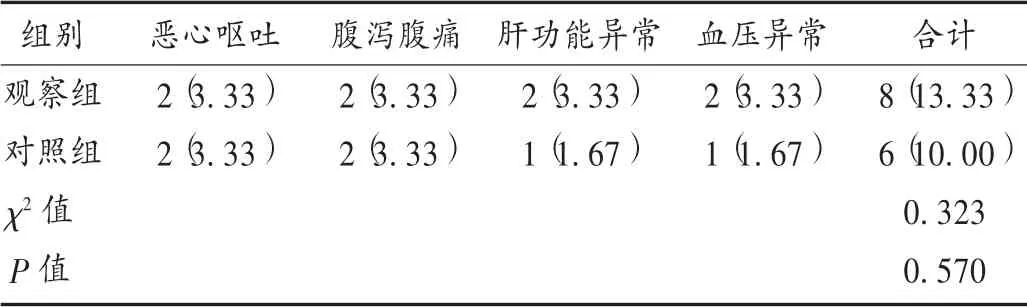
表6 兩組患者不良反應發生情況比較[例(%),n=60]Tab.6 Comparison of incidence of adverse reactions between the two groups[case(%),n=60]
3 討論
幻聽是重性精神分裂癥的常見癥狀,在精神科臨床最常見,可作為臨床診斷、判斷精神分裂癥嚴重程度及療效的重要依據,患者的行為能力和生活質量均受到嚴重影響,應給予積極、有效的干預[10]。臨床既往治療頑固性幻聽多是從精神分裂癥的角度進行干預。經顱電刺激是目前臨床常用的一種物理治療手段,通過對患者顱腦部位給予低頻脈沖電流刺激,電流在線圈中產生磁場,電刺激信號作用于患者大腦的相應功能區域,對大腦功能產生興奮或抑制效應,從而改善神經功能細胞的紊亂狀態,但經顱電刺激難以根治頑固性幻聽,并易復發[11],仍需聯合其他治療方案以進一步提高療效。

表5 兩組患者臨床療效比較[例(%),n=60]Tab.5 Comparison of clinical efficacy between the two groups[case(%),n=60]
帕利哌酮為新型抗精神分裂癥藥物,是利培酮的活性代謝產物,治療作用良好。本研究結果顯示,觀察組相比于對照組的臨床療效有明顯提升,表明小劑量帕利哌酮對于頑固性幻聽有良好的治療效果;觀察組患者的PANSS,AHRS,SDSS等癥狀評分均明顯低于對照組,表明小劑量帕利哌酮的應用能改善患者的精神分裂癥癥狀,降低幻聽癥狀程度,進而改善患者的社交功能障礙。帕利哌酮通過拮抗機體的5-HT3受體和DA2受體,阻斷突觸前膜對5-HT的再攝取,延長和增強5-HT的作用[12-13]。另外,帕利哌酮對腎上腺素受體和組胺受體均有一定的阻斷作用,可進一步增強對精神分裂癥的治療效果[14]。頑固性幻聽的發生表明患者的精神分裂癥癥狀加重,伴隨著多種精神活動相關的神經遞質(包括NMDA,5-HT,DA)水平的異常改變[15]。本研究結果顯示,觀察組患者治療后的NMDA,5-HT,DA水平均低于對照組,表明帕利哌酮的應用能糾正患者神經遞質水平的異常升高,從分子生物學角度證實了帕利哌酮對頑固性幻聽的良好治療作用。此外,頑固性幻聽患者在病情進展過程中伴隨著神經電生理活動的異常。本研究結果顯示,觀察組患者治療后的神經電生理指標水平明顯高于對照組,從電生理角度證實了聯合治療方案對頑固性幻聽的良好效果[16]。且觀察組加用小劑量帕利哌酮后,患者的不良反應未明顯增加。
綜上所述,小劑量帕利哌酮聯合經顱電刺激治療頑固性幻聽可明顯改善患者的癥狀評分、神經遞質水平和神經電生理指標。

