基于整合藥理學策略的黃芪-丹參抗心肌梗死作用機制研究?
劉志超,陳金紅,高晟瑋,馬 莉,王治中 ,陸安民,王保和,谷旭放△
(1.天津中醫藥大學,天津 300193;2.天津中醫藥大學第二附屬醫院,天津 300150)
隨著2018年《心肌梗死全球定義(第四版)》指南的修訂和發布,急性心肌梗死的診斷與治療更加明確[1]。亞洲地區各國的研究也表明,早期出現癥狀與使用藥物介入治療的死亡率低于直接介入治療的死亡率有關[2,3],而國內則呈現快速增長態勢[4]。抗栓治療是貫穿整個急性心肌梗死臨床治療的方案,包括經皮冠狀動脈介入治療(percutaneous coronary intervention,PCI)術后,患者需要長期服用抗血小板、穩定斑塊治療[5]。盡管指南中指出,以抗栓治療為主,但存在一定風險,包括出血事件、消化系統不良反應。因而課題組致力于探索出一種新的治療策略,通過中醫藥的輔助治療起到“增效減毒”作用。
急性心肌梗死根據其癥狀、證候表現,屬于中醫學“胸痹”“真心痛”范疇,最早可追溯至《黃帝內經》中有所記載。現代中醫專家對急性心肌梗死的證候演變規律進行總結并達成共識,即氣虛、血瘀、痰濁為常見病因病機,證候組合中,以氣虛血瘀證為主[6]。黃芪-丹參是中醫臨床益氣活血常用藥對,現代藥理學研究也表明[7],黃芪-丹參配伍提取物在缺血性心肌中能夠有效延緩心肌重塑的進展。
本研究初步對黃芪-丹參組合的相互作用以及對急性心肌梗死的治療作用進行分子機制預測性挖掘,建立可信度較高的研究體系,從分子層面篩選丹參黃芪配伍抗心肌梗死氣虛血瘀證的關鍵活性成分及靶點,為課題后續研究把握較為精準的方向。
1 數據庫建立與研究方法
1.1 數據庫建立
利用整合藥理學平臺[8](http://www.tcmip.cn /)的中藥成分數據庫、證候相關分子挖掘,結合2015年版《中國藥典》中規范藥材命名及成分名稱,進行虛擬數據資料建庫。檢索“黃芪”“丹參”主要生物活性成分,自主命名數據作為備用。
1.2 藥物靶標預測
利用TCMIP通過提取黃芪-丹參藥物成分的化學分子指紋,并將其與Drug Bank(https://www.drugbank.ca/)數據庫中獲美國食品藥品監督管理局(food and drug administration,FDA)批準的抗冠心病心肌梗死藥物指紋進行比對,平臺利用Tanimoto系數對結果進行評分,選定評分>0.8的為相似性藥物,將相似性藥物靶點作為黃芪-丹參藥物組合的潛在機制靶點[9]。
1.3 疾病、證候靶標確定
以“myocardial infarction”作為疾病關鍵詞,在GeneCard(https://www.genecards.org/)數據庫、TTD數據庫(http://bidd.nus.edu.sg/BIDD-Databases/TTD/TTD.asp)、DrugBank數據庫(https://www.drugbank.ca/)、OMIM數據庫(https://omim.org/)、DIGSEE數據庫(http://210.107.182.61/geneSearch/)中進行檢索全疾病相關靶標,利用Uniprot數據庫(https://www.uniprot.org/uniprot/)轉換蛋白名稱,獲取基因名稱。最終利用Microsoft Office Excel文本進行去重,整理疾病靶標,建立疾病數據庫。
再以“myocardial infarction”作為疾病關鍵詞錄入整合藥理學平臺疾病/證候靶標數據庫中進行檢索,證素[10]輸入心胸刺痛、胸部悶滯,動則加重,伴乏力、短氣、汗出等進行關鍵詞檢索,提取相應證候靶點信息。
1.4 PPI網絡構建、分析與可視化
通過整合藥理學平臺的網絡分析模塊蛋白互相作用網絡進行拓撲分析,以“節點連接度”的2倍中位數為卡值,選取中藥靶點-疾病基因的關鍵節點(hubs);在此基礎上,以“節點連接度”(degree)“節點緊密度”(closeness)“節點介度”(betweenness)的中位數為截取值,選取同時滿足3個卡值的節點為黃芪-丹參的潛在靶點,然后對關鍵靶標網絡進行通路富集分析,選取統計值P值排名前20的通路,構建完整的“中藥-活性成分-核心靶標-關鍵通路”多層次關聯網絡,并進行可視化數據分析。采用TCMIP構建黃芪-丹參最密切關鍵靶點的PPI網絡;通過TCMIP分析平臺對關鍵靶基因進行GO功能富集分析和KEGG富集分析,利用Jvenn(http://www.bioinformatics.com.cn/static/others/jvenn/example.html)在線繪圖[11]獲取韋恩圖。
2 結果
2.1 黃芪-丹參成分靶標預測及分析
通過TCMIPV2.0平臺對黃芪、丹參化學成分的分析結果可知,黃芪共收集了27個化學成分,包括黃芪甲苷(astragaloside IV,AS-IV)、黃芪多糖(astragalus polysaccharides,APS)、異黃芪皂苷等,其中潛在靶標數量為218個。丹參共收集96個化學成分,主要為丹參素、丹酚酸B、丹酚酸A、丹參酮Ⅰ、隱丹參酮、丹參酮ⅡA等,其中潛在靶標數量151個。
對黃芪、丹參后選靶標進行基因功能分析和通路富集分析發現,其功能多與類固醇激素介導的信號通路、離子跨膜轉運、神經系統過程通路、細胞內受體信號通路、氨基丁酸信號通路、γ-氨基丁酸信號通路(γ-aminobutyric acid,GABA)、膜電位調節、氧化還原過程通路等相關。這些候選靶標參與通路的信息發現主要在神經遞質的調節、心肌能量代謝、脂類代謝等通路。
2.2 心肌梗死疾病靶標及相關基因
研究者對全疾病相關潛在靶標合并去重后共計1062個,其中與黃芪-丹參藥對組合密切相關的共同靶向基因共計49個,如韋恩圖(見圖1)。這些靶點的作用機制主要從調控炎性因子(白介素-2、白介素-6、白介素-8)[12]、凝血因子-2(Recombinant Coagulation Factor II,F2)[13]、基質金屬肽酶[14]、過氧化物酶體增殖物激活受體γ(peroxisome proliferative activated receptor gamma,PPARG)[15]、腫瘤壞死因子[16]、磷脂酰肌醇-4-磷酸3-激酶催化亞單位2型α[17]、eNOS[18]、血管內皮生長因子[19]、前列腺素內過氧化物合酶[20]、細胞凋亡蛋白酶[21]、前列腺素內過氧化物合酶[22]等共同作用下發揮作用。

圖1 心肌梗死疾病靶標及相關基因韋恩圖
2.3 心肌梗死氣虛血瘀證素靶標
根據中醫學對氣虛血瘀證的描述,劃分證素包括胸悶、胸痛、乏力、短氣、汗出、舌紫暗、脈虛無力等。其中血瘀證素(胸悶胸痛)包含159個相關靶標,氣虛證素(乏力短氣、汗出)包含143個相關靶標。
2.4 黃芪-丹參抗心肌梗死候選基因的GO富集分析
表1示,通過對黃芪-丹參-心肌梗死候選靶標進行基因功能分析和通路富集分析,羅列出候選作用靶標(P值前20的)所具有的功能。由此可見,黃芪-丹參候選靶標參與的通路,主要涉及在細胞增殖的負調節、細胞凋亡過程的負調控、細胞介導因子、DNA轉錄、基因表達調控等多方面。

表1 黃芪-丹參抗心肌梗死的候選基因的GO富集分析
2.5 黃芪-丹參抗心肌梗死核心靶標的KEGG富集分析
黃芪-丹參抗心肌梗死關鍵網絡靶標的KEGG通路富集分析結果(見表2),靶標主要涉及白介素、腫瘤域突變體、卵巢腫瘤結構域蛋白酶、eNOS、TGF-β受體信號傳導激活Sma和Mad相關蛋白(Sma -and Mad -related protein,Smad)通路、激酶非活性BRAF對加速纖維肉瘤蛋白(rapidly accelerated fibrosarcoma,RAF)信號的異常激活等角度。

表2 黃芪-丹參抗心肌梗死核心靶標的KEGG富集分析
2.6 黃芪-丹參抗心肌梗死的“中藥-成分-靶點-通路”多維網絡分析
圖2示,基于黃芪-丹參藥靶與心肌梗死靶標的PPI 網絡信息,進行構建黃芪-丹參治抗心肌梗死的“中藥-成分-靶標-通路”多維網絡圖,不同顏色的節點是按照基因間相互作用的緊密度進行聚類。圖2可直觀看出,黃芪-丹參藥對通過中藥材的多成分,從而達到多途徑、多層次、多靶點、多環節的抗心肌梗死作用,能有效預測到中藥、證素、疾病、靶點之間可能存在的聯系,此外復雜的網絡圖也間接反映出藥物之間相互作用的復雜程度。黃芪-丹參藥對組合共包含123個化學成分,潛在靶標369個,這些成分通過聯合調控白介素、腫瘤域突變體、卵巢腫瘤結構域蛋白酶、eNOS、TGF-β、激酶非活性BRAF等靶標,直接或間接參與炎癥信號通路、雌激素信號通路、SMAD通路、RAF信號的異常激活、調控基因的轉錄等作用。
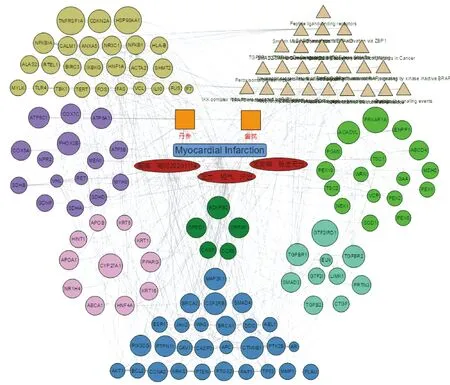
圖2 黃芪-丹參抗心肌梗死的“中藥-成分-靶點-通路”多維網絡分析
3 討論
闡明中醫證候的本質,一直是中醫學者們力求解決的科學問題之一。中醫證候往往被拆解為多個證素進行深入挖掘,即按照證候表現將證素劃分到某一西醫疾病范疇內,然后再進行分子量級的基礎實驗研究,研究本身具有科學意義,但研究成果與中醫的聯系往往較牽強附會。此外,天然藥物的成分較為復雜,成分之間的協同/拮抗作用尚未完全闡明,因而以單體活性成分代替生藥進行生物學研究欠為妥當。整合藥理學結合中藥成分、證候要素、疾病靶點的多層次研究,從藥物自身出發,能夠較為完善地完成中藥-證素-疾病-靶標-通路的銜接性研究,形成中醫藥現代研發體系,從分子角度解釋中醫療效內涵。
本研究旨在探討中藥抗心肌梗死氣虛血瘀證證候本質,完善現有證據,并提出新的中醫證候本質研究策略。目前國內諸多團隊都在進行這一工作,其中韓晶巖教授團隊對此進行了深入研究[23],對芪參益氣滴丸通過心肌能量代謝途徑、心肌線粒體復合物及其亞單位、調控線粒體復合物去乙酰化酶-1、小G蛋白家族的Ras同系物家族成員A(ras homolog family member A,RhoA)/Rho相關卷曲螺旋蛋白激酶-1(rho-associated coiled-coil kinases1,ROCK1)、細胞骨架、心肌結構、心功能、心臟微循環動態等綜合研究,部分闡明了心氣虛血瘀的科學內涵,揭示了補氣活血的作用機理,及其主要成分協同作用的機理,支撐了益氣活血藥物在治療心肌缺血再灌注損傷和心肌肥厚方面的應用。
本研究借助智能化數據挖掘平臺TCMIP v2.0和國際通用靶標、基因數據庫,對益氣活血藥對黃芪-丹參的藥物候選靶標與疾病進行關聯,并以網絡可視化形式展現出來,預測其可能靶標和分子信號通路。分析結果表明,黃芪-丹參能夠聯合調控炎性因子、信號通路、調節能量代謝、調控基因轉錄。此外,多維網絡分析顯示,黃芪-丹參潛在靶標與炎癥靶標的共同生物進程調控細胞周期蛋白依賴性激酶抑制劑(cyclin-dependent kinase inhibitor,CDKN)轉錄與其心梗機制密切相關,在乏力、短氣證素表現中也較為明顯。該通路的支持文獻表明,細胞周期蛋白依賴性激酶抑制劑對冠心病的易感性也有一定影響[24],用模仿CDKN2A /2B基因作用的藥物進行治療可能是一種延緩動脈粥樣硬化的有前途療法[25]。此課題將繼續深入開展對該通路的動物、細胞實驗,以期對心肌梗死氣虛血瘀證的進一步揭示。

