兩種類型的雙向性室速1例
甘云鳳 劉杰
患者女,81歲,因“腹痛3 d,暈厥1次”于2019年7月12日就診于我院急診科,有高血壓病史10年,平時以“利血平”控制血壓。急診查體:體溫36.2 ℃,心率111次/min,呼吸23次/min,血壓117/82 mmHg,神清,心界不大,劍突下輕壓痛。實驗室檢查結果顯示:氨基末端腦鈉肽前體3 466.04 pg/mL,心肌肌鈣蛋白I(cTnI)>50 ng/mL(正常范圍0~0.5 ng/mL),肌酸激酶同工酶45.7 ng/mL(正常范圍0~5 ng/mL),肌紅蛋白147.85 ng/mL(正常范圍0~50 ng/mL),超敏C反應蛋白輕度增高。電解質正常。急診心電圖(圖1)由心電圖醫師初診如下:① 竇性心動過速;② 頻發室性早搏;③ 急性前壁心肌梗死。臨床擬診急性心肌梗死隨即收入我院心內科,予以急診冠脈造影,造影結果顯示冠脈均衡型,左主干極短,前降支血管光滑未見明顯狹窄,TIMI 3級;回旋支血管光滑未見明顯狹窄,TIMI 3級;右冠血管光滑未見明顯狹窄,TIMI 3級。冠脈造影后復查心電圖(圖2)顯示:寬QRS波心動過速,aVF導聯出現竇性P波(圖2中箭頭所示),部分P波考慮埋藏于QRS波群和T波中,提示房室分離,Ⅱ、Ⅲ、aVL、aVF導聯的QRS波方向呈上下交替變化,心電軸呈無人區電軸(圖2中虛線框C組波形所示)、右偏電軸(圖2中虛線框B組波形所示)交替變化,V1導聯均呈Qr型,診斷為雙向性室速。
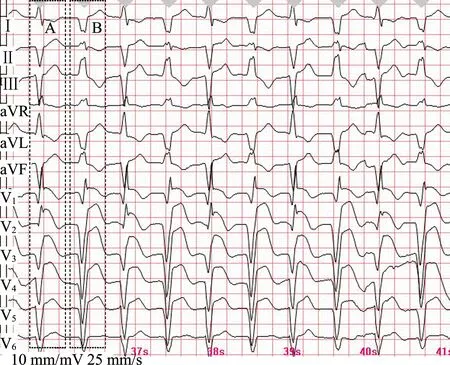
寬QRS波心動過速,未見明顯P波,部分肢體導聯主波方向上下變化,心電軸呈交替左偏(虛線框A組波形)與右偏(虛線框B組波形),胸導聯電軸左偏波形在V1、V2導聯呈qr型,電軸右偏波形在V1導聯呈qr型,應診斷為雙向性室速。
患者入院當天23:00左右(冠脈造影術后約9 h),突然出現心悸、全身濕冷伴血壓下降至82/50 mmHg、心率下降至35~40次/min,呈室性逸搏心律(圖3)。當班醫師立即予多巴胺升壓治療,查肌紅蛋白進一步增高,高敏肌鈣蛋白T:7 155 pg/mL(顯著增高)。床旁心臟彩超示:左房稍增大(左房內徑37 mm),左室舒張末期內徑37 mm,左室后壁厚度9 mm,射血分數61%,室間隔增厚(厚度13 mm),主動脈動度降低,左室舒張功能減弱(二尖瓣舒張期血流頻譜E/A<1)。腹部彩超未見特殊異常。患者血流動力學改變、心室率緩慢,予以植入臨時心臟起搏器。臨床修正診斷為重癥心肌炎,予以營養心肌、加用糖皮質激素抗炎、大劑量維生素C抗氧化等治療。患者病情好轉,予以拔除臨時心臟起搏器,出院2 d后(7月14日)隨訪心電圖示竇性心律、左前分支阻滯(圖4)。
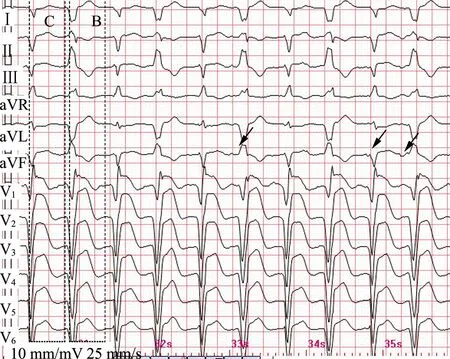
心電圖仍呈寬QRS波心動過速,診斷為雙向性室速。
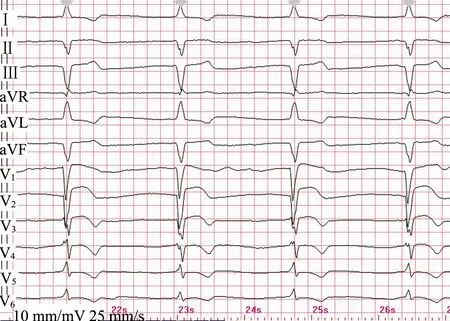
圖3 突發心悸時室性逸搏心律心電圖
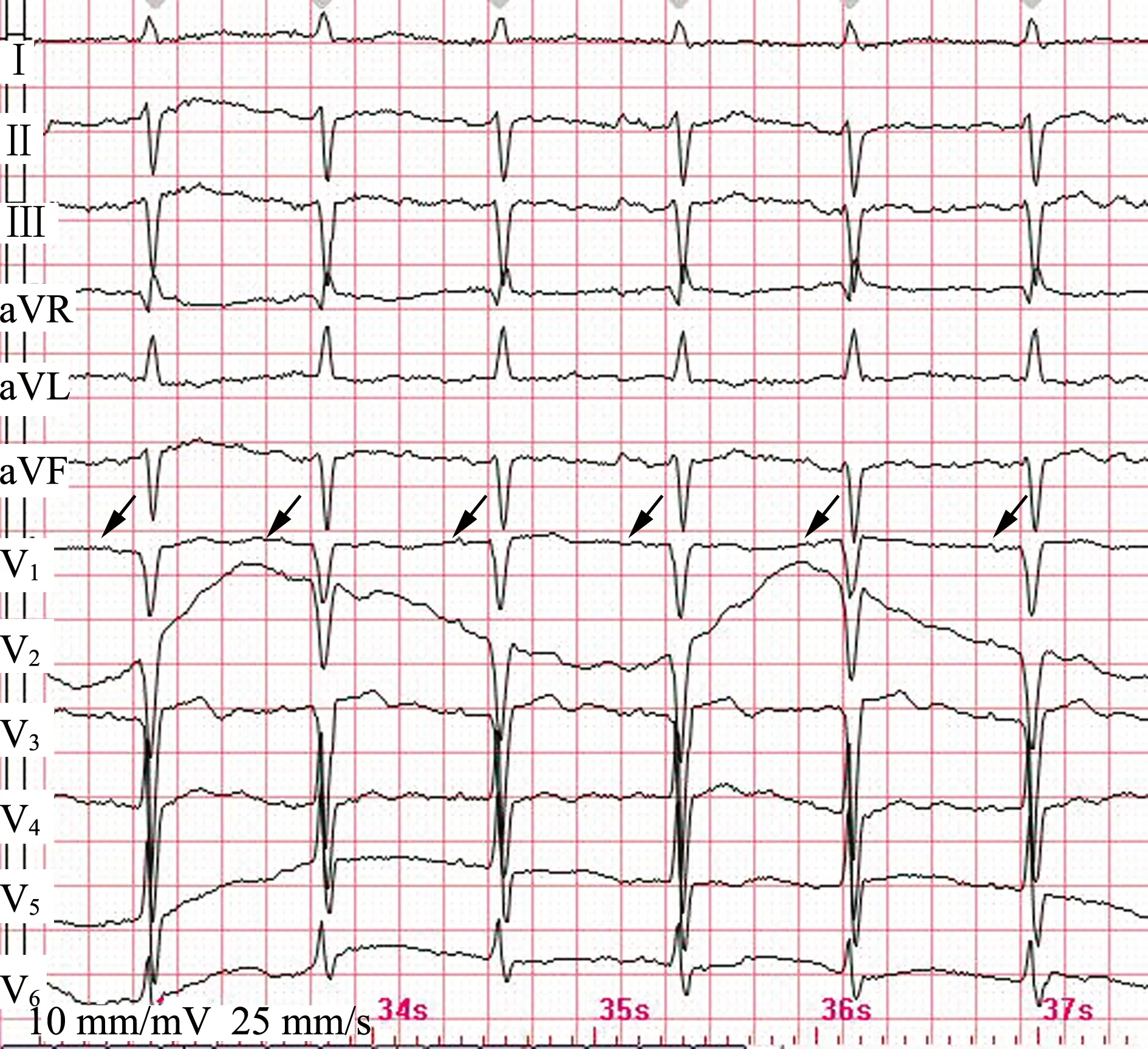
心電圖診斷:① 竇性心律(箭頭處為P波);② 左前分支阻滯;③ 前間壁異常Q波;④ T波改變。
討論雙向性室速是一種罕見且嚴重的心律失常,1922年Schwensen[1]首次報道了1例因洋地黃中毒引起的雙向性室速。雙向性室速的特征性心電圖表現[2]主要有以下幾點:① 同一肢體導聯兩種形態的QRS波形交替出現(可見正常寬度或寬大的QRS波呈上下交替);② 胸導聯通常表現為左束支和右束支阻滯樣形態交替變化;③ 心室率多為140~180次/min,RR間期整齊或長短交替;④ 發作時間通常是短暫的或非持續性的,有時僅僅持續數分鐘或數秒鐘,而且可以自行終止或反復發作;⑤ V1導聯可以呈QS型或R型。本例圖1-2中無明顯P波或未見與QRS波有順傳關系的P波,QRS波寬大畸形,RR間期相對規則;在圖1中肢體導聯Ⅰ、Ⅱ、Ⅲ、aVL、aVF以及圖2中肢體導聯Ⅱ、Ⅲ、aVL、aVF的QRS波方向呈上下交替變化,符合雙向性室速的診斷。雙向性室速需要注意與竇性心律伴室性早搏或室性早搏二聯律進行鑒別(本例圖1最初被診斷為竇性心動過速伴頻發室性早搏,正是因為沒有仔細尋找P波痕跡、總結P波規律)。二者的鑒別要點如下:① 尋找是否有P波,PR間期是否相等,即P波與QRS波是否有順傳關系;② 是否有竇性下傳波形,并與之對比。本例患者恢復竇性節律時(圖4)雖然電軸與圖1中A種波形都呈電軸左偏,但竇性下傳時可以看到規律的PR間期,QRS波寬度正常,胸導聯V1、V2呈QS型,而圖1中A種波形胸導聯為qr型與竇性下傳波形不一致,所以更支持A種波形為室性搏動。雙向性室速的病因不同,如兒茶酚胺敏感性室速的特征性心電圖表現之一就是雙向性室速,其為遺傳性鈣離子通道疾病,與RyR2和CASQ2基因突變有關[3]。在沒有遺傳性離子通道疾病的情況下,雙向性室速的機制尚不明確,對此Baher等[4]提出“乒乓機制”,認為可能存在兩個或多個不同觸發閾值的心室異位灶,在試驗中,當心率超過1個異位點的閾值時,在正常竇性搏動動作電位后激發一次延遲后除極,引起室性早搏,呈室性早搏二聯律,同時引起心率增快;達到第2個異位點閾值時,觸發該部位延遲后除極并產生室性異位搏動,兩個位點交替發放沖動,形成雙向性室速;若多個部位激動,則可誘發多形性室速。本例患者急性起病,出現惡性室性心律失常、心力衰竭、心源性休克,根據歐洲心臟病學會心肌病和心包疾病工作組的意見,當不能用非炎癥性心肌病或冠心病等其他疾病解釋時,應該考慮心肌炎[5]。心肌炎的特征組織學改變為炎癥細胞在心肌間質內浸潤,伴有心肌細胞變性、壞死,特別是在心肌炎急性期伴有大量炎癥細胞浸潤[6]。有研究顯示,心肌炎的急性期更容易發生多形性室速,而在恢復期則多為單源性室性心律失常[7],說明室性心律失常和炎癥介質及心肌細胞損傷程度相關。結合以上資料,筆者推測,本例雙向性室速的機制可能為炎癥細胞浸潤,導致局部心肌細胞自律性增加并達到閾值,從而產生動作電位。兩個局部異位搏動點分別位于左后分支處(圖1 A組波形)與左前分支處(圖1 B組波形)時,可出現圖1所示的類右束支阻滯圖形伴電軸左右交替;第3個異位搏動點(圖2中C組波形)可能位于主動脈瓣與二尖瓣環連接部(有資料顯示V1導聯qR型還經常見于主動脈瓣與二尖瓣環連接部)[8],C組與B組波形位點交替發放沖動,則可出現圖2中的雙向性室速。
雙向性室速臨床上很少見,若發展為多形性室速或心室顫動,則病死率很高,治療上需要考慮到基礎疾病及病因。本例患者考慮為重癥心肌炎,其出現心源性休克后我們立即予以多巴胺升壓,及時加用糖皮質激素,大量維生素C抗氧化、輔酶Q營養心肌等治療,在心室率顯著緩慢的情況下植入臨時心臟起搏器,該患者預后較好。

