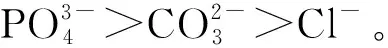磁性納米復合材料Fe3O4@UiO-66-NO2的合成及其吸附性能研究
李石雄,楊少龍,唐艷瑩,龍詩茵,陳瑜歡,李賢就
(1.梧州學院 機械與資源工程學院,廣西 梧州 543002;2.廣西大學 化學與化工學院,廣西 南寧 530004)
隨著我國紡織印染業的迅速發展,染料廢水的排放急劇增加[1-3]。亞甲基藍(MB)作為一種典型的污染物逐漸成為現階段染料廢水治理的重點[4-6]。目前常用的廢水處理方法有吸附法、沉淀法、膜分離法、電化學法、光降解催化法、微生物處理法等[7-13]。與其他方法相比,吸附法具有操作簡單、成本低、不產生二次污染等優點。
金屬有機骨架材料(MOFs)是一類新型的材料,由剛性有機連接金屬簇組成具有網絡結構的多孔骨架材料。與傳統的多孔材料相比,MOFs具有比表面積較大、孔隙率高、結構多樣且可調的特點[14],因此廣泛地應用在催化、傳感、吸附、生物醫學等領域[15-20]。UiO-66-NO2是Zr-MOFs中的一種新型多孔材料,具有比表面積大、孔隙率高、熱穩定性和化學穩定性良好等優點[21-24]。磁性納米復合材料因其“核/殼”微型結構而常用作吸附劑,在外部磁場下可快速地實現固液分離。Fe3O4就是一種常用的磁性納米材料,已經被廣泛地負載在各種吸附劑上[25-27]。可以預見,將Fe3O4負載在UiO-66-NO2上,制備得到Fe3O4@UiO-66-NO2會擁有金屬有機骨架材料的高孔隙率、大比表面積、良好穩定性等優點,同時擁有磁性材料可重復利用的特點,在吸附方面將有廣泛的應用前景。
為此,本試驗對磁性納米復合材料Fe3O4@UiO-66-NO2的合成及其吸附性能進行研究。采用水熱法制備Fe3O4@UiO-66-NO2,通過控制磁性納米Fe3O4的用量,制備一系列含不同磁性納米Fe3O4量的 Fe3O4@UiO-66-NO2,對所得樣品進行X射線衍射(XRD)圖譜分析、掃描電鏡(SEM)形貌分析、紅外光譜(IR)分析、熱重(TG)分析。并采用亞甲基藍吸附試驗研究溫度、pH離子對其吸附性能的影響,旨在為合成大比表面積的磁性納米吸附劑提供理論基礎。
1 材料與方法
1.1 主要試劑及儀器
氯化鋯(純度98%,薩恩化學技術有限公司);氯化鈉、氯化鈣、六水合三氯化鐵、碳酸鈉、磷酸鈉、納米四氧化三鐵、無水甲醇、氫氧化鈉、N,N二甲基甲酰胺(DMF)(分析純,廣東光華科技股份有限公司);亞甲基藍(分析純,天津市大茂化學試劑廠);濃硫酸(純度98%,西隴科學股份有限公司);2-硝基對苯二甲酸(BDC-NO2)(分析純,Damas-beta試劑有限公司);去離子水(為梧州學院無機及分析化學實驗室自制)。
紫外可見分光光度計(UV-2601型,北京瑞利分析儀器有限公司);X-射線衍射儀(DX-2700BH型,丹東浩元儀器有限公司);掃描電鏡(JSM-IT800型,日本電子株式會社);紅外光譜儀(Frontie,珀金埃爾默企業管理有限公司);熱重分析儀(TGA-1450B,廣州曉分儀器有限公司)。
1.2 Fe3O4@UiO-66-NO2的制備
稱取2.097 4 g ZrCl4和1.900 2 g BDC-NO2置于裝有270 mL DMF溶液的燒杯中,采用超聲波使溶液分散均勻后,將其放入18個23 mL聚四氟乙烯內襯中(每個內襯中分得15 mL混合液)。再向每個內襯里加入0.05 g磁性納米Fe3O4,密封反應釜,120 ℃烘箱下保持24 h,反應結束后,自然冷卻至室溫,取出并收集反應物轉移至6個等量的離心管內,加入適量的無水甲醇和水置于離心機中(4 000 r/min,3 min)洗滌3次,收集沉淀于蒸發皿內。在120 ℃的烘箱中干燥8 h,研磨產物,獲得Fe3O4@UiO-66-NO2棕色粉末。按照上述步驟,控制磁性納米Fe3O4的加入量,分別合成加入0.050 0,0.100 0,0.150 0 g磁性納米Fe3O4于UiO-66-NO2的合成過程中以獲取不同的Fe3O4@UiO-66-NO2。根據Fe3O4在Fe3O4@UiO-66-NO2中的含量不同,將它們分別名命為5.01%Fe3O4@UiO-66-NO2(1)、10.32%Fe3O4@UiO-66-NO2(2)、15.18%Fe3O4@UiO-66-NO2(3)。所合成的材料見圖1。

a.UiO-66-NO2;b.1;c.2;d.3
1.3 吸附劑對亞甲基藍(MB)的吸附
1.3.1 染料溶液的配置及標準曲線的建立
配置質量濃度為5 mg/L的MB溶液,在400~800 nm 波長范圍內進行紫外-可見光光譜掃描。試驗發現,MB的最大吸收波長(λmax)為663 nm。由于染液濃度與λmax處的吸光度符合朗伯比爾定律,可據此建立標準曲線,MB溶液標準曲線為A=0.649Cx+0.004 3,R2=0.998 6。
1.3.2 吸附量與去除率的計算
Fe3O4@UiO-66-NO2對MB的吸附量(q,mg/g)和去除率(R,%)的計算公式分別為
式中,C0是MB的初始濃度(mg/L),Ct是t時刻MB的濃度(mg/L),V是MB溶液的體積(L),m是吸附劑質量(g)。
1.3.3 吸附性能試驗
1.3.3.1 溫度對吸附性能的影響
取4組50 mL,5 mg/L的MB溶液于4個250 mL的燒杯中,在恒溫水浴鍋中依次設置溫度為30,35,40,45 ℃,每組加入0.010 0 g的吸附劑。分別加熱時間到15,30,60,90,120 min,取樣分析溶液中的MB濃度。
在探究溫度對吸附性能影響的試驗中,試驗溫度分別為30,35,40,45 ℃。除以上溫度變量外,其余試驗全部在室溫下進行,量取50 mL初始濃度為5 mg/L的MB溶液,加入0.010 0 g的復合吸附劑,進行2 h的吸附試驗,取樣過濾,測其吸光度,根據染料溶液標準曲線計算得出相應時刻的染料溶液質量濃度數據。
1.3.3.2 pH對吸附性能的影響
取4組50 mL,5 mg/L的MB溶液于4個250 mL的燒杯中,在35 ℃的恒溫水浴鍋中加入0.010 0 g的吸附劑。調制溶液的pH為5,6,7,8。分別在15,30,60,90,120 min取樣分析溶液中的MB濃度。
1.3.3.3 金屬陽離子對吸附性能的影響
室溫下,配制多組離子(分別含金屬陽離子Na+、Ca2+、Fe3+)濃度為0.1,0.01,0.001 mol/L的5 mg/L的MB溶液。分別取4組上述不同的溶液于4個250 mL的燒杯中,在35 ℃的恒溫水浴鍋中加入0.010 0 g的吸附劑。分別在15,30,60,90,120 min取樣分析溶液中的MB濃度。
1.3.3.4 無機陰離子對吸附性能的影響
2 結果與討論
2.1 表征分析
2.1.1 X-射線衍射圖譜分析
為探究所制備樣品的晶體結構,對材料進行了XRD檢測,得到的XRD圖譜見圖2。觀察到磁性納米Fe3O4在波長220,311,400 nm處有強的衍射峰,并且在磁性納米復合材料1、2、3都可以觀察到衍射峰的存在,表明磁性納米復合材料被成功合成;磁性納米復合材料1、2、3的衍射圖都與UiO-66-NO2和模擬的UiO-66晶體特征峰相似,這表明合成的過程中未改變晶體結構。
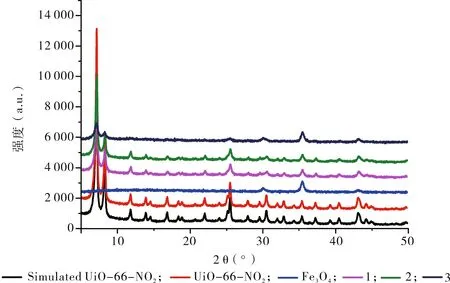
圖2 Fe3O4、1、2、3、UiO-66-NO2和模擬的UiO-66-NO2的XRD
2.1.2 掃描電鏡(SEM)結果分析
為探究所制備樣品的尺寸和形貌,對其進行了SEM檢測分析。磁性納米復合材料1、2、3的檢測結果見圖3-b、3-c、3-d。圖像顯示這些Fe3O4@UiO-66-NO2為球形結構,尺寸為1~20 μm。

a.UiO-66-NO2;b.1;c.2;d.3
2.1.3 紅外光譜(IR)分析
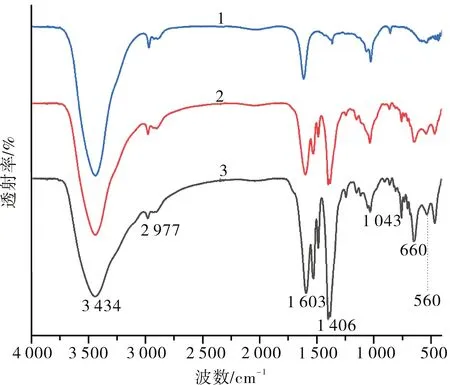
圖4 磁性納米復合材料1、2、3的紅外光譜
2.1.4 熱重分析(TG)
為探究所制備樣品的熱穩定性,對其進行了TG分析檢測,測定溫度為0~900 ℃。磁性納米復合材料1、2、3的檢測結果見圖5。以磁性納米復合材料3為例,樣品在0~350 ℃的熱損失比為21.04%,質量變化主要為復合吸附劑表面的水分蒸發。在350~650 ℃的熱損失比為28.92%,質量變化主要為復合吸附劑表面的結構發生分解。復合吸附劑在650~900 ℃平衡的熱損失比為59.96%,小于UiO-66-NO2在835~900 ℃平衡的熱損失比66.73%,LXJ-3的質量變化主要為復合吸附劑經充分燃燒后所剩余的ZrO2和Fe3O4,UiO-66-NO2則剩余ZrO2,此時復合吸附劑表現出優異的熱穩定性。
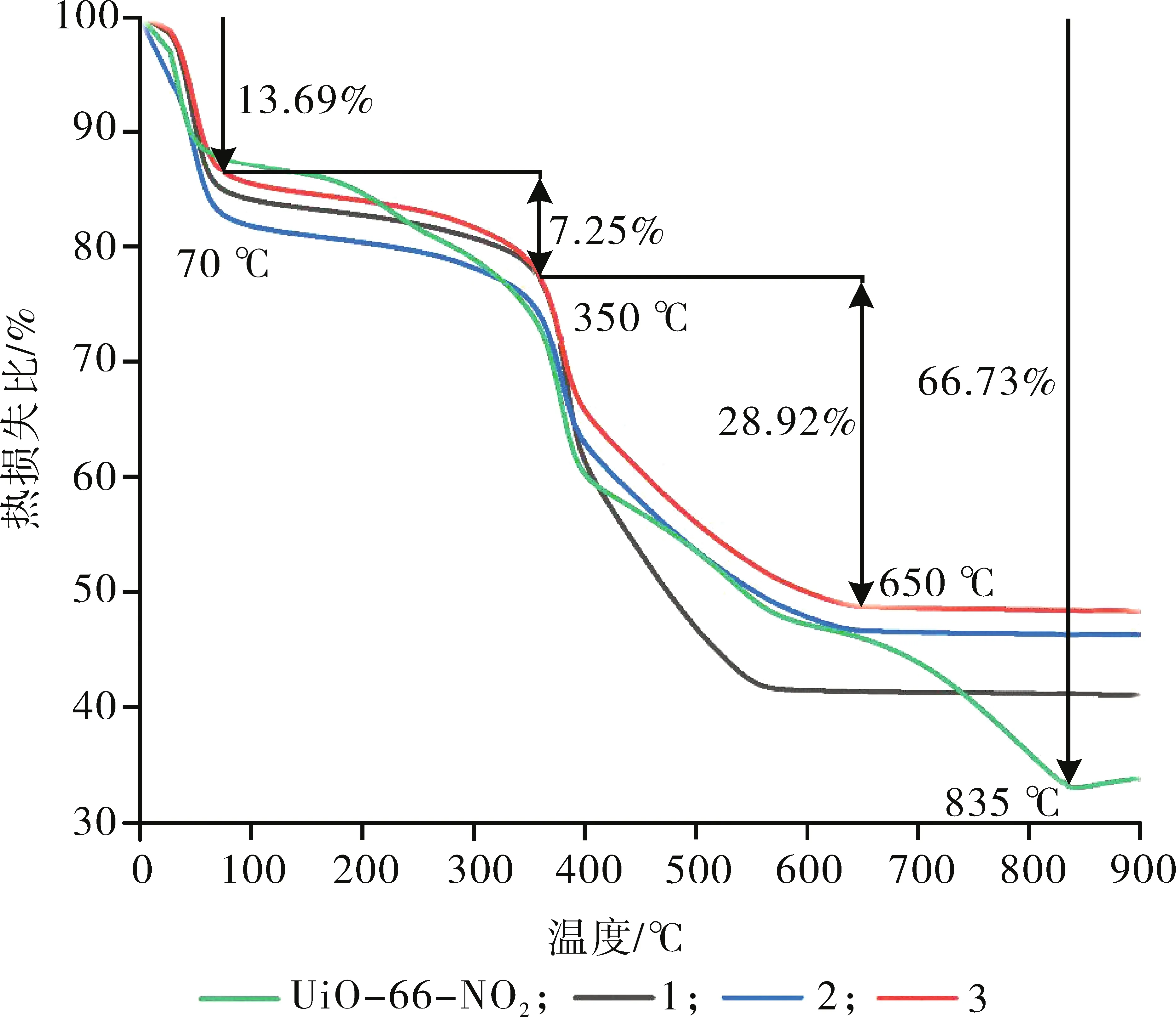
圖5 UiO-66-NO2、1、2、3的熱重分析結果
2.1.5 N2吸附/解吸曲線
通過在77 K條件下N2吸附的BET模型來進一步確定磁性納米復合材料并分析其吸附性能。測試分析結果(圖6)表明,其N2吸附/解吸曲線類似于UiO-66-NO2,均屬于“S”型吸附曲線。其中,UiO-66-NO2的比表面積為544 m2/g。但是,由于加入了不同量的Fe3O4導致磁性納米復合材料的比表面積均小于UiO-66-NO2。磁性納米復合材料1的比表面積為450 m2/g;磁性納米復合材料2的比表面積為420 m2/g;磁性納米復合材料3的比表面積為324 m2/g。
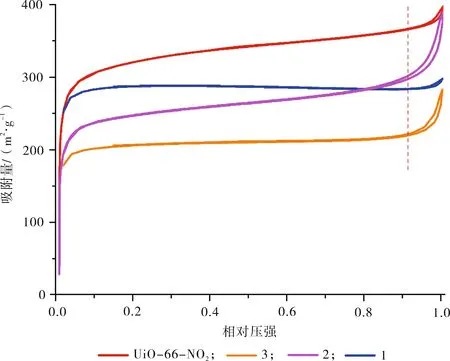
圖6 UiO-66-NO2、1、2、3的N2吸附/解吸曲線
2.2 吸附性能
2.2.1 不同吸附劑吸附性能比較
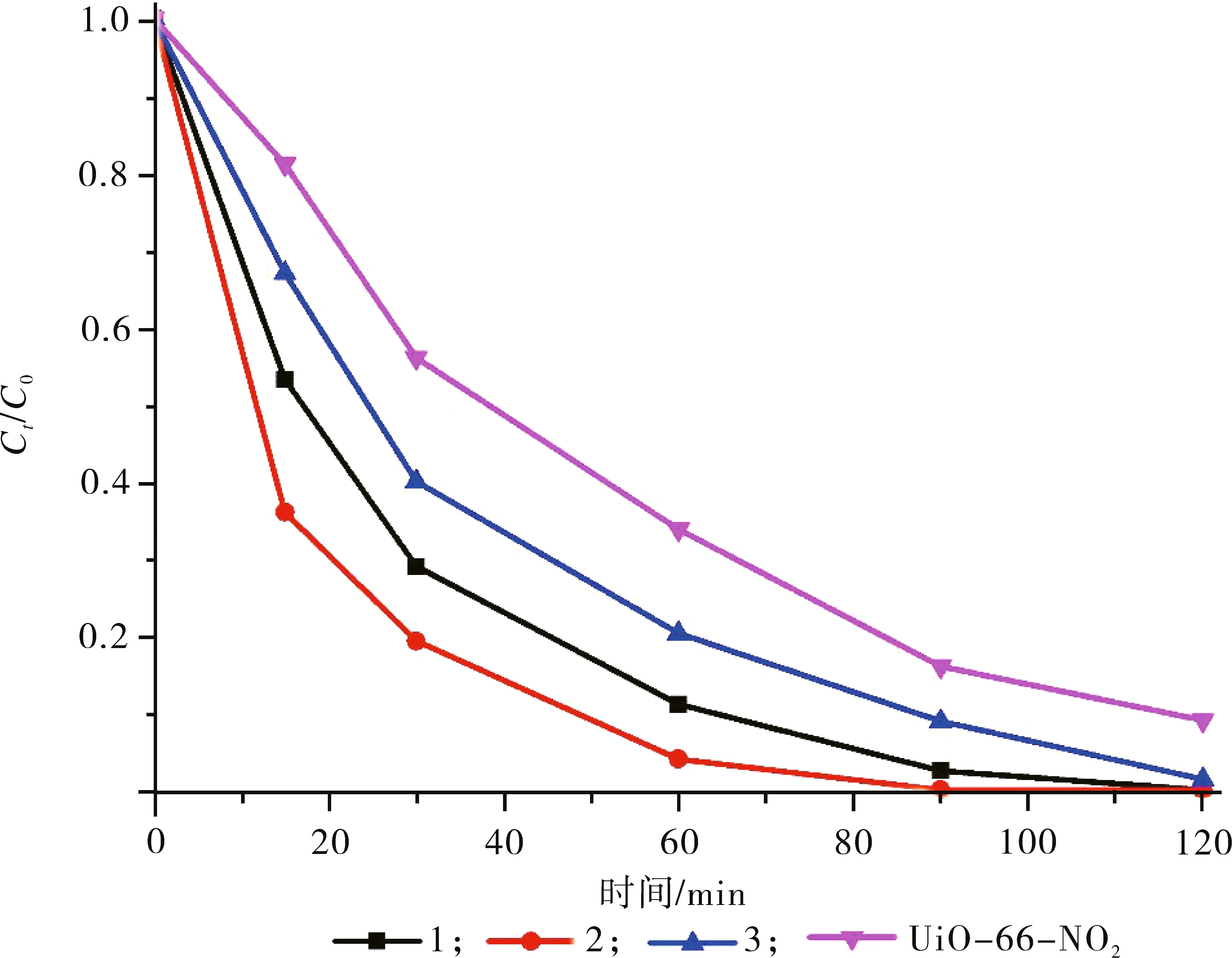
圖7 不同吸附劑吸附MB的性能
以UiO-66-NO2為參比吸附劑,在溫度25 ℃、吸附120 min的條件下,研究磁性納米復合材料對MB的吸附性能。試驗結果(圖7)表明參比吸附劑UiO-66-NO2吸附120 min能吸附去除91%的MB,平均吸附速率為0.037 9 mg/(L·min),吸附量為22.75 mg/g;磁性納米復合材料3吸附120 min能吸附去除98.6%的MB,平均吸附速率為0.041 1 mg/(L·min),吸附量為24.65 mg/g;磁性納米復合材料2吸附90 min能吸附去除100%的MB,平均吸附速率為0.055 6 mg/(L·min),吸附量為25 mg/g;磁性納米復合材料1吸附90 min能吸附去除97.5%的MB,平均吸附速率為0.054 2 mg/(L·min),吸附量為24.38 mg/g。通過比較分析平均吸附速率和吸附量可以發現,磁性納米復合材料的吸附性能均優于參比吸附劑UiO-66-NO2,并且磁性納米復合材料2的性能最好,對MB的去除率達100%、吸附量為25 mg/g。
2.2.2 溫度對吸附性能的影響
試驗結果(圖8)表明,參比吸附劑UiO-66-NO2(圖8-a)的最佳吸附溫度為30 ℃,此時其吸附120 min能吸附去除96.1%的MB,平均吸附速率為0.040 0 mg/(L·min),吸附量為24.03 mg/g;由圖8-b、8-c和8-d可見,磁性納米復合材料1、2、3的最佳吸附溫度均為35 ℃。在此溫度條件下磁性納米復合材料1、2、3(圖8-b、8-c、8-d)吸附60 min后,對MB的去除率分別為99.00%、100.00%、94.00%,平均吸附速率分別為0.082 5,0.083 3,0.078 3 mg/(L·min),吸附量分別為24.75,25.00,23.50 mg/g。通過溫度對吸附性能的影響試驗可以發現,磁性納米復合材料的最佳吸附溫度為35 ℃,此時3種磁性納米復合材料的吸附能力強弱為2>1>3。
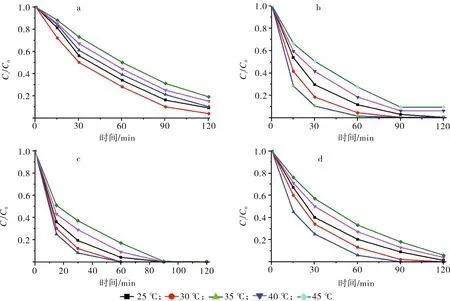
a.UiO-66-NO2;b.1;c.2;d.3
2.2.3 pH對吸附性能的影響
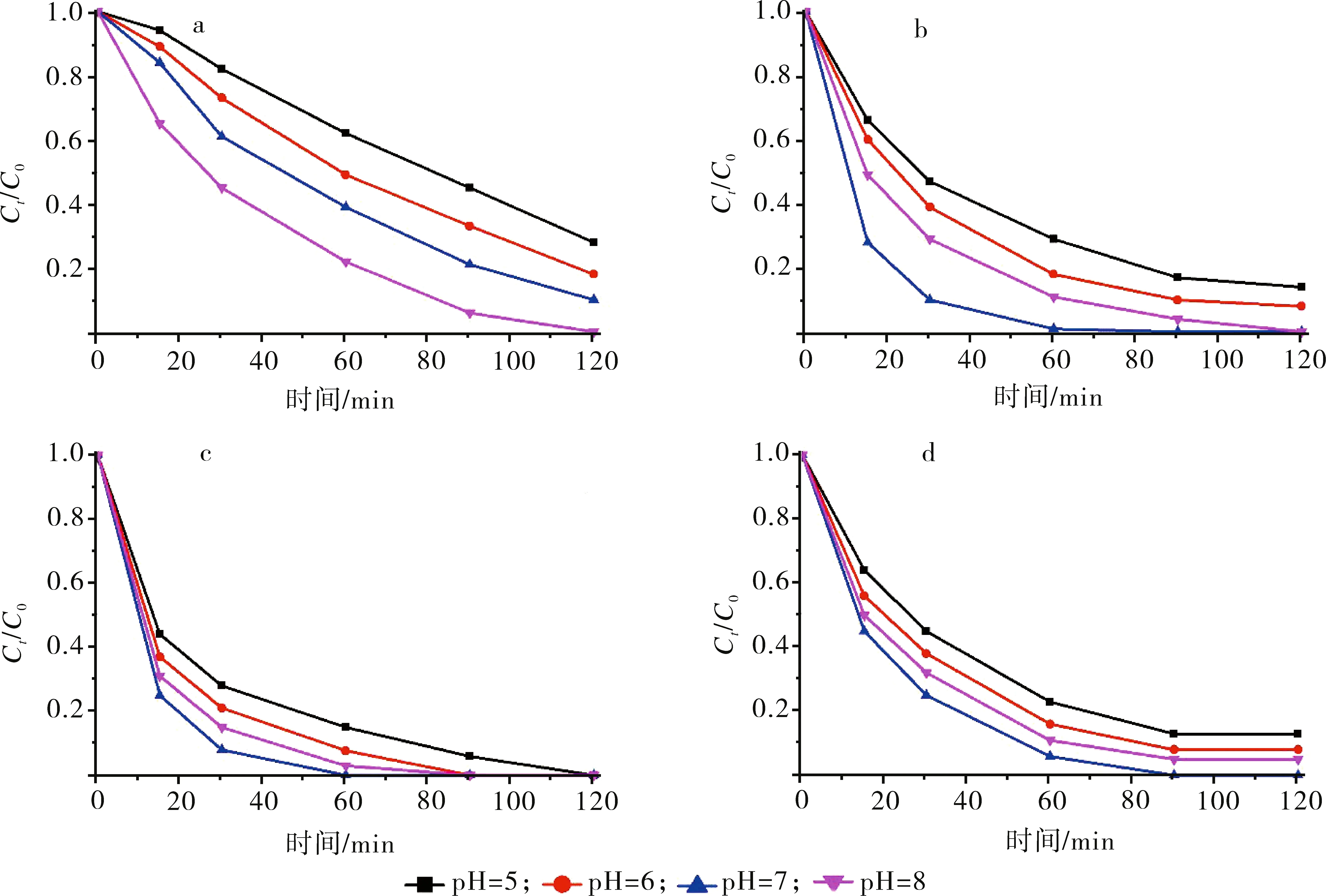
a.UiO-66-NO2;b.1;c.2;d.3
試驗結果表明,對于參比吸附劑UiO-66-NO2(圖9-a),在pH為5,6,7,8條件下,吸附120 min,對MB的去除率分別為72.00%、82.00%、90.12%、100.00%,可見溶液中最佳的pH為8,該條件下平均吸附速率為0.041 6 mg/(L·min),吸附量為25.00 mg/g。對于磁性納米復合材料1(圖9-b),在pH為5,6,7,8條件下,吸附90 min,對MB的去除率分別為83.00%、90.00%、99.00%、96.00%,平均吸附速率分別為0.046 1,0.050 0,0.082 5,0.053 3 mg/(L·min),吸附量分別為20.75、22.50、24.75、24.00 mg/g;對于磁性納米復合材料2(圖9-c),在pH為5、6、7、8條件下,吸附90 min,MB的去除率分別為85.00%、92.30%、100.00%、97.00%,平均吸附速率分別為0.070 8,0.076 9,0.083 3,0.080 8 mg/(L·min),吸附量分別為21.25,23.08,25.00,24.25 mg/g;對于磁性納米吸附劑3(圖9-d),在pH為5、6、7、8不同條件下,吸附90 min,對MB的去除率分別為87.00%、92.00%、94.00%、95.00%,平均吸附速率分別為0.048 3,0.051 1,0.078 3,0.052 8 mg/(L·min),吸附量分別為21.75,23.00,23.50,23.75 mg/g。由圖9-a、9-b和9-c可知,3種磁性納米復合材料的最佳吸附pH均為7。由于MB屬于陽離子型堿性染料,帶正電荷,而含有-NO2的參比吸附劑具有弱酸性,所以其最佳的吸附pH為8。但是,將Fe3O4加入到UiO-66-NO2之后所形成的磁性納米復合材料,改變了UiO-66-NO2的酸堿性和表面電荷,導致了其最佳吸附pH為7。
2.2.4 金屬陽離子對吸附性能的影響
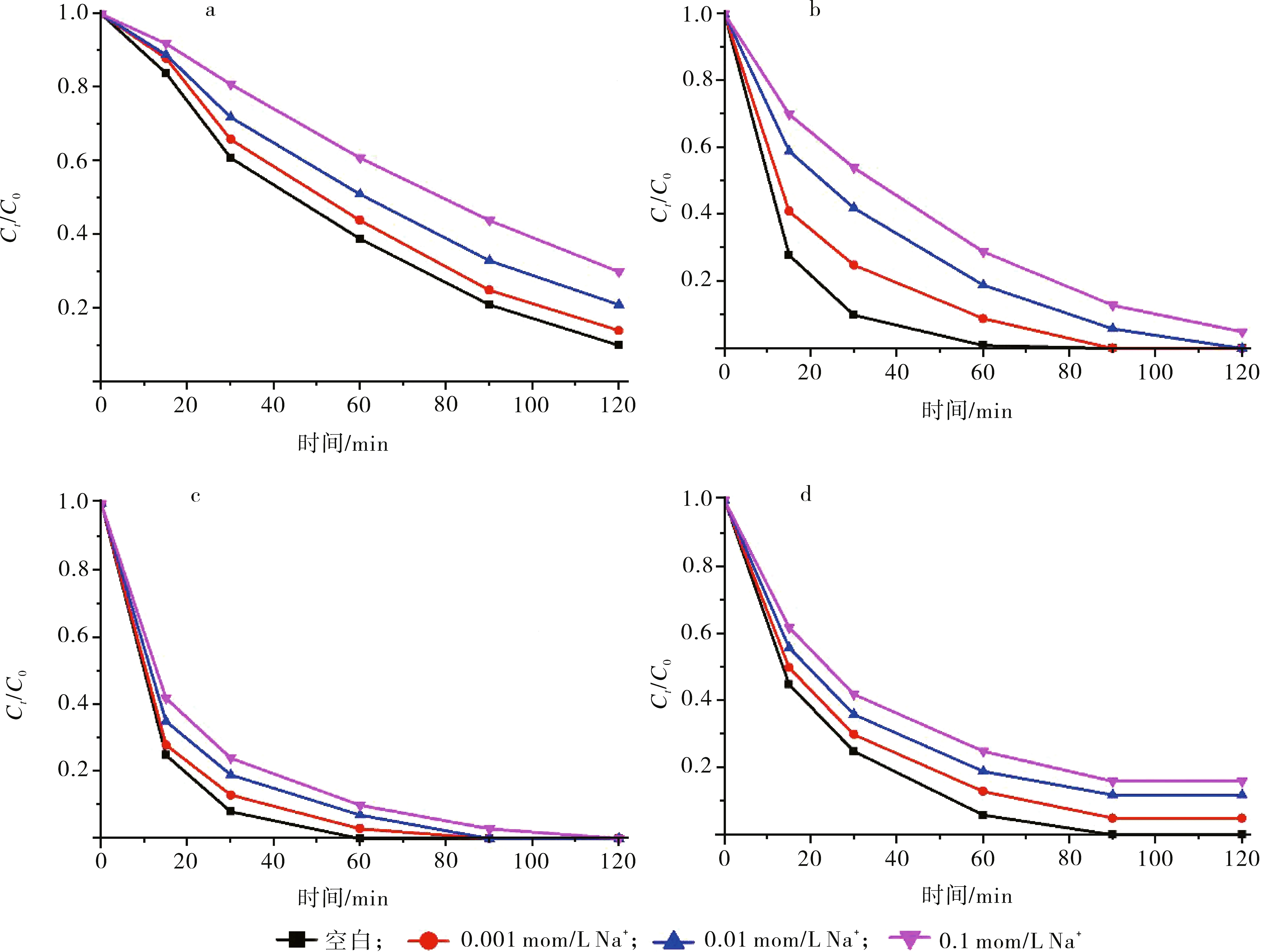
a.UiO-66-NO2;b.1;c.2;d.3
在金屬Na+與MB混合體系中,隨著Na+濃度的增大,抑制吸附劑吸附MB的作用就越明顯(圖10)。在沒有離子影響吸附劑吸附MB的時候,參比吸附劑UiO-66-NO2(圖10-a)、磁性納米吸附劑1(圖10-b)、2(圖10-c)和3(圖10-d),吸附60 min,MB的去除率分別為61%、99%、100%、94%;然而當0.001~0.1 mol/L的Na+與5 mg/L的MB共存時,對參比吸附劑UiO-66-NO2吸附120 min,對MB的去除率分別為86%、79%、70%;當0.001~0.1 mol/L的Na+與5 mg/L的MB共存時,磁性納米復合材料1吸附60 min,MB的去除率分別為91%、81%、71%;當0.001~0.1 mol/L的Na+與5 mg/L的MB共存時,磁性納米復合材料2吸附60 min,對MB的去除率分別為97%、93%、90%;當0.001~0.1 mol/L的Na+與5 mg/L的MB共存時,磁性納米復合材料3吸附60 min,對MB的去除率分別為87%、81%、75%。
當0.001~0.1 mol/L的Ca2+與5 mg/L的MB共存時,參比吸附劑UiO-66-NO2(圖11-a)吸附120 min,對MB的去除率分別為78%、72%、66%;當0.001~0.1 mol/L的Ca2+與5 mg/L的MB共存時,磁性納米復合材料1(圖11-b)吸附120 min,對MB的去除率分別為83%、69%、57%;當0.001~0.1 mol/L的Ca2+與5 mg/L的MB共存時,磁性納米復合材料2(圖11-c)吸附120 min,對MB的去除率分別為94%、90%、86%;當0.001~0.1 mol/L的Ca2+與5 mg/L的MB共存時,磁性納米復合材料3(圖11-d)吸附120 min,對MB的去除率分別為83%、75%、67%。所以,在0.001~0.1 mol/L的Ca2+與5 mg/L的MB共存時,離子對吸附劑吸附MB也起到抑制作用,并且抑制作用也隨著濃度的升高而變得明顯。
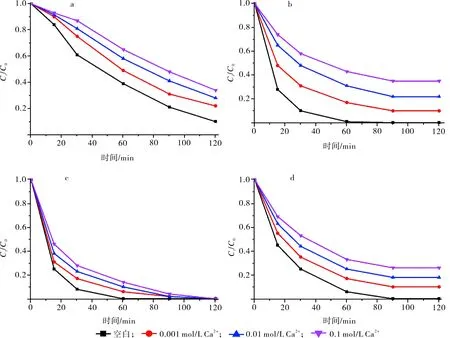
a.UiO-66-NO2;b.1;c.2;d.3
當0.001~0.1 mol/L的Fe3+與5 mg/L的MB共存時,參比吸附劑UiO-66-NO2(圖12-a)吸附120 min,對MB的去除率分別為73%、65%、58%;當0.001~0.1 mol/L的Fe3+與5 mg/L的MB共存時,磁性納米復合材料1(圖12-b)吸附120 min,對MB的去除率分別為79%、65%、52%;當0.001~0.1 mol/L的Fe3+與5 mg/L的MB共存時,磁性納米復合材料2(圖12-c)吸附120 min,對MB的去除率分別為89%、85%、77%;當0.001~0.1 mol/L的Fe3+與5 mg/L的MB共存時,磁性納米復合材料3(圖12-d)吸附120 min,對MB的去除率分別為78%、70%、62%。所以,在0.001~0.1 mol/L的Fe3+與5 mg/L的MB共存時,離子對吸附劑吸附MB也起到抑制作用,并且抑制作用也隨著濃度的升高而變得明顯。
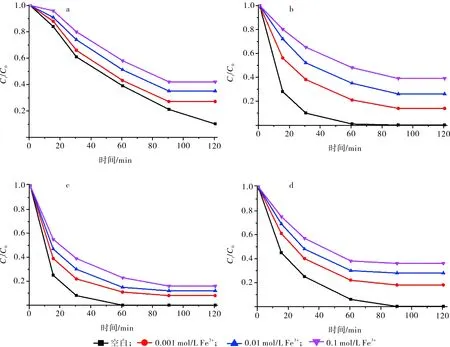
a.UiO-66-NO2;b.1;c.2;d.3
通過金屬陽離子對吸附MB性能的影響試驗可以發現,金屬陽離子與MB共存時,金屬陽離子對吸附劑吸附MB均起抑制作用,并且抑制作用隨著濃度的升高而變得明顯。這可能是因為金屬陽離子半徑比較小,優先被吸附在磁性納米復合材料的表面,阻礙了其直接吸附MB,從而影響了其吸附MB的性能。金屬陽離子抑制吸附劑吸附MB的作用遵循著Fe3+>Ca2+>Na+。
2.2.5 無機陰離子對吸附性能的影響
由于所配制的無機陰離子均是使用鈉鹽,所以在Cl-與MB混合體系中,Cl-對吸附劑吸附MB的抑制作用同Na+(圖10-a),均是隨著濃度的增大,抑制作用變得明顯。
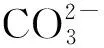
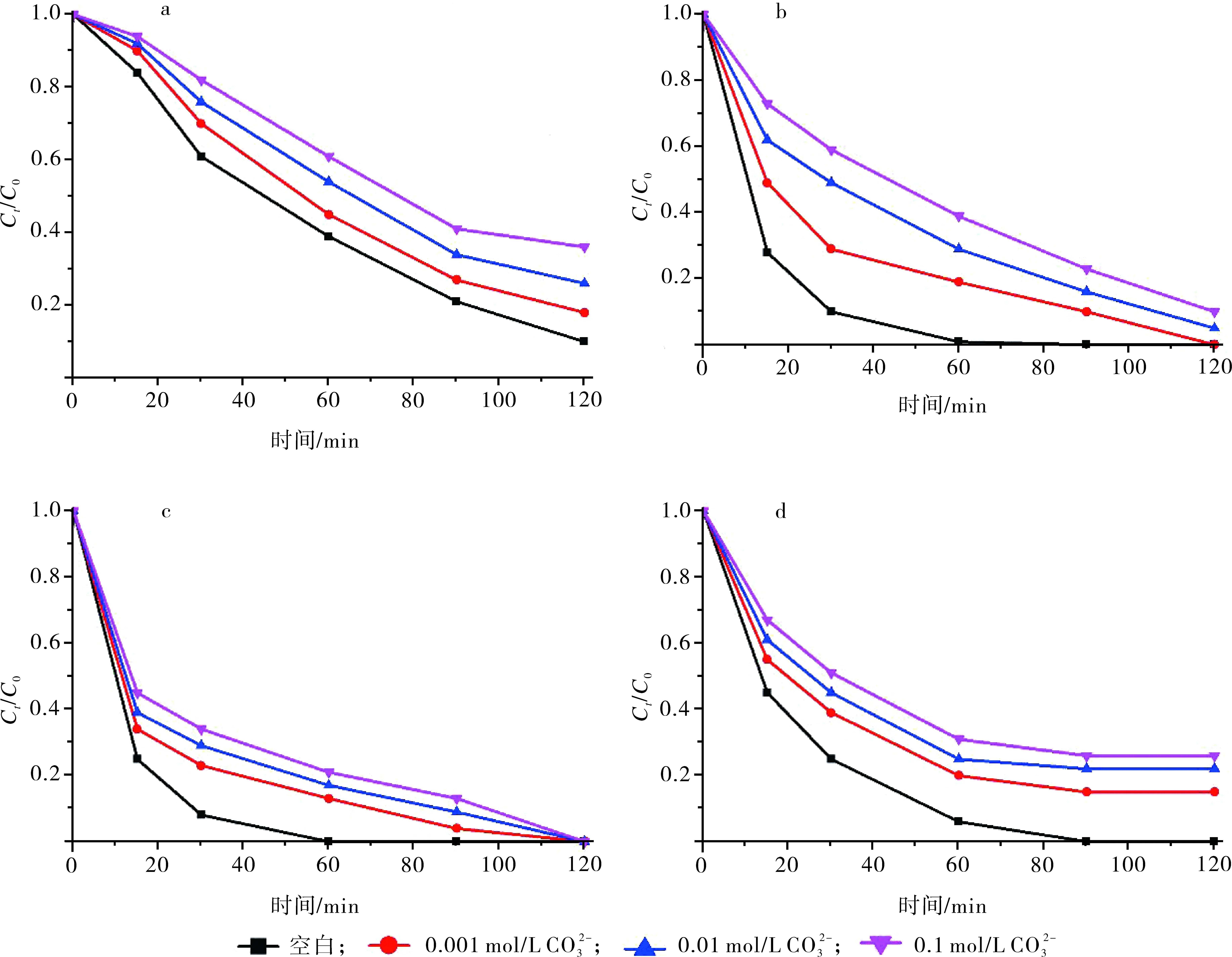
a.UiO-66-NO2;b.1;c.2;d.3
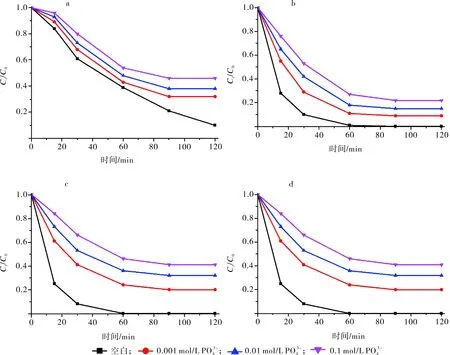
a.UiO-66-NO2;b.1;c.2;d.3
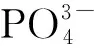
3 結論