原核持續時間預測胚胎發育潛力的研究
李柔,周靜,2,廖宏慶,2*,周俊,2
(1.南華大學附屬第二醫院,衡陽 421001;2.衡陽南華星輝生殖健康專科醫院,衡陽 421001)
自時差成像(time-lapse imaging,TLI)技術廣泛應用于胚胎觀測后,胚胎學家從中獲取了大量的形態動力學信息,為準確評估和選擇優質胚胎提供了新方法。如何準確有效地利用動力學參數篩選出優質胚胎,是當前胚胎學家研究的熱點。
受精是嚴格有序的生理過程,是指成熟的精子與次級卵母細胞相互作用并結合成為受精卵。精卵開始融合時,次級卵母細胞被激活,單倍染色體開始向細胞中央移動,核膜形成,雌原核(female pronucleus)顯現;同時精子核在進入卵子后,核膜發生崩解,精子核染色質解聚,新形成的原核膜包在染色質外周,形成雄原核(male pronucleus),雌雄原核形成的時間對應TLI觀測下的原核出現時間(time of PN appearance,tPNa)。有學者指出,tPNa與精子染色質的重塑過程息息相關[1]。伴隨著雌雄原核的發育,DNA合成和染色質的復制同步進行,隨后兩原核的核膜消失,染色體互混,該時間點對應了原核消失時間(time of PN fading,tPNf)。研究顯示tPNf與胚胎后期的囊胚形成[2]、種植[3]、活產[4]和染色體異常[5]有關。配子轉變為胚胎后,細胞周期將重新啟動[6],從減數分裂向有絲分裂過渡。原核持續時間(原核消失時間-原核出現時間,即tPNf-tPNa)包含有絲分裂的分裂間期和分裂期的前期,其中分裂間期會完成DNA分子的復制和相關蛋白質的合成,為胚胎后續的卵裂進行活躍的物質準備。
原核的形態動力學是影響哺乳動物胚胎發生的重要因素[7]。原核持續時間可反映胚胎內遺傳物質的準備時長,該參數可否對胚胎發育潛力作出預測,在現有的研究中尚未闡明。本研究對922枚正常受精胚胎的原核持續時間及后期發育情況進行回顧性分析,旨在尋找有助于胚胎選擇的新指標。
資料與方法
一、研究對象
收集2018年9月至2021年1月在衡陽南華星輝生殖健康專科醫院行TLI系統觀測的922枚正常受精胚胎作為研究對象。
納入標準:新鮮取卵周期;行短時IVF、卵胞漿內單精子注射(ICSI)正常受精來源的胚胎;排除異常受精胚胎。
二、診療回顧
1.控制性促排卵、配子采集及人工授精:根據患者情況制定個性化治療方案,包括激動劑長方案、拮抗劑方案、氯米酚方案以及自然周期取卵等。結合B超及激素水平監測卵泡生長情況,待主導卵泡直徑達18~20 mm后采用10 000 U HCG(珠海麗珠制藥)扳機,34~36 h后行陰道B超引導下卵泡穿刺取卵術。男方禁欲3~7 d,于取卵當日通過手淫法取精。根據雙方病史、精液情況選擇短時IVF或ICSI助孕。短時IVF授精時間為HCG扳機后39.5 h,將精子按1.5×106/ml的濃度與卵子共孵育,5 h后進行脫顆粒,并將其轉移至TLI系統中。ICSI授精時間為HCG扳機后41 h,將成熟卵母細胞行單精子卵胞漿內顯微注射,轉移至TLI系統中觀察培養。
2.受精評估與胚胎培養:利用時差顯微鏡觀察原核形成情況,若形成2個清晰原核視為正常受精,形成1個或2個以上原核為異常受精,未形成原核考慮為未受精。胚胎培養采用卵裂胚培養液(COOK,美國)和囊胚培養液(COOK,美國),培養箱環境為6.0%CO2、5.0%O2、37℃。
3.TLI系統及形態動力學參數:本研究所采用的TLI系統是Primo Vision EVO+(Vitrolife,瑞典),它將培養箱與倒置顯微鏡結合,通過數據線將胚胎發育過程中采集到的圖片傳輸至培養箱外的電腦中,每間隔10 min對胚胎進行1次拍攝,通過圖片信息來收集胚胎發育過程中的動力學參數。此培養系統使用專用16孔微孔培養皿(Vitrolife,瑞典),每孔存放1枚胚胎,對應不同編號以示區分。每次觀測的胚胎數不超過16枚。
動力學參數:tPNa:至少可見1個清晰原核的時間;tPNf:兩個原核均消失的時間;原核持續時間:tPNf-tPNa。
4.胚胎評估:D3優質卵裂胚參考Istanbul共識中的優質胚胎標準:受精后第3天胚胎細胞數為7~9個、細胞大小符合發育階段、碎片程度小于10%、無多核化的胚胎為優質胚胎。囊胚評級按Gardner評分標準,包括囊胚腔大小、內細胞團以及外胚滋養層3個指標,評分≥3BB的囊胚視為優質囊胚。
5.結局指標及定義:優質卵裂胚形成率=優質卵裂胚總數/正常受精胚胎總數×100%;囊胚形成率=總囊胚數(D5+D6)/行囊胚培養胚胎總數×100%;優質囊胚形成率=優質囊胚數(D5+D6)/行囊胚培養胚胎總數×100%;臨床妊娠率=臨床妊娠周期數/移植(鮮胚+凍胚)周期數×100%(為保證統計結果的準確性,僅對單胚胎移植的周期數據進行統計分析);移植4周后B超檢查見宮內孕囊定義為臨床妊娠。
三、分組分析
首先根據原核持續時間的長短(以15 h為界)將所有納入研究的胚胎分為兩組:≤15 h組(n=388)和>15 h組(n=534),比較兩組胚胎的發育情況,探討該參數對胚胎發育潛力的預測意義。
再根據D5、D6胚胎的發育情況,將行囊胚培養的764枚胚胎分為成囊組(n=558)和未成囊組(n=206),比較兩組胚胎的原核持續時間是否存在差異;考慮到授精方式可能對胚胎的發育動力學參數產生影響,根據不同原核持續時間和授精方式將胚胎進一步分為:≤15 h IVF組(n=216)和>15 h IVF組(n=317)、≤15 h ICSI組(n=103)和>15 h ICSI組(n=128),分別比較IVF、ICSI受精胚胎在不同原核持續時間囊胚形成相關指標的差異。
進一步將原核持續時間>15 h組細分為3個亞組:>15~17 h組(n=250)、>17~19 h組(n=147)和>19 h組(n=137),比較各組胚胎發育情況及妊娠結局。
四、統計學方法
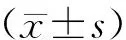
結 果
一、不同原核持續時間胚胎的發育情況及移植結局
本研究共納入TLI系統觀測的922枚正常受精胚胎。原核持續時間>15 h組的囊胚形成率、優質囊胚形成率和臨床妊娠率較≤15 h組顯著下降(P<0.05),而兩組間優質卵裂胚形成率無統計學差異(P>0.05)(表1)。

表1 不同原核持續時間組胚胎發育情況及移植結局比較(%)
二、行囊胚培養的胚胎發育情況比較
本研究中共有764枚正常受精胚胎在TLI系統觀測下行囊胚培養。
1.不同囊胚培養結局的分組分析:根據D5、D6胚胎發育情況分為成囊組(n=558)和未成囊組(n=206)。統計結果顯示,未成囊組的原核持續時間較成囊組顯著延長(P<0.05)(表2)。
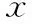
表2 成囊組與未成囊組原核持續時間比較(-±s)
2.不同原核持續時間及授精方式的分組分析:無論采用IVF或是ICSI受精,原核持續時間>15 h組胚胎的囊胚形成率、優質囊胚形成率均較≤15 h組顯著下降(P<0.05)(表3)。

表3 不同原核持續時間/授精方式的胚胎囊胚培養結局比較(%)
三、原核持續時間>15 h的胚胎細化分組分析
3組中,原核持續時間>19 h組的優質卵裂胚形成率較>15~17 h組、>17~19 h組顯著下降(P<0.05);隨著原核持續時間的延長,囊胚形成率顯著下降(P<0.05)。3組間優質囊胚形成率呈現下降趨勢,但無統計學差異(P>0.05);臨床妊娠率在3組間無統計學差異(P>0.05)(表4)。

表4 原核持續時間>15 h的胚胎發育情況亞組分析(%)
討 論
對胚胎進行評估并篩選出具有發育潛力的胚胎是輔助生殖治療中較為關鍵和核心的步驟之一。TLI技術作為非侵入性評估系統,為胚胎學家準確評估和選擇優質胚胎提供了新方法。有研究發現,整倍體胚胎與非整倍體胚胎間發育速度存在差異,可將動力學參數作為胚胎優選的候選指標,有望改善臨床結局[8]。
原核出現至原核消失的時間段內,胚胎處于活躍的物質準備階段,需要進行一系列DNA分子的復制和相關蛋白質的合成。本研究結果顯示:與原核持續時間≤15 h組相比,>15 h組其囊胚形成率、優質囊胚形成率和臨床妊娠率均顯著下降(P<0.05);未成囊組的原核持續時間較成囊組顯著延長(P<0.05);當原核持續時間>15 h,隨著時間的延長,囊胚形成率顯著下降(P<0.05),優質囊胚形成率也呈現下降趨勢,但尚無統計學差異(P>0.05)。結果提示原核持續時間對于胚胎的成囊情況有一定的預測意義。可能的機制如下:(1)原核持續時間延長可能反映胚胎存在DNA損傷或染色體異常。DNA損傷是一種常見事件,可導致染色體DNA的突變或缺失,繼而對后續的胚胎發育產生影響。胚胎發育過程中,若DNA出現損傷,可誘發DNA損傷應答,包括DNA修復、細胞周期檢查點激活以及觸發凋亡通路[9],使得細胞周期進程減慢或阻滯細胞周期進程[10]。(2)DNA復制進程遲緩也可能使原核持續時間延長,與線粒體供能不足相關。線粒體產生的ATP是細胞的主要能量來源[11],ATP作為卵母細胞成熟、受精及胚胎發育的能量保證[12],對胚胎的發育起著關鍵作用。越來越多的證據表明,卵母細胞線粒體是各種應激源的關鍵作用靶點,應激誘導的線粒體功能改變將導致卵母細胞質量及胚胎發育潛力下降[11]。
本研究中,囊胚形成率在原核持續時間>15 h的胚胎分組中隨著時間的推移出現顯著下降,而優質卵裂胚形成率在原核持續時間>19 h亞組才出現下降趨勢。胚胎基因組激活(embryo genome activation,EGA)和轉錄活躍的開始標志著從卵母細胞到合子基因程序的轉變,這一過程在人類胚胎發生在4~8細胞階段[13]。如前所述,原核持續時間延長可能反映了胚胎存在DNA的突變或缺失,但在早期卵裂階段,胚胎在轉錄上是沉默的[14],DNA異常對胚胎發育的影響在該時期尚未充分體現,僅通過D3發育情況進行胚胎選擇存在一定局限性。囊胚形成是胚胎早期發育過程的一個重要階段,多種基因參與囊胚的分化和發育[15]。Uysal等[16]將與DNA甲基化發生相關的基因Dnmt1、Dnmt3a敲除,發現缺乏這些關鍵基因的胚胎多數發生退化或停滯于二細胞階段,只有具備完整且正常激活的基因組,胚胎才有可能發育至囊胚。與D3優胚率相比,原核持續時間的長短可初步判定胚胎是否具有正常的基因組成,因此,在篩選具有發育潛力的胚胎上更占優勢。
對于不同授精方式的胚胎,當原核持續時間>15 h,后期發育為囊胚、優質囊胚的可能性均顯著下降,該時長對IVF、ICSI胚胎的囊胚發育情況的預測同樣有效。IVF中,精子需穿過卵丘細胞和透明帶,經歷精卵識別、精卵結合以及精卵質膜融合等復雜步驟。ICSI技術借助顯微操作系統,直接將單個精子注射入卵母細胞誘導其受精;然而,實施操作前需人工去除卵母細胞周圍的卵丘細胞,注射精子時會對卵母細胞產生損傷。與IVF相比,ICSI具有侵入性,侵入性的操作是否影響胚胎發育是胚胎學家較為關心的問題[17]。Sayed等[18]的報道中將IVF與ICSI胚胎的tPNf進行比較,發現IVF胚胎的tPNf較ICSI延遲0.28 h;Cruz等[19]指出,兩種授精方式的胚胎早期發育參數存在差異,但該差異是由參數的起點不同所致,與胚胎質量無明顯關聯。我們的數據表明,原核持續時間并未受授精方式的顯著影響,與Cruz等[19]的研究結果一致。
綜上所述,無論采用何種授精方式,原核持續時間≤15 h的胚胎囊胚形成率及囊胚質量均顯著高于原核持續時間>15 h的胚胎;原核持續時間對胚胎發育潛力有一定的預測價值,有望成為胚胎優選的新指標。本研究的不足在于移植的胚胎數量較少,以及部分隨訪資料缺失,未將活產率及活產兒后期的健康狀況作為結局指標。在未來的探索中仍需進一步擴大樣本量來加以驗證,還可以通過遺傳學分析等手段,去探究不同原核持續時間與胚胎正常核型的關系。

