胚胎移植術后宮內合并宮角單卵雙胎妊娠1例報道
李小玉,郝鎂娟,王慧君
(河北省滄州中西醫結合醫院生殖醫學科,滄州 061000)
宮內合并宮外妊娠(heterotopic pregnancy,HP)是指胚胎在宮腔內和其他部位同時種植并發育的一種病理性妊娠狀態,宮內合并宮角妊娠(cornual heterotopic pregnancy,CHP)則是指宮內和宮角同時妊娠的復合形式。宮角妊娠約占所有異位妊娠的4.2%[1]。有文獻表明,單純宮角妊娠孕婦的病死率較其他部位異位妊娠(ectopic pregnancy,EP)婦女病死率要高5~6倍[2]。HP在自然周期妊娠婦女中極少見,CHP則更為罕見,宮內合并宮角單卵雙胎妊娠者目前尚未見報道。體外受精-胚胎移植(IVF-ET)助孕后,HP的發生率約為1%~3%[3]。本文報道1例宮內合并宮角單卵雙胎妊娠患者在積極腹腔鏡手術準備前提下,經減胎術減滅宮角妊娠,保留宮內妊娠。
一、病例資料
患者,女,32歲,因“原發性不孕,雙側輸卵管積水”入院。2015年于外院行首次IVF-ET助孕,獲卵6枚,成胚4枚,移植2枚胚胎未孕,凍融移植2枚胚胎,左側輸卵管異位妊娠后保守治療。2016年,因雙側輸卵管積水行腹腔鏡手術治療,術中分離盆腔粘連后行子宮輸卵管通液,示雙側輸卵管通暢。2018年5月于我科接受助孕治療,助孕前子宮內膜病理結果提示慢性子宮內膜炎,給予藥物治療后采用拮抗劑方案促排卵,獲卵2枚,成胚2枚,移植后未孕。2020年6月再次就診,采用卵泡期長方案促排卵,獲卵5枚,成胚4枚,因促排卵過程中B超顯示左側輸卵管積液故該周期行全胚冷凍。2020年8月行左側輸卵管積液穿刺術,后自然周期準備內膜解凍移植2枚胚胎,HCG陽性后,未獲臨床妊娠。2020年9月行左側輸卵管封堵術。后擇期采用降調節人工周期方案準備內膜后解凍移植2枚胚胎,移植后25 d行陰道B超示:宮內單孕囊,大小1.6 cm×0.7 cm,內可見卵黃囊、胎芽及原始心管搏動;于左宮角處見1.7 cm×1.4 cm大小孕囊,內可見2個卵黃囊及胎芽(圖1A),其一可見原始心管搏動,胎心慢,約100次/min,另一未見原始心管搏動。收入院后完善術前準備進行減胎治療。2020年12月17日,備血及腹腔鏡術前準備后,在陰道B超引導下對宮角處的妊娠囊行胚胎減滅術(圖1B、C)。以17G穿刺針將左側宮角處妊娠囊內2個卵黃囊、胎芽抽出,顯微鏡下查找可見體節。術中觀察宮腔內妊娠囊內可見胎心搏動,宮角孕囊內出血,無腹腔內出血,術后繼續給予止血保胎藥治療。減胎后2 h復查陰道B超示宮內妊娠囊內可見胎心搏動,左宮角處存在雜亂回聲,大小約3.0 cm×2.8 cm,盆腔未見積液。術后第1天復查血常規未見異常。減胎后陰道少量出血,2 d后血止,繼續住院觀察3 d無不適后出院。出院后定期復查彩超,孕12周彩超檢查示:宮內孕,單活胎(圖1D),頸項透明層(NT):0.12 cm;左側宮角處可探及大小5.7 cm×4.7 cm×4.0 cm的雜亂回聲包塊。孕18周彩超示:宮內孕,單活胎;左側宮角探及大小約4.4 cm×3.3 cm的囊實性包塊,邊界不清,形態不規則,內可見多發液性暗區。孕25周彩超示:宮內孕,單活胎,頭位,雙頂徑6.6 cm,球拍狀胎盤。
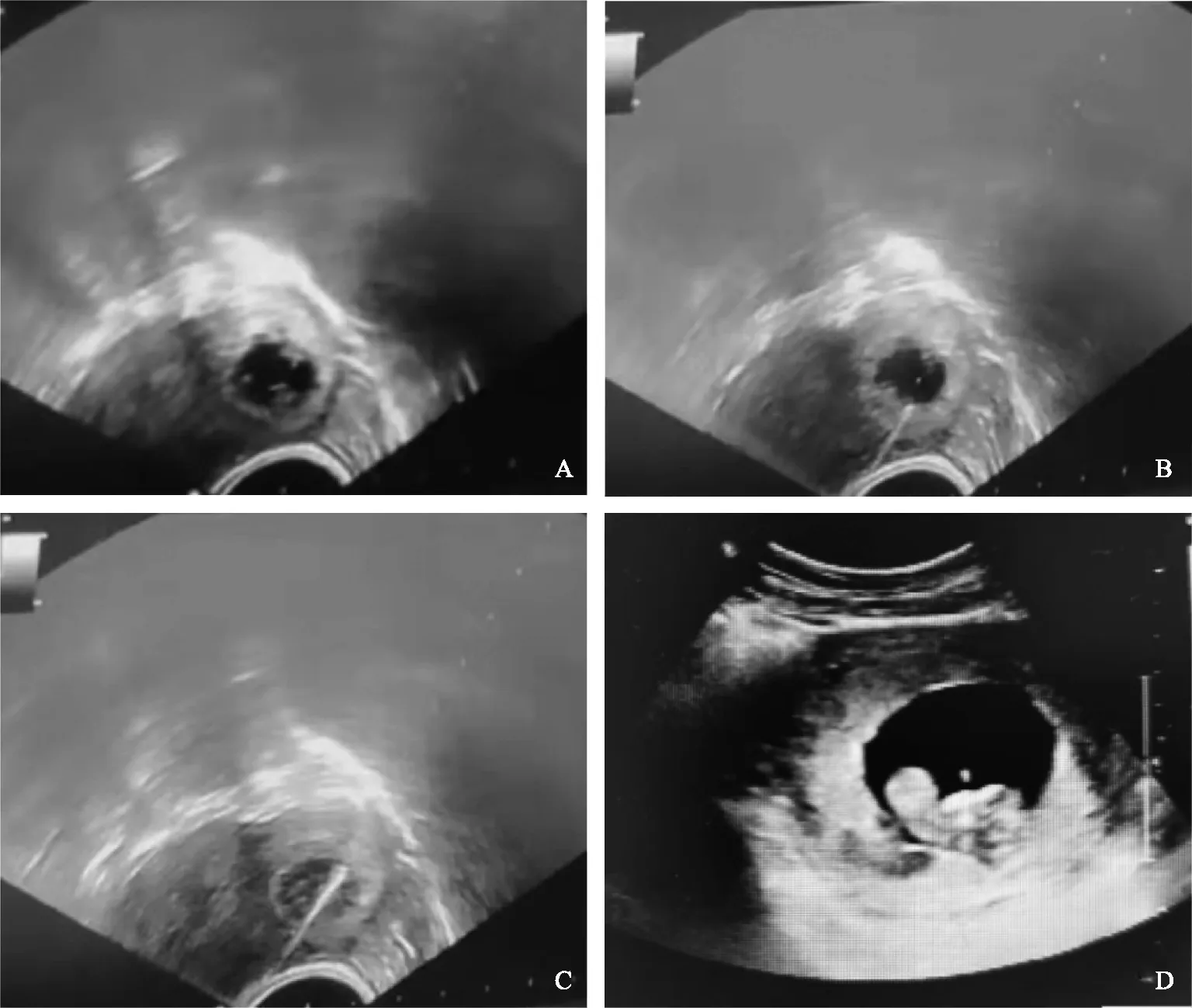
A:宮角處孕囊,內可見2個胎芽;B:減胎術中,減滅孕囊中偏下方胎芽;C:減胎術中,減滅孕囊中偏上方胎芽;D:孕12周胎兒。
二、討論
自然妊娠時CHP的發生較罕見,宮內合并宮角單卵雙胎妊娠者目前尚未見報道。隨著輔助生殖技術(ART)在不孕癥患者中的廣泛應用,CHP在助孕患者中的發生率略有升高[4],有文獻統計,通過IVF-ET助孕后妊娠的育齡婦女中,CHP的發生率約在0.02%[5]。其發生的主要原因包括既往盆腔炎性疾病史、輸卵管妊娠史或腹腔手術史、子宮內膜炎病史等。在輔助生殖技術(ART)過程中,因促排卵方案可使多個卵泡同時發育,超生理水平的雌激素會使子宮內膜容受性降低,從而增加EP風險。移植時,如果移植管頂端太靠近宮腔底部,可導致子宮異常收縮,降低胚胎在宮腔子宮內膜內種植的幾率,增加EP風險[6]。本例患者曾有雙側輸卵管積水史和EP史,行腹腔鏡下盆腔粘連松解術后左側輸卵管再次積水。雖行左側輸卵管封堵術,但子宮內膜炎癥亦可能與其宮角妊娠有關。有研究報道,存在輸卵管積水、子宮內膜炎的患者可能因某些炎癥因子的趨化作用,導致胚胎定植于子宮以外的位置形成EP[7],本例患者病史與之相似。另外,多個胚胎移植會增加該周期EP的風險,而單囊胚移植會大大降低EP的發生率[8]。人類胚胎是以囊胚的形式種植在子宮內膜后繼續發育。進行囊胚培養并選擇單囊胚移植,可在獲得較高種植率的同時降低EP發生率[9]。故現在越來越多的學者推薦在IVF-ET中選擇單囊胚移植。
CHP的治療方案不同于單純的EP。由于宮角部位解剖結構的特殊性,宮角妊娠一旦破裂,內出血較多,易導致失血性休克,因此無論選擇保守治療還是手術治療,都需在治療過程中密切注意出血情況,尤其是內出血情況。因宮角孕囊與宮內孕囊在解剖結構上相近,所以在處理宮角妊娠時需盡量減少對子宮的刺激,操作輕柔,避免引起強烈的子宮收縮致使宮內流產;同時應避免使用甲氨蝶呤等胚胎毒性藥物。治療過程中需密切進行彩超監測,一旦出現陰道出血、宮腔內出血或腹腔內出血,及時進行相應處理。
CHP的治療方法需個體化。因宮角處的內膜較正常子宮腔內的內膜薄,故宮角部胚胎往往在發育過程中發生自然流產或胚胎停育。Sentilhes等[10]報道了1例CHP,但宮角部妊娠無胎心,采用期待治療后,宮內妊娠維持到足月分娩。本例患者宮角處的單卵雙胎中其中一個無胎心,另一胎心搏動慢。胎心慢的胚胎可能會進一步發展為胚胎停育,可以考慮期待治療;但期待治療過程中,仍有異位包塊持續增長、破裂的風險。采用保守治療的患者多選擇經陰道B超引導下宮角妊娠減胎術,此項操作有較高的技術要求,屬四級手術,需由減胎經驗豐富的主任醫師進行操作。因宮角部包塊與宮內正常胚胎距離較近,推薦使用胚胎抽吸法,避免使用氯化鉀、甲氨蝶呤等殺胚藥,以免通過微循環影響宮內胎兒發育。需注意的是,保守治療后仍有宮角部包塊破裂出血的可能性,術后需嚴密監測B超。本例患者宮角妊娠為單卵雙胎,考慮到期待治療過程中仍有極大可能出現子宮破裂,故未選用期待治療,而是在做好腹腔鏡手術準備的前提下,行宮角妊娠減胎術。減胎術中發現宮角妊娠囊內出血,術后及時應用止血藥物,并嚴密監測B超,未有宮角繼續出血及腹腔內出血的情況。有文獻報道,保守治療組的活產率低于腹腔鏡或開腹手術治療組,流產率則比手術治療組高[5]。CHP的手術治療分為開腹手術和腹腔鏡手術,手術方式主要為宮角楔形切除術或宮角切開取胚術。對于病情穩定者可選用腹腔鏡手術,手術創傷較開腹手術小,預后好。對于包塊已經破裂、生命體征不平穩、失血性休克患者應選用開腹手術。采用宮角楔形切除術還是宮角切開取胚術,目前仍存在分歧。有學者認為,患側宮角楔形切除術會使子宮角部失去正常解剖結構,從而使孕期子宮破裂的風險增加,并對宮內妊娠的影響較大,流產率增加[11]。亦有學者認為,雖然宮角切開取胚術創傷小,但胚胎組織殘留可能會導致持續性EP包塊增大、破裂、出血甚至危及生命[12]。也有學者認為兩種方法均安全有效[13]。
本例患者孕12周時,B超檢查提示宮內胎兒發育良好,左側宮角處包塊較前增大,繼續嚴密監測。孕18周時宮角處包塊縮小。孕25周時彩超未探及異常包塊。對于CHP減胎術后是否能夠經陰道分娩目前尚有爭議。孫小麗等[13]統計該院5例宮內合并宮角/輸卵管間質部妊娠患者,1例因個人因素孕35+3周行剖宮產,余4例均孕足月行剖宮產,新生兒結局均良好。考慮到經陰道分娩可能增加子宮破裂風險,選擇剖宮產似乎更利于母兒安全,但仍需進一步分析探討。
綜上,隨著不孕癥患者增多,輔助生殖中心對促排卵藥物的使用越來越多,IVF-ET技術的應用越來越廣泛,隨之而來的是HP的發生率逐年上升。如何降低這一并發癥,成為生殖醫學領域亟需解決的問題。臨床工作中,對于有內膜炎性疾病的患者,建議先治療內膜炎性疾病;有輸卵管積水的患者,建議移植前先給予適當處理,必要時可以結扎或切除患側輸卵管;胚胎移植時建議進行囊胚培養并選擇單囊胚移植,以降低異位妊娠發生率;一旦發現HP,需盡早診斷、及時處理,并進行嚴密監測,避免出現包塊破裂危及患者生命;對于CHP,是選擇保守治療還是手術治療,需綜合評估患者病情后進行個體化決策。

