CEA,CA125,NSE,CYFRA21-1診斷肺癌的臨床價值
黃彩霞 周紹堅
摘要:目的 探討肺癌患者應用細胞角蛋白19片段21-1(CYFRA21-1)、神經元特異性烯醇化酶(NSE)、糖類抗原(CA125)、血清癌胚抗原(CEA)診斷的臨床價值。方法 將100例2019.1-2020.1收治的肺癌患者作為試驗組研究對象,另將同期于我院收治的100例肺良性病變患者作為參照組研究對象,對于所有患者均予以CYFRA21-1、NSE、CA125、CEA聯合診斷,對于腫瘤標志物水平進行對比分析。結果 試驗組CYFRA21-1、NSE、CA125、CEA水平均高于參照組,P<0.05。結論 肺癌患者應用CYFRA21-1、NSE、CA125、CEA進行聯合檢測,具有較高的陽性檢測效果,在提高臨床檢出率的同時,還可明顯劃分肺癌患者機體組織的分型,值得運用與推廣。
關鍵詞:血清癌胚抗原;糖類抗原;肺癌診斷;烯醇化酶
【中圖分類號】R563 【文獻標識碼】A 【文章編號】1673-9026(2022)03--01
目前,肺癌是世界死亡率以及發病率最高的一種惡性腫瘤[1]。肺癌起病往往較為隱匿,絕大多數患者在確診時,病情已處于中晚期階段,對患者生活質量已構成嚴重影響,威脅其生命安全[2]。組織病理學以及細胞學檢查是確診肺癌的主要方式,但該類檢查存在標本不易獲取以及創性取材等因素,故在臨床早期,對肺癌患者開展診斷工作時,具有一定難度,隨著免疫學在臨床中不斷發展血清腫瘤標志物被逐漸應用于肺癌早期診斷以及后期治療效果評價中,但單一腫瘤標志物在診斷肺癌中仍缺乏足夠的特異度與靈敏度,故臨床逐漸將單一標志物檢測改變為聯合檢測[3]。鑒于此,本文就肺癌患者應用細胞角蛋白19片段21-1(cytokeratin frangment 19,CYFRA21-1)、神經元特異性烯醇化酶(neuron-specifie enolase,NSE)、糖類抗原(caibo-hydrate antingen125,CA125)、血清癌胚抗原(carcinoem-bryonic antigen,CEA)檢測的臨床價值進行探討,闡述如下。
1資料與方法
1.1一般資料
納入我院2019.1-2020.1收治的100例肺癌患者作為試驗組,另將同期在我院進行常規體檢的100例肺良性病變患者作為參照組,試驗組男女各50例,年齡28-75歲,平均(46.56±1.27)歲;參照組男女各49、51例,年齡28-75歲,平均(46.48±1.21)歲。兩組基線資料對比無差異,P>0.05。本次研究均經我院倫理委員會批準同意。
納入標準:(1)所有患者均經組織學或細胞學確診[4];(2)患者基本資料與病歷資料完整;(3)行全身骨掃描以及腹部B超、腹部CT、頭顱、胸部等檢查[5];(4)以往未接受手術以及放化療;(5)經相關檢查無高血壓、充血性心力衰竭、肝腎功能不全、糖尿病等并發癥。
剔除標準:(1)不具備明確病理組織診斷者;(2)缺乏全身骨掃描或影像學檢查者;(3)存在其他嚴重的感染性或傳染性疾病者;(4)哺乳期或妊娠期者;(5)存在其他惡性腫瘤患者;(6)凝血功能障礙者;(7)存在干擾本次研究開展的相關因素者;(8)本次研究中途自行退出者。
1.2方法
均在清晨時取所有患者5ml靜脈血,以每分鐘2500r離心10min后將血清分離,放置冰箱(-80°)保存。使用新產業提供的配套試劑盒使用化學發光法進行測定,測定CEA、CA125、NSE、CYFRA21-1水平。
1.3觀察指標
分別檢測兩組血清水平(CYFRA21-1、NSE、CA125、CEA)。判定標準:陽性標準超過參考值范圍,當檢測值大于參考范圍時便可判斷為陽性。在上述腫瘤標志物中若檢測出任何一項則均作為陽性診斷結果。各指標參考范圍:CYFRA21-1(0.00-3.30ng/mL)、NSE(<20.0ng/mL)、CA125(35U/mL)、CEA(0.00-5.00ng/mL)。
1.4統計學處理
采用SPSS22.0統計軟件對所得數據進行分析處理,計量資料用(x±s)表示,t檢驗,以P<0.05為差異具有統計學意義。
2結果
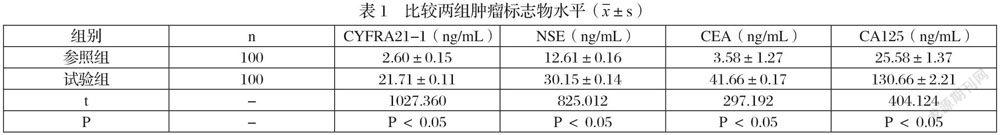
試驗組CEA、PROGRP、CYFRA21-1、NSE、SCC水平均高于參照組,P<0.05,見表1。
3討論
隨著人們生活水平逐漸提高,健康體檢已被廣泛普及至日常生活中,肺癌死亡率與發病率通過健康體檢得到明顯降低,但仍存在居高不下的現象[6]。肺癌患者在病發初期,因臨床癥狀較為隱匿,極易出現誤診與漏診的現象,導致患者錯過最佳治療時機。隨著臨床免疫學的不斷發展,肺癌普查已將腫瘤標志物作為其首選項目,篩查單一的腫瘤標志物對臨床癥狀具有一定應用價值,但特異度與靈敏度較低,無法早期診斷肺癌,同樣能夠造成漏診。故此,無法滿足臨床對診療的需求。
通過采用CYFRA21-1、NSE、CA125、CEA四種腫瘤標志物聯合檢測,可有效提高臨床檢出肺癌的概率,為患者初步診斷以及后期治療提供依據[7]。單一腫瘤標志物往往在檢測過程中,僅僅只能檢測出某種類型肺癌,若類型不符便會出現漏診。臨床只有將各類腫瘤標志物聯合檢測方能同時檢測出患者肺癌類型,以此降低臨床漏診率與靈敏度。本次研究結果表明,試驗組CYFRA21-1、NSE、CA125、CEA腫瘤標志物水平均高于參照組,P<0.05。表明肺癌患者各項水平均高于正常人群,通過四種腫瘤標志物水平可直接反映出患者疾病陽性與陰性,同時可通過上述指標判斷患者肺癌嚴重程度,為后期治療提供實際性的理論依據。與此同時,相關研究表明[8],CYFRA21-1、NSE、CA125、CEA單獨對肺癌患者加以檢測,發現以CYFRA21-1敏感度最高,以CA125特異度最高。由此揭示在多項聯合檢測中,隨著聯合檢測的指標不斷增加,其敏感性隨之增加,特異性可逐漸降低,各項聯合檢測中以含有CYFRA21-1敏感度較好,以結合CA125特異度較好。臨床在對血清腫瘤標志物進行單項檢測中,可發現不同肺癌病理存在一定的靈敏度,但其價值相對有限,而CEA檢測應用于肺癌診斷中價值最高,尤其在肺腺癌中具有較高的提示價值,但其特異度較低。將腫瘤標志物開展聯合檢測的應用價值往往要遠高于任何一項單一檢測。故CYFRA21-1、NSE、CA125、CEA四種腫瘤標志物聯合檢測能夠作為體檢篩查或高危人群的指標。
綜上所述,肺癌患者應用CYFRA21-1、NSE、CA125、CEA四種腫瘤標志物聯合檢測,不僅能夠便于臨床醫師有效判斷,還能夠為患者疾病預后以及治療方案提供幫助,臨床應用價值較高。
參考文獻:
[1]丁運生,林雨虹,楊靜,等. 血清CYFRA21-1、NSE、CEA、CA125及SCCA聯合檢測在肺癌診斷中的價值研究[J]. 中國腫瘤外科雜志,2020,12(5):460-464.
[2]南陽光,周俊. CEA、CYFRA21-1、NSE、CA125聯合檢測在肺癌診斷中的應用效果[J]. 實用癌癥雜志,2018,33(4):527-529.
[3]張穎,董秀鵬,杜靜,等. 腫瘤標志物CYFRA21-1、SCC、CEA、NSE、CA125檢驗在肺癌診斷中的價值[J]. 現代腫瘤醫學,2018,26(11):1701-1703.
[4]劉濤,楊燕,劉博,等. 聯合檢測胸腹腔積液sCD44V6,CEA,CYFRA21-1,CA199,NSE,CA125對良惡性疾病鑒別診斷價值研究[J]. 現代檢驗醫學雜志,2020,35(2):53-55,64.
[5]龔紅娟,蔡錦洪,龔菊蘭. 血清CYFRA21-1、CEA、NSE、CA199、CA125聯合檢測在肺癌診斷中的價值[J]. 貴州醫藥,2019,43(3):450-453.
[6]黃芳,薛麗,宋琳嵐,等. 胸水和血清CEA、CA125、CYFRA21-1、NSE和Pro-GRP聯合檢測對肺癌的診斷價值[J]. 現代腫瘤醫學,2018,26(13):2054-2058.
[7]趙虹,紀秋野,王博揚. 流式熒光發光法聯合檢測肺癌患者血清CEA、CYFRA21-1、CA125及NSE的性能評價[J]. 中國實驗診斷學,2019,23(8):1434-1437.
[8]陳一超,輦偉奇,冉靜,等. 腫瘤標志物聯合檢測對肺癌診斷、病理分型和臨床分期的臨床價值[J]. 國際檢驗醫學雜志,2018,39(1):32-37.
3134500589272

