介孔Fe2O3/SiO2催化乙酸和環己醇酯化反應條件的研究*
朱慧鑫,覃 利,張凱洋,李春梨,張銀海,懷敬龍,劉曉雪,李顥**
(1.長江大學 化學與環境工程學院,湖北 荊州 434023;2.長江大學 農學院,湖北 荊州 434000)
乙酸環己酯是無色透明液體,具有蘋果香氣,是很好的有機溶劑和香料,廣泛用于軟飲料、冰淇淋、冰制食品糖果和烘烤食品中,也常用作涂料、油漆的溶劑等[1-2]。目前,工業上常用乙酸和環己醇為原料,濃硫酸為催化劑合成乙酸環己酯。但是,這種方法存在產品質量差、設備腐蝕嚴重、后處理工藝復雜、污染環境等缺點[3]。
固體酸催化劑的獨特優勢主要表現在固體酸催化劑對設備的腐蝕性小,易于分離回收,高溫穩定性好,可以活化再生,減少了廢棄物的排放,便于化工連續操作,是一種環境友好型催化劑[4-5]。目前,固體酸的種類有沸石、金屬氧化物、硫酸化金屬氧化物、雜多化合物、碳基固體酸、陽離子交換樹脂、固載化液體酸和天然黏土等[6]。
最近,我們課題組制備了一系列不同Fe含量的介孔Fe2O3/SiO2催化劑,采用乙酸和環己醇的酯化反應評價了樣品的催化性能,篩選出較合適的Fe/Si物質的量比為0.71[7]。本文以介孔Fe2O3/SiO2[n(Fe)/n(Si)=0.71]為催化劑,研究了反應條件對酯化反應的影響,并篩選出了較合適的反應條件。
1 實驗部分
1.1 實驗試劑和儀器
正硅酸四乙酯,吐溫40(T-40),九水合硝酸鐵,鹽酸,無水乙醇,硫酸,冰乙酸,環己醇,乙酸環己酯,環己烷,氫氧化鈉,均為分析純。
磁力攪拌器,電熱恒溫鼓風干燥器,箱式馬弗爐,三口燒瓶,分水器,球形冷凝管,恒溫磁力攪拌器。
1.2 介孔Fe2O3/SiO2催化劑的制備
介孔Fe2O3/SiO2[n(Fe)/n(Si)=0.71]催化劑的制備步驟,詳見參考文獻[7-8]。
1.3 酯化反應
乙酸和環己醇的酯化反應在一個裝有分水器和回流冷凝管的三口燒瓶中進行,磁力攪拌,恒溫油浴加熱。典型的反應條件為:環己醇 12.0 mL,乙酸 4.7 mL(環己醇/乙酸物質的量比為1.4),帶水劑 6.0 mL,催化劑 0.4 g,反應溫度 140 ℃,反應時間 4 h。反應結束后,采用酸堿滴定法分析反應液中乙酸的含量,酯化率的計算公式為:
酯化率=(V0-Vt)/V0×100%
式中,V0和Vt分別為反應初始和結束時取樣滴定所消耗標準NaOH溶液(0.50 mol/L)的體積(mL)。
2 結果與討論
2.1 催化劑的表征
在前面的報道中,采用了XRD、UV-Vis和氮氣吸附-脫附等溫線的手段對Fe2O3/SiO2[n(Fe)/n(Si)=0.71]催化劑進行了表征。結果表明,介孔Fe2O3/SiO2[n(Fe)/n(Si)=0.71]催化劑樣品中存在菱方結構的Fe2(SO4)3和α-Fe2O3,Fe3+主要是以四配位或者六配位的狀態存在,催化劑的比表面積和介孔體積分別為 208.4 m2/g 和 0.30 cm3/g[7]。
2.2 乙酸和環己醇酯化反應條件的優化
2.2.1 環己醇/乙酸物質的量對乙酸和環己醇酯化反應的影響
采用介孔Fe2O3/SiO2為催化劑,研究了其催化乙酸和環己醇的酯化反應。在固定其它反應條件不變的情況下(環己醇 12.0 mL,帶水劑 6.0 mL,催化劑 0.4 g,反應溫度 130 ℃,反應時間 4 h。),考察了環己醇/乙酸物質的量對酯化反應的影響,結果見圖1。
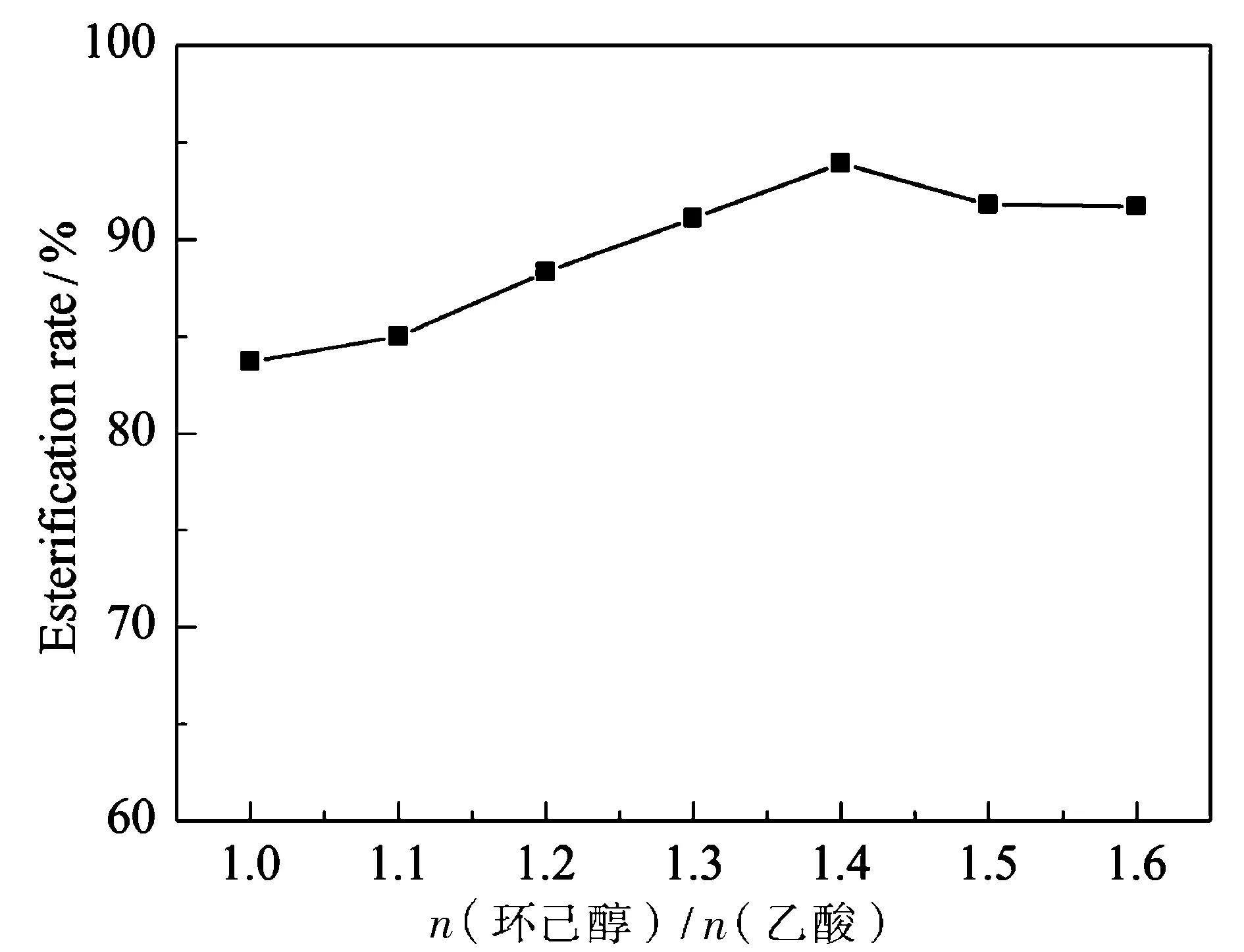
圖1 環己醇/乙酸物質的量比對Fe2O3/SiO2 催化乙酸和環己醇酯化反應的影響
2.2.2 催化劑用量對乙酸和環己醇酯化反應的影響
在研究了環己醇/乙酸物質的量比對乙酸和環己醇酯化反應影響的基礎上,考察了催化劑用量對酯化反應的影響,結果見圖2。不加催化劑進行反應時,酯化率為45.7%,說明乙酸和環己醇在催化劑不存在時可以進行酯化反應,不過其酯化率較低。加入 0.2 g 催化劑后,酯化率突然增加,說明催化劑的加入,對酯化反應起到很明顯的促進作用。隨著催化劑加量從 0.2 g 增加到 0.4 g,酯化率緩慢增加;繼續增大催化劑用量,酯化率無明顯變化。因此,較合適的催化劑用量為 0.4 g。
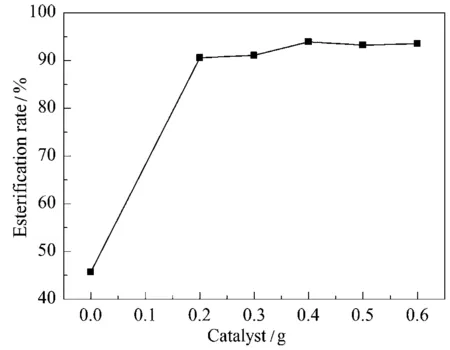
圖2 催化劑用量對Fe2O3/SiO2催化乙酸和環己醇酯化反應的影響
2.2.3 反應溫度對乙酸和環己醇酯化反應的影響
在研究了環己醇/乙酸物質的量比和催化劑用量對乙酸和環己醇酯化反應影響的基礎上,繼續考察了反應溫度對酯化反應的影響,結果見圖3。當反應溫度為 100 ℃ 時,酯化率為73.5%;隨著反應溫度從 100 ℃ 升高至 140 ℃,酯化率迅速增加至96.5%;繼續升高反應溫度,酯化率變化不大,且有可能發生副反應。因此,較合適的反應溫度為 140 ℃。
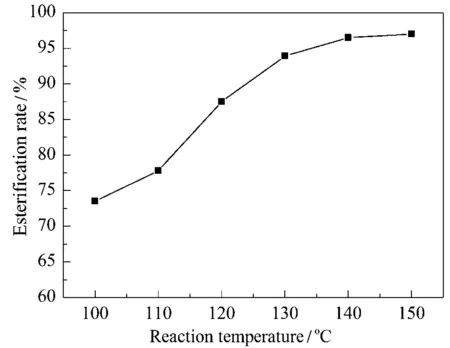
圖3 反應溫度對Fe2O3/SiO2催化乙酸和環己醇酯化反應的影響
2.2.4 帶水劑用量對乙酸和環己醇酯化反應的影響
在研究了環己醇/乙酸物質的量比、催化劑用量和反應溫度對乙酸和環己醇酯化反應影響的基礎上,繼續考察了帶水劑用量對酯化反應的影響,結果見圖4。由圖4可見,不加帶水劑時,Fe2O3/SiO2給出了92.0%的酯化率,說明乙酸和環己醇的酯化反應也可以進行。不過,加入帶水劑環己醇后,酯化率增加。當帶水劑的用量從 3.0 mL 增加到 6.0 mL 時,催化劑的酯化率逐漸增大至96.5%;繼續增大帶水劑的加量,酯化率突然降低。可能是帶水劑用量過多導致反應體系溫度降低,使得反應平衡常數降低[9]。因此,較合適的帶水劑用量為 6.0 mL。
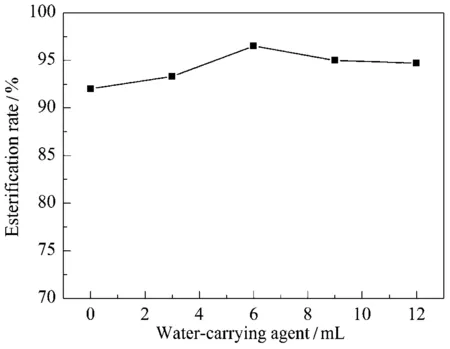
圖4 帶水劑用量對Fe2O3/SiO2催化乙酸和環己醇酯化反應的影響
2.2.5 反應時間對乙酸和環己醇酯化反應的影響
在研究了環己醇/乙酸物質的量比、催化劑用量、反應溫度和帶水劑用量對乙酸和環己醇酯化反應影響的基礎上,繼續考察了反應時間對酯化反應的影響,結果見圖5。當反應時間為 1 h 時,Fe2O3/SiO2給出了87.6%的酯化率。隨著反應時間的從 1 h 增加到 4 h,酯化率逐漸增加;繼續延長反應時間,酯化率變化不大。因此,較合適的反應時間為 4 h。
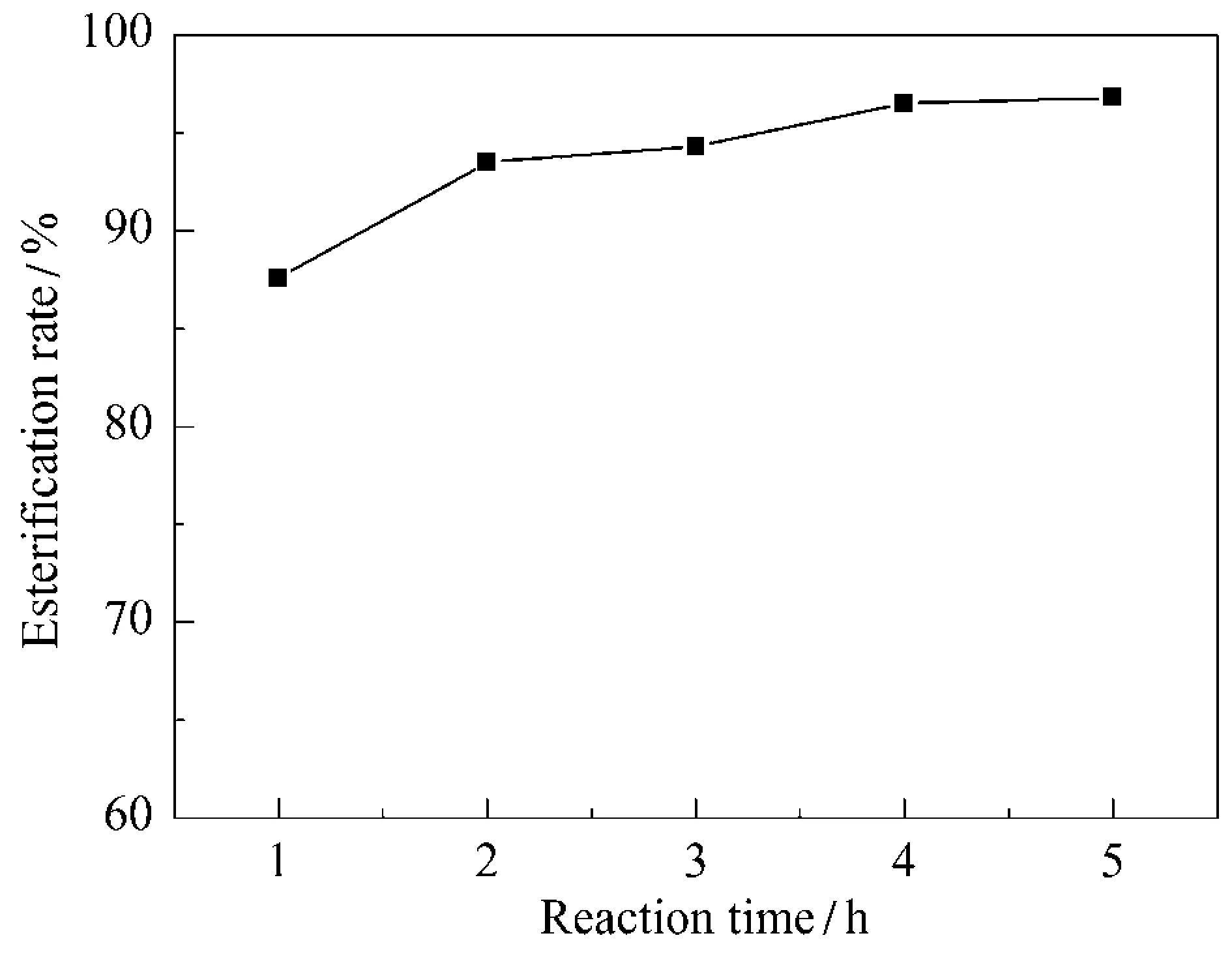
圖5 反應時間對Fe2O3/SiO2催化乙酸和環己醇酯化反應的影響
3 結論
采用介孔Fe2O3/SiO2[n(Fe)/n(SiO2)=0.714]為催化劑,詳細考察了環己醇/乙酸的物質的量比、催化劑用量、反應溫度、帶水劑用量和反應時間對酯化反應的影響。較優化的反應條件為:環己醇 12.0 mL,乙酸 4.7 mL,環己醇/乙酸物質的量比為1.4,帶水劑 6.0 mL,催化劑 0.4 g,反應溫度 140 ℃,反應時間 4 h。在優化的條件下,酯化率可達96.5%。本研究將為乙酸環己酯的工業化生產提供一定的參考。

