TIC參數(shù)定量評(píng)估強(qiáng)力霉素改善失血性休克液體復(fù)蘇期腎再灌注損傷*
羅燁 李明星 陳曉梅 朱雨潔 何婧
(西南醫(yī)科大學(xué)附屬醫(yī)院超聲醫(yī)學(xué)科,四川 瀘州 646000)
失血性休克是臨床常見的急危重癥,是全身炎癥和器官損傷的主要驅(qū)動(dòng)因素,腎臟常因失血性休克的強(qiáng)烈影響造成急性腎損傷;治療失血性休克首選方法即為補(bǔ)液,以便盡快恢復(fù)血容量,而腎臟損傷反而加重,這種病理現(xiàn)象稱為失血性休克再灌注損傷(Hemorrhagic shock and reperfusion injury,HS-RI)[1]。研究[2-3]表明,強(qiáng)力霉素是四環(huán)素類藥物,除具有抗菌作用外,也能改善失血性休克復(fù)蘇后的腎損傷。本研究擬通過制備SD大鼠急性重度失血性休克液體復(fù)蘇期模型,使用超聲造影TIC參數(shù)評(píng)估強(qiáng)力霉素改善失血性休克復(fù)蘇期再灌注損傷后腎皮質(zhì)血流灌注的改變,分析TIC參數(shù)與實(shí)驗(yàn)室指標(biāo)的相關(guān)性,探討TIC參數(shù)在評(píng)估強(qiáng)力霉素治療腎HS-RI的應(yīng)用價(jià)值。
1 材料與方法
1.1 實(shí)驗(yàn)動(dòng)物及分組 SPF級(jí)雄性SD大鼠24只,8~10周齡,體質(zhì)量(300±50)g,由成都達(dá)碩實(shí)驗(yàn)動(dòng)物有限公司提供,許可證號(hào)SCXK(川)2020-03,于恒溫動(dòng)物房(25℃)適應(yīng)性喂養(yǎng)7天,自由進(jìn)食飲水,術(shù)前6 h禁食禁飲。隨機(jī)將大鼠分為假手術(shù)組(Sham組)、失血性休克再灌注組(HS-RI組)和強(qiáng)力霉素干預(yù)組(Dox組),每組8只。Dox組于術(shù)前30 min給予10 mg/kg強(qiáng)力霉素經(jīng)尾靜脈注入,Sham組及HS-RI組注入等量生理鹽水。本研究獲得醫(yī)院倫理委員會(huì)批準(zhǔn)。
1.2 動(dòng)物模型建立 腹腔注射肝素鈉溶液 (10 mg/kg)全身肝素化,15 min后腹腔注射10%水合氯醛(3 mL/kg)麻醉大鼠,頸部及右側(cè)腹股溝區(qū)備皮,仰臥位固定,用鑷子牽出鼠舌,防止舌后綴,碘伏消毒備皮區(qū)域。沿頸部正中切開皮膚,逐層鈍性分離,游離出左側(cè)頸總動(dòng)脈,置入20G 留置針并固定,經(jīng)三通管連接生物多導(dǎo)生命監(jiān)測(cè)儀,待顯示屏上血壓曲線穩(wěn)定時(shí),記錄此時(shí)的數(shù)值作為原始平均動(dòng)脈壓(Mean arterial pressure,MAP)。以同樣的方法分離出右側(cè)股總動(dòng)脈,置入24G留置針作為放血通道,放血至40% MAP,維持 1 h,建立重度失血性休克定壓模型,左側(cè)股總靜脈置入24G留置針作為補(bǔ)液通道,復(fù)蘇液為2:1的乳酸鈉林格注射液和羥乙基淀粉130/0.4氯化鈉注射液,通過補(bǔ)液通道輸入復(fù)蘇液至血壓回升至80%MAP,再灌注模型建立成功,拔管、結(jié)扎血管,縫合皮膚,術(shù)后大鼠清潔飼養(yǎng),自由飲水進(jìn)食。Sham組未行放血及補(bǔ)液處理,其他手術(shù)操作與兩組相同。
1.3 超聲造影檢查 所有大鼠于術(shù)后24 h后水合氯醛麻醉,右側(cè)腎區(qū)及左側(cè)腹股溝區(qū)剃毛并固定。分離出左側(cè)股總靜脈并置入24G留置針,建立推注超聲造影劑通道。采用Siemens ACUSON S3000 超聲診斷儀,9L4變頻線陣探頭,在二維模式下掃查右腎,將探頭置于最大冠狀切面,轉(zhuǎn)換為造影模式,設(shè)置相關(guān)參數(shù):頻率5.0MHz,深度4.0 cm,機(jī)械指數(shù)(MI)0.07,超聲造影劑采用sonovue,使用5 mL生理鹽水配置成六氟化硫(SF6)微泡混懸液,經(jīng)左側(cè)股總靜脈置管按0.4 mL/kg劑量團(tuán)注,隨即注入0.5 mL生理鹽水沖管,連續(xù)觀察右腎造影3 min,并保存動(dòng)態(tài)圖像。通過超聲診斷儀內(nèi)置分析軟件(Auto tracking contrast quantification,ACQ)進(jìn)行定量分析,選取同一深度、與聲束垂直、面積為0.05 mm2的腎皮質(zhì)區(qū)中份為感興趣區(qū)域(ROI),繪制時(shí)間-強(qiáng)度曲線(Time-intensity curve,TIC)并獲取相關(guān)參數(shù),包括峰值強(qiáng)度(peak intensity,Peak)、達(dá)峰時(shí)間(Time to peak,TP)、曲線下面積(Area under the curve,AUC)及平均渡越時(shí)間(Mean transition time,MTT)。所有參數(shù)由同一操作者測(cè)量3次,取平均值。
1.4 腎功能檢查 超聲造影結(jié)束后,通過下腔靜脈取血3 mL,離心后取上層血清,用于檢測(cè)血肌酐(Creatinine,Crea)及尿素氮(Urea nitrogen,Urea)水平。
1.5 病理學(xué)檢查 取血結(jié)束后,經(jīng)左側(cè)股總靜脈置管注入空氣處死大鼠,迅速取大鼠右腎組織,沿冠狀面均分為兩份,一份用10%中性甲醛固定液固定,石蠟包埋,切片后行HE染色,鏡下觀察病理形態(tài)改變;另一份用ELISA法檢測(cè)基質(zhì)金屬蛋白酶-2(Matrix metalloproteinase-2,MMP-2)、基質(zhì)金屬蛋白酶-9(Matrix metalloproteinase-9,MMP-9)及腫瘤壞死因子-α(Tumor necrosis factor-α,TNF-α)水平。
2 結(jié)果
2.1 各組大鼠超聲造影TIC及相關(guān)參數(shù)比較 通過對(duì)3組大鼠超聲造影繪制TIC整體分析可見,Sham組TIC上升快速達(dá)峰,達(dá)峰后快速下降至基礎(chǔ)水平;HS-RI組及Dox組TIC上升至峰值及下降較Sham組明顯減慢;Dox組TIC較HS-RI組上升及下降均有明顯增快,見圖1。與Sham組比較,HS-RI組和Dox組的Peak、AUC增加,TP、MTT延長(zhǎng)(P<0.05);與HS-RI組比較,Dox組Peak、AUC減小,TP、MTT縮短(P<0.05),見表1。
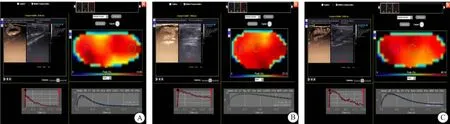
圖1 各組大鼠腎皮質(zhì)血流灌注TIC圖Figure 1 TIC diagram of renal cortical blood perfusion in each group注:A.Sham組;B.HS-RI組;C.Dox組

表1 各組大鼠腎皮質(zhì)TIC參數(shù)比較Table 1 Comparison of TiC parameters in renal cortex of rats in each group
2.2 各組大鼠腎功能結(jié)果比較 與Sham組比較,HS-RI組和Dox組的血Crea及Urea水平升高(P<0.05);與HS-RI組比較,Dox組Crea及Urea水平降低(P<0.05),見表2。

表2 各組大鼠Crea及Urea比較Table 2 Comparison of Crea and Urea of rats in each group
2.3 各組大鼠腎組織MMP-2、MMP-9和TNF-α水平 與Sham組相比,HS-RI組和Dox組大鼠腎組織勻漿中的MMP-2、MMP-9及TNF-α水平升高,除Dox組中的MMP-9水平比較差異無統(tǒng)計(jì)學(xué)意義,余指標(biāo)經(jīng)較差異均有統(tǒng)計(jì)學(xué)意義(P<0.05)。與HS-RI組相比,Dox組中的MMP-2、MMP-9及TNF-α水平降低(P<0.05)。見表3。

表3 各組大鼠腎組織MMP-2、MMP-9和TNF-α水平比較Table 3 Comparison of MMP-2,MMP-9 and TNF-α in renal tissue of rats in each group
2.4 TIC參數(shù)與實(shí)驗(yàn)室指標(biāo)相關(guān)性分析 TP、MTT及AUC與Crea、Urea、MMP-2及TNF-α呈高度正相關(guān)(P<0.05);TP、MTT及AUC與MMP-9呈中度正相關(guān);Peak與Crea、Urea、MMP-2、MMP-9及TNF-α呈中度正相關(guān)(P<0.05),見表4。
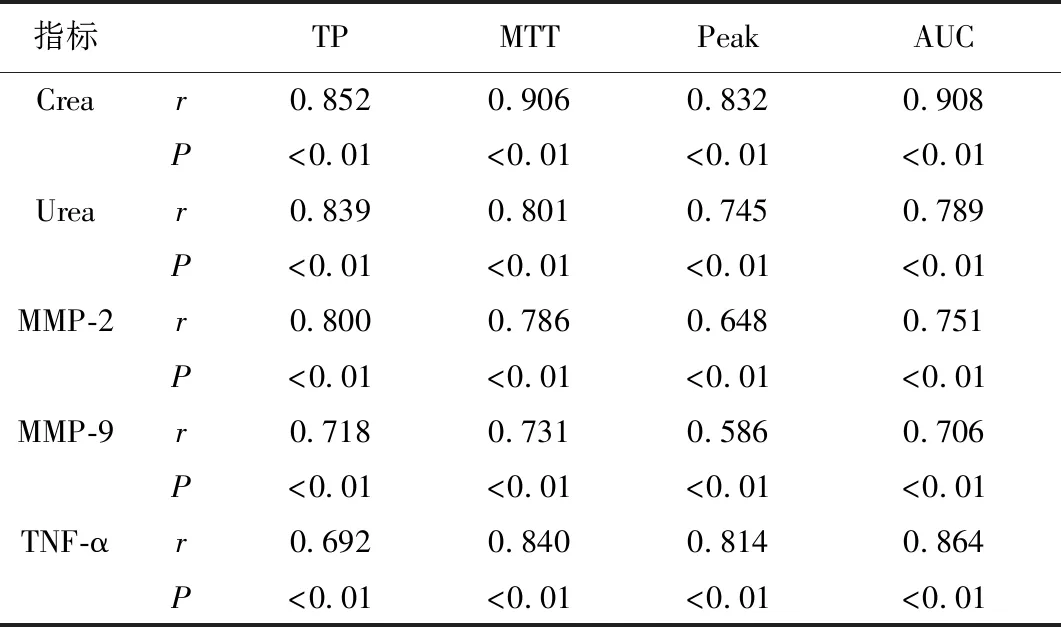
表4 TIC參數(shù)與實(shí)驗(yàn)室指標(biāo)相關(guān)性分析Table 4 Correlation between TIC parameters and laboratory indexes
2.5 病理結(jié)果 Sham組腎皮質(zhì)腎小球結(jié)構(gòu)完整清晰,腎小管排列整齊,未見變性或壞死,間質(zhì)無異常改變;HS-RI組部分腎小管上皮細(xì)胞腫脹、壞死,局部腎小管內(nèi)可見蛋白管型,間質(zhì)內(nèi)可見少許炎細(xì)胞浸潤(rùn);Dox組部分腎小管上皮細(xì)胞腫脹、空泡樣變,間質(zhì)偶見少許炎細(xì)胞浸潤(rùn),見圖2。
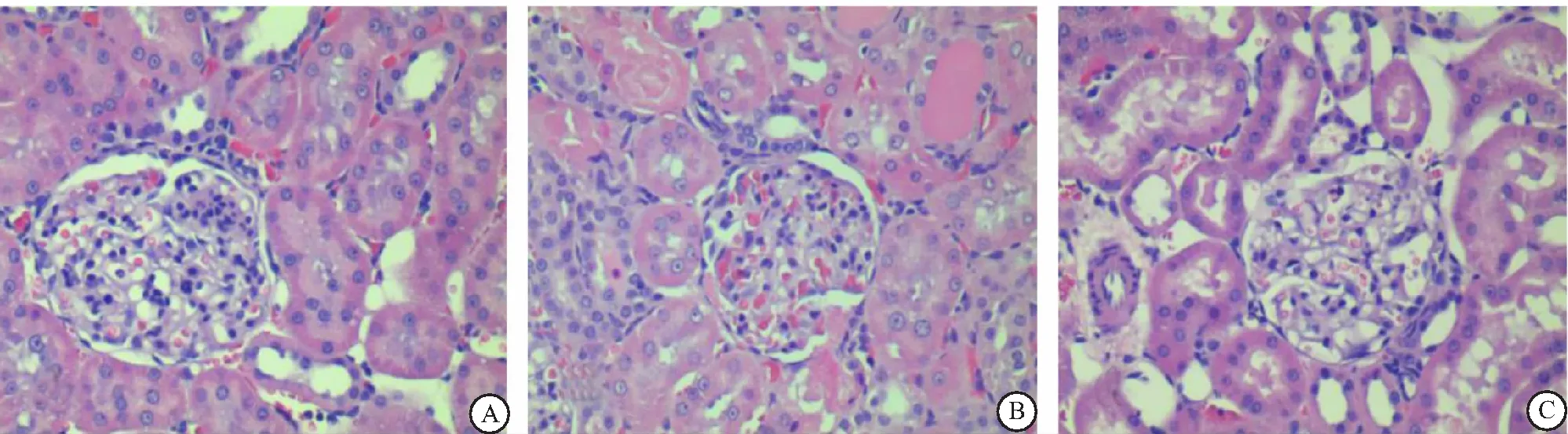
圖2 各組大鼠腎臟病理圖(200×)Figure 2 Renal pathology of rats in each group注:A.Sham組;B.HS-RI組;C.Dox組
3 討論
失血性休克是一種低血容量性休克,全球每年估計(jì)有190萬人死亡,其中150萬人死于身體創(chuàng)傷,導(dǎo)致休克的出血原因差異很大,包括創(chuàng)傷、產(chǎn)婦出血、胃腸道出血、圍手術(shù)期出血和動(dòng)脈瘤破裂等[4]。盡管通過液體復(fù)蘇恢復(fù)了血流動(dòng)力學(xué),但失血性休克和復(fù)蘇后可能發(fā)展為系統(tǒng)性炎癥反應(yīng)綜合征(Systemic inflammatory response syndrome,SIRS),導(dǎo)致多器官損傷和功能障礙即多器官功能障礙綜合征(Multiple organ dysfunction syndrome,MODS)。腎臟血供豐富,缺乏側(cè)枝循環(huán),再灌注過程更易損傷。腎臟血流動(dòng)力學(xué)的改變可影響腎功能,腎皮質(zhì)的血流灌注量占腎血流量的90%,因此檢測(cè)腎皮質(zhì)血流灌注的變化可以間接反映腎損傷程度[5-6]。超聲造影技術(shù)能動(dòng)態(tài)檢測(cè)宏觀血流及微循環(huán)改變[7],目前有許多文獻(xiàn)報(bào)道了超聲造影技術(shù)鑒別在甲狀腺結(jié)節(jié)、肝腫物、前列腺結(jié)節(jié)等良惡性的應(yīng)用,超聲造影能顯示腫瘤內(nèi)微血管的分布圖像,獲得關(guān)于細(xì)小血管的相關(guān)信息[8-10]。超聲造影劑SonoVue主要成分是SF6微泡,直徑1~5 μm,不含人體蛋白成分,在血液中穩(wěn)定性好,能進(jìn)入各組織器官的毛細(xì)血管網(wǎng),不進(jìn)入組織間隙,15 min幾乎全部經(jīng)呼吸排除,不經(jīng)肝腎代謝,無肝腎禁忌,是理想的血池顯像劑。與核醫(yī)學(xué)、MRI及CT等檢查技術(shù)比較,超聲造影技術(shù)評(píng)估組織血流灌注具有操作簡(jiǎn)單、重復(fù)性好、費(fèi)用低、無放射性及腎毒性等優(yōu)勢(shì)。
TP反映造影劑開始注入至峰值強(qiáng)度的時(shí)間,MTT反映了造影劑開始注入至廓清到峰值強(qiáng)度一半的時(shí)間。HS-RI的主要機(jī)制與炎癥反應(yīng)、細(xì)胞凋亡、微循環(huán)障礙、鈣超載等有關(guān)[11-14],HS-RI發(fā)生后在過量的氧自由基、TNF-α、IL1-β等誘發(fā)下,內(nèi)皮細(xì)胞、成纖維細(xì)胞及白細(xì)胞等細(xì)胞內(nèi)MMP-2和MMP-9表達(dá)上調(diào),導(dǎo)致毛細(xì)血管內(nèi)皮功能障礙、破壞毛細(xì)血管基底膜與內(nèi)皮細(xì)胞的緊密連接及降解細(xì)胞外基質(zhì),使血漿向組織間隙滲出,引起血液濃縮,造成血流的粘滯狀態(tài)[15-17];同時(shí)MMP-2和MMP-9進(jìn)一步激活的炎癥因子如IL-1、TNF-α、TGF-β等大量釋放,加劇炎癥反映,導(dǎo)致內(nèi)皮細(xì)胞上黏附大量白細(xì)胞,引起腎皮質(zhì)微循環(huán)障礙[18],造成了腎皮質(zhì)血流灌注減慢。因此超聲造影微泡在腎皮質(zhì)中的灌注速度和廓清速度減慢,在TIC參數(shù)上表現(xiàn)為TP與MTT延長(zhǎng)。AUC是反映ROI內(nèi)一段時(shí)間內(nèi)的造影劑累積總積分值,HS-RI導(dǎo)致大量炎癥細(xì)胞淤積于毛細(xì)血管內(nèi),炎癥細(xì)胞對(duì)造影劑微泡有一定的吞噬作用,被吞噬的造影劑保持聲學(xué)活性可被檢測(cè),而且造影劑微泡廓清速度的減慢,因此TIC參數(shù)表現(xiàn)為AUC值增大[19]。Peak代表了ROI中造影劑達(dá)到峰值時(shí)的信號(hào)強(qiáng)度,與造影劑微泡的灌注速度、廓清速度及炎癥細(xì)胞的吞噬作用有關(guān),在TIC參數(shù)中Peak值也表現(xiàn)為增大。研究表明,作為外源性的基質(zhì)金屬蛋白酶抑制劑,強(qiáng)力霉素可以改善腎HS-RI引起的炎癥反應(yīng)、氧化應(yīng)激及細(xì)胞凋亡,最重要的是能降低MMP-2和MMP-9的含量與活性[20-22]。Peak值作為反映造影劑達(dá)到峰值時(shí)的信號(hào)強(qiáng)度的瞬時(shí)指標(biāo),無不明顯累積效應(yīng),不能較好反映藥物干預(yù)前后腎皮質(zhì)血流灌注的改變,因此Peak值不能作為評(píng)估腎皮質(zhì)血流灌注變化的參數(shù)[23]。強(qiáng)力霉素對(duì)MMP-2和MMP-9的抑制可以改善內(nèi)皮細(xì)胞功能障礙、維持毛細(xì)血管基底膜完整及降低微循環(huán)阻力,使得腎皮質(zhì)血流灌注得以改善,因此造影劑微泡在腎皮質(zhì)中的灌注及廓清速度增快,在Dox組TIC參數(shù)上表現(xiàn)為TP和MTT縮短,同時(shí)強(qiáng)力霉素能改善炎癥反應(yīng),降低炎癥細(xì)胞對(duì)超聲造影劑的吞噬作用,故在TIC參數(shù)上表現(xiàn)為AUC及Peak值的降低。本研究結(jié)果表明,HS-RI組大鼠腎皮質(zhì)血流灌注出現(xiàn)明顯改變,與Shams組相比,在TIC參數(shù)上表現(xiàn)為TP、MTT延長(zhǎng),Peak、AUC增加,這與孫曉穎等[24]的實(shí)驗(yàn)結(jié)果一致。
血清Crea和Urea指標(biāo)作為臨床工作中常用的評(píng)估腎臟功能指標(biāo),但腎臟的代償能力強(qiáng),在腎損傷早期Crea和Urea依然能維持在正常水平[25]。超聲造影可以更敏感、精確地反映急性腎損傷早期腎臟血流灌注狀態(tài),因此超聲造影相關(guān)參數(shù)在腎損傷早期就會(huì)出現(xiàn)改變[26],在反映腎功能改變較血清Crea和Urea具有更高靈敏度。本研究中HS-RI組病理組織切片表現(xiàn)為部分腎小管上皮細(xì)胞腫脹、壞死,蛋白管型及炎細(xì)胞浸潤(rùn),血清Crea及Urea水平較Sham組明顯升高(P<0.05),腎組織勻漿中MMP-2、MMP-9及TNF-α水平也較Sham組升高(P<0.05);Dox組病理表現(xiàn)為部分腎小管上皮細(xì)胞腫脹、空泡樣變,偶見少許炎細(xì)胞浸潤(rùn),Crea、Urea、MMP-2、MMP-9及TNF-α等指標(biāo)較HS-RI組顯著改善(P<0.05)。病理及實(shí)驗(yàn)室指標(biāo)結(jié)果證實(shí)強(qiáng)力霉素對(duì)失血性休克液體復(fù)蘇后的腎再灌注損傷有保護(hù)作用。將TIC參數(shù)與Crea、Urea、MMP-2、MMP-9及TNF-α等指標(biāo)進(jìn)行Pearson相關(guān)性分析發(fā)現(xiàn),各TIC參數(shù)與腎功能指標(biāo)Crea及Urea呈顯著正相關(guān)(P<0.01),即Crea及Urea值越高,各TIC參數(shù)值越大;各TIC參數(shù)與MMP-2、MMP-9及TNF-α也呈顯著正相關(guān)(P<0.01),即MMP-2、MMP-9及TNF-α值越高,各TIC參數(shù)值越大,這表明各TIC參數(shù)與各實(shí)驗(yàn)室指標(biāo)間具有很強(qiáng)的平行性,TIC參數(shù)能在一定程度上反映腎功能變化。
有研究[2]報(bào)道,強(qiáng)力霉素在急性失血性休克液體復(fù)蘇之前和之后給予有相似的保護(hù)作用,具有減輕出血后腎損害的臨床療效。在本研究中,強(qiáng)力霉素在復(fù)蘇前給予,實(shí)驗(yàn)結(jié)果也顯示了強(qiáng)力霉素對(duì)腎臟的保護(hù)作用。本實(shí)驗(yàn)不足之處:①動(dòng)物樣本量相對(duì)較少。②本實(shí)驗(yàn)通過麻醉及全身肝素化建立的重度失血性休克液體復(fù)蘇模型與實(shí)際臨床情況有所出入。③僅選擇24 h一個(gè)時(shí)間點(diǎn)作為研究較為局限。目前這類實(shí)驗(yàn)研究較少,若想確定診斷腎功能損傷程度的TP、MTT及AUC的有效閾值,則還需進(jìn)一步的研究。
4 結(jié)論
強(qiáng)力霉素可以減輕失血性休克液體復(fù)蘇后腎功能損傷,改善腎皮質(zhì)血流灌注,超聲造影TIC參數(shù)如TP、MTT與AUC可定量評(píng)估藥物干預(yù)前后腎皮質(zhì)血流灌注變化情況,有望為臨床早發(fā)現(xiàn)、早干預(yù)該類疾病提供一種新的方法。

