過表達PnSMO1.1基因顯著增強裂葉牽牛耐鹽性
唐 龍,趙宇瑋
(1.西安交通大學(xué) 人居環(huán)境與建筑工程學(xué)院,陜西 西安 710049;2.西北大學(xué) 生命科學(xué)學(xué)院,陜西 西安 710069;3.陜西省生物技術(shù)重點實驗室,陜西 西安 710069)
大多數(shù)真核細胞都可以合成甾醇類物質(zhì),其中膽固醇是脊椎動物特有的甾醇,麥角甾醇是大多數(shù)真菌和一些單細胞藻類的主要甾醇。而大多數(shù)高等植物細胞往往含有很復(fù)雜的甾醇類物質(zhì)組成。24-乙基甾醇(谷甾醇和豆甾醇)是最主要的植物甾醇,占比超過總甾醇量的60%,24-甲基甾醇則占據(jù)了植物細胞總甾醇里剩余40%中的絕大部分,對脊椎動物維持細胞正常生理活性起到至關(guān)重要作用的膽固醇,在植物細胞中含量較少[1]。植物中甾醇類物質(zhì)的功能,可總結(jié)為3個方面:首先,它們是膜脂的重要組成部分,在質(zhì)膜中的含量與磷脂近似,在溫度等條件變化時,承擔著調(diào)節(jié)植物細胞膜的流動性和選擇透性的作用[2]。其次,甾醇類物質(zhì)還能通過動態(tài)調(diào)整膜上脂筏等微區(qū)的裝配,充當多個信號通路的信號轉(zhuǎn)導(dǎo)中心[3]。并且,甾醇是植物體內(nèi)多種生化物質(zhì)合成的前體,如甾醇衍生物油菜素類固醇,就是一類參與高等植物生長和發(fā)育調(diào)控的重要激素。甾醇衍生的物質(zhì)還參與植物響應(yīng)生物和非生物因素的應(yīng)答反應(yīng)[4]。
裂葉牽牛(Pharbitisnil(L.) Ching或Ipomoeanil,英文名:Japanese Morning Glory)是一種旋花科一年生草本植物。該植物全株表皮具有刺毛,果實為球形蒴果,無表皮毛,成熟后內(nèi)有種子5~6 顆[5-6]。裂葉牽牛常常被當作模式植物,研究開花調(diào)控以及花發(fā)育遺傳等[7-8]。裂葉牽牛的花期為7—9 月,光周期類型為嚴格的短日照型[9]。盡管在我國及日、韓等東亞國家被作為傳統(tǒng)園藝植物和藥用植物廣泛種植,但裂葉牽牛是原產(chǎn)美洲熱帶的外來物種,其生境偏好與我國本地種圓葉牽牛(Pharbitispurpurea(L.) Voisgt)相似。因而分布廣泛,可與許多土著牧草、農(nóng)作物等形成種間競爭關(guān)系。分析裂葉牽牛對非生物因素耐受性和機制,是預(yù)測其潛在入侵能力重要的依據(jù)。
目前,裂葉牽牛應(yīng)答非生物因素水平的相關(guān)分子機制依然不清楚。有研究顯示:通過轉(zhuǎn)基因過量表達裂葉牽牛PnAMP1和PnAMP2基因,可以顯著增強轉(zhuǎn)基因番茄對真菌的抗性。在使用裂葉牽牛作為試驗材料進行脂代謝研究的過程中發(fā)現(xiàn),過表達牽牛甲基甾醇單加氧酶基因(PnSMO1.1)可以顯著提高轉(zhuǎn)基因植物對培養(yǎng)基中200 mmol/L NaCl的耐受性。過量積累植物甾醇類物質(zhì)有可能顯著提升植物對非生物逆境的抗性[10]。為了揭示相關(guān)的分子機制,本研究首先通過子房注射法,構(gòu)建了過表達PnSMO1.1的裂葉牽牛轉(zhuǎn)基因株系;測量不同濃度NaCl處理條件下,各株系種子苗的根相對生長量、下胚軸相對生長量以及葉片丙二醛含量、相對電導(dǎo)率和油菜素內(nèi)酯物質(zhì)積累量,以便說明過表達PnSMO1.1是如何影響裂葉牽牛轉(zhuǎn)基因植物的生長及其可能的耐鹽性機制。
1 材料和方法
1.1 試驗材料
所用植物裂葉牽牛種子由陜西省生物技術(shù)與生化工程重點實驗室保存。萌發(fā)前的種子先用濃硫酸浸泡處理40 min,然后棄去濃硫酸,再用自來水沖洗10 min,置于無菌水中浸泡過夜,使其充分吸脹。第2天,將種子接種到直徑90 mm,盛有無菌水浸潤濾紙的培養(yǎng)皿中,在 25 ℃,16 h光照/ 8 h黑暗 (LD) 條件下發(fā)芽1 d。將露白的種子轉(zhuǎn)接到長19.5 cm×寬14.5 cm×高11.0 cm育苗盒并在 25 ℃、LD 條件下生長5 d。然后,將幼苗定植到直徑約25 cm的塑料花盆中,培養(yǎng)介質(zhì)為蛭石/營養(yǎng)土/金剛砂(1∶1∶1)的混合營養(yǎng)土。定植種子苗在連續(xù)光照25 ℃條件下培養(yǎng)至種子采收完畢。培養(yǎng)室光源是由三基色熒光燈提供的強度為60 μmol/(m2·s)白光。
后續(xù)遺傳轉(zhuǎn)化及生化檢測所用植物材料均取自這些種植于西北大學(xué)生命科學(xué)學(xué)院溫室(34.3°N,108.9 E)的實生苗。
1.2 PnSMO1.1基因的克隆及表達載體構(gòu)建
采用鹽酸胍法結(jié)合苯酚/氯仿提取法,從使用100 mmol/L NaCl溶液處理24 h的裂葉牽牛4 周齡種子苗葉片中分離總RNA[11]。以約1 μg 總RNA為模板,使用PrimeScriptTMⅡ 1st Strand cDNA Synthesis Kit試劑盒(TaKaRa Co.,Ltd,中國遼寧),按照反應(yīng)程序合成cDNA。按照NCBI收錄的PnSMO1.1基因(GenBank Access:XM_019314878.1)序列,設(shè)計并合成用于PCR擴增該基因全長ORF的引物對P1和P2。引物的具體序列如下:P1:ACGCGTCGACATGTCAATTCAACATTACAC(下劃線序列為用以載體構(gòu)建的SalⅠ限制性內(nèi)切酶切割位點),P2:GGAATTCCTAGTCAACTTTAATATCTTC(下劃線序列為用以載體構(gòu)建的EcoR Ⅰ限制性內(nèi)切酶切割位點)。
以約0.1 μg 前述逆轉(zhuǎn)錄合成的cDNA為模板,PCR擴增PnSMO1.1基因全長ORF。然后將長度為1 089 bp的PCR擴增片段,按照預(yù)先分別設(shè)計在引物5′端的SalⅠ和EcoRⅠ限制性酶切位點,連接到雙元表達載體pRI 101-AN質(zhì)粒的T-DNA區(qū),使其置于在組成型表達的CaMV-35S啟動子和NOS終止子的控制之下,構(gòu)建用于過表達PnSMO1.1基因的雙元植物表達載體質(zhì)粒。取重組質(zhì)粒連接產(chǎn)物,轉(zhuǎn)化大腸桿菌DH5α感受態(tài)細胞,并委托生工公司(Sangon,中國上海)對所攜帶目標基因序列進行測定。經(jīng)測序驗證,擴增序列與NCBI收錄的XM_019314878.1基因序列完全一致的植物表達載體質(zhì)粒被命名為pRI-PnSMO1.1,后續(xù)用于植物遺傳轉(zhuǎn)化試驗,該質(zhì)粒T-DNA區(qū)的結(jié)構(gòu)示意圖見圖1。
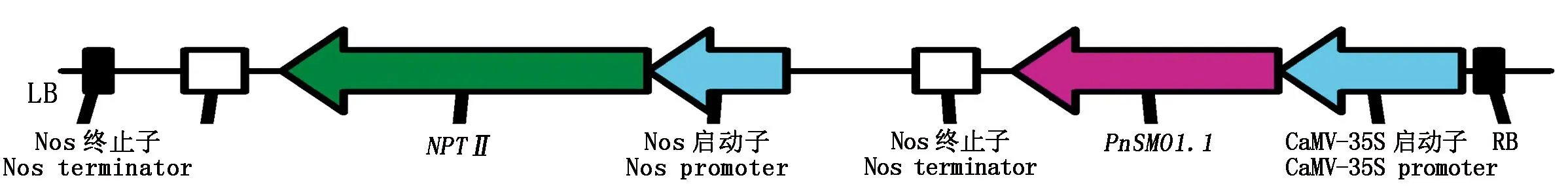
圖1 pRI-PnSMO1.1質(zhì)粒T-DNA區(qū)結(jié)構(gòu)Fig.1 Diagram of T-DNA region in pRI-PnSMO1.1 plasmid
1.3 子房注射法轉(zhuǎn)化裂葉牽牛
將攜帶pRI-PnSMO1.1質(zhì)粒的DH5α大腸桿菌接種至200 mL添加了終濃度為50 μg/mL卡那霉素的新鮮LB液體培養(yǎng)基中,37 ℃培養(yǎng)過夜。待培養(yǎng)物OD600≈0.65,13 000 r/min 離心3 min收集細菌。再使用購自天根生化科技有限公司(中國北京)的高純質(zhì)粒大提試劑盒,制備和純化pRI-PnSMO1.1質(zhì)粒,使用ddH2O將純化的質(zhì)粒DNA稀釋至100 ng/μL,在-80 ℃冰箱保存。直至實施植物子房注射前1 h,將凍存的質(zhì)粒從-80 ℃冰箱取出,并置于冰上緩慢融化。
子房注射當日9:00—10:00,待裂葉牽牛花朵完全綻放時,剝?nèi)?片萼片,暴露出其所覆蓋的花托與子房聯(lián)合部。用微量注射器吸取約5 μL pRI-PnSMO1.1質(zhì)粒溶液,從花托上部緩慢刺穿子房外壁,并將目標質(zhì)粒緩慢注射入子房。子房注射完成后,將受體植物轉(zhuǎn)移至溫室中正常培養(yǎng)直至結(jié)實。
1.4 pRI-PnSMO1.1基因整合及表達的檢測
收獲所有經(jīng)子房注射裂葉牽牛花朵正常發(fā)育而來的種子。將這些種子用0.1%的升汞水溶液表面消毒5 min后,用充足的無菌水洗去種皮上殘留的升汞。再將其播種于不補充任何植物生長調(diào)節(jié)物質(zhì),添加100 mg/L卡那霉素篩選劑的1/2 MS瓊脂培養(yǎng)基上,于25 ℃,連續(xù)光照條件下萌發(fā)。在卡那霉素篩選條件下能夠萌發(fā),且在保持100 mg/L卡那霉素篩選壓力下繼代28 d不發(fā)生白化的裂葉牽牛種子苗被標記為假定的T1轉(zhuǎn)基因植物。
從不同株系假定的T1轉(zhuǎn)基因植物上分別收集0.1 g幼嫩的葉片組織使用十二烷基磺酸鈉(SDS)法提取總DNA[12]。進而以這些總DNA為模板,采取PCR方法驗證目標基因及抗生素篩選標簽基因在轉(zhuǎn)化植物中的定位情況。PnSMO1.1基因的驗證PCR引物為,pSS:5′-TGGTGATTTCAGCGTGTC-3′(位于pRI 101-AN質(zhì)粒CaMV35S啟動子區(qū)內(nèi)部)和pSA:5′-GGCGTATGGCAGCATT-3′(位于PnSMO1.1基因CDS編碼區(qū)內(nèi)部),預(yù)期擴增片段長度為970 bp。卡那霉素抗性基因NPT Ⅱ的PCR擴增引物為,pNS:5′-CTCTGATGCCGCCGTGTT-3′和pNA:5′-CCCTGATGCTCTTCGTCCA-3′,預(yù)期擴增片段長度為399 bp。PCR程序設(shè)置如下:94 ℃預(yù)變性3 min;95 ℃變性30 s,55 ℃退火30 s,72 ℃延伸1 min,循環(huán)39 次;最終在72 ℃總延伸5 min。PCR產(chǎn)物經(jīng)1%瓊脂糖凝膠電泳檢測。
將經(jīng)過PCR鑒定為陽性轉(zhuǎn)基因植株的T1種子苗轉(zhuǎn)移至盛有營養(yǎng)土、蛭石、金剛砂等比例混合而成介質(zhì)的花盆中,置于25 ℃溫室中培育。種子苗先置于16 h光照/8 h黑暗的長日照條件下生長45 d,然后將溫室的光照條件改為8 h光照,16 h黑暗的短日照條件,繼續(xù)培養(yǎng)2 d以誘導(dǎo)裂葉牽牛開花,接著再在連續(xù)光照條件下培養(yǎng)至全部種子被收獲。從T1PCR陽性轉(zhuǎn)基因植株收獲的種子萌發(fā)的卡那霉素抗性植株作為T2轉(zhuǎn)基因植物,用于后續(xù)表型測定試驗。
1.5 不同NaCl濃度條件下轉(zhuǎn)基因裂葉牽牛生長的測定
將來自3 個不同來源T2轉(zhuǎn)基因株系的2 日齡裂葉牽牛種子苗(分別命名為SMO1、SMO2和SMO3)和同步萌發(fā)的野生型對照(Wild-type,WT)以及未經(jīng)改造的空載體pRI 101-AN轉(zhuǎn)化植物(BL)種子苗各6 株分別移入添加0,50,100,150,200 mmol/L NaCl的1/2 MS水溶液中繼續(xù)培養(yǎng)7 d,分別于不同濃度NaCl處理后的第4,7天測量不同株系植物的根長和下胚軸長度。把同一單株前后2個測量日測得數(shù)據(jù)作差,計算觀測期內(nèi)根的相對生長量ΔR和下胚軸的相對生長量ΔH,每個株系測定6個單株的相關(guān)生長數(shù)據(jù)作為樣本的生物學(xué)重復(fù)。
1.6 不同NaCl濃度條件下轉(zhuǎn)基因裂葉牽牛葉片丙二醛含量的測定
轉(zhuǎn)基因株系SMO1、SMO2、SMO3和WT以及BL幼苗先在1/2 MS水溶液浸潤的濾紙上培養(yǎng)21 d。然后用含有不同濃度氯化鈉(分別為0,50,100,150,200 mmol/L)的1/2 MS液體培養(yǎng)基對所有待試植株進行處理。5 d后,分別取0.1 g SMO1、SMO2、SMO3、WT和BL幼苗新鮮葉片組織作為材料,采用硫代巴比妥酸(TBA)法[13]測定上述試驗材料中MDA的含量。
1.7 不同NaCl濃度條件下轉(zhuǎn)基因裂葉牽牛葉細胞液相對電導(dǎo)率的測定
為了評估鹽生條件下不同株系植物細胞膜的滲透性變化,根據(jù)Zhang等[14]的方法測定了SMO1、SMO2、SMO3、WT和BL等株系幼苗在不同NaCl濃度條件下的相對電導(dǎo)率(Relative electrolytic conductivity,rEC)。植物材料的預(yù)處理方法同1.6。分別從完全發(fā)育的SMO1、SMO2、SMO3、WT和BL植物最小葉片的中部取直徑約為1 cm葉圓盤。將收集到的葉圓盤放置在含有30 mL蒸餾水的螺帽的單獨試管中。轉(zhuǎn)移到150 r/min室溫搖床孵育3 h,用DDS-303A型電導(dǎo)率探測器(中國上海)測定溶液(EC1)的電導(dǎo)率。將相同的樣品放入沸水中30 min,并將溶液冷卻到室溫后測定第2次讀數(shù)(EC2)。用來表征植物細胞電解質(zhì)泄漏程度的相對電導(dǎo)率(rEC):rEC=EC1/EC2×100%。
1.8 不同NaCl濃度條件下轉(zhuǎn)基因裂葉牽牛葉油菜素內(nèi)酯物質(zhì)含量的測定
使用同1.6描述的預(yù)處理方法準備植物材料。分別取SMO1、SMO2、SMO3、WT和BL幼苗新鮮葉組織作為材料,使用Wang等[15]描述的高效液相色譜-電噴霧電離-串聯(lián)質(zhì)譜 (HPLC-ESI-MS/MS) 方法對內(nèi)源性油菜素內(nèi)酯物質(zhì)含量進行定量測定。
1.9 統(tǒng)計分析
采用方差分析(ANOVA)比較方法,分析了PnSMO1.1基因轉(zhuǎn)化的裂葉牽牛株系與野生型植物及空載體轉(zhuǎn)化對照植物株系抗逆相關(guān)生理指標的差異顯著性。數(shù)據(jù)統(tǒng)計分析由 SPSS 12.0 軟件完成,所有圖表均使用 Origin 8.0 軟件繪制完成。數(shù)據(jù)均來自同一株系6個不同生物學(xué)重復(fù)植株各自測量數(shù)據(jù)的平均值±標準差。
2 結(jié)果與分析
2.1 子房注射法對裂葉牽牛進行遺傳轉(zhuǎn)化結(jié)果分析
裂葉牽牛從開花、坐果到種子成熟一般需要45~60 d,在整個生活史中共形成12~14 朵花。在實施子房注射時,植株上最初形成5~6 朵花,最終結(jié)實率極低,大部分實施了子房注射的花朵最終都沒有結(jié)實。而7~14 朵花,隨著植株的逐漸生長壯大,子房注射后的結(jié)實率有了明顯提高。在整個試驗周期中,累計對2 541 朵不同花期的花朵實施了子房注射,共收獲924 粒自然成熟的種子,其中收獲自31 朵花的75 粒能在150 mmol/L卡那霉素篩選條件下萌發(fā),轉(zhuǎn)化率約為1.22%。
2.2 目的基因在T1轉(zhuǎn)基因裂葉牽牛中的PCR結(jié)果
對75 個卡那霉素抗性植株的基因型進行PCR檢測(圖2),其中56 株目標基因PnSMO1.1的PCR檢測結(jié)果為陽性,61 株抗性篩選標簽NPTⅡPCR檢測結(jié)果為陽性,其中52 株P(guān)nSMO1.1基因和NPTⅡPCR結(jié)果均為陽性的植株,被認為是T1轉(zhuǎn)基因植株。
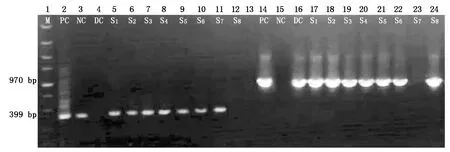
M.DL5000 DNA Marker;PC.pRI-PnSMO1.1質(zhì)粒DNA為模板的PCR陽性對照;NC.pRI 101-AN空載體轉(zhuǎn)化系植株基因組DNA為模板的PCR空白對照;DC.PnSMO1.1基因cDNA為模板的陽性對照;S1—S8.不同的假定SMO1-1基因過表達株系基因組DNA為模板的PCR擴增結(jié)果;2—12.卡那霉素抗性基因NPT II的PCR擴增結(jié)果;14—24.目標基因PnSMO1.1的PCR擴增結(jié)果。
2.3 不同濃度NaCl條件下轉(zhuǎn)基因裂葉牽牛的生長
對SMO1、SMO2、SMO3、WT和BL等株系幼苗在測量周期內(nèi)的根長相對生長量檢測結(jié)果顯示,在正常生理非脅迫條件下,不同株系植物種子苗在3 d測定內(nèi)的根長相對生長量沒有顯著差異。在50 mmol/L NaCl處理下,植株的根都受到了顯著抑制而生長緩慢,不同轉(zhuǎn)基因株系間也表現(xiàn)出顯著差別,其中SMO1株系幼苗表現(xiàn)出顯著高于其他2個轉(zhuǎn)基因株系植株的根相對生長量。在100~200 mmol/L NaCl處理下,PnSMO1.1過表達植株的根長的增加量顯著大于WT和BL對照植株(圖3)。這表明:PnSMO1.1基因的過表達顯著增強了轉(zhuǎn)基因裂葉牽牛根的生理耐受能力。

不同大寫字母表示NaCl濃度間差異顯著;不同小寫字母表示株系間差異顯著(P<0.05)。圖4—7同。
不同濃度NaCl濃度條件下,PnSMO1.1過表達植株與WT和BL對照植株下胚軸相對生長量的測定結(jié)果顯示,NaCl濃度的增加對裂葉牽牛下胚軸生長的影響小于其對根長增加的影響。在100,150 mmol/L NaCl處理下,SMO1、SMO2和SMO3轉(zhuǎn)基因株系的下胚軸相對生長量高于WT和BL對照植株,而在200 mmol/L NaCl處理下,SMO2和SMO3轉(zhuǎn)基因株系的相對生長量與BL對照植株的無顯著差異(圖4)。
這一結(jié)果表明,PnSMO1.1基因的過表達可以顯著提高轉(zhuǎn)基因植物根組織對100 mmol/L以上NaCl的耐受性(P<0.05)。
2.4 不同NaCl濃度處理下裂葉牽牛各株系葉片丙二醛的含量
丙二醛(Malondialdehyde,MDA)是脂質(zhì)過氧化的產(chǎn)物,與細胞膜上多不飽和脂肪酸的氧化降解密切相關(guān)。SMO1、SMO2、SMO3、WT和BL等株系在無NaCl影響條件下幼苗葉片中的MDA含量處于較低水平且無顯著差異,隨NaCl處理濃度的增加,所有被測植物株系中MDA含量均顯著上升。但過表達PnSMO1.1基因的轉(zhuǎn)基因裂葉牽牛葉片的MDA含量,在各NaCl處理濃度水平下均低于對應(yīng)的WT對照植株,而空載體轉(zhuǎn)化對照系BL的MDA積累量與WT植株差異不顯著(圖5)。
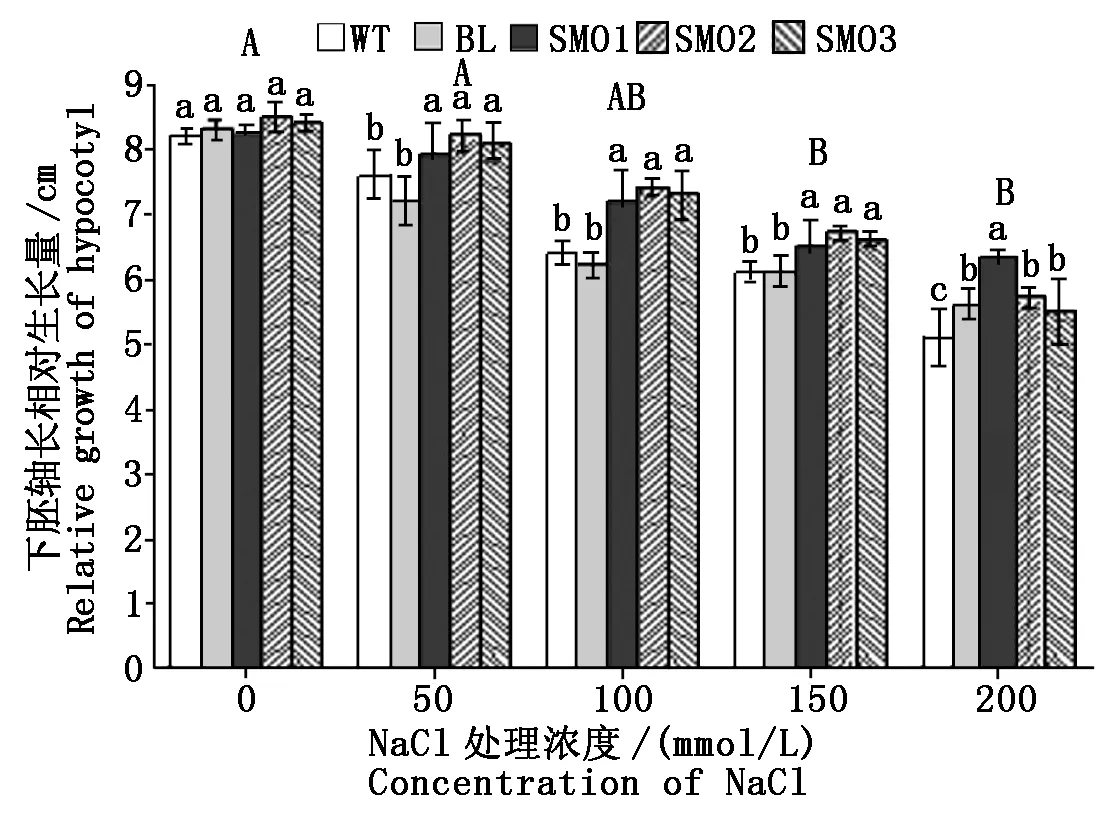
圖4 不同濃度NaCl處理下植株下胚軸相對生長量Fig.4 Relative growth of hypocotyl length of different plants under treatment of various NaCl concentrations

圖5 不同濃度NaCl處理下植株葉片中MDA含量Fig.5 The content of MDA in leaves of different plants under treatment of various NaCl concentrations
2.5 不同NaCl濃度處理下裂葉牽牛各株系葉片細胞電導(dǎo)率
隨著NaCl濃度的升高,不同株系裂葉牽牛種子苗葉片的相對電導(dǎo)率(rEC)測量值均隨之顯著升高(P<0.05)(圖6)。在相同的NaCl濃度條件下,WT和BL植株葉片中的rEC值顯著高于3個轉(zhuǎn)基因過表達株系SMO1、SMO2和SMO3植物葉片rEC。在200 mmol/L NaCl條件下,WT幼苗的rEC達到了未受NaCl影響時WT植株對應(yīng)值的4.72倍。而同樣在200 mmol/L NaCl條件下,SMO1、SMO2和SMO3幼苗的rEC值僅僅是相同株系種子苗在未受到NaCl影響時的該值的3.86~3.92 倍。當從正常生長狀態(tài)轉(zhuǎn)移到200 mmol/L NaCl濃度條件下,轉(zhuǎn)基因植物葉片細胞與對應(yīng)野生型細胞相比,其膜結(jié)構(gòu)損傷和細胞內(nèi)外的電解質(zhì)滲漏均顯著較輕。

圖6 不同濃度NaCl處理下植株葉片相對電導(dǎo)率Fig.6 The relative conductivity in leaves of different plants under treatment of various NaCl concentrations
2.6 不同NaCl濃度處理下裂葉牽牛各株系葉油菜素內(nèi)酯的含量
為了測試PnSMO1.1過表達是否能影響轉(zhuǎn)基因植株的內(nèi)源油菜素甾醇類化合物(Brassinolides,BRs)的含量,分別測定并比較了WT、BL和3個不同PnSMO1.1過表達株系植物體內(nèi)油菜素甾醇的含量,包括油菜素內(nèi)酯(Brassinolide,BR)、油菜素甾酮(Castasterone,CS) 和6-脫氧油菜素甾酮(6-deoxocastasterone,6-deoxoCS)(以鮮質(zhì)量計)。結(jié)果顯示,在不同NaCl濃度處理下,WT和BL植物葉片內(nèi)CS含量基本無顯著差別,僅在NaCl濃度為100 mmol/L時,BL植株測量值高于WT。但PnSMO1.1過表達株系植物與同等NaCl濃度條件下的WT和BL植株相比,其葉片內(nèi)的6-deoxoCS含量均顯著增加(P<0.05),而CS積累量則相對顯著減少(僅在NaCl濃度為100 mmol/L時,SMO2植株測量值與WT相當,但仍顯著低于BL植株)(圖 7)。油菜素內(nèi)酯在裂葉牽牛中的含量較低,未能在當前試驗對象中檢出。
3 討論
裂葉牽牛常常被當作模式植物。然而,目前還沒有建立裂葉牽牛高效組織培養(yǎng)體系的報道,因此植物轉(zhuǎn)基因相關(guān)的成熟方法不能被直接用來研究該植物的遺傳轉(zhuǎn)化。在農(nóng)桿菌介導(dǎo)法對裂葉牽牛實施遺傳轉(zhuǎn)化的報道中,獲得次生胚胎轉(zhuǎn)化幼苗的實際轉(zhuǎn)化率較低[16-17],甚至有些裂葉牽牛的遺傳轉(zhuǎn)化研究報道僅限于獲得T0轉(zhuǎn)基因愈傷組織的階段[18]。鑒于花粉管導(dǎo)入或子房注射等方法已成功應(yīng)用于玉米、小麥、瓜類、黃瓜以及棉花等作物的轉(zhuǎn)基因育種工作[19],本研究使用子房注射法對裂葉牽牛進行了遺傳轉(zhuǎn)化。對2 541 朵裂葉牽牛實施子房注射,實際獲得卡那霉素抗性植株75 株,其中56 株的PCR鑒定結(jié)果顯示,目標轉(zhuǎn)基因已經(jīng)成功整合到裂葉牽牛的基因組DNA中,實際轉(zhuǎn)化效率約為1.22%,能滿足進一步在裂葉牽牛中開展功能基因組研究的需要。因此,將攜帶目標基因序列的植物雙元表達質(zhì)粒DNA注射到花朵子房中,是一種穩(wěn)定有效的裂葉牽牛遺傳轉(zhuǎn)化方法。
4-甲基甾醇和4,4-二甲基甾醇是真核生物體內(nèi)甾醇類合成的中間體,通常被認為是膽固醇、麥角甾醇和植物甾醇生物合成的前體[20]。植物機體發(fā)生代謝抑制或遺傳損傷時,往往會導(dǎo)致4-甲基甾醇和4,4-二甲基甾醇2種物質(zhì)的過度積累,從而引發(fā)嚴重的細胞和發(fā)育異常[21]。對甲基甾醇功能研究的相關(guān)報道顯示,它們既能在動物體內(nèi)充當減數(shù)分裂激活劑,如調(diào)控免疫系統(tǒng)發(fā)育;也能在植物體內(nèi)充當信號分子,如調(diào)控生長素信號傳導(dǎo)[22-23]。從擬南芥cDNA 文庫中克隆得到,長度分別為801,783 bp 的AtSMO1和AtSMO2基因是最早被鑒定的甲基甾醇加氧酶。核苷酸序列比對分析結(jié)果顯示:AtSMO1和AtSMO2基因編碼的蛋白質(zhì)與來自釀酒酵母的甾醇-4α-甲基氧化酶編碼基因ERG25的相似性分別為32%和 29%[24]。進一步的研究報道顯示,AtSMO1和AtSMO2基因分別編碼2種不同類型的 C-4-甲基甾醇氧化酶,進而分別控制植物體內(nèi)4-甲基甾醇和4,4-二甲基甾醇的豐度。對沙漠植物白花牛角瓜的研究報道證明,SMO1和SMO2基因的表達受到了干旱信號和光照信號的誘導(dǎo),表現(xiàn)出表達節(jié)律性,同時還控制了植物體內(nèi)β-谷甾醇生物合成[25]。這些已有的研究結(jié)果表明,SMO基因及其表達產(chǎn)物可能在植物抗逆過程中起重要作用,并可能影響植物內(nèi)源油菜素內(nèi)酯信號物質(zhì)的合成。
裂葉牽牛體內(nèi)過表達甲基甾醇加氧酶基因PnSMO1.1能夠顯著增加不同濃度NaCl條件下根組織的生長量,并顯著改善了葉片組織中由丙二醛含量和相對電導(dǎo)率表征的細胞水平上的耐鹽性生理表現(xiàn)。這些結(jié)果與前人使用外源低濃度油菜素內(nèi)酯物質(zhì)處理植物,促進根組織生長的結(jié)果一致[26]。此外,過表達PnSMO1.1基因,顯著地增加了轉(zhuǎn)基因裂葉牽牛植株中的內(nèi)源油菜素內(nèi)酯信號物質(zhì)6-脫氧油菜素甾酮的含量。特別值得注意的是,在200 mmol/L NaCl條件下,轉(zhuǎn)基因株系植株體內(nèi),6-脫氧油菜素甾酮的積累量達到了野生型對照系植株的1.58 倍和空載體轉(zhuǎn)化系對照植物的1.61倍。另外一種重要的內(nèi)源油菜素內(nèi)酯類物質(zhì)是油菜素甾酮,當NaCl濃度低于100 mmol/L,該物質(zhì)的含量在轉(zhuǎn)基因株系與對照株系之間相似。但當NaCl濃度達到或高于150 mmol/L,所有轉(zhuǎn)基因株系植株中的油菜素甾酮含量均降低到顯著低于對照系的含量。上述結(jié)果表明:油菜素甾酮等內(nèi)源油菜素內(nèi)酯物質(zhì)不是簡單線性調(diào)控植物營養(yǎng)生長和耐受過程,其在逆境下的動態(tài)平衡才是決定植物耐受性的關(guān)鍵。這個結(jié)果與以前的發(fā)現(xiàn)吻合,即細胞內(nèi)油菜素內(nèi)酯物質(zhì)的穩(wěn)態(tài)平衡,而不是它們的絕對累積量,對于逆境條件下根系維持生長起著至關(guān)重要調(diào)控作用[27]。
總之,以NaCl濃度處理作為鹽脅迫條件時,過表達PnSMO1.1基因,可導(dǎo)致轉(zhuǎn)基因植物體內(nèi)油菜素內(nèi)酯物質(zhì)積累量呈現(xiàn)顯著的變化,但某一油菜素內(nèi)酯物質(zhì)積累量的線性變化并不破壞轉(zhuǎn)基因植物體內(nèi)所有油菜素內(nèi)酯物質(zhì)的整體平衡。這種內(nèi)源油菜素內(nèi)酯物質(zhì)整體平衡的動態(tài)微調(diào),可能導(dǎo)致了轉(zhuǎn)PnSMO1.1基因植物在細胞生理和營養(yǎng)生長調(diào)控2 個水平上耐鹽性的顯著增強。

