VNTR特異性引物在甜菜育性鑒定中的應用
張 輝,王 良,付增娟,李曉東,趙尚敏,鄂圓圓,鄭文哲,張自強,張必周,張惠忠
(內蒙古自治區農牧業科學院,內蒙古 呼和浩特 010031)
甜菜是2年生常異花作物,是重要的蔗糖榨取原料。2年生作物的生育周期較長,制約了育種工作的進程。目前,國內生產上使用的甜菜品種幾乎都是單粒雜交種,而單粒雜交種的制備離不開優質單粒不育系的選育工作,需要對花期授粉雜交進行完整有效的控制。但是甜菜的花非常小,并且屬于無限花序,不利于人工去雄工作。因此,細胞質雄性不育(CMS)的利用為甜菜雜交種的發展提供了一種快捷高效的途徑[1]。Owen[2]提出了歐文假說,根據歐文假說的理論,質核互作型甜菜的不育性狀是由細胞質基因(S)和細胞核基因(xxzz)共同控制的。質核互作型單粒不育系的保持必須是由單粒保持系(基因型為Nxzxz,N為細胞質可育基因)與其對應的不育系(基因型為Sxzxz,S為細胞質不育基因)雜交成對保持。Matsuhira等[3]研究發現,x基因位于Ⅲ號染色體上,并克隆了x的1個等位基因Rf1,其基因產物是類似于酵母線粒體蛋白質量控制的OMA1蛋白。Suketomo等[4]研究發現,在中國水稻野生型細胞質雄性不育系中,線粒體增強核基因逆向調控雄性不育的表達,導致花粉敗育。當恢復系的表達減少時,育性恢復。PPR2基因編碼含有五肽重復域的蛋白質,不負責育性恢復,而育性是通過降低逆向調控雄性不育的表達來恢復。Arakawa等[5]研究發現,甜菜育性相關的基因rf1與育性恢復的等位基因極為相近,但是它是一個非恢復等位基因,對其他育性基因存在協同作用。
在甜菜育種工作中,不育系的利用能大大提高雜交育種的效率。通常在花期進行粒性和育性調查進而對保持系和不育系材料進行有效選擇。但在調查過程中難免存在漏查和誤查,從而導致后代選擇的材料出現不純的現象。Nishizawa等[6]研究發現,在甜菜線粒體基因組有4個不相關的串聯重復位點,并發現TR1位點插在重組重復序列(rrn26)。TR1由32 bp的串聯重復片段組成,在7個基因型的甜菜中被檢測出存在2~13個不同的重復數,開發出了TR1、TR2、TR3和TR4引物。Cheng等[7]利用VNTR分子標記的方法對42個中國甜菜育種系正常和雄性不育型細胞質進行了鑒定分析,發現在所檢測的42個育種系中,14個具有完全正常的細胞質,11個只有歐文細胞質,其余17個同時包括正常和歐文細胞質。Cheng等[8]利用4種線粒體微型衛星技術研究了葉用和觀賞甜菜種質資源的多樣性,鑒定了11個多位點單倍型,對不同類型的細胞質進行了梳理分類。分子鑒定技術可以在苗期進行實驗室鑒定工作,為育種工作者提供較準確的數據支撐和參考。
本研究將TR1鑒定引物應用于2年生甜菜保持系和不育系胞質類型鑒選中,旨在為加快甜菜不育系選育、縮短育種進程提供理論指導和技術支持。
1 材料和方法
1.1 試驗材料
甜菜保持系材料為960767,不育系材料為N9849,其他待鑒定的試驗材料28份,均為內蒙古自治區農牧業科學院自育或引進材料。其中保持系960767和不育系N9849已經過多年田間調查驗證并經過分子鑒定應用[9],為已成型穩定的成對保持系和不育系材料。其他鑒定材料為經過田間性狀調查待鑒定胞質類型的材料,具體材料名稱見表1。

表1 試驗材料名稱Tab.1 Test materials names
1.2 試驗方法
1.2.1 取樣 在試驗材料苗期取甜菜植株中心的新鮮幼嫩葉片2~3片,稱0.8~1.2 g。
1.2.2 葉片的粉碎 將取樣后的新鮮嫩葉置于超低溫冷凍干燥機凍干48 h,干燥后的樣品分裝置于2 mL的離心管中,然后裝入鋼珠,用高通量破碎機將葉片打碎成粉末狀,之后即可用于DNA的提取。凍干后的葉片可以在干燥的環境下長期保存。
1.2.3 DNA的提取 選用新型植物基因組DNA提取試劑盒(天根),對已經進行破碎處理的葉片進行DNA提取,操作按照試劑盒說明書進行。
1.2.4 DNA的檢測 將提取后的DNA樣品5 μL與6×Loading Buffer緩沖液1 μL預混后點樣5 μL,使用1%的瓊脂糖凝膠在1×TAE的電泳緩沖液中進行電泳,電泳條件為120 V,30 min 左右。用凝膠成像系統紫外光檢測電泳結果。
1.2.5 PCR擴增 引物:可變數量的串聯重復TR1引物,序列為:5′-AGAACTTCGATAGGCGAGAGG-3′,5′-GCAATTTTCAGGGCATGAACC-3′[10]。PCR反應體系為15 μL:包括 7.5 μL 2×Taq Master Mix,1 μL上游引物(0.5 μmol/L),1 μL下游引物(0.5 μmol/L),3 μL DNA(0.3 ng/μL),2.5 μL ddH2O。PCR 反應程序:94 ℃預變性5 min;94 ℃變性 30 s,55 ℃ 退火30 s,72 ℃延伸1 min,循環35 次;72 ℃延伸 10 min,4 ℃保存。
1.2.6 PCR 擴增產物的檢測 將PCR擴增后的產物點樣5 μL,使用 1%瓊脂糖凝膠1×TAE的電泳緩沖液進行電泳,在 120 V 電壓下電泳 30 min 左右,凝膠成像儀照相保存圖片。
1.2.7 田間育性性狀調查 在甜菜開花始期(種株開花達到 15%)進行田間性狀調查,調查內容為甜菜花藥的發育狀況、花粉粒的特征和散粉的能力。2年生甜菜育性類型分為 5 類:全不育型、半不育一型、半不育二型、半可育型、可育型[11]。具體性狀類型見參考文獻[12]。
2 結果與分析
2.1 DNA提取和檢測
選用新型植物基因組DNA提取試劑盒(天根)對樣品進行全基因組DNA的提取,1%的瓊脂糖凝膠進行檢測,點樣孔上樣量為5 μL,經檢測提取的DNA濃度可以用來進行PCR檢測,DNA檢測結果見圖1 。

1—28.除去960767和N9849的其他試驗材料的電泳檢測結果。1—28.The electrophoresis detection results of the other test materials excluding 960767 and N9849.
2.2 細胞質育性分子標記鑒定
試驗總共檢測了30個試驗材料的787個植株樣品,共檢測出598份結果。在這598份材料中共檢測出750 bp條帶的細胞質類型116份,材料分別為960767、T152、T328、T334、T306、T360;檢測出500 bp條帶的細胞質類型300份,材料分別為N9849、T766、T154、N122、I-1、B-3、Z-1、41419、10320、B-3-23、S865、S301、S151、S327、S333、S115、S305、S153、S359、S137、S163和S313;檢測出大于500 bp小于750 bp條帶的細胞質類型84份,材料分別為T302、T116;同時含有500,750 bp的細胞質類型9份,材料分別為T302、I-1和B-3的不同植株。970767和N9849為多年田間選育鑒定的試驗材料,田間性狀表現為可育型和全不育型,為成對穩定的保持系和不育系,經TR1引物分子標記鑒定檢測后,960767和N9849檢測到的條帶分別為750,500 bp,即750 bp條帶為N1型細胞質,500 bp條帶為S型細胞質(圖2)。圖3顯示了部分材料經TR1引物PCR擴增后的檢測結果,檢測材料分別為T334、S333、S115、T116、T302、S301、960767、I-1、B-3、Z-1、41419、10320、B-3-23。這些材料中只有960767和T334為N1型細胞質,而T302和T116為特異性類型,其經過PCR檢測后條帶位置為500~750 bp(圖3)。將T302、T116、S301和S115再次取樣經TR1引物檢測(圖4),驗證后確定T302和T116檢測后的條帶位置為500~750 bp。結合連續幾年的田間調查情況可知,T302和S301分別為可育型和全不育型材料,并且T302對S301具有不育性狀的保持能力,因此,T302、T116類型屬于另外一種N2型細胞質,其微衛星串聯重復序列重復數為9,而N1類型細胞質微衛星串聯重復序列為18。同時含有500,750 bp條帶的T302、I-1和B-3部分植株為同時包括正常和歐文細胞質的材料,屬于特質性材料[5,7]。圖5,6分別為部分田間調查性狀為可育和不育型材料經TR1引物PCR擴增后的檢測結果。圖5中T766存在一植株檢測條帶與其他不一致,為N1胞質類型,可能由于選擇過程中不同株系材料本身存在差異或存在雜株現象。將所有檢測材料按照條帶位置的不同進行胞質類型分類,具體結果見表2。

1—8.保持系材料960767不同植株的TR1引物檢測結果;9—17.不育系材料N9849不同植株的TR1引物檢測結果。1—8.The TR1 primer test results of different plants of maintainer material 960767;9—17.The TR1 primer test results of different plants of sterile line material N9849.

1.T334;2.S333;4,5.S115;3,6.T116;8,10.T302;7,9.S301;11,12.960767;13—15.I-1;16—18.B-3;19—21.Z-1;22—24.41419;25—26.10320;27—28.B-3-23。

1—5.不育型材料S301不同植株樣品檢測;6—10.不育型材料S115不同植株樣品檢測;11—15.N2型細胞質材料T302不同植株樣品檢測;16—20.N2型細胞質材料T116不同植株樣品檢測。1—5.Detection of different plants of sterility material S301;6—10.Detection of different plants of sterile material S115;11—15.Detection of different plants of N2 cytoplasmic materials T302;16—20.Detection of different plants of N2 cytoplasmic materials T116.

1—6.960767不同植株檢測;7—13.T152不同植株檢測;14—20.T328不同植株檢測;21—27.T334不同植株檢測;28—31.T306不同植株檢測;32—35.T360不同植株檢測;36—40.T302不同植株檢測;41—44.T116不同植株檢測;45—48.T766不同植株檢測;49—54.N122不同植株檢測。
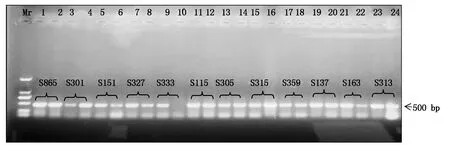
1—2.S865不同植株檢測;3—4.S301不同植株檢測;5—6.S151不同植株檢測;7—8.S327不同植株檢測;9—10.S333不同植株檢測;11—12.S115不同植株檢測;13—14.S305不同植株檢測;15—16.S315不同植株檢測;17—18.S359不同植株檢測;19—20.S137不同植株檢測;21—22.S163不同植株檢測;23—24.S313不同植株檢測。
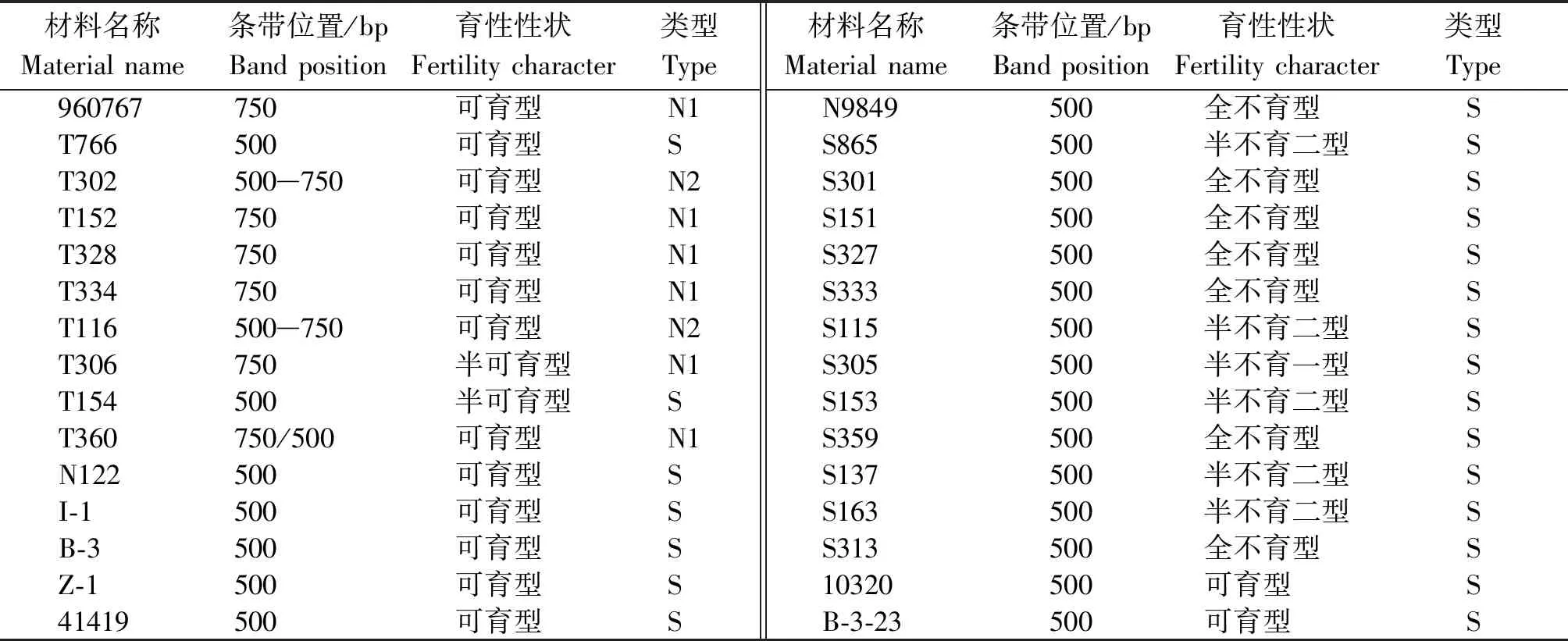
表2 不同試驗材料經TR1引物擴增鑒定及田間育性調查Tab.2 Identification of amplification and field breeding investigation by TR1 primers of different test materials
2.3 田間育性性狀調查
根據花粉育性調查標準進行田間育性性狀調查可知,30份試驗材料共計調查了787個植株樣品,其中可根據調查結果將試驗材料分為以下幾類:可育型包括960767、T766、T302、T152、T328、T334、T116、T360、N122、I-1、B-3、Z-1、41419、10320、B-3-23,這些材料均存在大量花粉并進行開裂;半可育型,包括T306、T154,這些材料含有無受精能力的花粉粒及少量正常的花粉粒;全不育型,包括N9849、S301、S151、S327、S333、S359、S313,這些材料無花粉,或含少數小孢子退化的花粉粒,花粉不開裂;半不育一型,包括S305,其具有退化的小孢子或較之略發達的花粉粒,但不開裂;半不育二型,包括S865、S115、S153、S137、S163,這些材料有花粉膜,可見花粉孔,含多個花粉粒,但無受精能力,花藥幾乎不開裂。田間調查結果對應分子鑒定結果T766、T154、N122、I-1、B-3、Z-1、41419、10320、B-3-23均為可育型,但鑒定其胞質類型屬于S型細胞質,根據歐文理論,這些材料的細胞核基因應該含有可育基因x,因此,這些材料在具體應用時不建議選作保持系材料。而S865、S115、S305、S153、S137、S163屬于S型細胞質,但花粉顏色呈淡黃和橙色,在選育過程中建議再進行隔離套袋純化,待選擇較純后再用于不育系的選擇。
3 結論與討論
甜菜在選育過程中育性恢復基因是一個非常復雜的性狀,這個復雜性可能是由于遺傳基因的主效和微效因子Rfs,在這個過程中還有環境因素的影響。Tourmente等[13]發現,可變數目的串聯重復序列(VNTRs)在真核生物基因組中豐富且普遍存在。這些序列與多個基因座雜交,并且本質上是高變的,因此被證明對遺傳分析具有高度的信息性。Buard等[14]發現,串聯重復序列通常分為微衛星序列(重復單元的長度為5 bp或更短)和微型衛星序列(重復單元的長度5~100 bp)。盡管微衛星和微型衛星有相似的結構特征,但它們似乎在幾個方面不同。例如,微衛星起源的密切聯系并且與DNA復制或錯配修復系統中的缺陷相關的變異是明顯的[15-16]。而同源重組過程,包括基因轉換和重復之間的不平等交換,被認為有微衛星參與[17-21]。植物線粒體基因組的一個基本標志是其跨重復序列重組的傾向。所有測序的重組重復序列都沒有序列基序,這表明重組是通過同源機制而不是位點特異性機制發生的。這增加了植物線粒體基因組也可能包含類似小衛星VNTRs的可能性。
甜菜線粒體基因組的可變數目串聯重復序列(VNTRs)已被證明提供了一種快速和復雜的方法來區分正常細胞質和雄性不育細胞質的不同來源[5,10,22]。本研究利用其開發的TR1引物對國內部分品系材料進行細胞質鑒定,以成型的成對保持系和不育系材料作為對照,初步摸清了被檢測材料的細胞質類型。檢測到30份材料中T766、T154、N122、I-1、B-3、Z-1、41419、10320、B-3-23為與選育方向不一致的材料,均為可育型,但屬于S型細胞質,根據歐文理論,這些材料的細胞核基因應該含有顯性可育基因x,需要根據育種要求進行調整。T302和T116為具有不育系保持能力的另外一種細胞質類型,被認定為N2型細胞質類型。由于N2型細胞質和S型細胞質在條帶上差異較小,在今后的選育過程中,應該結合串聯重復序列的重復數檢測進行鑒別,為今后的不育系選育提供技術指導和參考。在檢測中還有部分材料檢測到不同植株間存在差異,或者兼有2種條帶類型,推測應該是在試驗中存在收獲混雜及樣品污染等情況。雖然該項技術不能涵蓋所有的甜菜類型,但在結合田間選育后能做出較為準確的判斷。眾多的科研人員從事育性基因相關的機理研究[23-25],相信未來細胞質和細胞核特異性引物的有效結合應用將更有效地推進分子輔助選擇在甜菜育種中的應用。

