HOMA-IR對糖尿病腎病不良預(yù)后的預(yù)測價值研究*
張菁菁,徐 婉,肖 婧,高 凌
湖北文理學(xué)院附屬醫(yī)院,襄陽市中心醫(yī)院內(nèi)分泌科,湖北襄陽 441021
隨著人們生活、飲食水平的提高及運動量的減少,糖尿病患者的人數(shù)逐年升高。國際糖尿病聯(lián)合會預(yù)測,全球糖尿病患者人數(shù)從2013年開始,在未來的22年里可能由3.82億增加到5.92億[1-2]。我國也是糖尿病的高發(fā)國家,據(jù)不完全統(tǒng)計,我國每天新發(fā)糖尿病患者約1.6萬,其中3 000人死于各種并發(fā)癥,20~80歲的人群中,我國糖尿病患者有9 240萬,其中有20%~40%的患者可進展為糖尿病腎病(DN)[3]。DN是糖尿病最常見及嚴(yán)重的并發(fā)癥之一,發(fā)病機制復(fù)雜,早期起病隱秘,多數(shù)患者不予重視,是我國導(dǎo)致慢性腎衰竭的首要原因[4-6]。胰島素抵抗是指不能滿足機體對葡萄糖的攝取、利用或機體靶器官對循環(huán)中一定量的胰島素敏感性降低,產(chǎn)生的生物學(xué)效應(yīng)水平低于實際應(yīng)有水平的一種狀態(tài),是在遺傳因素和環(huán)境因素的復(fù)雜相互作用下緩慢進展的病理過程,也是代謝綜合征發(fā)病的中心環(huán)節(jié),常見于肥胖和2型糖尿病,其臨床特征表現(xiàn)為高胰島素血癥[7]。有研究表明,胰島素抵抗不僅是糖尿病和心血管疾病的獨立預(yù)測因素,也是發(fā)生腎損傷,導(dǎo)致終末期腎病的獨立危險因素[8-9]。DN患者體內(nèi)胰島素抵抗加重,胰島素抵抗通過腎素-血管緊張素系統(tǒng)導(dǎo)致血流動力學(xué)改變,炎癥因子和氧化應(yīng)激反應(yīng)損傷從而促進DN患者蛋白尿的進展,而且隨著糖尿病腎病進展,胰島素抵抗逐漸加重,二者相互作用,導(dǎo)致病情惡化。因此本研究旨在通過比較不同DN預(yù)后患者的胰島素抵抗情況,為臨床早期對DN預(yù)后的精準(zhǔn)預(yù)測提供臨床理論依據(jù)。
1 資料與方法
1.1一般資料 選取2012-2015年在本院首次診斷為2型DN患者212例。所有患者均隨訪60個月,按隨訪5年內(nèi)是否發(fā)展為終末期腎病將患者分為預(yù)后良好組(134例)和預(yù)后不良組(78例)。2型糖尿病診斷符合2型糖尿病診斷標(biāo)準(zhǔn),并已行胰島功能檢測排除1型糖尿病。排除標(biāo)準(zhǔn):1型糖尿病;繼發(fā)性糖尿病;妊娠期糖尿病;急慢性感染;惡性腫瘤;各種原發(fā)性腎臟病;合并結(jié)締組織疾病導(dǎo)致的繼發(fā)性腎臟病;近期有創(chuàng)傷及手術(shù);隨訪60個月因各種原因死亡患者。
1.2方法
1.2.1記錄患者的性別、年齡、身高、體質(zhì)量、糖尿病病程 受試者均過夜空腹8~12 h,晨起抽靜脈血送生化室測定空腹血糖、空腹胰島素、糖化血紅蛋白、血肌酐、同型半胱氨酸(Hcy)、胱抑素C,留24 h尿測尿微量清蛋白,計算尿清蛋白排泄率(UAER)。根據(jù)空腹胰島素和空腹血糖計算胰島素抵抗指數(shù)(HOMA)-IR和HOMA-β。
1.2.2檢測方法 采用放射免疫法測定空腹胰島素;采用氧化酶法測定空腹血糖;采用高壓液相法(美國BIO-RAD公司)測定糖化血紅蛋白;采用全自動生化分析儀測定肌酐、胱抑素C水平;采用貝克曼化學(xué)發(fā)光分析儀測定Hcy水平;采用高效免疫比濁法檢測尿微量清蛋白水平,根據(jù)24 h尿量計算UAER,取3次測定值的均值。計算穩(wěn)態(tài)模型HOMA-IR=空腹胰島素×空腹血糖/22.5,HOMA-β=20×空腹胰島素/(空腹血糖-3.5)。
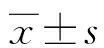
2 結(jié) 果
2.1兩組DN患者一般臨床資料比較 兩組患者UAER、肌酐、胱抑素C、Hcy及HOMA-IR比較,差異有統(tǒng)計學(xué)意義(P<0.05)。其他臨床資料如性別、年齡、體質(zhì)量指數(shù)(BMI)、糖尿病病程、高血壓、冠心病、腦血管病、空腹血糖、糖化血紅蛋白及HOMA-β比較,差異無統(tǒng)計學(xué)意義(P>0.05)。見表1。

表1 兩組DN患者一般臨床資料比較(n/n或
2.2DN患者HOMA-IR與一般臨床資料的相關(guān)性分析 以HOMA-IR為因變量,各臨床指標(biāo)(連續(xù)變量)為自變量,經(jīng)Pearson相關(guān)分析結(jié)果顯示,DN患者HOMA-IR與BMI、UAER、肌酐、胱抑素C、Hcy呈正相關(guān)(P<0.05),見表2。

表2 DN患者HOMA-IR與一般臨床資料的相關(guān)性分析
2.3影響DN患者不良預(yù)后的Cox單因素和多因素分析 以60個月內(nèi)發(fā)展為終末期腎病為因變量,以表1中所有臨床指標(biāo)為自變量代入Cox回歸模型進行單因素分析,結(jié)果顯示,UAER、肌酐、胱抑素C、Hcy及HOMA-IR在單因素分析中差異有統(tǒng)計學(xué)意義(P<0.05)。將單因素分析中差異有統(tǒng)計學(xué)意義的指標(biāo)代入多因素分析,校正和控制混雜變量后,結(jié)果顯示,UAER及HOMA-IR為影響DN患者疾病無進展生存時間的獨立危險因素(P<0.05)。其中HOMA-IR每增加1個單位,DN患者60個月內(nèi)進展為終末期腎病的風(fēng)險增加2.032倍。見表3、4。

表3 影響DN患者不良預(yù)后的Cox單因素分析

表4 影響DN患者不良預(yù)后的Cox多因素分析
2.4HOMA-IR預(yù)測DN不良預(yù)后的ROC曲線分析 根據(jù)HOMA-IR預(yù)測DN患者不良預(yù)后的ROC曲線選取最佳截斷值,以HOMA-IR為19.6作為最佳截斷值來預(yù)測DN患者不良預(yù)后的靈敏度和特異度分別為85.5%和76.2%,ROC曲線下面積(AUC)為0.825(95%CI:0.763~0.894,P<0.05),見圖1。

圖1 HOMA-IR預(yù)測DN不良預(yù)后的ROC曲線
2.5兩組DN患者隨訪60個月疾病無進展生存率比較 以HOMA-IR的最佳截斷值將所有納入患者分為兩組(HOMA-IR<19.6組(171例)和HOMA-IR≥19.6組(41例),Kaplan-Meier生存分析結(jié)果顯示,HOMA-IR<19.6組患者12、36、60個月疾病無進展生存率分別為91.2%、73.1%、68.4%,HOMA-IR≥19.6組12、36、60個月疾病無進展生存率分別為82.6%、52.5%、41.5%,兩組DN患者隨訪60個月疾病無進展生存率比較,差異有統(tǒng)計學(xué)意義(P<0.05)。見圖2。

圖2 兩組DN患者隨訪60個月疾病無進展生存率比較
3 討 論
DN已成為糖尿病最常見及嚴(yán)重的并發(fā)癥之一。我國33.6%的糖尿病患者并發(fā)有腎損傷,DN已成為我國慢性腎衰竭的主要原因,此外我國慢性腎臟病的患病率為10.8%,其中有36.4%的患者有糖尿病基礎(chǔ)病,DN患者的病死率遠遠高于單純的糖尿病患者[3]。常見DN的發(fā)病機制主要有遺傳因素、糖脂代謝異常、腎素-血管緊張素系統(tǒng)、激肽釋放酶-激肽系統(tǒng)、炎癥因子作用及微循環(huán)障礙等[9-10]。由此可見,DN是一個復(fù)雜的臨床綜合征,發(fā)病機制多種多樣。近期有研究發(fā)現(xiàn),胰島素抵抗在DN的發(fā)生和發(fā)展中起重要的作用,糖尿病患者發(fā)病的中心環(huán)節(jié)和致病基礎(chǔ)就是胰島素抵抗,胰島素抵抗在腎臟功能失調(diào)中起重要推進性作用,胰島素抵抗可通過胰島素直接損傷、促進生長因子作用、激活腎內(nèi)RAS系統(tǒng)、增加內(nèi)皮素產(chǎn)生和活性、損傷足細胞等多種途徑參與DN的發(fā)生和發(fā)展[11]。因此,探索影響DN患者生存和預(yù)后的影響因素,深入研究胰島素抵抗在DN的發(fā)生、發(fā)展中的作用,對于早期防治DN具有十分重要的臨床意義。
本研究通過比較預(yù)后良好和預(yù)后不良兩組DN患者一般臨床資料發(fā)現(xiàn),隨訪60個月內(nèi)發(fā)展為終末期腎病的DN患者HOMA-IR明顯高于預(yù)后較好的DN患者。進一步通過Pearson相關(guān)性分析,結(jié)果顯示,DN患者HOMA-IR與BMI、UAER、肌酐、胱抑素C、Hcy呈正相關(guān),UAER及HOMA-IR為影響DN患者疾病無進展生存時間的獨立預(yù)測因素,其中HOMA-IR每增加1個單位,DN患者60個月內(nèi)進展為終末期腎病的風(fēng)險增加2.032倍,以上研究結(jié)果提示胰島素抵抗和蛋白尿與DN患者的遠期預(yù)后密切相關(guān)。SLOAN[12]使用穩(wěn)態(tài)模型評價HOMA-IR,研究HOMA-IR與蛋白尿的關(guān)系發(fā)現(xiàn),胰島素抵抗可導(dǎo)致腎小球足細胞蛋白變性而致尿蛋白。DE COSMO等[13]的研究表明,胰島素抵抗所導(dǎo)致的高血壓、血脂紊亂等代謝綜合征是腎功能惡化的獨立危險因素,它們共同加速了DN的病程發(fā)展。SHIM等[14]的研究也發(fā)現(xiàn),尿蛋白是DN的早期標(biāo)志物,以及疾病進展的獨立危險因素,以胰島素抵抗為中心的代謝綜合征與蛋白尿密切相關(guān),參與了腎小球濾過率的下降,改善胰島素抵抗的藥物能減少2型糖尿病患者的尿蛋白。以上研究再次證實了本研究結(jié)論,此外本研究通過繪制HOMA-IR預(yù)測DN不良預(yù)后的ROC曲線,獲得其最佳截斷值,以HOMA-IR的最佳截斷值將所有患者分為兩組,Kaplan-Meier生存分析結(jié)果顯示,HOMA-IR<19.6組患者12、36、60個月疾病無進展生存率高于HOMA-IR≥19.6組,提示當(dāng)DN患者HOMA-IR≥19.6時,60個月內(nèi)進展為終末期腎病的風(fēng)險較大,以HOMA-IR來預(yù)測DN患者的預(yù)后具有較高的臨床應(yīng)用價值。胰島素抵抗促進尿蛋白和腎損傷,加速DN進展,其可能機制為胰島素抵抗及其相關(guān)的高胰島素血癥可上調(diào)RAS系統(tǒng)的活性,觸發(fā)一系列細胞信號傳導(dǎo)通路,通過激活關(guān)鍵的轉(zhuǎn)錄因子介導(dǎo)細胞損傷和炎性反應(yīng),在細胞信號的作用下,相關(guān)細胞產(chǎn)生各種炎癥因子,導(dǎo)致炎癥、氧化應(yīng)激反應(yīng)、細胞損傷、纖維化和腎小球濾過率的降低,足細胞變形消失,內(nèi)皮細胞功能紊亂,腎小球基底膜的改變和腎小管的損傷導(dǎo)致尿蛋白的產(chǎn)生,造成DN的進展[15-17]。
綜上所述,胰島素抵抗通過上調(diào)DN患者體內(nèi)腎素-血管緊張素系統(tǒng),改變血管內(nèi)皮細胞分泌的血管活性介質(zhì),使腎臟血管內(nèi)皮細胞受損,催化生成腎臟活性氧并參與氧化應(yīng)激反應(yīng)及通過影響腎臟血流動力學(xué)、腎小球濾過率、腎小管重吸收從而導(dǎo)致腎損傷。HOMA-IR對DN患者預(yù)后具有較好的預(yù)測價值,HOMA-IR≥19.6的DN患者5年內(nèi)發(fā)展為終末期腎病風(fēng)險較大。
- 國際檢驗醫(yī)學(xué)雜志的其它文章
- VEGF、S-100P及clusterin在腱鞘巨細胞瘤中的表達情況及臨床意義
- 2型糖尿病患者血清S100A12、sRAGE與頸動脈內(nèi)膜中層厚度的相關(guān)性研究*
- 成人流感樣病例13種病原體檢測情況及多重PCR毛細電泳片段分析法檢測的臨床應(yīng)用
- 普通培養(yǎng)法聯(lián)合革蘭染色Nugent評分在BV相關(guān)GV鑒別診斷中的臨床應(yīng)用
- 血清sCD54、presepsin水平對多發(fā)性骨髓瘤的診斷價值及與患者預(yù)后的關(guān)系
- miR-125b、miR-29a、miR-425-5p在子宮內(nèi)膜癌患者血清中表達水平變化及臨床意義

