基于網絡藥理學高脂血癥中醫藥治療靶點預測
★ 張璋 張婉晴 單思(.江西中醫藥大學藥學院 南昌 330004;.江西中醫藥大學中醫基礎理論分化發展研究中心 南昌 330004)
高脂血癥是由于人體脂質代謝異常使血漿中脂質和脂蛋白水平異常,表現為血清膽固醇、甘油三酯或低密度脂蛋白的水平升高,或高密度脂蛋白水平降低[1]。該病常見于中老年人,但是隨著社會發展和競爭壓力增大,吸煙飲酒人群的擴大,高脂血癥的發病率不斷增長,患者的也越來越年輕化。高脂血癥是導致動脈粥樣硬化的重要致病因素,動脈粥樣硬化又是導致心腦血管疾病的元兇。在青年時期高脂血癥沒有癥狀表現,但它實際不斷侵蝕血管上皮細胞,逐漸增加血液黏度,形成血管硬化,引發高血壓、心絞痛、心肌梗死、中風,腎性高血壓、腎功能衰竭,肝損傷,侵害機體細胞,機體酸化,肥胖,降低人體抵抗力。在前期基于數據挖掘對中醫藥治療高脂血癥中藥用藥規律研究找出治療高脂血癥3個中藥組合(組合1:半夏、陳皮、茯苓、白術;組合2:山楂、大黃、丹參、決明子、何首烏、澤瀉;組合3:枸杞子,山茱萸,山藥,熟地黃)[2]。網絡藥理學整合強大的生物信息學數據庫和IPA軟件分析,提高了研究對象的針對性和前瞻性,為后續的驗證研究提供清晰思路和更多的想象空間。為探析這三個中藥組合治療高脂血癥的作用機制,進一步通過網絡藥理學方法預測分析中藥組合及高脂血癥的分子作用網絡和作用位點。
1 研究方法
1.1 高血脂癥人類相關基因數據獲取
利用Gene Cards數據庫,以hyperlipidemia為關鍵詞,查找高脂血癥的人類相關基因,獲取高脂血癥Gene Symbol。
1.2 藥物活性成分數據的獲取
聯合利用TCMSP數據庫、TCMID、BATMANTCM數據庫,檢索藥物組合1(茯苓、白術、陳皮、半夏)、藥物組合2(澤瀉、決明子、大黃、丹參、山楂、何首烏)、藥物組合3(熟地黃、山藥、山茱萸、枸杞子)化學成分,檢索詞均為藥物中文拼音。
TCMSP檢索到的藥物組合1(茯苓、白術、陳皮、半夏)、藥物組合2(澤瀉、決明子、大黃、丹參)、藥物組合3(熟地黃、山藥、山茱萸、枸杞子)化學成分利用ADME參數,篩選藥物活性化合物。參考數據庫建議標準制定篩選標準:分子量180~500,生物利用度(OB)≥30%,類藥性(DL)≥0.18,藥物半衰期(HL)≥4h且有PubChem_Cid的成分。TCMSP檢索不到的山楂利用TCMID檢索,何首烏利用BATMAN-TCM檢索。檢索到的藥物組合化合物取交集繪制韋恩圖。
1.3 藥物靶點預測
有機小分子生物活性數據庫PubChem查找各藥物的分子信息,輸入PubChem_Cid查找并獲取靶蛋白Canonical SMILES。將相應的Canonical SMILES粘貼至Swiss Target Prediction數據庫預測化合物潛在作用靶點,按Pro>0.1篩選并獲取相應靶蛋白Common Name。
分別將各藥物組合活性成分靶蛋白與高脂血癥相關基因靶點取交集繪制韋恩圖,提取交集靶標基因;并將三個藥物組合同時與高脂血癥相關基因靶點取交集繪制韋恩圖,提取交集靶標基因。
1.4 構建藥物預測靶點和高脂血癥相關基因分子網絡
分別將藥物組合對應靶蛋白Common Name及高脂血癥的相關基因Gene Symbol,以excel格式上傳至IPA軟件的Dataset Files。運行Core Analysis模塊進行網絡分析,分別構建藥物組合和高脂血癥相關基因的分子網絡。
1.5 比較分析藥物預測靶點及高脂血癥相關基因共同作用的生物學通路及作用位點
利用IPA軟件中的Comparison Analyses模塊,比較分析藥物組合預測靶點及高脂血癥的人類基因的生物學通路;進一步選取部分共同作用的通路進行深入研究,篩選出二者在共同作用的生物學通路中的作用位點。結合通路結果和位點篩選結果,分析預測藥物組合治療高脂血癥可能的分子網絡機制。
2 結果
2.1 高血脂癥靶點數據
截止至2020年5月,GeneCards數據庫檢索到高脂血癥的人類相關基因,即疾病靶點154個。
2.2 藥物活性成分篩選
截止2020年5月,利用TCMSP數據庫對藥物組合1(茯苓、白術、陳皮、半夏)、藥物組合2(澤瀉、決明子、大黃、丹參)、藥物組合3(熟地黃、山藥、山茱萸、枸杞子)化學成分,以相對分子質量180~500,生物利用度≥30%,類藥性(drug-likeness,DL)≥0.18,藥物半衰期≥4 h,且有PubChem_Cid的成分為標準。剔除重復值后,藥物組合1(茯苓、白術、陳皮、半夏)、藥物組合2(澤瀉、決明子、大黃、丹參)、藥物組合3(熟地黃、山藥、山茱萸、枸杞子)篩選最終獲得有效活性成分23、50、29個。利用TCMID數據庫檢索到山楂活性成分94個。利用BATMAN-TCM檢索到何首烏活性成分25個。通過將檢索到的藥物組合的化學成分提取交集繪制韋恩圖可發現,各藥物組合之間既有獨有成分亦有部分相同活性成分,見圖1。推測各藥物組和可能通過相同的生物通路或者作用靶點發揮作用。
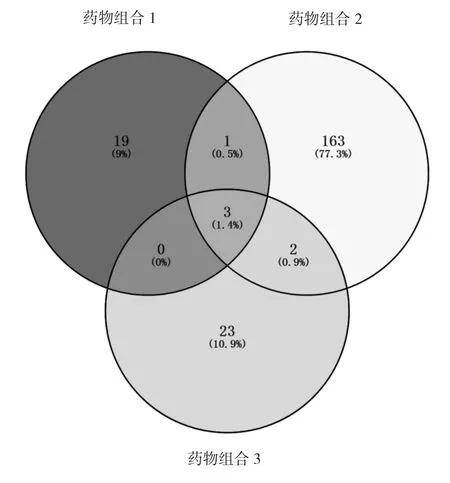
圖1 各藥物組合活性成分韋恩圖
2.3 靶蛋白數據的獲取篩選及高脂血癥疾病靶點提取結果
根據PubChem數據庫和Swiss Target Prediction數據庫,獲取各藥物組合有效活性成分,以Excel格式上傳IPA數據庫,數據庫比對后,匹配藥物組合1、藥物組合2、藥物組合3靶蛋白分別387、181、388個(Pro>0.1)。通過檢索GeneCards數據庫得到的高脂血癥疾病相關靶標共154個,與藥物組合1、藥物組合2、藥物組合3活性成分預測靶標相映射,分別得到交集靶標20、9、15個。見表1、圖2。即為藥物組合1、藥物組合2、藥物組合3活性成分作用于高脂血癥的潛在靶點。
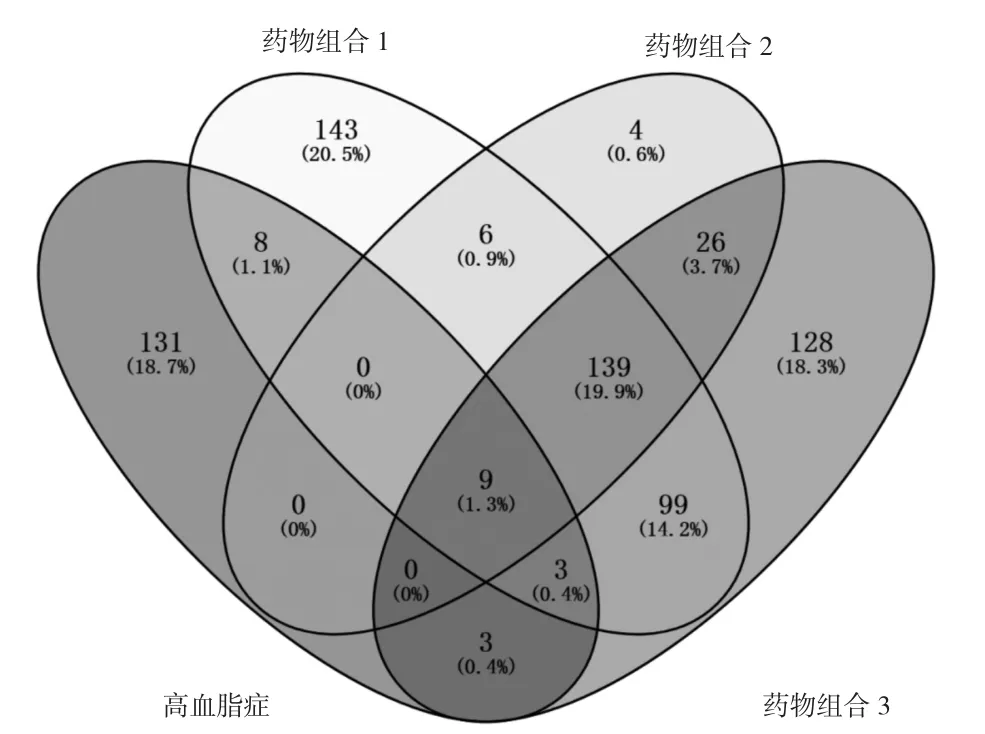
圖2 藥物組合預測靶點與高血脂靶點癥韋恩圖

表1 藥物組合作用于高脂血癥潛在交集靶標
2.4 構建藥物組合和高脂血癥分子網絡
分別將藥物組合靶蛋白及高脂血癥相關基因導入IPA進行Core Analysis分析,結果顯示,構建的各個分子網絡錯綜復雜,功能多樣,但亦有共同的交聯分子及功能。見表2、圖3。圖中每個節點代表一個分子,其中灰色的節點為網絡相關基因,中心區域著色的為藥物組合與高血脂癥交聯的分子,中心區域紅線內著色分子(PPARA、PPARD、SQLE)為3組藥物組合共有交聯分子,SLC10A2為藥物組合1獨有。未涂色的為構建網絡所需的相關分子。實線表示分子間直接作用關系,虛線表示分子間接作用關系。

表2 藥物組合靶蛋白與高脂血癥分子網絡
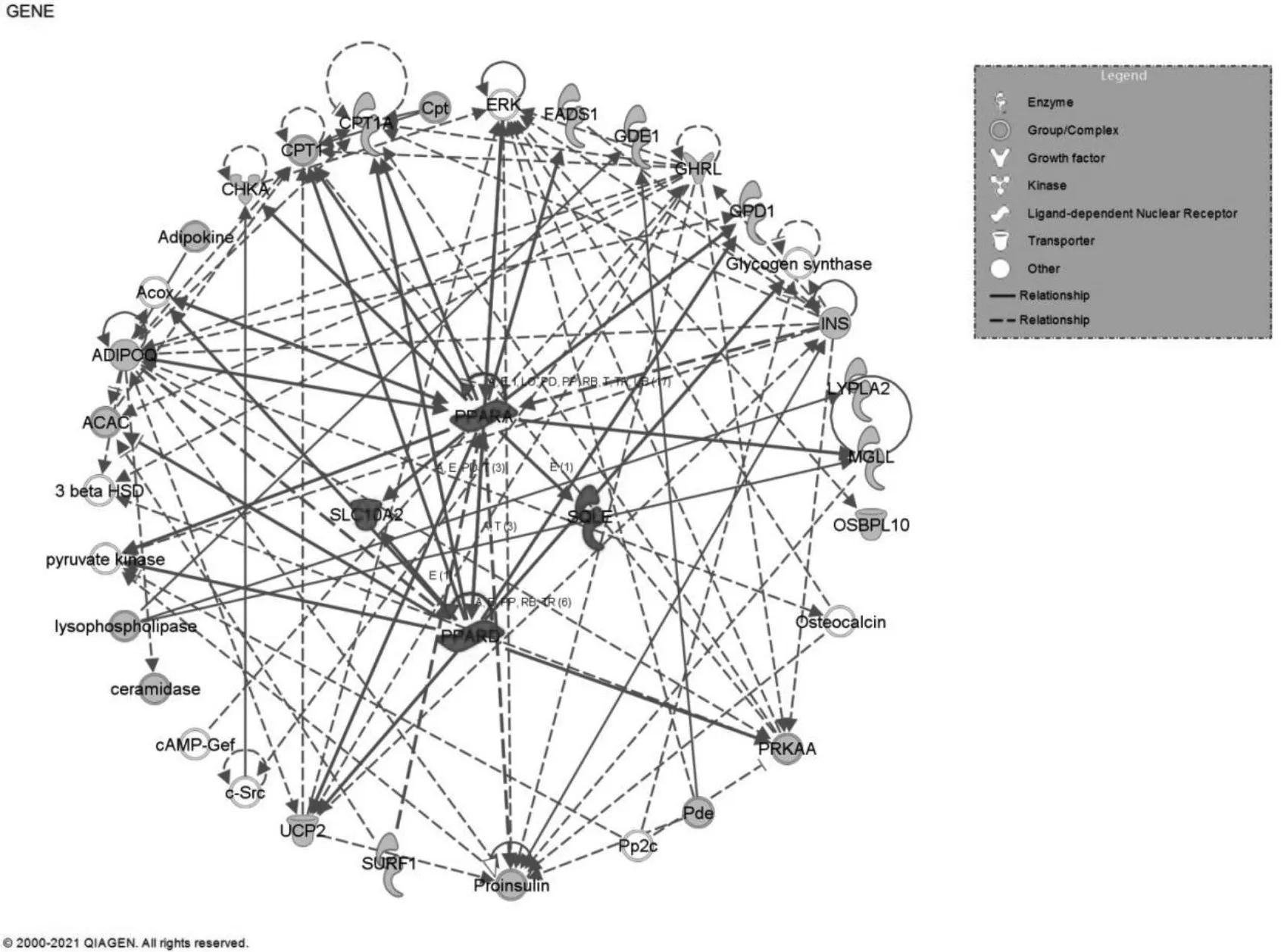
圖3 藥物組合作用于高血脂癥相關基因分子網絡圖
2.5 藥物與高脂血癥生物學通路比較與作用位點分析
通過IPA軟件的Comparison Analysis分析,比較分析藥物組合靶蛋白和高血脂癥相關基因作用的生物學通路,結果發現四者共同作用通路有296條,以炎癥、免疫以及細胞增殖、凋亡和遷移相關通路為主。見圖4。提示藥物組合活性成分可能通過干預炎癥、免疫以及代謝相關通路治療高脂血癥。
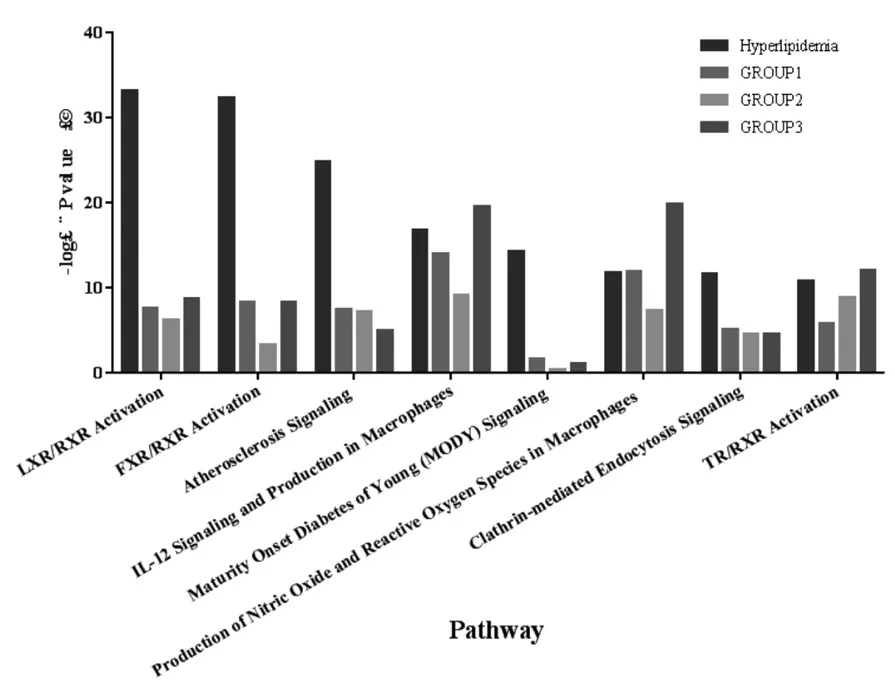
圖4 藥物組合與高脂血癥共同作用的生物通路
藥物組合活性成分靶蛋白和高脂血癥相關基因共同交聯靶分子有ABCB1(三磷酸腺苷黏合轉運體B1)、AKT1(AKT絲氨酸/蘇氨酸蛋白激酶1)、ALOX5(花生四烯酸5-脂氧合酶)、APP(淀粉樣β前體蛋白)、CXCR1(趨化因子受體1)、EGFR(表皮生長因子受體)、AR(雄激素受體)、ESR1(雌激素受體1)、F2(凝血因子II)及IL2(白介素2)等27個。基于以上分析結果選取了一條LXR/RXR信號通路,在通路中邊框涂色標記的MMP9(基質金屬蛋白酶9)、HMGCR(3-羥基3-甲基戊二酰輔酶A還原酶)、NOS(一氧化氮合酶)等多個位點為藥物組合活性成分靶蛋白參與高脂血癥相關通路的作用位點。見圖5。圖中每個節點代表一個分子,其中灰色的節點為網絡相關基因,未涂色的為構建通路所需的相關分子。實線表分子間直接作用關系,虛線表分子間接作用關系。紅色圈分子為藥物組合1、2、3共同作用位點、綠色圈分子為藥物組合1獨有作用位點,藍色圈分子為藥物組合3獨有作用位點

圖5 藥物活性成分靶蛋白和高血脂癥相關基因共同作用LXRRXR信號通路作用位點
3 討論
中醫學中并無高脂血癥病名,屬中醫學“脂濁”“痰”“痰濁”“痰瘀”“血瘀”“眩暈”“胸痹”“真心痛”及“消癉”等范疇。中醫學對高脂血癥病因病機認識有先天稟賦、飲食不節、過逸少勞、情志因素、痰濁不化、瘀血阻滯、臟腑失調等不同,通過化痰祛濁、活血祛瘀、健脾祛濕、疏肝理氣、溫陽補腎等治法,達到扶正祛邪、標本兼治、調整陰陽。
前期研究中藥物組合1有茯苓、白術、陳皮、半夏等中藥,從結構上看類似二陳湯組成,化痰藥為基礎。藥物組合2有澤瀉、決明子、大黃、丹參、山楂、何首烏等中藥,活血化瘀藥為基礎。藥物組合3有熟地黃、山藥、山茱萸、枸杞子等中藥,補益肝腎藥為基礎。3個組合在中醫治療中可針對不同證候類型辨證施治,在治療高脂血癥過程中是否具有共同的機制尚未知。
聯合Gene、PubChem數據庫和IPA軟件分析技術能夠預測藥物和疾病的分子機制和作用靶點,為生物學網路和通路研究提供新思路[3],3個組合和高脂血癥構建的分子網絡較復雜,表達多樣性的生物功能,3個藥物組合與高血脂癥共有的交聯分子PPARA、PPARD、SQLE。分析結果提示:藥物組合活性成分可能通過干預LXR/RXR信號通路等炎癥、免疫以及代謝相關通路治療高脂血癥。通過信號通路中的MMP9、HMGCR、NOS等位點來干預HLP。MMP9表達在高脂血癥臨床病理因素中發揮重要的作用,表達水平可能代表疾病嚴重程度的一個指標[4-9]。通過藥物降低MMP9,可以調節血脂,穩定斑塊,降低IMT值,抗AS,對原發性高脂血癥合并其他疾病有較好療效[10-11]。HMGCR活性大小影響膽固醇合成速度,是膽固醇合成關鍵酶。不僅山楂、決明子、澤瀉等中藥復方提取物能下調HMGCR表達降低高脂血癥模型大鼠血脂水平[12],因為下調HMGCR表達能夠抑制膽固醇生物合成,進而調節脂質代謝紊亂[13-15],阿托伐他汀酯也是通過調節PPAR信號通路和HMGCR基因表達來調節血脂水平[16]。有關文獻提示NOS的活力提升有助于提高血管內皮細胞分泌NO的能力,改善血管內皮功能,改善細胞形態;促進細胞增殖;抑制細胞凋亡,抑制炎癥反應,損傷的血管內皮細胞有保護作用,可調節血脂代謝[17-20]。如山楂濃縮汁極顯著提高了肝臟中NO含量和NOS活性,對高脂血癥小鼠有一定的降血脂作用[21]。3個藥物組合可針對不同中醫辨證分型病人施于治療,MMP9、HMGCR、NOS可能是以上3個藥物組合共同對HLP的作用靶點,可以提示我們治療HLP的基礎靶點應該包括此類靶點,進一步提示藥物組合活性成分可能通過干預炎癥、免疫以及代謝相關通路治療HLP。

