外泌體介導白血病發展進程研究概況
★ 朱大誠 吳慧婷(江西中醫藥大學 南昌 330004)
白血病屬于造血系統惡性增殖性疾病,根據法、美、英協作組分型標準,可將其分成急性髓系白血病(AML)、急性淋巴細胞白血病(ALL)、慢性粒細胞白血病(CML)、慢性淋巴細胞白血病(CLL)四大類。由于造血干細胞在不同階段出現失控性增殖、凋亡受阻等導致除骨髓外其他組織被大量克隆性白血病細胞累積、浸潤,引起出血、貧血、感染和不同程度的肝、脾、淋巴結腫大等一系列臨床表現,嚴重者還可引發繼發性的敗血癥、高尿酸血癥等。自2010年起,在我國因癌癥死亡排序中白血病位于前十位,至2017年白血病次均總費用持續增長,年均增長速度約4%[1];放眼全球,2015年因癌癥導致死亡,白血病占據一半以上[2-3]。目前,臨床上治療白血病方法還是以造血干細胞移植、化療為主,使患者不僅處于被動狀態,還要承受巨大的經濟負擔和治療帶來的副作用。以上一串串觸目驚心的數字無不提醒廣大醫務工作者,尋找高新、潛在的治療白血病手段迫在眉睫。
外泌體研究問鼎諾貝爾醫學獎,主要原因是其分布廣泛,并參與多種生物學功能,如代謝性疾病、神經系統疾病、腫瘤生長發展、血管新生等方面。最早發現外泌體是在免疫反應和抵抗癌癥中起到了細胞間通訊的作用,根據外泌體種類、數目、大小和內含物可對不同腫瘤做出初步診斷。國內外學者研究表明,外泌體可通過促進白血病細胞增殖、輔助免疫逃逸、抑制白血病細胞自噬、促血管新生等促進白血病的發生,在治療方面,外泌體能直接靶向造血干細胞、監測白血病復發和耐藥狀態,還可作為藥物載體和疫苗免疫增強劑發揮治療白血病的作用[4-6]。基于此,本文主要以外泌體介導白血病的發病機制及診斷治療為切入點,從上述幾個方面對外泌體介導白血病發展進程展開討論。與同類綜述不同之處在于,本文搜集文獻較新、內容上完整度更高、更全面,寫作初衷希望醫務工作者能通過閱讀本文從機制上規避白血病病人腫瘤細胞或體液中的外泌體給臨床治療過程中帶來的負面影響,并開拓外泌體在抗腫瘤研究中的新思路。
1 外泌體概述
1.1 外泌體的形成
1983年外泌體首次在綿羊網織紅細胞培養上清液中被發現,它是由活細胞分泌的直徑在40~100 nm且具有脂質雙分子層結構的膜性囊泡。外泌體在人體中的分布十分廣泛,在血液、脊髓液、唾液、尿液等體液中都有其存在。外泌體膜上可以攜帶脂質、核酸、蛋白質等生物活性物質,并將其傳遞給受體細胞,從而改變細胞的生理或病理功能,故外泌體又被稱為細胞間的信使[7]。外泌體的合成與分泌(見圖1):首先由細胞膜內陷形成內體(A),并轉運所需的跨膜蛋白、內吞體分選轉運復合體、凋亡相關基因-2受體蛋白等,將一些泛素化“貨物”以出芽形式形成一個個小囊泡,小囊泡再匯聚成大型多泡體(MVBs)(B),MVBs可直接與細胞膜融合,將小囊泡釋放到細胞外(C),這些被釋放的小囊泡即為外泌體。
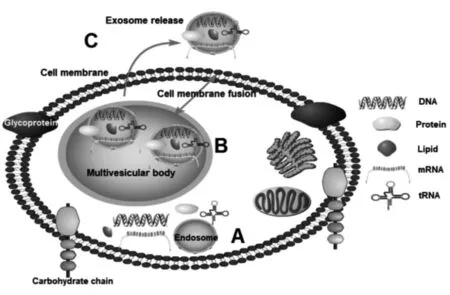
圖1 外泌體的合成與分泌
1.2 外泌體的特征
在外泌體被發現后的十年間,其被科學家誤認為是細胞排泄出的“垃圾”產物,直至1996年在抗原提呈細胞(APC)分泌的外泌體中發現,其可以刺激T細胞體外增殖和誘導體內抗腫瘤免疫反應。外泌體之所以能掀起科研的熱潮,和它攜帶的各種膜標志物、活性蛋白、核酸等多種生物信息來完成細胞間通訊密不可分,在機體癌癥的發生和進展中發揮著類似“順豐快遞”的作用,這也正是外泌體的特色所在。
外泌體中攜帶親本細胞來源的豐富的蛋白質、DNA、mRNA、microRNA、磷脂等重要生物信息成分,主要通過三種方式參與細胞RNA轉運、免疫應答等生理及病理過程。一是在細胞基質中,外泌體膜蛋白可以被具有特異性蛋白酶剪切,剪切下來的碎片作為配體與受體結合,使受體接收“新的”生物學信號。二是親本細胞蛋白可以直接與靶細胞膜蛋白結合,從而激活靶細胞細胞內的信號通路。三是外泌體膜可以直接與靶細胞膜融合,釋放非特異性的蛋白質、非編碼RNA、核酸等[8-9]。通過ExoCarta數據庫發現,目前構成外泌體總共包括41 860種蛋白質、3 408種mRNA、2 838種microRNA,其中蛋白質的種類和含量決定了外泌體親本細胞的來源。主要常見的有組織相容性復合體(MHC)、熱休克蛋白(HSP70、HSP90等)、跨膜蛋白(CD63、CD9、CD81等)、合成MVBs的蛋白質(ALIX、TSG101等)等[10-11]。根據外泌體所含蛋白質種類的不同可以將外泌體進行鑒定與分離,換句話說,以上蛋白或分子可作為外泌體的特殊標志物,為外泌體發揮細胞間信號轉遞、抗原呈遞、免疫治療等作用帶來了可靠保障。
2 外泌體介導白血病發生機制
通過比較外泌體的分子成分時發現,來自腫瘤細胞的外泌體和正常細胞的外泌體的核酸與蛋白質組分存在明顯區別[12]。是什么原因導致這種差異?經研究發現,這是因為外泌體與促白血病細胞增殖、幫助其躲避免疫應答、抑制白血病細胞自噬及促血管內皮細胞生長等惡性生物學行為有關(見圖2)。為此,以下將圍繞外泌體是如何巧妙地通過這四個經典途徑介導白血病的發生展開簡要闡述。

圖2 外泌體介導白血病機制
2.1 促進白血病細胞增殖
腫瘤細胞的惡性增殖是癌癥的基本特征。腫瘤來源的外泌體對親本細胞有促增殖、抗凋亡的作用。通過miRNA陣列顯示,miR-3613-3p是癌相關成纖維細胞(CAFs)外泌體中的miRNA,通過下調CAFs外泌體中miR-3613-3p可靶向調控細胞因子信號轉導抑制因子2(SOCS2)表達,從而抑制乳腺癌細胞的增殖和轉移,但miRNA在CAFs外泌體中的作用和分子機制仍不清楚[13]。CLL細胞來源的外泌體富含miR-202-3p,miR-202-3p的靶基因通過Gli-Hedgehog信號通路以增加Fused抑制蛋白表達,從而輔助腫瘤細胞的生存和增殖[14]。經實時熒光定量PCR(qRT-PCR)和蛋白印跡(WB)實驗分析顯示,LAMA84細胞來源的外泌體通過可激活受體細胞 ERK、NF-kB和 Akt 信號通路,使抗凋亡分子BCL-w、BCL-xl和survivin的mRNA和蛋白水平升高,及使促凋亡分子BAD、BAX和PUMA降低,以便刺激白血病細胞的增殖[15]。Circ_0009910是一種新型的白血病相關環狀RNA,在HL-60和MOLM-13細胞外泌體中circ_0009910呈現上調趨勢,若阻斷circ_0009910可抑制HL-60和MOLM-13細胞的增殖和細胞周期進程,同時伴有較低的B細胞淋巴瘤Bax蛋白增加[16]。另外,外泌體對兒童急性淋巴細胞白血病(PALL)細胞的增殖也有一定影響,通過分離PALL患者血清中的外泌體,發現PALL-Exo中的miR-181a呈現過表達情況,并能通過調控增殖基因(PCNA、Ki-67)等誘導白血病B細胞系的細胞發生增殖,換句話說,外泌體miR-181a抑制劑可能是治療PALL的新靶點(見圖2)[17]。
2.2 實現免疫逃逸
腫瘤免疫逃逸是指腫瘤細胞通過各種機制逃避來自機體免疫系統識別及攻擊,從而達到在機體內增殖和生存的目的。白血病來源的外泌體攜帶免疫抑制分子并將其傳遞給受體免疫細胞,主要通過抑制巨噬細胞、Treg細胞、NK細胞等免疫細胞功能,實現免疫抑制和降低抗腫瘤免疫應答,從而幫助白血病細胞逃避機體免疫細胞識別。Hong C S等[18]開發了小鼠AML PDX模型,發現完全移植的AML PDX小鼠產生的外泌體特征與捐贈細胞用于移植的AML患者血漿中分離的外泌體相似,移植白血病細胞產生攜帶人類白血病相關抗原的外泌體,AML衍生的外泌體攜帶免疫抑制蛋白傳遞給受體免疫細胞,抑制其功能。研究證實,用K562來源的外泌體處理人骨髓間充質干細胞(BMSCs)和小鼠巨噬細胞,結果表明外泌體處理BMSCs導致NO產量增加和ROS產量減少,以及巨噬細胞中IL-10過表達和iNOS轉錄水平的下調,調節巨噬細胞的氧化還原電位,引導巨噬細胞向腫瘤相關巨噬細胞極化,從而影響骨髓生態位,創造對腫瘤有利的微環境[19]。有研究發現,將CLL來源的外泌體或hY4單獨轉移到單核細胞可促進IL-6、CCL2、PD-L1的表達(見圖2),從而驅動TLR信號有助于腫瘤細胞躲避免疫攻擊,導致病情發展迅猛[20]。雖然BAG6的外泌體自身就存在缺陷,但在CLL晚期患者血漿中可溶性BAG6 水平明顯升高,這可能與其促進白血病細胞參加免疫逃逸相關[21]。
2.3 抑制自噬
自噬幾乎存在于所有真核生物中,適度的自噬有利于清除損傷的細胞器和出現錯誤折疊的蛋白質。在細胞、分子水平上,不僅絲狀偽足可以作為外泌體內化的部位,使這些細胞突起的動態解構過程中內吞作用增強,而且自噬相關蛋白質復合物也能參與外泌體的發生,二者在機制上交互通信,在功能上相輔相成,對維持細胞適應性和穩態起著重要的作用。同K562比較,K562R(IMT)細胞中的外泌體釋放PI3K/Akt/mTOR信號靶標和自噬活性顯著增加,達沙替尼通過下調Akt/mTOR活性,下調beclin-1和Vps34的表達,從而防止外泌體釋放和抑制自噬(見圖2),促進對伊馬替尼耐藥的CML細胞發生凋亡[22]。自噬對白血病細胞常表現出雙重性,但關于其與外泌體的相關研究還有待加強,未來就外泌體-自噬相互作用很有可能成為攻克白血病復發和耐藥的新型策略[23]。
2.4 促血管新生
血管的新生能為癌細胞提供營養,也是癌癥惡化的標志之一。有研究顯示,AML細胞來源的外泌體含有血管內皮生長因子(VEGF)和VEGF受體的mRNA,可以誘導人臍靜脈內皮細胞(HUVECs)表達VEGFR及促進HUVECs糖酵解,導致HUVECs增殖血管重構和獲得化療耐藥性,這些發現可能有助于開發針對AML來源的外泌體新的治療策略[24]。有學者發現,內皮細胞通過攝取CLL來源外泌體后,形成管腔樣結構能力增強,其機制可能與外泌體富集miR-146a、miR-155、miR-150的調控相關[25]。CLL患者的細胞內氯離子通道蛋白1(CLIC1)顯著增加,并在CLL細胞分泌的外泌體中顯著富集,外泌體通過轉移CLIC1來調控ITGβ1-MAPK /ERK信號,加速HUVECs轉移和血管生成,提示CLIC1可能是CLL外泌體在腫瘤微環境中的治療靶點(見圖2)[26]。還有研究表明,CML細胞來源的外泌體可直接與內皮細胞相互作用,促進血管新生[27]。
3 分子標志物參與白血病靶向診斷
現有白血病診斷方法不利于其早期診斷,存在誤診率高、重復性低的現象。同健康人比較,白血病患者血清中含有大量外泌體,并攜帶親本細胞來源的特異性的致病信息分子,如microRNA受外泌體表面膜保護,具備較好的穩定性,因此可作為理想的分子標志物,用于白血病的靶向診斷和預后。田淼等[28]采用solexa法對7例 AML 患者和7 例健康對照者血漿外泌體中 miRNAs進行測序,發現2個新miRNAs和211個已知的差異表達miRNAs, 其 中 miR-155-5p、miR-335-5p、xxxm0038-5p及miR-451a差異顯著,通過對上述4種miRNA進行富集分析和靶基因預測,發現AML 患者血漿中外泌體 miRNA特異性明顯,這一發現對進一步研發AML白血病標記物診斷和無創診斷方法有深遠的意義。劉靜茹等[29]對提取THP-1和HL-60細胞中外泌體,并對HL-60外泌體進行鑒定,通過流式細胞術發現其中存在特異性抗原分子CD81及CD63,該方法能夠快速、簡便地為白血病早期診斷提供依據。AML的生物標記物FLT3、NPM1、MMP9、IGF-IR和 CXCR4及 涉 及 白 血病復發的mRNA同時出現在AML外泌體中[30]。Moloudizargari M[31]發現在白血病患者血清中分泌更多的外泌體,其中miR-155、miR-17-5p、miR-1246和Let-7b等作為非侵入性生物標志物呈現高穩定性和特異性表達。呂云飛[32]通過qRT-PCR檢測到AML患者外周血外泌體含量明顯增高,其中Let-7b、miR-660、miR-532高表達的患者總生存期和無事件生存期相對更長。Xu Y C等[33]通過納米跟蹤、深度RNA測序等技術,找到BMSCs外泌體對AML細胞的影響及其潛在的miRNA介導機制,在KG-1a細胞中,BMSCs來源的外泌體可能通過hsa-miR-124-5p作用,促進細胞凋亡及抑制周期進程,這些發現突出了白血病來源的外泌體在細胞表達中的貢獻,及其作為生物標志物和治療策略靶標的潛在價值。
4 外泌體在白血病治療中的作用
4.1 藥物遞送
因外泌體具有脂質雙分子結構,其中的miRNA可受其保護,不易被RNase水解,具有靶向性強、生物兼容性、高穩定性、以及能跨越血腦屏障等獨特優勢,因此外泌體能作為較理想的藥物遞送載體[34]。迄今為止,外泌體作為藥物載體所載運的“貨物”主要包括基因類藥物(siRNA、mRNAs及非編碼RNA等)、抗癌類藥物(紫杉醇、阿霉素)和增強免疫等等。Bellavia D等[35]利用HEK293T 細胞來表達與IL-3片段融合的外泌體蛋白Lamp2b,搭載伊馬替尼的IL3-Lamp2b外泌體能夠靶向作用于CML細胞并抑制體內、外癌細胞增殖。Altanerova U等[36]研究提出,將氧化鐵納米顆粒標記MSC后,其可以釋放含有氧化鐵的外泌體,當腫瘤細胞內吞該外泌體時,外部交變磁場誘導熱療后, 能發揮消融腫瘤細胞的作用。另外,關于植物外泌體的研究也在不斷深入,特別是在中醫藥抗腫瘤方面,如在人類血液中能檢測到吃過植物食物的miRNA,古言藥食同源,也許就能達到異曲同工之妙;再有通過NCBI GEO數據庫證實健康人體組織RNAseq原始數據樣本和黃芩、半枝蓮、柴胡等中藥外泌體中miRNA確實可以進行跨界轉運,以此發揮抗炎、抗腫瘤等多種作用,這一發現對于利用攜帶miRNA 中藥外泌體治療腫瘤來說也是一個新的契機[37-39]。如,外泌體能作為姜黃素載體,通過外泌體將姜黃素遞送至腫瘤細胞中以促癌細胞毒性,抑制腫瘤細胞生長,顯著增加姜黃素生物利用度,為開發新型抗癌藥物提供依據[40-41]。
4.2 免疫療法
外泌體好似一把雙刃劍,在白血病發病機制中起著負面作用,但在治療白血病中又蘊含巨大潛能,如外泌體已應用于白血病的疫苗接種和作為白血病有效免疫治療劑。Yao Y等[42]基于樹突狀細胞(DC)攝取白血病細胞來源的外泌體(LEX)攜帶有親本的抗原,將L1210 白血病細胞植入DBA/2小鼠中,并分別給予L1210 白血病細胞分泌的外泌體(LEXL1210)、組成DC/LEXL1210復合體,通過分離免疫小鼠T細胞,發現來自經LEXL1210與DC/LEXL1210免疫小鼠的T細胞對 L1210 細胞具有殺傷活性且后者更強。Huang F等[43]發現慢病毒shRNA能沉默親本白血病細胞中TGF-β1的表達,與未修飾LEX相比,LEXTGF-β1si免疫能更有效地促進CD4+T細胞增殖和Th1型細胞因子的分泌,刺激更強的特異性細胞毒性淋巴細胞(CTL)應答和NK細胞毒作用,對小鼠免疫接種LEXTGF-β1si后,能抑制腫瘤生長和延長其生存期,提示外泌體免疫疫苗在免疫治療白血病方面具有很大的潛力。Hus I等[44]在2008年證實了針對CLL的自體DC疫苗接種的潛在效果,結果顯示外周血中白血病細胞和Tregs的數量降低,且對其他惡性血液病的研究也表現出類似的作用。還有,外泌體在MSC中也發揮免疫抑制作用,注射MSC來源外泌體是有效的移植物宿主反應(GvHD)治療方法,能夠減少外周血單個核細胞分泌細胞因子TNF-α、IFN-γ 和 IL-1β[45]。
5 小結與展望
綜上,本文以外泌體為主線,扼要闡明了其參與白血病的發生與發展,從機制引入,到作為生物標志物參與到白血病靶向診斷,最后落足于藥物遞送和疫苗免疫療法。如前文所述,外泌體血管內皮細胞對外泌體攝取能力過強、白血病來源的外泌體通過“蒙騙”和“偽裝”手法助力腫瘤細胞躲避免疫應答,為癌細胞創造更安全的增殖環境等,這些也能作為科研學者找到新的抗癌研究的切入點。
伴隨外泌體在科研圈嶄露頭角,對其諸多研究還有待繼續深入,就像Thery所說,現在對于外泌體的認識,就好比20世紀中后期對于免疫的認識,只知道B細胞能產生抗體,但無法識別與捕獲[46]。的確,現階段關于外泌體與血液腫瘤的研究腳步逐漸放緩,其原因主要有三。一是外泌體“表型”界定問題:盡管外泌體分離、純化方法多樣,但蛋白質種類繁多,某些生物黏液效率低、聚合物無法上下兼容等問題給外泌體分離帶來了阻礙,外加鑒定手段及條件受限,更是難上加難;二是外泌體機制問題:如外泌體攜帶各的種蛋白質和核酸是如何釋放和攝取的等微觀機制給人以猶抱琵琶半遮面之感,同時關于外泌體-自噬交互通信,MVBs運輸中多種媒介物的異質性和同一性等問題也不甚明了,另外如何大量生產外泌體作為藥物載體,并提高裝載效率也值得思考和研究;三對于外泌體應用問題:白血病細胞中攜帶大量外泌體,不同種類的外泌體作為口服或瘤內注射尚沒有使用次數和劑量標準[47],量-時-效關系十分模糊,以及充當生物標志物還形成詳盡的分析以及鮮明的規律。
外泌體的研究領域涉及了中醫藥學、腫瘤學、微生物學、再生醫學等主要學科,諸多學科與外泌體的交叉探索,呈現出百花齊放的外泌體研究領域。“欲窮千里目,更上一層樓”,借此機會筆者寄希望于學術界同仁對于外泌體的研究,如致力于提高外泌體作為納米級藥物載體裝載率、利用轉基因小鼠實驗補充熒光示蹤捕捉外泌體路徑、外泌體對受體細胞的靶向調控和開發疫苗等方面的研究,為外泌體未來能廣泛應用于臨床實踐提供科學依據和借鑒。

