2-甲氧雌二醇對(duì)胎兒生長(zhǎng)受限胎盤(pán)血管內(nèi)皮功能的影響
花玉蓉,朱 怡,吳金婷,金彥琪
(南通大學(xué)附屬婦幼保健院婦產(chǎn)科,江蘇 南通 226001)
胎兒生長(zhǎng)受限(fetal growth restriction,F(xiàn)GR)是新生兒圍產(chǎn)期重要疾病類型,不僅會(huì)導(dǎo)致新生兒病亡率增加,還會(huì)誘使患兒在成年后心血管疾病及耐糖量異常發(fā)生風(fēng)險(xiǎn)增加[1-2]。目前已經(jīng)明確FGR的發(fā)生與胎盤(pán)血管重塑及滋養(yǎng)層細(xì)胞生物學(xué)行為異常有關(guān),滋養(yǎng)層細(xì)胞與血管內(nèi)皮細(xì)胞之間增殖、分化存在輕微協(xié)調(diào)機(jī)制,而這一機(jī)制需要胎盤(pán)組織分泌細(xì)胞因子參與。血管緊張素-2(angiotensin 2,Ang-2)為典型的血管生成激活因子,胎盤(pán)組織中Ang-2水平減少,一方面會(huì)抑制滋養(yǎng)細(xì)胞分化增殖,導(dǎo)致胎盤(pán)血管發(fā)育被抑制,胎盤(pán)血氧缺乏;另一方面其又可以經(jīng)由抑制凋亡及促進(jìn)遷移影響血管內(nèi)皮細(xì)胞功能,進(jìn)而導(dǎo)致FGR發(fā)病[3]。2-甲氧雌二醇(2-methoxyestradiol,2-ME)為17β-雌二醇2號(hào)位被細(xì)胞色素P450羥化,經(jīng)由兒茶酚氧位甲基轉(zhuǎn)移酶(catechol O-methyltransferase,COMT)催化作用形成代謝產(chǎn)物[4]。已有研究顯示,在氧氣缺乏情況下,2-ME可以經(jīng)由促進(jìn)滋養(yǎng)細(xì)胞的遷移、增殖作用誘導(dǎo)滋養(yǎng)層細(xì)胞分化為高侵襲性滋養(yǎng)細(xì)胞,進(jìn)而促進(jìn)滋養(yǎng)細(xì)胞侵入細(xì)胞外基質(zhì),保證正常妊娠[5]。目前已經(jīng)了解到FGR的發(fā)生與胎盤(pán)發(fā)育有關(guān),且2-ME在滋養(yǎng)細(xì)胞分化中發(fā)揮重要作用,而2-ME在FGR中的作用及其在胎盤(pán)血管形成中的作用尚未完全明確。因此,本研究對(duì)FGR孕婦外周血、臍血及胎盤(pán)組織的2-ME水平變化進(jìn)行探討,并應(yīng)用體外細(xì)胞實(shí)驗(yàn)分析2-ME對(duì)胎盤(pán)血管形成的影響,為后期從代謝方面分析FGR發(fā)病機(jī)制提供參考意見(jiàn)。
1 資料與方法
1.1 一般資料
選擇2019年5月至2020年12月期間南通大學(xué)附屬婦幼保健院收治的FGR孕婦66例及正常產(chǎn)檢孕婦50例為研究對(duì)象,將其分為研究組和健康組。
納入標(biāo)準(zhǔn):①依據(jù)有關(guān)文獻(xiàn)[6]中對(duì)應(yīng)標(biāo)準(zhǔn)判定孕婦是否存在FGR;②均為單胎妊娠,且為孕晚期;③應(yīng)用剖宮產(chǎn)進(jìn)行分娩;④孕婦及其家屬同意參與本研究,本研究獲我院醫(yī)學(xué)倫理委員會(huì)批準(zhǔn)同意。排除標(biāo)準(zhǔn):①存在心臟疾病、慢性高血壓、甲狀腺功能異常、肝腎疾病或者糖尿病;②存在產(chǎn)科合并癥或者其他內(nèi)科合并癥;③多胎妊娠孕婦;④存在感染性疾病或者免疫異常疾病。
研究組的年齡為21~32歲,平均(26.59±4.19)歲;分娩孕周為36~40周,平均(38.29±0.94)周;孕次1~3次,平均(2.13±0.53)次;產(chǎn)次1~3次,平均(2.15±0.43)次。健康組的年齡為20~33歲,平均(26.79±4.53)歲;分娩孕周為36~40周,平均(38.59±0.81)周;孕次1~3次,平均(2.43±0.46)次;產(chǎn)次1~3次,平均(2.34±0.34)次。兩組一般資料比較差異均無(wú)統(tǒng)計(jì)學(xué)意義(P>0.05),存在可比性。
1.2 方法
1.2.1 收集臍血和胎盤(pán)組織樣本及人胎盤(pán)微血管內(nèi)皮細(xì)胞
采集研究組和健康組孕婦晨起空腹靜脈血2mL,待其分娩后立即收集臍血3mL,同時(shí)選取1塊(1cm×1cm×0.2cm)靠近臍帶附著位置全層的胎盤(pán)組織,將其置于液氮中凍存。
將人胎盤(pán)微血管內(nèi)皮細(xì)胞(human placental microvascular endothelial cells,hPMEC)在達(dá)爾伯克改良伊格爾培養(yǎng)基(dulbecco′s modified eagle medium,DMEM)(含有10%胎牛血清)中培養(yǎng),hPMEC細(xì)胞置于5%CO2及37℃環(huán)境下細(xì)胞培養(yǎng)箱中培養(yǎng),至hPMEC細(xì)胞生長(zhǎng)到80%~90%融合時(shí)需應(yīng)用胰蛋白酶進(jìn)行傳代,獲得處于對(duì)數(shù)生長(zhǎng)期進(jìn)行后續(xù)細(xì)胞增殖、遷移及小管形成實(shí)驗(yàn)。
1.2.2 實(shí)驗(yàn)材料
2-ME、COMT、Ang-2酶聯(lián)免疫吸附試劑盒購(gòu)自武漢伊萊瑞特生物科技股份有限公司,組織裂解液購(gòu)自北京鼎國(guó)昌盛生物技術(shù)有限責(zé)任公司,二喹啉甲酸(bicinchoninic acid,BCA)蛋白試劑盒購(gòu)自上海睿時(shí)生物科技有限公司,一抗與二抗購(gòu)自Bioss公司,增強(qiáng)型化學(xué)發(fā)光試劑(enhanced chemiluminescence,ECL)顯影劑購(gòu)自上海李記生物科技有限公司,hPMEC購(gòu)自中國(guó)科學(xué)院上海細(xì)胞庫(kù),DMEM培養(yǎng)基購(gòu)自廣州市超博科技有限公司,噻唑藍(lán)(thiazolyl blue tetrazolium bromide,MTT)試劑盒購(gòu)自北京索萊寶公司,Transwell細(xì)胞小室購(gòu)自康寧醫(yī)療器械有限公司,Matrigel基質(zhì)膠購(gòu)自上海浩然生物技術(shù)有限公司。
1.2.3 外周血和臍血及胎盤(pán)組織指標(biāo)的測(cè)定
1.2.3.1 外周血和臍血2-ME水平的測(cè)定 以1 000r/min離心10min處理標(biāo)本,獲得上清液,應(yīng)用酶聯(lián)免疫吸附試劑盒測(cè)定其水平,對(duì)應(yīng)測(cè)定均按照試劑盒說(shuō)明書(shū)中步驟進(jìn)行操作。
1.2.3.2 胎盤(pán)組織COMT水平的測(cè)定 采用蛋白印跡法進(jìn)行測(cè)定,取合適的胎盤(pán)組織,應(yīng)用組織裂解液充分降解,以12 000r/min離心5min,獲得上清液,抽提胎盤(pán)組織蛋白,應(yīng)用BCA蛋白試劑盒測(cè)定抽提蛋白濃度,隨后應(yīng)用十二烷基硫酸鈉聚丙烯酰胺凝膠電泳(sodium dodecyl sulfate polyacrylamide gel electrophoresis,SDS-PAGE),測(cè)定目的蛋白及對(duì)應(yīng)內(nèi)參蛋白(GAPDH)表達(dá)情況,完成SDS-PAGE后蛋白轉(zhuǎn)移到聚偏二氟乙烯膜(polyvinylidenedifluoride,PVDF)上,轉(zhuǎn)移完成后進(jìn)行洗膜處理,應(yīng)用5%脫脂奶粉進(jìn)行封閉。添加一抗后,在4℃環(huán)境下進(jìn)行過(guò)夜孵育,第2d洗膜后,添加二抗置于37℃環(huán)境下孵育1h。孵育完成再次洗膜,添加ECL顯影劑置于暗室曝光顯影。目的蛋白相對(duì)表達(dá)量為目的蛋白與內(nèi)參蛋白條帶灰度值之比。
1.2.4 細(xì)胞實(shí)驗(yàn)
1.2.4.1 細(xì)胞的處理 取處于對(duì)數(shù)期hPMEC,采用胰酶進(jìn)行消化,選擇存在10%胎牛血清DMEM培養(yǎng)液調(diào)成1×105/mL細(xì)胞懸液,接種至96孔板中,應(yīng)用無(wú)胎牛血清DMEM培養(yǎng)基培養(yǎng)24h,應(yīng)用5μmol/L、10μmol/L、15μmol/L濃度的2-ME處理培養(yǎng)細(xì)胞,作為2-ME處理組,而空白對(duì)照組則采用等量培養(yǎng)基處理,各組均設(shè)定5個(gè)復(fù)孔。
1.2.4.2 細(xì)胞增殖的測(cè)定 對(duì)培養(yǎng)細(xì)胞應(yīng)用2-ME處理后,繼續(xù)培養(yǎng)24h、48h,各孔均添加為5mg/mL濃度、20μL體積MTT繼續(xù)處理6h,6h后將孔內(nèi)液體吸去,應(yīng)用酶標(biāo)儀測(cè)定570nm位置吸光度值,最后相對(duì)抑制率=(1-2-ME處理組/空白對(duì)照組)×100%,最終結(jié)果為3次測(cè)定的均值。
1.2.4.3 細(xì)胞遷移的測(cè)定 應(yīng)用無(wú)血清培養(yǎng)基將消化后細(xì)胞配置成1×105/mL懸液,以100μL/孔接種到Transwell細(xì)胞上室中,下室則需要添加存在10%胎牛血清培養(yǎng)基500μL,培養(yǎng)12h后將其中培養(yǎng)液棄去,補(bǔ)充10%胎牛血清培養(yǎng)基,在37℃環(huán)境下培養(yǎng)48h,用棉簽將上層沒(méi)有遷移細(xì)胞輕輕擦去,應(yīng)用4%多聚甲醛固定,出現(xiàn)結(jié)晶紫顏色后置于100倍鏡下隨機(jī)選擇5個(gè)視野,計(jì)算遷移細(xì)胞數(shù)目,最終結(jié)果為3次測(cè)定的均值。
1.2.4.4 小管形成的測(cè)定 在培養(yǎng)板底部添加0.3mL的Matrigel基質(zhì)膠,將其鋪平后,在37℃環(huán)境下靜置處理10h,對(duì)消化后細(xì)胞采用無(wú)血清培養(yǎng)基配置成1×105/mL懸液,隨后以100μL/孔密度進(jìn)行接種,培養(yǎng)12h后將其中培養(yǎng)液棄去,添加存在10%胎牛血清培養(yǎng)基再次培養(yǎng)24h,在倒置顯微鏡下觀察小管的形成。
1.3 觀察指標(biāo)
觀察研究組和健康組孕婦外周血和臍血2-ME、胎盤(pán)組織COMT水平,分析外周血和臍血2-ME、胎盤(pán)組織COMT水平的相關(guān)性;分析不同濃度2-ME處理對(duì)hPMEC細(xì)胞增殖、遷移、小管新形成的影響。
1.4 統(tǒng)計(jì)學(xué)方法
2 結(jié)果
2.1 研究組與健康組孕婦外周血和臍血2-ME及胎盤(pán)組織COMT水平情況
研究組外周血2-ME水平顯著低于健康組(P<0.05),研究組與健康組臍血2-ME水平比較差異無(wú)統(tǒng)計(jì)學(xué)意義(P>0.05);研究組胎盤(pán)組織中COMT水平顯著低于健康組(P<0.05),見(jiàn)表1、圖1。
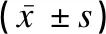
表1 研究組與健康組外周血和臍血2-ME及胎盤(pán)組織COMT水平的比較Table 1 The comparison of 2-ME levels in peripheral blood and cord blood and COMT levels in placental tissue between the two
2.2 外周血和臍血2-ME及胎盤(pán)組織COMT間相關(guān)性的分析
經(jīng)Pearson相關(guān)性分析顯示,外周血2-ME與臍血2-ME、胎盤(pán)組織COMT均呈正相關(guān)(P<0.05),臍血2-ME與胎盤(pán)組織COMT呈正相關(guān)(P<0.05),見(jiàn)表2。

表2 外周血2-ME和臍血2-ME及胎盤(pán)組織COMT間的相關(guān)性Table 2 The correlation among peripheral blood 2-ME,cord blood 2-ME and COMT in placental tissue
2.3 不同濃度2-ME處理組對(duì)hPMEC增殖影響的分析
不同濃度2-ME處理組(5、10、15μmol/L)的hPMEC在24h和48h的細(xì)胞抑制率均顯著低于空白對(duì)照組(F值分別為18.907、18.593,P<0.05),且隨著2-ME處理濃度的增加,24h和48h的細(xì)胞抑制率均逐漸下降(P<0.05),見(jiàn)表3。
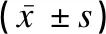
表3 不同濃度2-ME處理組對(duì)hPMEC增殖的影響Table 3 The effect of different concentrations of 2-ME on the proliferation of
2.4 不同濃度2-ME處理組對(duì)hPMEC遷移和血管內(nèi)皮細(xì)胞小管形成度影響的分析
不同濃度2-ME處理組(5、10、15μmol/L)的hPMEC遷移細(xì)胞數(shù)目和血管內(nèi)皮細(xì)胞小管形成度均顯著高于空白對(duì)照組(F值分別為25.751、42.215,P<0.05),且隨著2-ME處理濃度的增加,遷移細(xì)胞數(shù)目和血管內(nèi)皮細(xì)胞小管形成度均逐漸增加(P<0.05),見(jiàn)表4。
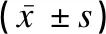
表4 不同濃度2-ME處理組對(duì)hPMEC遷移和血管內(nèi)皮細(xì)胞小管形成度的影響Table 4 The effect of different concentrations of 2-ME on hPMEC migration and endothelial cell tubule
3 討論
3.1 2-ME在FGR發(fā)生中的作用
FGR是重要的妊娠并發(fā)癥之一,在我國(guó)FGR發(fā)病率為3%~7%,F(xiàn)GR新生兒病死率高于正常新生兒的3~5倍,同時(shí)FGR新生兒近期與遠(yuǎn)期并發(fā)癥發(fā)生風(fēng)險(xiǎn)也顯著上升[7]。目前研究認(rèn)為胎盤(pán)血管形成異常所致胎盤(pán)血氧缺乏為FGR發(fā)生的重要原因,2-ME作為雌二醇重要代謝產(chǎn)物之一,主要通過(guò)胎盤(pán)COMT甲基化而誘導(dǎo)形成,在促進(jìn)血管形成、抑制細(xì)胞增殖及促進(jìn)細(xì)胞凋亡中發(fā)揮著重要作用[8]。本研究中,研究組外周血2-ME水平顯著低于健康組,研究組與健康組臍血2-ME水平比較差異無(wú)統(tǒng)計(jì)學(xué)意義,研究組胎盤(pán)組織中COMT水平顯著低于健康組,這些均顯示2-ME及COMT在FGR中發(fā)揮重要作用,分析原因認(rèn)為2-ME在缺氧情況下通過(guò)促進(jìn)血管形成、誘導(dǎo)絨毛滋養(yǎng)細(xì)胞增殖等過(guò)程改善胎盤(pán)血液循環(huán),進(jìn)而影響胎兒生長(zhǎng)[9]。COMT是誘導(dǎo)雌二醇轉(zhuǎn)化為2-ME的重要降解酶,經(jīng)由影響錳超氧化物歧化酶水平而使機(jī)體缺氧誘導(dǎo)因子1α水平保持穩(wěn)定,使血管內(nèi)皮細(xì)胞功能損傷,進(jìn)而誘導(dǎo)FGR發(fā)生[10]。本研究中,研究組與健康組臍血2-ME水平差異不大,可能是因?yàn)槟阁w2-ME不能有效地穿過(guò)胎盤(pán)屏障所致。本研究中對(duì)外周血和臍血2-ME及胎盤(pán)組織COMT間的關(guān)系探究顯示,各指標(biāo)均存在明顯正相關(guān)關(guān)系,提示三指標(biāo)可能共同介導(dǎo)了FGR發(fā)病,但其具體機(jī)制尚需進(jìn)一步研究證實(shí)。
3.2 2-ME在胎盤(pán)組織血管內(nèi)皮功能中的作用
研究顯示雌二醇可以抑制Ang-2所致心血管不良反應(yīng),而2-ME作為雌二醇重要代謝產(chǎn)物,在影響心血管病變中發(fā)揮著重要作用[11]。另一項(xiàng)體外研究顯示,2-ME通過(guò)調(diào)節(jié)磷脂酰肌醇3-激酶/絲氨酸-蘇氨酸蛋白激酶和核轉(zhuǎn)錄因子-κB信號(hào)通路抑制血管細(xì)胞粘附蛋白-1表達(dá),從而阻止單核細(xì)胞與血管內(nèi)皮細(xì)胞的粘附,顯示2-ME可以有效改善內(nèi)皮功能[12]。Zou等[13]應(yīng)用顱內(nèi)靜脈高壓大鼠模型及缺氧人臍靜脈內(nèi)皮細(xì)胞進(jìn)行了體內(nèi)與體外血管形成誘導(dǎo)實(shí)驗(yàn),發(fā)現(xiàn)經(jīng)2-ME處理可以有效抑制缺氧導(dǎo)致血管形成,其主要經(jīng)p53表達(dá)上調(diào)及ID-1表達(dá)下調(diào)發(fā)揮作用。國(guó)外一項(xiàng)對(duì)大鼠的動(dòng)物實(shí)驗(yàn)發(fā)現(xiàn),經(jīng)2-ME處理可以有效抑制慢性間歇缺氧大鼠肺血管形成,其主要經(jīng)影響肺動(dòng)脈平滑肌增殖、活性氧及細(xì)胞遷移等過(guò)程發(fā)揮抑制肺血管形成作用[14]。有研究表明,2-ME可以抑制多種腫瘤細(xì)胞增殖,且這種作用顯示為濃度與時(shí)間依賴性[15]。多項(xiàng)研究顯示,2-ME對(duì)于血管作用具有一定雙面性,其在不同類型疾病中經(jīng)由不同信號(hào)通路影響疾病發(fā)生與進(jìn)展[16-17]。為進(jìn)一步明確2-ME在胎盤(pán)血管形成中的作用,本研究選擇hPMEC進(jìn)行體外細(xì)胞實(shí)驗(yàn),其結(jié)果顯示,經(jīng)2-ME處理可以有效地促進(jìn)hPMEC增殖、遷移及血管內(nèi)皮細(xì)胞小管形成,并上調(diào)Ang-2分泌,且這一趨勢(shì)還會(huì)隨著2-ME濃度的增加而加重,表明2-ME可以有效地促進(jìn)hPMEC血管重塑,其可能經(jīng)上調(diào)Ang-2水平發(fā)揮作用,分析原因可能為2-ME通過(guò)上調(diào)Ang-2水平促進(jìn)滋養(yǎng)細(xì)胞增殖分化,進(jìn)而促進(jìn)胎盤(pán)血管形成。
綜上所述,F(xiàn)GR患者體內(nèi)2-ME水平異常,且與胎盤(pán)COMT水平變化有關(guān),2-ME可能影響胎盤(pán)組織血管內(nèi)皮功能及血管形成,進(jìn)而介導(dǎo)FGR發(fā)生,其中是否存在其他因素影響尚需進(jìn)一步研究證實(shí)。

