指向高階思維能力培養的基礎實驗復習課教學
許乃義 肖紅梅
摘要:以復習“實驗室制備CO2”為例,從反應原理、氣體成分、廢液處理等角度,培養學生分析、綜合、評價等高階思維能力。旨在引導教師復習基礎實驗時,充分發揮其教學過程的“主導”地位,設計高階學習活動,培養學生創新能力、問題解決能力、批判思維能力。
關鍵詞:高階思維能力;化學實驗;分析;綜合;評價
文章編號:1008-0546(2022)06-0062-03
中圖分類號:G632.41
文獻標識碼:B
doi: 10.3969/j .issn.1008-0546.2022.06.013
一、問題的提出
思維是人腦對外部客觀世界對象的能動的和具有創造性的觀念反映。化學思維屬于一種特殊的思維方法,是指在化學知識的掌握過程中,逐步形成的關于物質組成、結構、性質、變化的概念、定律、原理等來間接、概括地反映化學事物、獨具特色的一類思維活動。
化學高階思維是指學生圍繞具有挑戰性和劣構性的化學問題,從宏微結合、變化守恒的視角,借助于化學實驗、化學語言和化學模型,運用證據推理、分析、歸納、抽象和評價等方法,獲得結構化的化學核心知識.原理、養成創新精神和實踐能力的過程中形成的高水平心智活動[1]。
實驗教學對于培養學生化學思維能力的重要性不言而喻,2011年版《義務教育化學課程標準》明確提出了8個學生必須完成的基礎實驗,在進行新授課教學時,大多數老師均能按照教材上相關實驗的“實驗過程”,指導學生獨立完成實驗,但在復習這8個基礎實驗時,老師們往往采取視頻回放或講練習題的方式組織教學,這樣的復習課教學,學生的思維能力往往還停留在原有水平基礎之上。一次題為“‘實驗室制備CO:’專題復習”的市級公開教學上,在市教研員的精心指導下,筆者緊緊圍繞反應原理、氣體成分、廢液處理等教學環節,精心設計了指向培養學生化學高階思維的教學,現將本節課的教學主要環節進行整理分析,以饗讀者。
二、教學主要環節及設計意圖
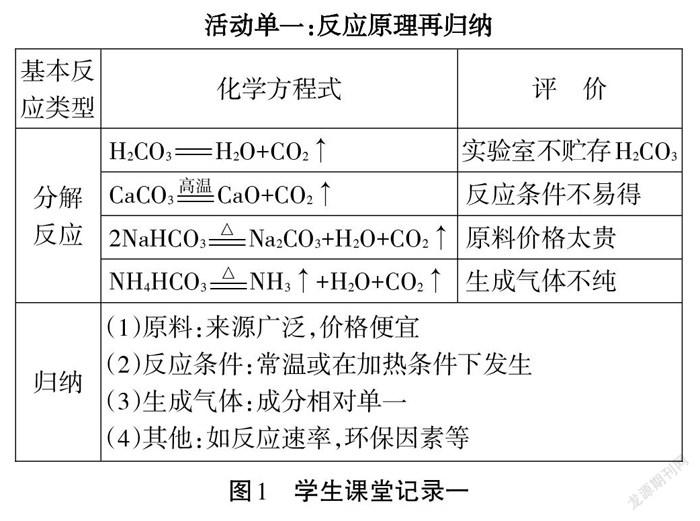
1.反應原理再歸納
問題1:我們知道,實驗室常用石灰石與稀鹽酸反應來制取CO2。請各組回憶一下,能生成CO2的反應還有哪些?
師:將學生分成五個小組,分別為化合反應組、分解反應組、置換反應組、復分解反應組、非基本反應類型組。
分解反應組:寫出相應化學反應方程式并進行評價和歸納,如圖1。
其他組記錄略。
設計意圖:從反應的基本類型的角度書寫相關反應化學方程式,通過小組間互動交流,達成知識共享,再通過過濾、篩選、加工、整理和組合,歸納出實驗室制取氣體在考慮反應原理時,要綜合考慮反應條件、原料來源、氣體純度、便于收集等因素,培養學生思維的有序性和完整性,形成“變化守恒”的化學高階思維能力。
問題2:為什么不用稀硫酸與塊狀石灰石反應制取CO2?如果用稀硫酸與粉末狀的石灰石反應,結果如何呢?
師:提供實驗儀器、相同濃度的稀鹽酸,不同濃度的稀硫酸、顆粒大小基本一致的塊狀石灰石、粉狀石灰石等。
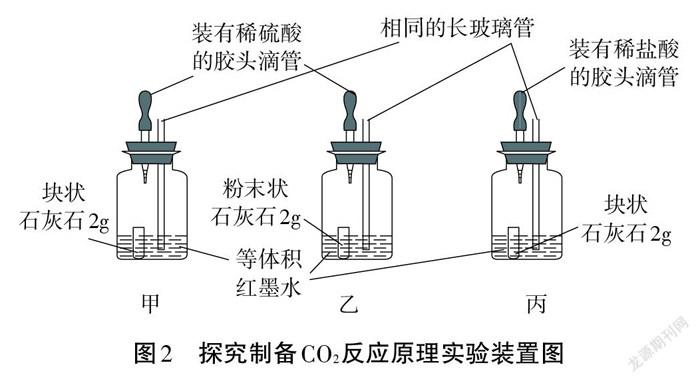
生:每小組按如圖2所示(每組裝置乙中所用稀硫酸濃度與其他組不同),分工完成實驗,記錄裝置甲中實驗現象,比較乙、丙裝置長玻璃管內紅墨水上升的速度快慢。
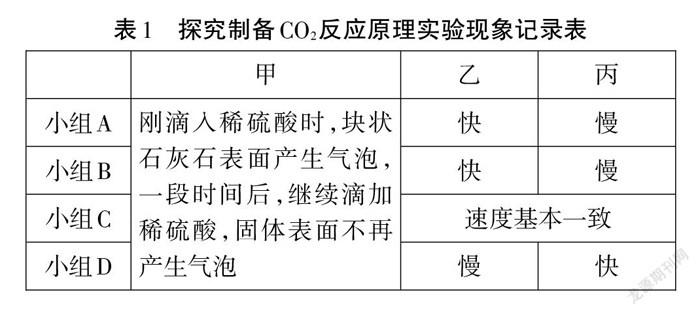
師:根據各組匯報結果,將相關實驗現象匯總整理,如表1。
小結:由于生成的CaSO4微溶于水,使得塊狀石灰石和稀硫酸的反應不能持續反應,但如果控制好稀硫酸的濃度,可用稀硫酸與粉末狀的石灰石反應制備CO2。
設計意圖:復習實驗室制取CO2的實驗基本操作,通過各組實驗的對比分析,得出影響反應速度的因素有酸的濃度、固體形狀等。通過“實證”,說明一定濃度的稀硫酸和粉狀石灰石也可以用來制取CO2,培養學生的創新能力和批判思維能力。
2.氣體成分再分析
問題1:在用澄清石灰水檢驗CO2氣體時,沒有看到澄清石灰水變渾濁,這是為什么呢?
師:提供實驗儀器及相關藥品:久置的石灰水、新制的石灰水、不同濃度的鹽酸、塊狀石灰石等。將學生分為三個大組:A組(正常現象組)、B組(久置的石灰水組)、C組(高濃度鹽酸組),其中A組分兩個小組,編號為A1、A2。
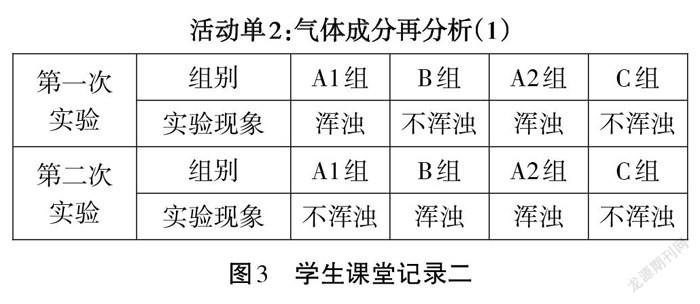
生:各小組按實驗桌上教師提供的儀器和藥品,進行檢驗C02的“第一次實驗”,并記錄實驗現象。在老師的指導下,B組和A1組將所用的“澄清石灰水”對換一下,C組和A2兩組將所用的“澄清石灰水”對換一下,進行檢驗CO2的“第二次實驗”,并記錄實驗現象。實驗現象記錄見圖3。
小結:通過A1組和B組的二次實驗對比,說明第一次實驗中B組所用的“澄清石灰水”已變質;通過A2組和C組的二次實驗對比,說明第一次實驗中C組所用的“稀鹽酸”濃度可能太高,導致生成的中CO2中混有HCl氣體。
設計意圖:通過解決“劣構性”的實際問題,培養學生批判思維能力。化學高階思維能力的培養一定要以挑戰性或解決劣構性的化學問題為主旨[2]。教師發揮主導地位,設計劣構性的化學實驗,學生自主實驗,通過“實證”和“推理”,對實驗現象做出合理判斷,培養學生的批判思維能力和問題求解能力等高階思維能力。
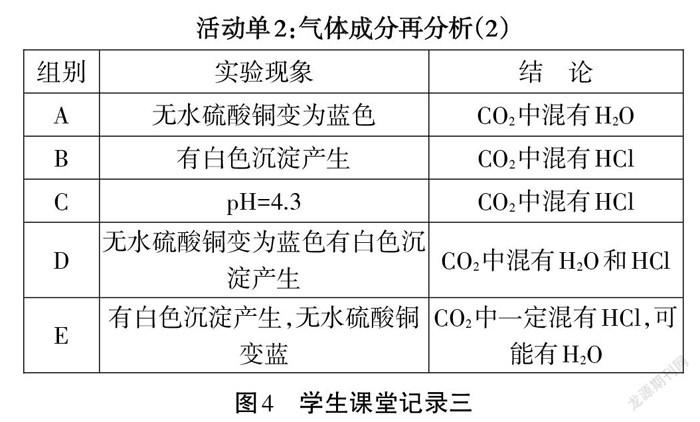
問題2:如何檢驗CO2中可能混有HCl和H2O?
師:指導學生完成實驗。
生:理論分析:鹽酸具有揮發性,CO2中可能混有HCl;CO2從溶液中逸出,CO2中可能混有H2O。 設計方案:用無水硫酸銅檢驗H2O;用硝酸酸化的硝酸銀溶液或pH計等檢驗HCl氣體。
實驗過程:A組:將生成的CO2氣體通過無水硫酸銅。B組:將生成的CO2氣體通過硝酸酸化的硝酸銀溶液。C組:將生成的CO2氣體通過水中一段時間,用pH計測量所得溶液的pH。D組:將氣體依次通過無水硫酸銅、硝酸酸化的硝酸銀溶液。E組:將氣體依次通過硝酸酸化的硝酸銀溶液、無水硫酸銅。實驗記錄見圖4。
小結:通過回顧雨水為什么呈酸性、什么樣的雨水是酸雨等問題,學生對C組實驗的原理有了進一步的認識。通過D和E的方案對比,總結出證明氣體成分中有H2O時,H2O應優先于其他成分先證明。綜合多種因素,認為D組方案最優。
設計意圖:分析、綜合、評價是高階思維的三個維度。在教師的引導下,學生通過理論分析雜質成分,并在對各組方案的評價基礎上,形成解決此類問題的一般思路,培養學生思維的有序性。通過對C組實驗方案的分析和評價,“認識定量研究對于化學科學發展的重大作用”[3],逐步形成用定性和定量兩個手段解決實際化學問題的思維方式。
3.廢液處理再評價
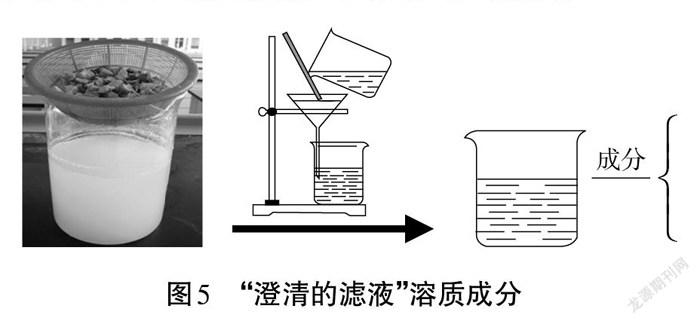
問題1:“澄清的濾液”中含有哪些溶質?
師:引導學生將圖2丙組實驗中塊狀石灰石與鹽酸反應后的產生的“廢物”,按如圖5所示進行處理,并提出問題:“澄清的濾液”中含有哪些溶質?
生:根據書寫化學方程式,得出“澄清的濾液”中一定含有氯化鈣,再依據質量守恒定律,得出“澄清的濾液”可能含有HCl。
師:如何檢驗“澄清的濾液”是否含有HCl?根據學生需要的藥品,將學生分為酸堿指示劑組、活潑金屬組、金屬氧化物組、堿組、碳酸鹽組。
生:每組進行實驗驗證并匯報各組實驗時的實驗現象。
小結:分析反應后溶液中溶質的成分時,首先根據化學方程式判斷一定含有可溶性的生成物,再根據參加反應的物質量之間的定量關系,判斷可能存在可溶性反應物。實驗方案的本質是利用HCl溶液呈酸性,而CaCl2溶液呈中性。
設計意圖:學生圍繞具有真實情境的化學問題,從“變化及守恒”的視角分析“澄清的濾液”中溶質的成分,逐步養成使用化學思維解決問題的自覺性。借助設計實驗方案,驗證“澄清的濾液”是否含有HCl?從而“不自覺”地再一次構建了“酸的通性”學習模型。學生在實驗的同時,也完成假設、推理、判斷、論證等思維過程。
問題2:如何除去“澄清的濾液”中含有的HCl?
師:引導學生對“澄清的濾液”中含有的HCl對環境可能造成的影響進行評價。指導學生通過設計實驗方案除去“澄清的濾液”中含有的HCl,并使除雜后所得溶液中溶質只有氯化鈣,對方案的可行性進行綜合性評價。
生:從對土壤及河流的危害等角度評價HCl對環境的影響。各組設計實驗方案,并列出清單,希望老師能提供藥品完成實驗。
師:根據各組列出的清單,引導學生對各組設計的實驗方案進行評價,形成“溶液中的除雜問題”這一特定題型的解題思路。
生:修訂和完善各組的實驗方案。總結出“溶液中的除雜問題”一般原則:(1)不增,即不增加新的可溶性雜質;(2)不減,即不減少目標物質的量;(3)易分,易從除去雜質后的混合物中分離出目標物質。通過討論為什么不用“鈣”來除去HCl,總結出對“溶液中的除雜問題”方案進行評價時,還要綜合考慮原料來源、經濟價值等因素。
師:在學生修訂和完善各組的實驗方案的基礎上提供相關藥品。
生:完成實驗。
設計意圖:在解決實際問題的實踐中形成人的思維結構。學生修訂和完善實驗方案的過程,就是對主體信息進行過濾、篩選、加工、整理和組合客體信息的過程[3]。總結“溶液中的除雜問題”一般原則的過程,學生思維從“無序”變得“有序”。教師發揮“主導”地位,組織學生討論“為什么不用‘鈣’來除去HCl”的過程,旨在引導學生主動尋求與他人的合作,汲取他人的知識和思維模式,從而提高自己的思維能力。
三、結語
基礎實驗是創新實驗的基礎,是培養學生高階思維的源泉,在課本原有實驗的基礎上進行適度挖掘、再度創造,同樣能使復習課的實驗教學精彩紛呈[4]。教師在組織復習基礎實驗時,可借助學生已有實驗基礎,再引導對該實驗派生出來的相關實際問題進行分析、綜合、評價,培養學生的高階思維能力。高階思維能力的的養成需要高階學習活動予以支持,高階學習是一種以學生為中心,開展問題求解的學習活動,是一種形成知識共享、互動合作的學習方式。每個基礎實驗能派生出哪些高階學習活動?這需要教師充分

