不明原因反復胚胎種植失敗和不明原因反復流產的病因學差異
曾中虹,楊一華
(廣西醫科大學第一附屬醫院廣西生殖醫學研究中心,南寧 530021)
不明原因反復胚胎種植失敗(unexplained recurrent implantation failure,URIF)和不明原因反復流產(unexplained recurrent spontaneous abortion,URSA)是生殖醫學臨床診治難點之一,目前對于URIF和URSA病因學方面研究尚少,它們仍是臨床上困惑最多、困難最大、爭議度最高的話題,如何明確并區分其病因是生殖醫學領域函待解決的難點。URIF和URSA的定義尚無統一說法,兩者在病因上部分重疊又明顯有別。本文通過梳理URIF和URSA兩者的定義以及可能的病因,厘清存在的爭議,為臨床診治以及科學研究提供參考。
一、妊娠建立的生理過程
根據目前已知的胚胎發育的生理過程,囊胚進入宮腔后經過定位、粘附和侵入,完成胚胎著床過程。胚胎著床后,胚外滋養層細胞開始分泌HCG,初期僅在外周血和尿中可以檢測到HCG而B超未能檢測到宮腔孕囊。隨著各胚層的發生與分化[1],超聲下最早出現孕囊[2](原始胚胎組織,被羊膜、血管網包裹的小胚胎),起初是一個空囊,隨后囊內的胚外內胚層、中胚層共同形成了卵黃囊壁,在此基礎上進一步發育為胚芽,于妊娠6周末在胚芽內可見節律的胎心跳動即原始心管搏動,后續各器官系統繼續分化和發育。這個連續的生理過程每一個階段都有可能出現妊娠丟失。妊娠過程示意圖見圖1。
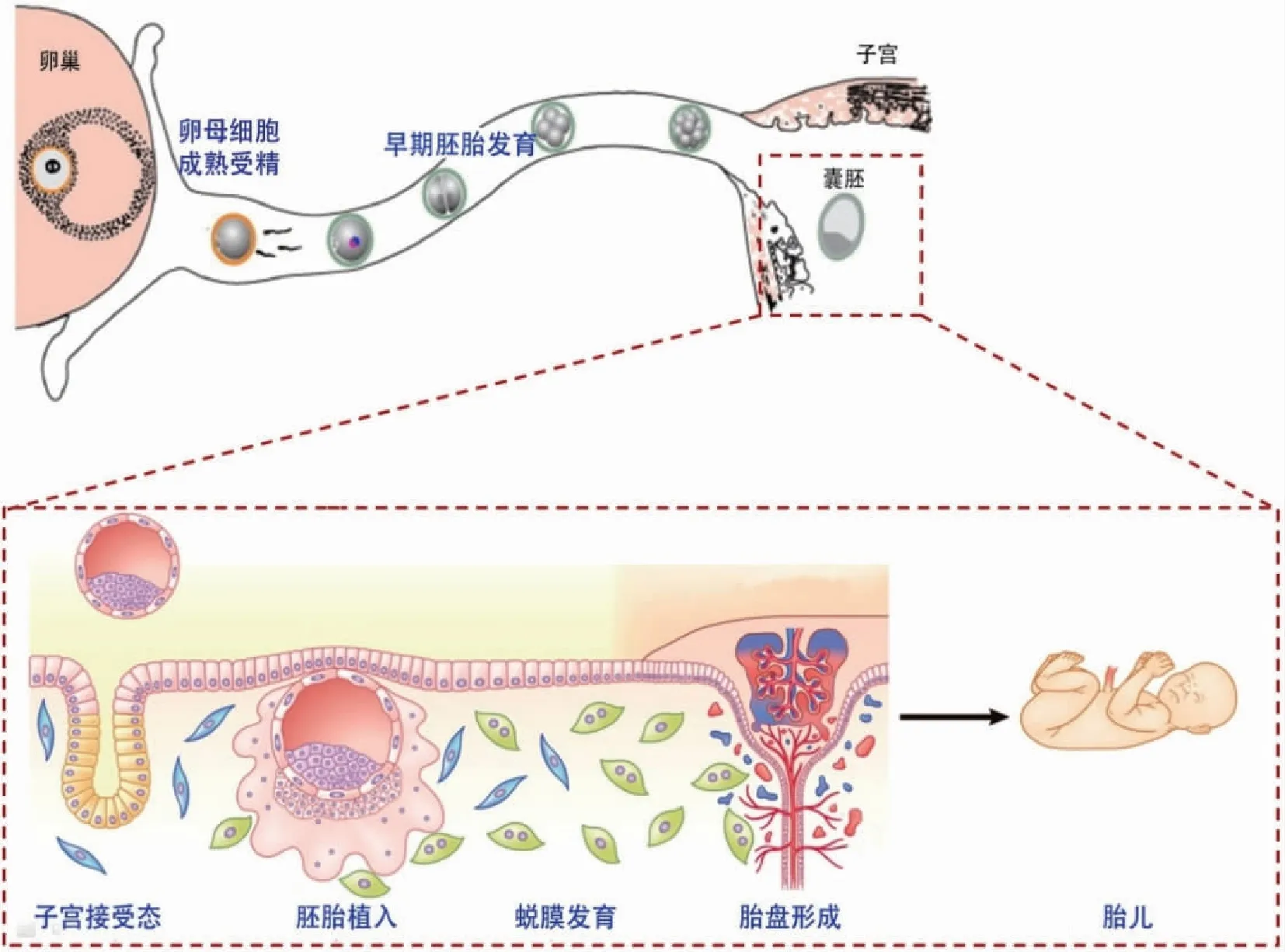
圖1 妊娠建立的生理過程示意圖[3]
二、URIF與URSA定義的異同
1.反復種植失敗(RIF)及URIF的定義:妊娠丟失可見于接受輔助生殖技術(ART)和未接受任何輔助生育治療而自然受孕的患者。近年來,選擇ART治療的患者顯著增加,因此出現特殊類型的“胚胎損失”即反復胚胎種植失敗(RIF)。目前國際上對RIF尚無統一的定義[4],2018年“中國胚胎植入前遺傳學診斷/篩查專家共識”定義RIF為患者移植3次及以上或移植高評分卵裂球期胚胎數4~6個或高評分囊胚數3個及以上均失敗[5]。根據臨床胚胎學家協會(ACE)發布的胚胎質量評分標準定義的高質量胚胎是5/C/C或以上評分的D3卵裂期胚胎,3/4/2或以上的囊胚[6]。隨著ART技術的不斷革新,不同的RIF定義中移植的周期數和移植胚胎數較以前均呈減少趨勢。
部分RIF患者經過常規的檢查評估仍無法確定其具體原因則可診斷為URIF[7]。受不同生殖中心篩查項目、醫療水平的限制,其發病率報道不一。目前關于URIF尚無共識的定義,屬于排除性診斷,臨床上一般參考URSA的排除標準。
2.反復流產(RSA)及URSA的定義:流產與胚胎植入失敗相比,是發生在胚胎著床以后的胚胎丟失事件。迄今為止,不同國家和地區對RSA定義中的流產次數、流產孕周、是否包括生化妊娠等內容存在差異。目前我國關于RSA的定義是發生3次或3次以上妊娠28周之前的妊娠丟失[8],但多數專家指出發生2次妊娠丟失就應當引起關注,臨床上發生3次和2次流產的病因和后續再流產率相似,且每次流產帶來的損害會降低再次懷孕的可能。RSA的病因復雜多樣,其中約50%病因不明即URSA。由于病因和發病機制不明,目前缺乏國際公認的URSA診斷標準,對其診斷仍采用排除法,即經過嚴格的、系統而全面的病因學篩查排除已知的所有病因(包括解剖學因素、遺傳學因素、感染因素、內分泌紊亂、血栓前狀態、免疫學異常和化學物理因素)后方可診斷。
URSA可以分為兩種類型[9]。Ⅰ型URSA,偶然發生于沒有潛在病理且預后良好的女性;Ⅱ型URSA,常發生于存在目前常規臨床檢查無法明確的某種潛在的病理且預后較差的女性。區分Ⅰ型和Ⅱ型URSA可以考慮以下要素:年齡、它們的定義、以往流產的次數以及懷孕后的核型。
3.RIF與RSA定義的異同:兩種妊娠丟失的定義尚無統一說法,兩者在病因上部分重疊又明顯有別(表1)。

表1 RIF與RSA定義比較
三、URIF及URSA兩者病因學的異同
(一)URIF的可能病因
1.胚胎因素:胚胎因素是導致移植失敗的最常見原因[10],是決定移植成功與否的要素,當胚胎質量較好時對內膜接受態的要求就相對寬松(如異位妊娠)。盡管患者移植的是優質胚胎,但胚胎的形態學評分不足以完全反映其發育和種植潛能[11]。在常規IVF過程中,我們僅憑借胚胎的發育情況和形態來判斷胚胎的優劣,并不能很好地篩選出染色體異常的胚胎。影響胚胎遺傳學異常的因素包括父母染色體異常、受精過程異常及胚胎發育異常等等。此外,高齡可引起配子和胚胎非整倍率增高、線粒體DNA損害增加、胚胎-內膜非同步性比例升高[12],從而導致胚胎著床率的降低。促排卵過程中藥物劑量、胚胎培養液、培養狀態以及是否污染等因素均與胚胎質量密切相關。
2.內膜相關因素:子宮內膜異位癥(EMs)是一種雌激素依賴性疾病,炎癥、免疫系統紊亂是其另一典型特征。隱匿性EMs是URIF的可能病因[13],與整合素表達減少和芳香化酶表達增加有關。慢性子宮內膜炎(CE)[14],由于其臨床表現不典型,病因尚不明確,診斷與治療均缺乏統一的標準,對其診斷主要依靠宮腔鏡檢查(內膜潮紅)及內膜病理活檢(CD38、CD138陽性)。CE可通過對蛻膜的干擾而影響內膜容受性[15]。此外,除了可能存在的子宮內膜病理因素,也有可能是由于種植窗發生偏移導致胚胎-內膜非同步化。
3.陰道微生物群和代謝組:有研究比對了URIF患者與第一個冷凍胚胎移植周期中獲得臨床妊娠的患者的陰道微生物群和代謝組,結果顯示URIF組中甘油磷脂和苯并吡喃含量降低[16]。甘油磷脂代謝的溶雙磷脂酸和前列腺素是影響胚胎著床和蛻膜的關鍵因素,而苯并吡喃作為選擇性雌激素受體調節劑可改變子宮內膜容受性從而影響胚胎種植;此外,URIF患者陰道微生物具有較高的微生物多樣性和較低的乳酸桿菌豐度,這與妊娠結局顯著相關[16]。
4.其他:過高的體質量指數(BMI)、過重的體力勞動、女方或男方吸煙史、不健康的生活方式以及某些基因問題均可能影響胚胎種植的成功率。研究表明,URIF患者中存在血清縮宮素水平升高的現象,可能與精神壓力或移植管長時間進入宮腔觸碰宮壁等有關,這些均可誘發子宮內膜異常的蠕動波[17],引起宮縮致使胚胎不易著床。此外,細胞源性微粒子(cMP)是由細胞在細胞激活或凋亡時釋放的小膜泡,幾乎在所有血栓性疾病和妊娠損耗中都發現其計數升高,它在本質上高度致血栓形成。體外受精和胚胎移植后cMP計數增加[18],這一發現為URIF的致病機理提供了新的見解。
(二)URSA的可能病因
URSA的病因具有復雜性和異質性特點,即同一患者可能存在2種或2種以上的病因,同一患者每次流產的原因可能相同也可能不同,提示在臨床工作中應關注其病因譜的變化。
1.胚胎異常:流產次數越多,再次流產的幾率就越高。在已知的病因當中,胚胎染色體異常仍然是導致反復流產的最常見原因。流產發生的越早,胚胎染色體異常的發生率越高,但隨著流產次數的增多,胚胎異常的機率反而下降。RSA可能是由于未能預防“劣質”胚胎的植入,因此,可被認為是自然質量控制的失敗[19]。當采用胚胎移植前遺傳學檢測(PGT)篩查丟棄“劣質”胚胎時,移植后的流產率明顯下降。
2.母-胎免疫平衡異常:妊娠被認為是成功的同種異體移植,胎兒免受母體免疫系統的攻擊是胎兒存活的關鍵。因此,妊娠成功取決于母-胎免疫耐受的建立和維持[20-21],而URSA的發生則是由于母-胎免疫耐受機制未能建立或被破壞進而導致母體對胚胎抗原產生免疫排斥的結果,因此,URSA也稱為同種免疫型RSA。細胞之間的正常交互對話有利于胚胎種植和生長發育的免疫微環境,反之,任何一個環節出現異常,則可能導致母-胎免疫耐受失衡及不良妊娠結局。迄今為止,這種特定免疫耐受的形成機制尚未闡明,主要涉及巨噬細胞[22]、NK細胞[23]、NKT細胞[24]、Th1/Th2細胞[25]、Th17/Treg[26]失衡。
3.人類白細胞抗原(HLA):正常情況下,父方的HLA抗原可刺激母體產生相應的HLA抗體(又稱封閉抗體),保護胎兒免受母體免疫系統的攻擊,如果夫婦的HLA相容性過高,母體對胚胎的父系抗原免疫識別功能不全,胎兒暴露于母體免疫系統的監視之下,使母體產生排斥反應從而導致流產[27]。此外,滋養層細胞上唯一表達的經典HLA抗原是HLA-C[28],對HLA-C的免疫反應可能與URSA有關。
4.內膜因素:RSA患者的子宮內膜可能對侵襲的滋養層產生排斥反應,另一種可能的解釋是,其子宮內膜更容易接受“劣質”胚胎[29],胚胎可成功著床但隨后流產。子宮灌注受損是URSA的可能原因之一,灌注受損后內膜缺血缺氧增加了流產的機率。此外,內膜搔刮對胚胎植入可能有改善作用,但其潛在危害可能會導致后續流產的發生,故臨床工作中應權衡其利弊。
5.其他:年齡同樣是URSA發生的高危因素,不良的生活習慣、飲食、睡眠也與URSA關系緊密。患有糖尿病、黃體功能不全、多囊卵巢綜合征等疾病可能會導致URSA,目前尚不明確具體的影響機制。感染與晚期流產、胎膜早破及早產相關,但是否與URSA相關尚未明確。部分基因異常導致URSA的機制尚未明確,仍需進一步驗證。此外,男性因素與URSA的關聯尚存在爭議[30],尚無足夠的證據顯示對男性異常因素進行干預能改善妊娠結局。
(三)URIF及URSA兩者病因學的異同
URIF與URSA在病因特點、影響因素、規律性以及臨床表現方面,存在著相當程度的重疊而又明顯不同(表2)。

表2 URIF及URSA的病因學比較
四、總結與展望
URIF與URSA近年來發病率有升高的趨勢,病因復雜且高度異質。本文通過對URIF與URSA可能病因的梳理總結和歸納分析,期望能夠幫助患者正確認識并科學對待這類疾病,保持良好的心態就診。主診醫生根據可能的病因及既往治療方案可不斷進行嘗試和調整。我國應盡快統一對URSA和URIF的定義及診斷標準,深入其病因學的探討與研究,這不僅有利于規范相關醫務人員診治相關患者,而且便于開展后續研究以及學術交流。此外,對患者應該積極開展科普宣傳和教育。

