加味當歸芍藥散聯合常規治療對氣虛血瘀型2 型糖尿病周圍神經病變患者的臨床療效
方翔宇王高岸邱世光吉貞料
(海南醫學院第二附屬醫院中醫科,海南 海口570311)
糖尿病周圍神經病變是糖尿病常見并發癥,以遠端對稱性肢體感覺異常為主要表現,包括肢體疼痛、蟻行蟲咬、麻木,甚至可引起肌肉萎縮,隨著病情發展而出現夏科氏關節病、糖尿病足[1]。2 型糖尿病是糖尿病主要類型,其比例高達95%,近年來發病率逐年升高[2]。糖尿病周圍神經病變的病機復雜,目前認為炎性因子及氧化應激失衡參與本病發生[3],患者表現為TNF-α 等促炎性因子水平升高,炎癥反應持續存在時,可引起氧化應激失衡,表現為SOD 活性降低,進而加重炎癥反應,故促進氧化應激反應平衡有助于阻斷惡性循環[4]。
2 型糖尿病屬于中醫“消渴病”范疇,而糖尿病周圍神經病變依據其發病特點可歸屬于“痹病”范疇,患者大多為中老年人,正氣虧虛,加之2 型糖尿病病機關鍵為陰虛燥熱,疾病日久瘀血內生,最終形成氣虛血瘀證[5]。加味當歸芍藥散是由婦科名方當歸芍藥散調整而來,方中加強了益氣化瘀藥物,符合相關治療需求,故本研究考察該方聯合常規治療對氣虛血瘀型2 型糖尿病周圍神經病變患者的臨床療效及其作用機制,現報道如下。
1 資料與方法
1.1 一般資料 2017 年5 月至2020 年6 月就診于海南醫學院第二附屬醫院的126 例患者,隨機數字表法分為對照組和觀察組,每組63例,2 組一般資料見表1,可知差異無統計學意義(P>0.05),具有可比性。研究經醫院倫理會審核批準。
表1 2 組一般資料比較(, n=63)Tab.1 Comparison of general data between the two groups(, n=63)

表1 2 組一般資料比較(, n=63)Tab.1 Comparison of general data between the two groups(, n=63)
1.2 診斷標準
1.2.1 西醫(2 型糖尿病周圍神經病變)參考文獻[6]報道,(1)多飲多食,口干,多尿,消瘦,空腹血糖≥7.0 mmol/L,隨機血糖≥11.1 mmol/L;(2)合并下肢麻木、疼痛、肌肉萎縮;(3)查體顯示踝反射、腱反射減弱;(4)肌電圖顯示下肢周圍神經傳導功能異常,主側神經傳導速度降低,MCV<45 m/s,SCV<40 m/s。
1.2.2 中醫(氣虛血瘀型)參考文獻[7]報道,主證乏力,下肢刺痛;次證麻木,灼熱感;舌淡紫可見瘀斑,脈細澀。
1.3 納入標準 (1)符合“1.2”項下診斷標準,要求住院治療;(2)初次接受治療;(3)不存在認知障礙,告知研究風險,簽署知情同意書。
1.4 排除標準 (1)對研究受試藥物過敏;(2)合并下肢動脈硬化閉塞、糖尿病足;(3)谷丙轉氨酶大于2 倍正常上限;(4)合并精神障礙,不配合治療;(5)既往有腦卒中病史,導致運動功能障礙;(6)發展為糖尿病腎病;(7)妊娠期婦女。
1.5 治療手段 對照組采用常規治療,包括降血糖、控制飲食、適當運動,并給予硫辛酸(江蘇萬禾制藥有限公司,0.1 g/片,國藥準字H20100158,批號20170306、20180601、20191104)0.2 g,每天3次,飯前服用;觀察組在對照組基礎上采用加味當歸芍藥散,組方藥材炙黃芪30 g、茯苓15 g、白術15 g、白芍15 g、當歸10 g、川芎10 g、澤瀉10 g、丹參10 g、地龍6 g、炙甘草6 g,乏力明顯者,加人參6 g;腹瀉者,加淮山藥15 g;食欲降低者,加砂仁6 g;下肢麻木明顯加大者,白芍劑量加至30 g,由醫院中藥房統一提供,每天1 劑。2 組均連續治療12 周。
1.6 指標檢測 (1)抽取患者空腹肘部靜脈血,采用ELISA 法檢測血清TNF-α 水平及SOD、CAT活性,其中TNF-α、SOD 檢測試劑盒由上海羽朵生物科技有限公司提供(批號20170302、20190403、20200106),CAT 檢測試劑盒由武漢博士德生物工程有限公司提供(批 號20170304、20181105、20191106);(2)采用ELISA 法檢測血清BDNF、IL-23 水平,相關檢測試劑盒由南京建成生物工程研究所提供(批 號 20170205、20190602、20200204);(3)采用葡萄糖氧化酶法檢測血清FBG、2 hPBG 水平;(4)檢測中醫證候評分[7],主證乏力(2分,偶有乏力,但程度輕,可自行緩解;4分,乏力反復發作,充分休息后可暫時緩解;6分,持續存在,充分休息后仍無法緩解)、下肢刺痛(2分,偶有發作;4分,反復發作,藥物干預后可緩解;6分,持續存在,藥物干預后仍不緩解,次證麻木(1分,感覺下肢麻木,可自行緩解,程度輕;2分,下肢麻木,程度較重,影響日常功能;3分,下肢麻木,程度嚴重,不可自行緩解)、灼熱感(1分,偶有發作;2分,下肢皮膚燒灼感明顯,日常生活不受影響;3分,燒灼感持續存在,日常生活受到影響);(5)采用肌電圖儀(型號NMD0066,重慶康如來科技有限公司)檢測腓總神經、正中神經MNCV;(6)不良反應發生率。
1.7 療效評價 參考文獻[7]報道,(1)顯效,治療后臨床癥狀明顯改善,神經傳導速度提高程度≥10%,中醫證候評分降低程度≥70%但<95%;(2)有效,治療后臨床癥狀有所改善,神經傳導速度提高程度≥5%但<10%,中醫證候評分降低程度≥30%但<70%;(3)無效,治療后臨床癥狀、神經傳導速度、中醫證候評分未明顯改善。
1.8 統計學分析 通過SPSS 22.0 軟件進行處理,符合正態分布的計量資料以()表示,組間比較采用t檢驗;計數資料以百分率表示,組間比較采用卡方檢驗(雙側檢驗)。P<0.05 表示差異具有統計學意義。
2 結果
2.1 血清TNF-α 水平及SOD、CAT 活性 由表2可知,治療后,2 組TNF-α 水平降低(P<0.05),SOD、CAT 活性升高(P<0.05),以觀察組更明顯(P<0.05)。
表2 2 組血清TNF-α 水平及SOD、CAT 活性比較(, n=63)Tab.2 Comparison of serum TNF-α levels and SOD,CAT activities between the two groups(, n=63)

表2 2 組血清TNF-α 水平及SOD、CAT 活性比較(, n=63)Tab.2 Comparison of serum TNF-α levels and SOD,CAT activities between the two groups(, n=63)
注:與同組治療前比較,#P<0.05;與對照組治療后比較,△P<0.05。
2.2 血清BDNF、IL-23 水平 由表3 可知,治療后,2 組BDNF 水平升高(P<0.05),IL-23 水平降低(P<0.05),以觀察組更明顯(P<0.05)。
表3 2 組血清BDNF、IL-23 水平比較(, n=63)Tab.3 Comparison of serum BDNF and IL-23 levels between the two groups(, n=63)

表3 2 組血清BDNF、IL-23 水平比較(, n=63)Tab.3 Comparison of serum BDNF and IL-23 levels between the two groups(, n=63)
注:與同組治療前比較,# P<0.05;與對照組治療后比較,△P<0.05。
2.3 血清FBG、2 hPBG 水平 由表4 可知,治療后,2 組FBG、2 hPBG 水平降低(P<0.05),以觀察組更明顯(P<0.05)。
表4 2 組血清FBG、2 hPBG 水平比較(, n=63)Tab.4 Comparison of serum FBG and 2 hPBG levels between the two groups(, n=63)

表4 2 組血清FBG、2 hPBG 水平比較(, n=63)Tab.4 Comparison of serum FBG and 2 hPBG levels between the two groups(, n=63)
注:與同組治療前比較,# P<0.05;與對照組治療后比較,△P<0.05。
2.4 MNCV 由表5 可知,治療后,2 組MNCV 升高(P<0.05),以觀察組更明顯(P<0.05)。
表5 2 組MNCV 比較(m/s,, n=63)Tab.5 Comparison of MNCVs between the two groups(m/s,, n=63)
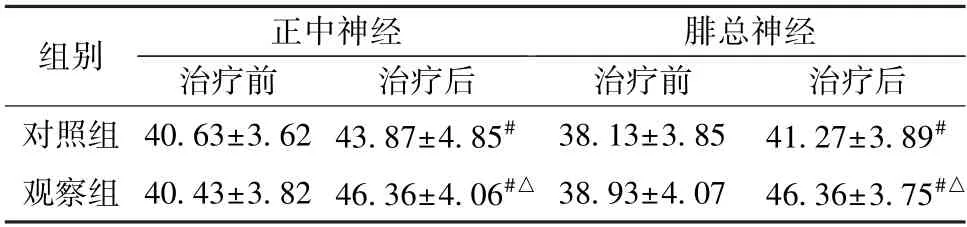
表5 2 組MNCV 比較(m/s,, n=63)Tab.5 Comparison of MNCVs between the two groups(m/s,, n=63)
注:與同組治療前比較,# P<0.05;與對照組治療后比較,△P<0.05。
2.5 中醫證候評分 由表6 可知,治療后,2 組中醫證候評分降低(P<0.05),以觀察組更明顯(P<0.05)。
表6 2 組中醫證候評分比較(分,, n=63)Tab.6 Comparison of TCM symptom scores between the two groups(score,, n=63)
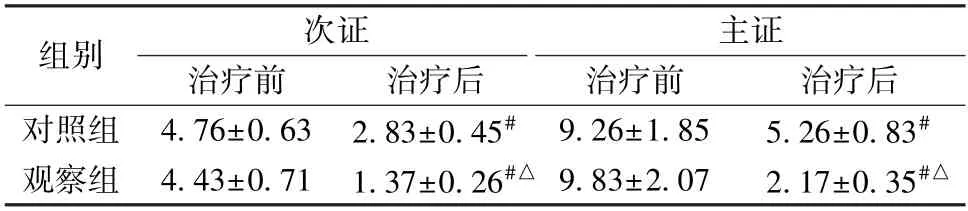
表6 2 組中醫證候評分比較(分,, n=63)Tab.6 Comparison of TCM symptom scores between the two groups(score,, n=63)
注:與同組治療前比較,# P<0.05;與對照組治療后比較,△P<0.05。
2.6 臨床療效 由表7 可知,觀察組總有效率高于對照組(P<0.05)。

表7 2 組臨床療效比較[例(%), n=63]Tab.7 Comparison of clinical efficacy between the two groups [case(%), n=63]
2.7 不良反應發生率 由表8 可知,2 組不良反應均以胃腸道反應、頭暈、皮疹為主,觀察組其發生率低于對照組(P<0.05)。

表8 2 組不良反應發生率比較[例(%), n=63]Tab.8 Comparison of incidence of adverse reactions between the two groups [case(%), n=63]
3 討論
2 型糖尿病周圍神經病變是臨床常見的糖尿病并發癥,目前認為其主要機制[8-9]如下:(1)免疫機制,長期高血糖狀態可抑制髓鞘蛋白分泌,可引起免疫損傷;(2)遺傳因素;(3)多元醇-氧化應激通路激活,Na+-K+-ATP 酶活性減退。
炎性因子與本病的關系已得到證實,其中IL-23 可刺激T 細胞產生,促使內皮細胞“捕獲”中性粒細胞,還可導致血小板功能活化,誘發微血栓形成[10-11];TNF-α 由單核巨噬細胞分泌產生,可通過內分泌、旁分泌等途徑參與調節胰島素調控,并可引發胰島素抵抗,增加糖尿病治療難度[12-14]。恢復氧化應激平衡已成為治療炎癥性疾病的重要思路,SOD 是關鍵的抗氧化因子,其活性降低與衰老關系密切[15-17];CAT 也具有較強的抗氧化活性,其活性降低也是促使自由基堆積的重要原因,并與病情嚴重程度呈負相關[17];BDNF 可影響神經元發育分化,患者由于神經損傷,其水平會代償性提高[18-19]。本研究發現,治療后觀察組血清SOD、CAT 活性及BDNF 水平高于對照組,TNF-α、IL-23水平更低。
糖尿病屬于中醫“消渴病”范疇,陰虛燥熱是其重要機制,患者大多為中老年人,正虛是發病基礎,并與勞欲過度、飲食不節等因素相關;陰虛則陽氣無以制約,虛熱內生,熱邪不去可耗傷陰液,使血液黏稠;燥熱亦可傷津,血液粘稠則運行不暢,故而瘀血內生。糖尿病周圍神經病變患者大多已經歷較長病程,正氣日漸虧虛,最終形成氣虛血瘀證。加味當歸芍藥散中炙黃芪入肺脾經,具有補益肺脾功效,肺氣充足則宗氣足,脾氣充足則氣血生化有源,為君藥;茯苓健脾滲濕,利尿安神,而白術燥濕健脾,兩者合用則化濕之力增,川芎祛風通絡,化瘀止痛,而丹參活血化瘀,通絡消腫,并且性偏寒,可清血分熱邪,避免瘀血郁久化熱,兩者合用氣血同調,上述4 味藥物合為臣藥;白芍入肝經,具有養血補肝、柔肝止痛功效,肝血充足則肝疏泄功能得以恢復,澤瀉利水滲濕,消腫,當歸養血補血,散瘀止痛,可加強全方補益之力,并且具有化瘀功效,地龍具有搜風通絡、化瘀功效,上述4 味藥物合為佐藥;炙甘草調和諸藥,為使藥。研究表明,茯苓、白術提取物有助于調節機體免疫功能[20],地龍中提取的吲激酶有較強的抗血栓功效[21],川芎中的川芎嗪可抑制炎性滲出[22];白芍中的白芍苷有鎮痛作用,而且可促進神經細胞修復[23]。
本研究發現,治療后觀察組血清FBG、2 hPBG水平,中醫證候評分,不良反應發生率低于對照組,腓總神經、正中神經MNCV,總有效率更高,其機制[24-27]主要包括(1)抑制TNF-α 活化,阻斷炎性風暴,減輕炎癥反應;(2)促進氧化應激平衡恢復,促進神經功能修復。
綜上所述,加味當歸芍藥散聯合常規治療可減輕氣虛血瘀型2 型糖尿病周圍神經病變患者炎癥反應,提高抗氧化能力,具有重要臨床意義。

