基于微流控芯片的鮭科魚類單核苷酸多態性分型系統構建
趙紫霞 許 建 吳碧銀, 曹頂臣 白慶利 徐 鵬 馬卓君
(1. 中國水產科學研究院, 北京 100141; 2. 上海海洋大學水產科學國家級實驗教學示范中心, 上海 201306; 3. 中國水產科學研究院黑龍江水產研究所, 哈爾濱 150070; 4. 廈門大學海洋與地球學院, 福建省海洋生物遺傳育種重點實驗室, 廈門 361102)
作為漁業資源養護的有效措施之一, 廣泛實施的增殖放流活動在保障漁業可持續發展、改善水域生態環境方面取得了積極成效[1—3], 而放流個體的準確識別是增殖放流效果評估的重要技術環節[4]。在早期增殖放流操作中, 多使用掛牌和剪鰭等物理標記法, 或者注射化學染料和熒光染料等化學標記法來標記識別放流個體, 需在放流前對苗種個體進行操作, 造成一定的物理損傷, 放流后也可能存在標記脫落、鰭條復生和染料褪色等風險導致無法識別。
隨著核酸檢測技術的飛速發展和基因組序列資源的大量發掘, DNA分子標記成為具備大規模應用可能的放流個體識別技術[5,6], 無須標記或檢測待放流苗種, 而僅需檢測放流苗種親本的遺傳信息并構建數據庫, 通過放流后野外捕撈個體的親子鑒定, 即可識別其中的放流個體并開展系統評估, 制定科學的增殖放流方案。此外, 捕撈個體的分子標記檢測信息還可以應用于群體遺傳學分析, 以監測野外種群遺傳結構及其年際變化[7]。
微流控(Microfluidics)是在微米尺度空間中對10–9至10–18L體積的微量流體進行精確操控處理的技術系統[8], 可將生物、化學等分析實驗中的樣品制備、反應、分離和檢測等基本操作單元集成到同一塊芯片上進行, 又稱為“芯片實驗室”(Lab-on-achip)。核酸檢測是微流控芯片的典型應用領域之一[9], 包括以數字聚合酶鏈式反應(digital Polymerase Chain Reaction, dPCR)為代表的核酸絕對定量分析, 以及不同通量的分子標記分型檢測等。微流控芯片具有集成化、自動化和微型化的特點, 用于分子標記分型時, 能夠大幅縮減手動加樣次數和人工判讀環節, 具有快速、高效、避免人為失誤和交叉污染的優點, 在處理大規模樣本時還具有低成本優勢。
本研究擬針對增殖放流個體識別的應用場景,開發基于微流控芯片的單核苷酸多態性(Single Nucleotide Polymorphism, SNP)標記分型系統, 以中國土著鮭科魚類細鱗鮭(Brachymystax lenok)等樣本為例, 測試其用于親權鑒定和群體遺傳分析的可靠性。
1 材料與方法
1.1 實驗材料
細鱗鮭、哲羅鮭(Hucho taimen)、山女鱒(Oncorhynchus masou masou)和美洲紅點鮭(Salvelinus Fontinalis)養殖群體樣本采自中國水產科學研究院黑龍江水產研究所渤海冷水性魚類試驗站、中國水產科學研究院房山試驗基地、北京市懷柔區和四川省都江堰市冷水魚養殖場。細鱗鮭野生群體樣本采自黑龍江蘿北江段、烏蘇里江虎頭江段、鴨綠江丹東江段和額爾齊斯河布爾津河段。剪尾鰭貼至干燥濾紙上, 56℃烘干6h, 常溫暫存。
1.2 核酸提取
使用海洋動物基因組DNA提取試劑盒(天根生化)提取待測個體鰭條DNA, 通過瓊脂糖凝膠電泳檢測核酸完整性, 使用Nano Drop 8000紫外可見光分光光度計(Thermo Fisher)檢測核酸濃度。
1.3 微流控芯片SNP位點篩選
使用Axiom 57K虹鱒(Oncorhynchus mykiss)芯片(Affymetrix)檢測細鱗鮭、哲羅鮭、山女鱒和美洲紅點鮭個體各8尾, 分型實驗由紐勤生物科技(上海)有限公司完成, 使用Affymetrix Power Tools和SNPolisher軟件(Affymetrix)讀取分型數據。使用PLINK 1.09軟件[10]進行分型結果過濾、統計、哈迪溫伯格平衡(Hardy-Weinberg Equilibrium, HWE)和連鎖不平衡(Linkage Disequilibrium, LD)檢驗, 個體質量控制標準和位點質量控制標準均設為分型率(Call Rate, CR)>80%, 入選多態性位點標準設為最小等位基因頻率(Minor Allele Frequency, MAF>5%, HWE閾值設為P>0.05, LD閾值設為r2<0.2。
1.4 微流控芯片探針合成與分型檢測
使用Primer Premier 6.0軟件評估設計SNP擴增引物和分型探針, 每個SNP位點設計2條擴增引物和2條分型探針, 其中特異性靶標擴增引物(Specific Target Amplification, STA)和位點特異性引物(Locus Specific Primer, LSP)分別位于SNP位點上下游側翼序列, 2條等位基因特異性探針(Allele Specific Probe, ASP)的3′端位于突變位點, 分別對應兩種基因型, 擴增引物和分型探針由富魯達(上海)公司和生工生物工程(上海)公司合成。使用EP1平臺及SNPtype 96.96動態芯片(Fluidigm)開展分型檢測,檢測樣本共計192個, 包括有準確系譜記錄的細鱗鮭家系子代96尾, 候選親本36尾, 野外捕撈個體11尾, 使用前述Axiom 57K虹鱒芯片檢測過的驗證樣本48尾, 以及無模板對照1個。通過Fluidigm SNP genotyping analysis software 4.1軟件讀取分型結果,質控閾值設為85, 對缺失和低質量分型數據進行人工復檢。使用CERVUS 3.0.7軟件[11]進行遺傳多態性統計, 并對96尾細鱗鮭家系子代樣本進行親權鑒定。使用STRUCTURE 2.3.4軟件[12]進行群體遺傳結構分析。
2 結果
2.1 屬間共享多態性位點篩查
使用Axiom 57K虹鱒芯片[13]檢測4個物種32尾個體樣本, 所有個體全部通過CR>80%的質控標準。所檢測的4個物種分屬鮭科內的4個屬, 包括哲羅鮭屬(哲羅鮭)、大麻哈魚屬(山女鱒)、紅點鮭屬(美洲紅點鮭)和細鱗鮭屬(細鱗鮭)各1種, 以種屬為基本單元篩查多態性SNP位點, 在該芯片包含的57501個虹鱒SNP標記中, 獲得多態性位點共計35346個。屬間多態性SNP位點的分布如圖 1所示,包括群體間共享的和群體特異性的多態位點, 其中4個屬共享的多態性位點847個, 用作微流控芯片備選位點。
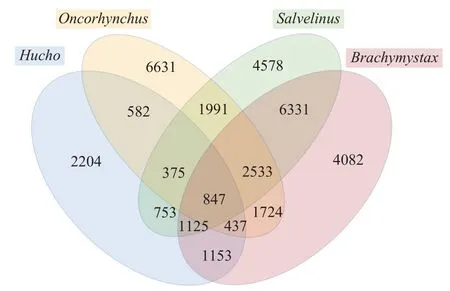
圖1 鮭科魚類4個屬間共享多態性SNP位點韋恩圖Fig. 1 Venn diagram for distribution of shared polymorphic SNPs among 4 genera of salmonid family
2.2 用于微流控芯片設計的SNP位點選擇
圖2顯示了847個共享多態性SNP位點在32尾樣本群體中的MAF分布, 結果顯示有356個位點的MAF值等于0.5, 數目占到多態性位點總數的42.0%,表現出異于正常分布的特征。提取原始分型數據可見, 大量MAF值等于0.5的位點在32尾檢測個體中全部表現為雜合子。以同一物種群體為基本單元進行HWE檢驗(圖 3), 在微流控芯片備選位點中剔除顯著偏離HWE的位點397個。
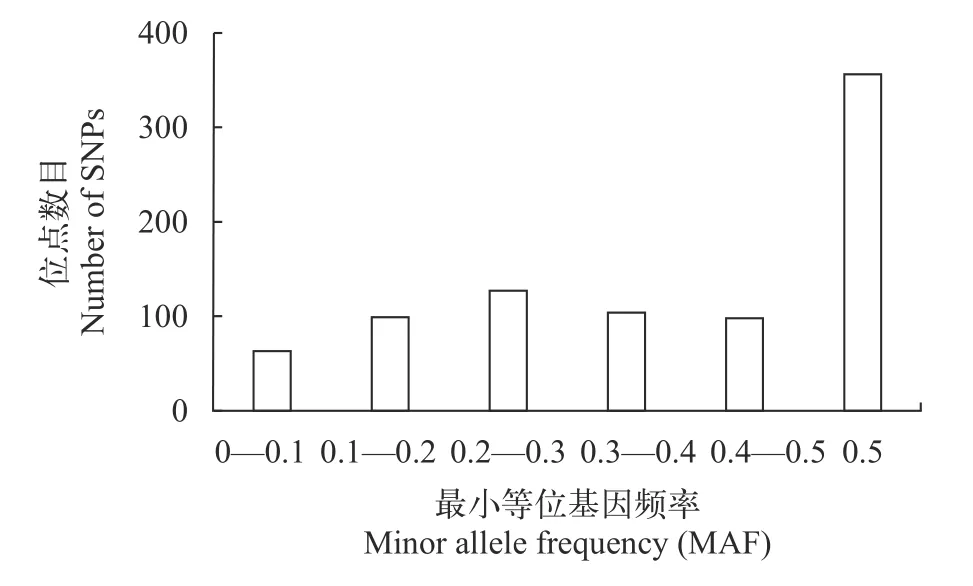
圖2 共享多態性SNP位點在48尾鮭科魚類樣本中的最小等位基因頻率分布Fig. 2 Minor Allele Frequency (MAF) distribution of the shared polymorphic SNPs among 48 salmonid samples genotyped
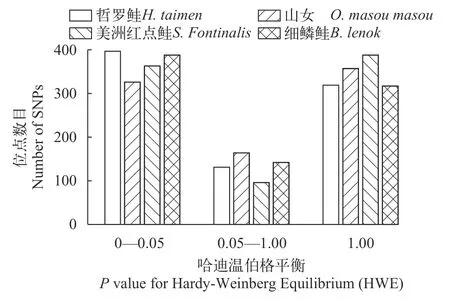
圖3 共享多態性SNP位點在4個鮭科魚類群體中的哈迪溫伯格平衡檢驗P值分布Fig. 3 P value distribution for Hardy-Weinberg Equilibrium(HWE) of the shared polymorphic SNPs in 4salmonid populations genotyped
在32尾樣本群體中進行LD檢驗, 檢測基因組內緊密連鎖的位點, 剔除r2值高于0.2的位點126個。從剩余324個共享多態性位點中, 挑選側翼序列GC含量適中、能成功設計SNPtype分型探針的位點96個, 用于微流控芯片構建, 入選位點及其側翼序列信息見表 1。
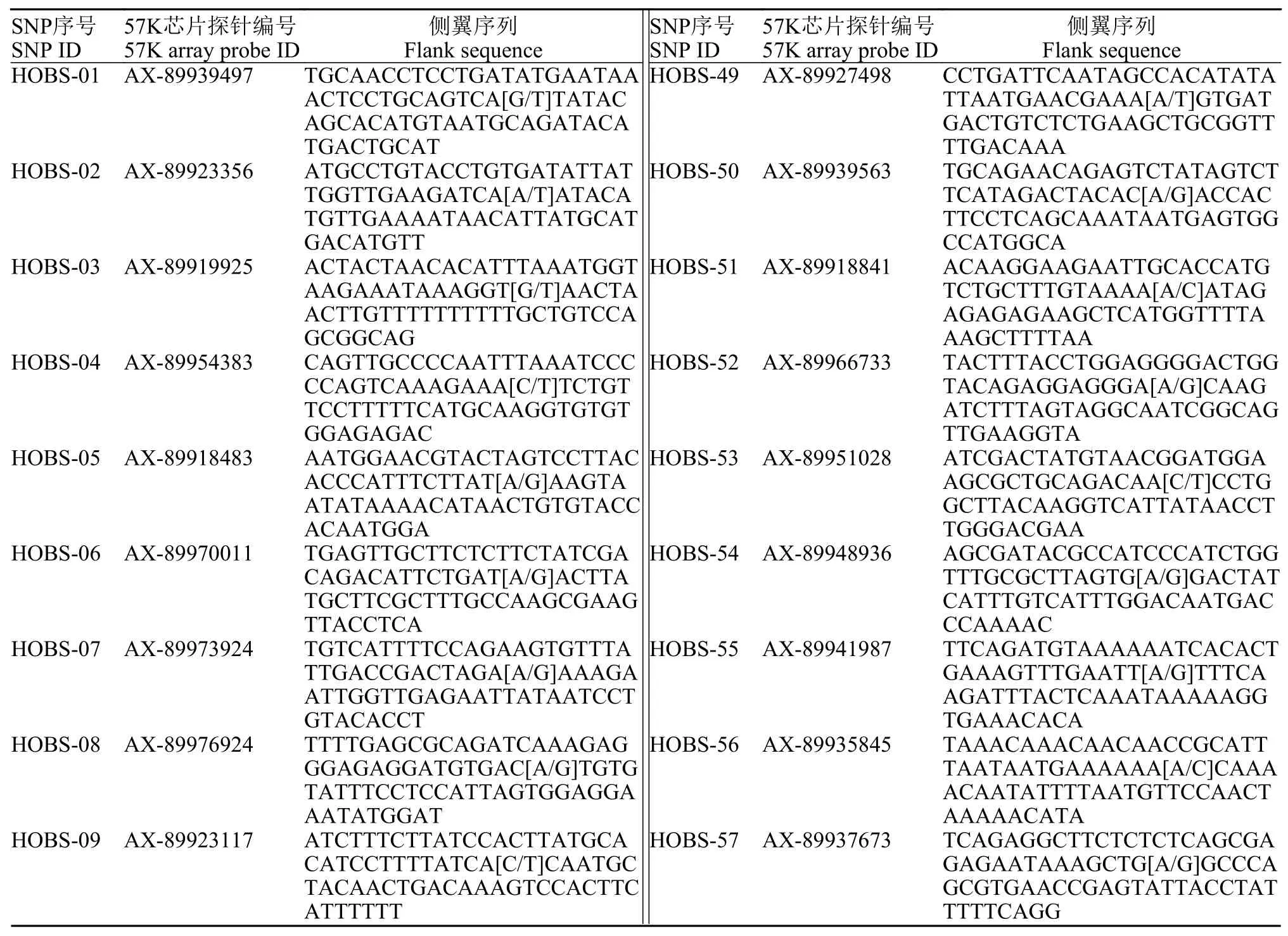
表1 微流控芯片96個SNP位點的序列信息Tab. 1 Sequences of the 96 SNP markers for the microfluidic chip
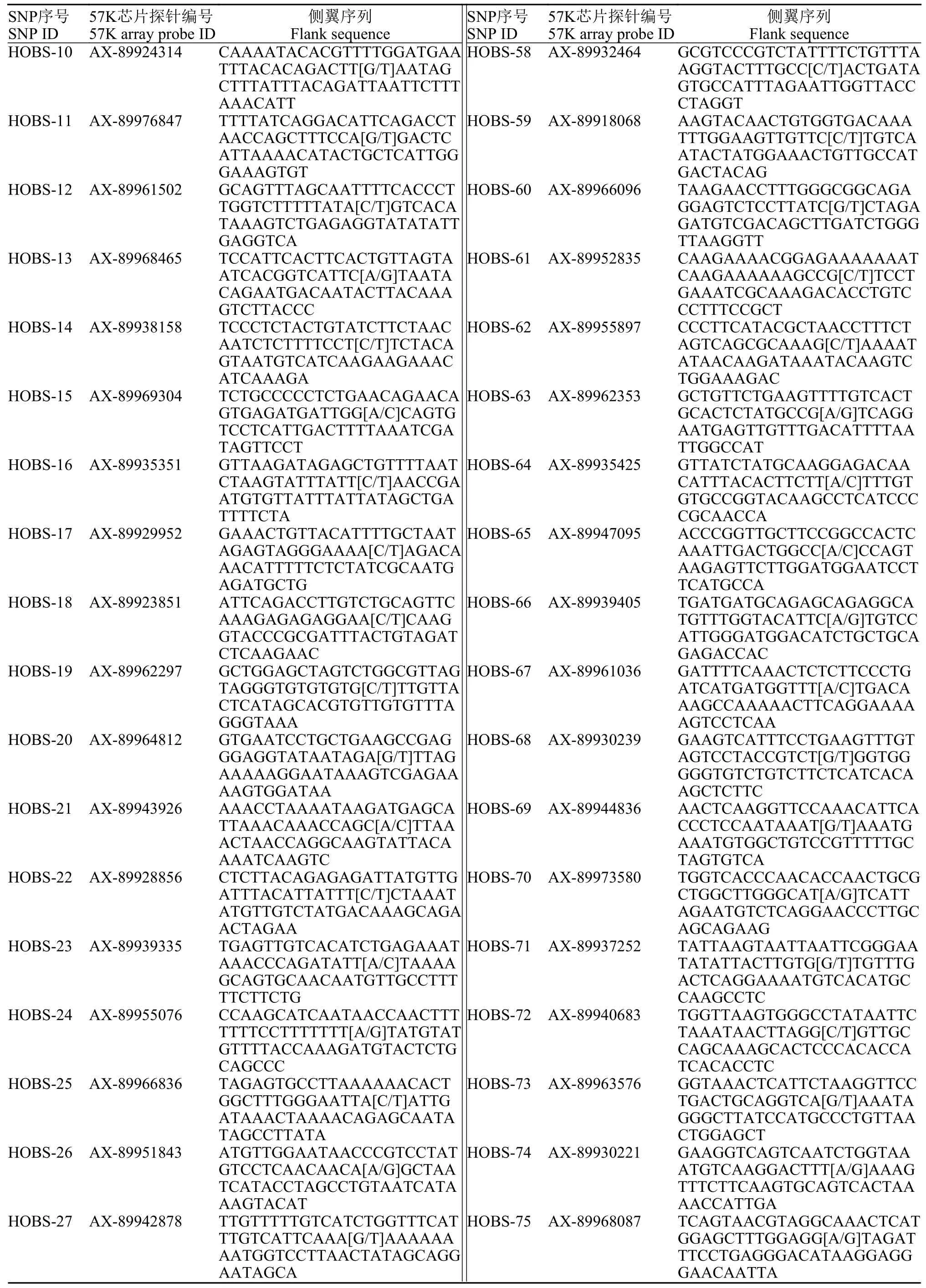
續表1

續表1
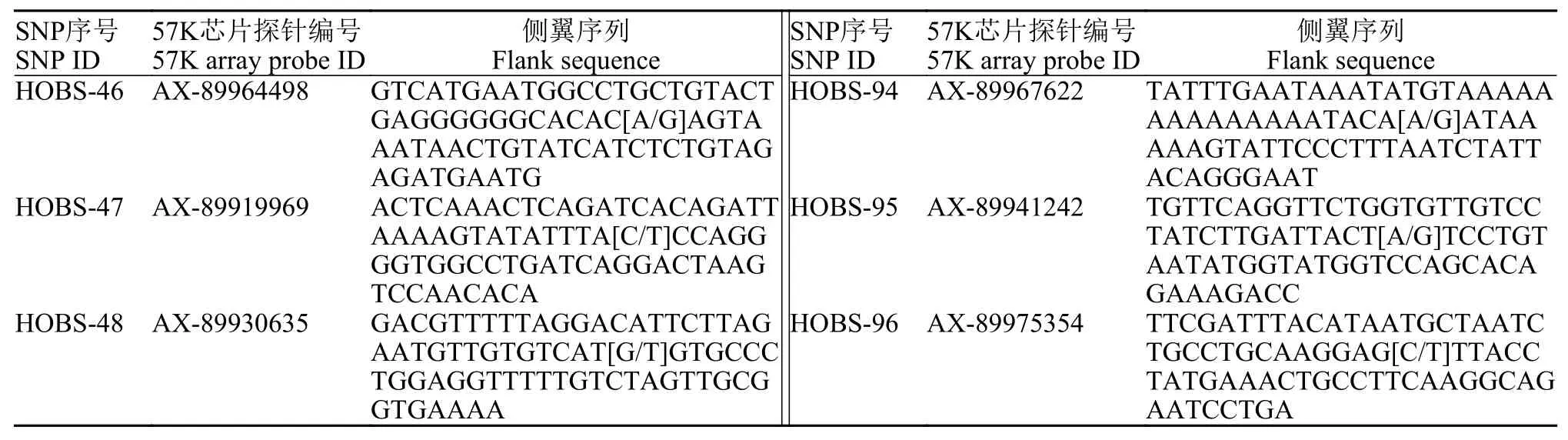
續表1
2.3 微流控SNP芯片檢測
使用SNPtype 96.96微流控芯片對表 1所列96個SNP位點完成分型檢測, 共檢測191尾鮭鱒個體樣本, 以及用滅菌去離子水代替個體DNA的無模板對照樣本1個。圖 4以位點HOBS-01為例展示分型結果, G基因型使用SNPtype-FAM探針(494/518 nm),T基因型使用SNPtype-HEX探針(535/556 nm),GG、GT 和TT三種基因型樣本各自成簇分布, 并與無模板對照樣本顯著區分。在總計18336個分型反應中, 分型成功18084個, 分型成功率為98.63%。SNPtype 96.96微流控芯片檢測樣本中48尾個體與Axiom芯片檢測樣本相同, 對應4608個分型反應的檢測結果一致性為97.92%, 不一致的情況主要表現為某一種芯片分型失敗, 結果缺失。
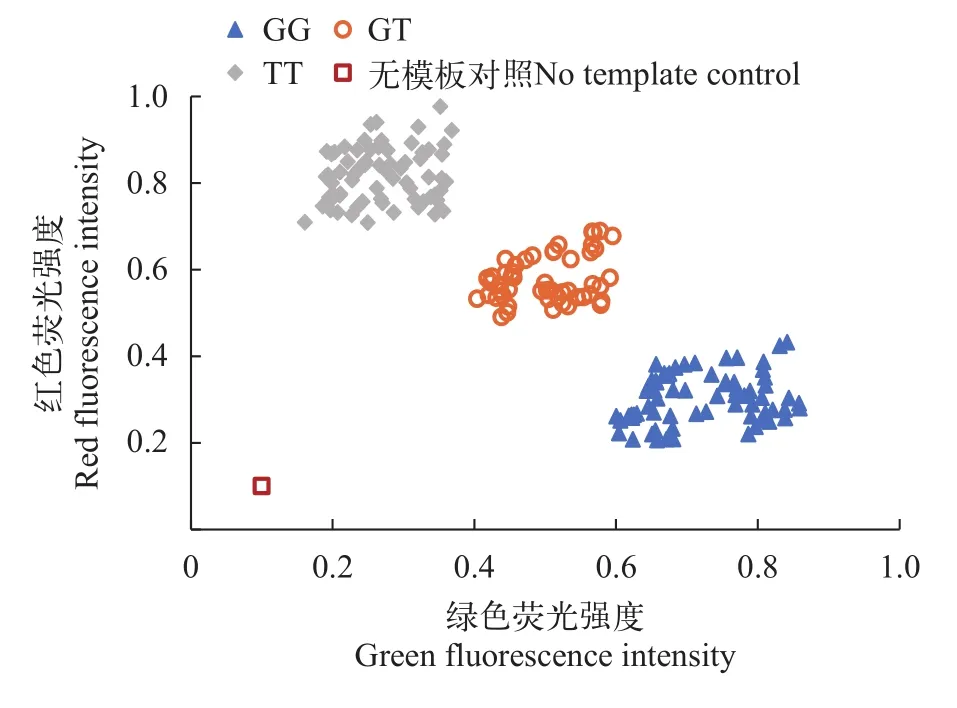
圖4 微流控芯片位點HOBS-01在191尾鮭科魚類樣本中的分型結果Fig. 4 Genotyping results for SNP HOBS-01 of the microfluidic chip in 191salmonid samples
2.4 細鱗鮭家系親權鑒定
基于SNPtype 96.96微流控芯片分型數據, 使用CERVUS 3.0.7軟件對96尾細鱗鮭子代樣本和36尾候選親本進行親權鑒定, 并與系譜記錄進行比較,結果表明無論是單親本鑒定還是雙親本鑒定, 基于96個位點分型數據的親權鑒定結果均與真實系譜相符。計算各位點第一親本非排除率(Non-exclusion probability for first parent , NE-1P)和雙親非排除率(Non-exclusion probability for parent pair, NEPP), 將芯片上96個位點同時用于單親本親權鑒定的NE-1P值為4.362×10–4, 同時用于雙親本親權鑒定的NE-PP值為6.538×10–12。
個體親權鑒定的準確性通過對數優勢比(Logarithm of odds, LoD)值來反映, 表示假設為真與假設為假的概率之比的對數值, 當LoD值為0時, 假設成立的概率為50%;當LoD為正值時, 認為假設為真的概率高于假設為假的概率, 通常設定LoD值高于3.1為閾值, 判定存在親子關系。根據NE-1P值和NE-PP值, 計算每尾子代個體與單親配對和雙親配組的LoD值(圖 5), 所有LoD值均遠大于零, 所有子代樣本的檢測結果都落在可靠象限內。
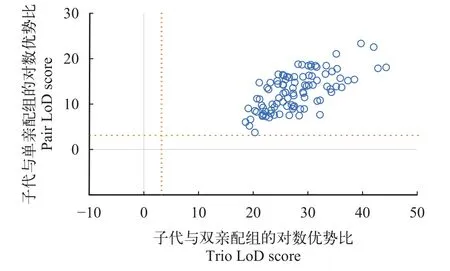
圖5 基于微流控芯片分型結果的96尾細鱗鮭家系子代樣本的親權鑒定準確性分析Fig. 5 Parent assignment analysis for 96 B. lenok offsprings based on genotyping results of the microfluidic chip
2.5 細鱗鮭群體遺傳結構分析
基于SNPtype 96.96微流控芯片分型數據, 使用STRUCTURE軟件對47尾不同來源的細鱗鮭樣本開展遺傳結構分析, 包括采自4個水域的野外捕撈個體11尾, 以及用于增殖放流的養殖群體雌性親本22尾, 雄性親本14尾。圖 6展示了假定祖源群體數(K)為4的STRUCTURE遺傳結構圖, 樣本呈現出按自然群體聚類的特征, 黑龍江、烏蘇里江、鴨綠江和額爾齊斯河野生群體各自對應一種祖源成分, 而養殖群體遺傳組成以烏蘇里江來源為主, 混雜少量其他祖源成分。

圖6 基于微流控芯片分型結果的47尾細鱗鮭樣本遺傳結構分析Fig. 6 STRUCTURE analysis of 47 B. lenok individuals based on genotyping results of the microfluidic chip
3 討論
3.1 針對特定用途的芯片設計
低密度SNP分型芯片已經在多個水產養殖物種中設計成功[14—17], 并應用于育種核心群體的親權鑒定、混合家系育種方案設計和遺傳參數估計, 但在用于增殖放流的漁業物種中尚無報道。本課題組曾將虹鱒SNP應用于我國常見鮭科養殖物種的遺傳多態性檢測[17], 成功開發低通量SNP芯片[18],可用于4個物種共享多態性SNP位點的分型檢測,但其檢測范圍局限于大麻哈魚屬和紅點鮭屬物種,未能涵蓋中國土著鮭科魚類如細鱗鮭和哲羅鮭等,而在漁業資源增殖放流實踐中, 為避免造成外來物種入侵風險, 放流對象以我國土著魚類為主[3,19,20]。因此, 需針對增殖放流物種對象, 重新篩選適宜的SNP位點開展芯片設計。
3.2 芯片位點遴選
本研究基于前一芯片應用經驗開展了位點遴選。在前一芯片設計中, 用于共享多態性位點發掘的樣本群體遺傳多樣性較低, 例如銀鮭(Oncorhynchus kisutch)群體中多態性位點僅占9.01%, 導致最終獲得的可用于探針設計的共享多態位點數目較少(89個)[18]。本研究中挑選了遺傳多樣性較為豐富的群體用于備選位點篩查, 所獲得的共享多態性位點數目明顯增加(847個, 圖 1), 使得芯片位點可以采用更嚴謹的入選標準, 并將側翼序列擴增效率不高或不適宜設計探針的位點剔除, 最終使微流控芯片的分型成功率提高到98.63%。
由圖 1顯示的4個屬間共享多態性位點分布情況可見, 屬間共享多態性位點數目主要取決于采樣群體自身的遺傳多樣性, 多態性位點豐富的群體與其他群體間的共享多態性位點數目較多, 而與其種屬系統發育關系無關, 以細鱗鮭為例, 雖然細鱗鮭屬與哲羅鮭屬的親緣關系更近, 而與大麻哈魚屬和紅點鮭屬親緣關系較遠[21], 但被測的細鱗鮭群體與山女鱒(5541)和美洲紅點鮭(10836)共享的多態性位點數卻多于哲羅鮭(3562)。
對847個共享多態性SNP位點的等位基因頻率分析(圖 2)顯示, 有高達42.0%的位點MAF值等于0.5, 其中大部分位點在所有被測個體中均表現為雜合子, 即基因型頻率異常。考慮到鮭科魚類共同祖先曾經在約9500萬年前經歷過全基因組復制事件[22], 基因組內的旁系同源序列極其豐富, 這些雜合子基因型可能并非來自同源染色體上的等位基因, 而是由目標位點的旁系同源序列導致的干擾性檢測結果。在所使用的虹鱒57K芯片設計中[13], 曾經通過雙單倍體群體檢測, 成功排除了虹鱒基因組內的旁系同源序列變異(Paralogous sequence variant, PSV)位點, 而本檢測將虹鱒芯片應用于近緣鮭科物種檢測, PSV再次大量出現。HWE檢驗的原理是通過檢測基因頻率和基因型頻率的平衡關系來進行群體遺傳分析, 因而在本研究檢測的非自然交配群體中, 也可以用于排除PSV位點。對獲得的共享多態性位點做HWE檢驗, 剔除了顯著偏離HWE的位點。為了保證位點的基因組覆蓋度, 通過LD檢驗剔除了緊密連鎖的位點。多個物種中的前期研究已表明[18,23], 96位點低密度芯片是魚類親權鑒定和個體識別的優選位點數目, 最終從備選位點中選擇96個高質量位點用于微流控芯片設計。
3.3 反應機理與信號識別
SNPtype微流控體系基于集成流體通路(Integrated fluidic circuit, IFC)構建, 在同一個控制系統下, 將微流控通道、控制閥門和多個反應艙集成在同一張芯片上, 首先使用STA引物和LSP引物對模板DNA進行PCR擴增反應, 擴增產物與2條ASP探針分別雜交, 檢測雜交后的熒光信號。純合子將檢出其等位基因探針對應的熒光標記信號, 而雜合子同時顯示兩種熒光標記物信號, 圖 4以1個GT顛換型SNP位點HOBS-01為例, 展示了192個樣本的微流控芯片分型結果, 以無模板對照為信號基線, 3種基因型樣本各自聚群, 并能夠清晰區分。
3.4 低通量SNP芯片的實用性分析
圖5和圖 6以細鱗鮭為檢測對象, 分別展示了應用微流控分型系統在親本鑒定和群體遺傳評估中的兩個應用實例。在干擾親本存在的條件下, 通過96個SNP位點分型結果可將96尾細鱗鮭子代個體分配至其真實親本, 無論單親本鑒定還是雙親本鑒定結果均落在可靠象限內(圖 5), 能夠準確重現復雜家系的真實系譜, 并滿足對野外捕撈個體是否來源于增殖放流苗種進行溯源的統計學要求。針對遺傳差異顯著的4個細鱗鮭群體, 基于96個SNP位點分型結果也可開展初步的群體遺傳學分析, 區分其祖源成分, 并用于放流群體的種質來源和遺傳結構評估(圖 6)。
過去三十余年中, 基于核酸分析的親權鑒定主要使用微衛星標記[24]。然而, 伴隨著下一代測序技術的蓬勃發展, 海量SNP標記的開發正在逐漸變革分子遺傳領域的技術方案選擇。由于微衛星標記在基因組內的數量和分布相對有限, 且新標記的開發驗證成本較高, 因而備選標記數量較少, 很難針對特定檢測場景需求, 實現個性化位點組合的精準設計。而SNP標記在基因組中廣泛存在, 來源于公共數據庫的二代測序數據和開放獲取的高通量芯片工具提供了海量的候選SNP位點, 且SNP標記具有易于自動化、標準化分析, 代際遺傳突變速率較低等優點[24—26], 研究者一直對基于SNP標記的遺傳分析應用寄予厚望。本研究提供了針對鮭科魚類增殖放流評估場景的技術解決方案及其應用實例,有力拓展了SNP標記分型技術在分子檢測領域的應用前景。
4 結論
基于微流控芯片構建包含96個鮭科共享多態性位點的SNP分型系統, 可成功開展細鱗鮭復雜家系的親權鑒定和群體遺傳結構初步評估, 適合應用于鮭科魚類增殖放流個體識別和種群遺傳結構動態評估, 以及在此基礎上開展的增殖放流效果評估。

