UPLC-MS/MS檢測女金丸中9種青霉素類抗生素殘留*
李應才,黃合琤,董麗榮,楊 野
(1.昆明市食品藥品檢驗所,云南 昆明 650032;2.昆明理工大學,云南 昆明 650500)
女金丸(水蜜丸)是由當歸等23味中藥,粉碎成細粉,過篩,混均,每100 g粉末用煉蜜35~50 g作為黏合劑,加適量水制成的固體制劑[1]。在蜜蜂養殖中,蜂農為了防病治病,會使用氯霉素、青霉素等各種抗生素,從而殘留在蜂蜜中[2-5]。青霉素類抗生素具有較多的不良反應,包括過敏反應、皮疹、白細胞數目減少、心率增加、惡心、嘔吐、血尿等,會累及多個系統及器官,使患者的器官功能受到損害,更有甚者會威脅生命安全[6-7]。目前有文獻報道蜂蜜中抗生素的檢測[8-11],但中藥丸劑中抗生素的檢測少有報道。中藥丸劑的制備,如果使用了抗生素殘留超標的蜂蜜,將帶入制劑中,對人體產生傷害。本試驗以女金丸(水蜜丸)為研究對象,采用超高效液相色譜-串聯質譜法[12-24],建立了一種快速、有效檢測女金丸中9種青霉素類抗生素殘留的檢測方法,為中藥丸劑中抗生素殘留的檢驗研究提供參考。
1 儀器與材料
1.1 儀器 AB SCIE 5500+QTRAP質譜儀,配ESI離子源(美國應用生物系統公司);超高效液相色譜儀(SHIMADZU LC40);AL104(萬分之一)電子分析天平(梅特勒-托利多儀器(上海)有限公司);MS105DU(十萬分之一)微量分析天平(梅特勒-托利多儀器(上海)有限公司);Milli-Q 7015超純水制備儀(MERCK MILLIPORE默克密理博);KQ5200DB數控超聲波清洗器(昆山市超聲儀器有限公司)。
1.2 試劑試藥 對照品9種青霉素混標(批號21020687)來源于北京壇墨質檢科技有限公司;色譜純乙腈購于Thermo Fisher公司,色譜純甲酸購于國藥集團化學試劑有限公司。女金丸為網絡購買樣品,共30批次。
2 實驗方法
2.1 實驗條件
2.1.1 液相色譜條件 色譜柱:ACQUITY UPLC BEH-C18(2.1 mm × 50 mm,1.7 μm);流動相:0.1%甲酸水溶液-乙腈;流速:0.2 mL·min-1;柱溫:40 ℃;進樣量:10 μL。按照表1進行梯度洗脫。
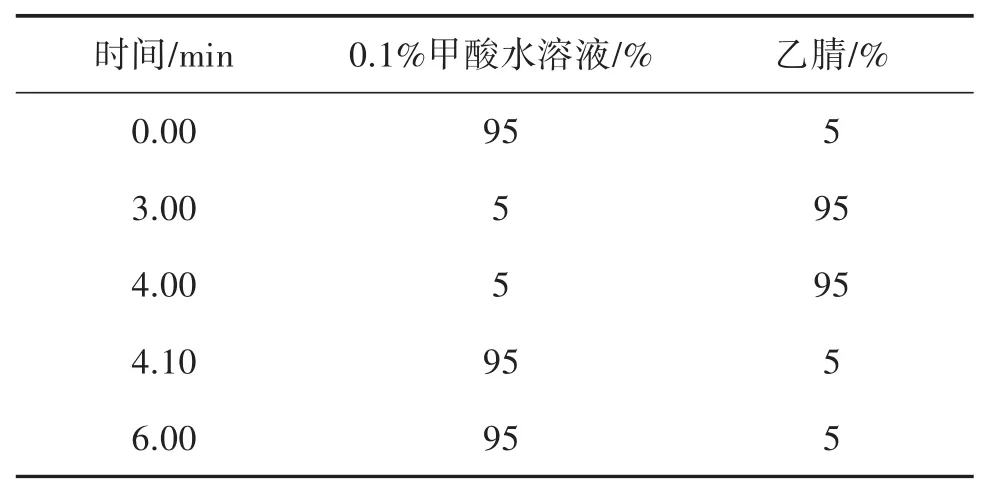
表1 梯度洗脫程序
2.1.2 質譜條件 采用SCIEX 5500+QTRAP質譜系統,電噴霧離子源(ESI源),多反應監測模式,離子源溫度為550℃,正離子模式掃描,離子源電壓為5.5 kv,噴霧氣(Gas1)55 Psi,輔助加熱氣(Gas2)55 Psi,氣簾氣30 Psi。優化得到各藥物的質譜參數見表2。

表2 各藥物質譜參數
2.2 溶液的制備
2.2.1 對照品溶液 精密稱取上述對照品適量,置于10 mL量瓶中,加水使其溶解并定容至刻度,搖勻,得九種青霉素混合對照品儲備液。
精密量取上述混合對照品儲備液適量,用20%乙腈溶液稀釋至需要濃度,得9種青霉素混合對照品工作溶液。
2.2.2 供試品溶液 取供試品適量,研細,取約2 g,精密稱定,置50 mL聚苯乙烯具塞離心管中,加入10 mL水,渦旋震蕩10 min。精密加入乙腈10 mL,渦旋混合1 min,再加入4.0 g無水硫酸鎂、1.0 g氯化鈉混合粉末,立即搖散,置振蕩器上劇烈振蕩3 min,離心(5 000 r/min)5 min。精密吸取5 mL上層清液,置于預先裝有100 mg C18、150 mg N-丙基乙二胺(PSA)、100 mg石墨化炭黑(GCB)的離心管中,渦旋2 min,離心(5 000 r/min)5 min。精密吸取上清液2 mL,置氮吹儀上于40℃水浴吹干,精密加入20%乙腈溶液1.0 mL,渦旋混勻,用0.22 μm微孔濾膜濾過,即得。
2.3 線性范圍、檢測限及定量限考察 精密吸取“2.2.1”項下的混合對照品溶液,用20%乙腈溶液稀釋成系列濃度的混合對照品工作溶液,按“2.1”項條件測定。以各對照品質量濃度(X,ng·mL-1)為橫坐標,以定量離子對峰面積(Y)為縱坐標,進行線性回歸計算,結果色譜峰面積與其質量濃度在一定的范圍內具有良好的線性關系,r均大于0.999。精密吸取“2.2.1”項下的混合對照品溶液,逐級稀釋后按“2.1”項條件測定,以離子對信噪比大于等于3考察其檢測限,以離子對信噪比大于等于10考察其定量限。結果見表3。
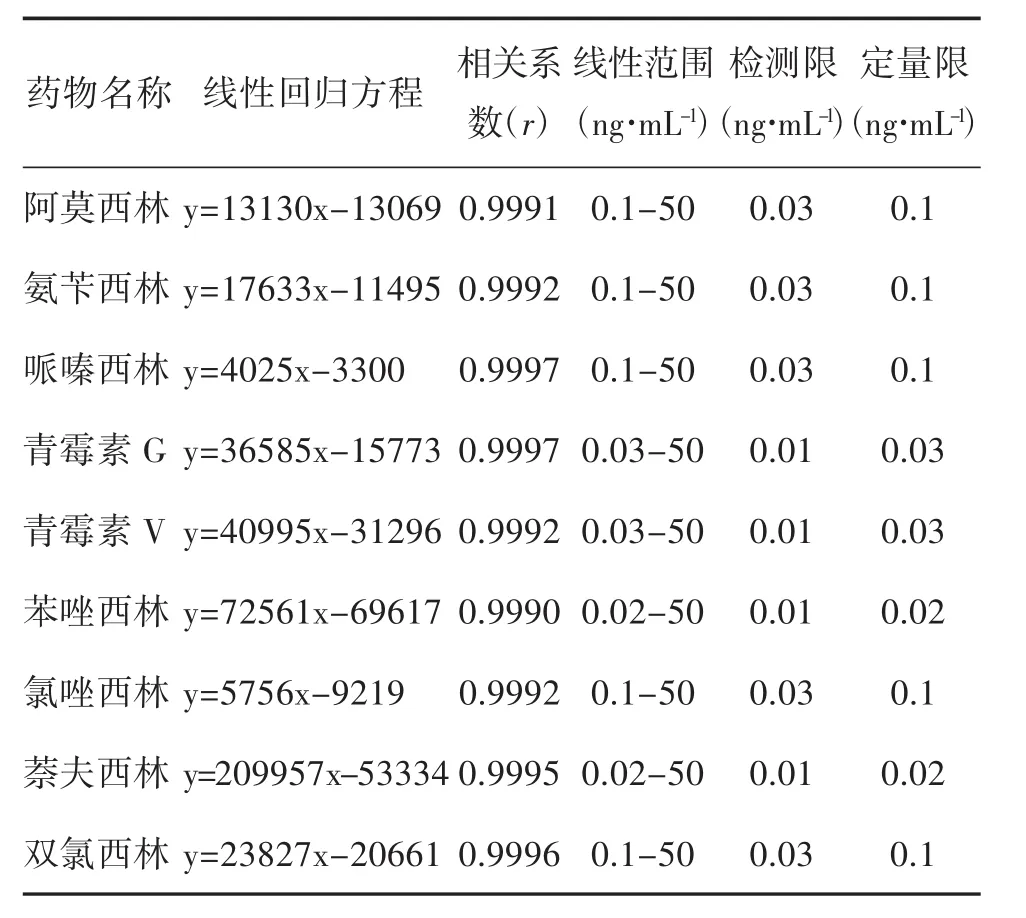
表3 各藥物成分線性關系、檢測限及定量限
2.4 精密度、重復性、穩定性實驗 精密吸取同一混合對照品工作溶液,按“2.1”項條件測定,連續進樣6次,其峰面積的RSD均小于4%,表明儀器精密度良好。精密稱取6份陰性樣品,每份約2.0 g,加對照品溶液,添加量為10.0 ng,按“2.2.2”項下方法制備成供試品溶液,按“2.1”項條件分別進樣測定,計算各添加藥物成分的含量,其平均含量RSD均小于4%,表明該方法重復性好。取同一份供試品溶液,在室溫下放置 0、2、4、6、8、12 h 后,按“2.1”項條件分別進樣測定,記錄各藥物成分峰面積并計算其RSD值,均小于4%,表明供試品溶液在室溫下放置12 h內穩定。結果見表4。
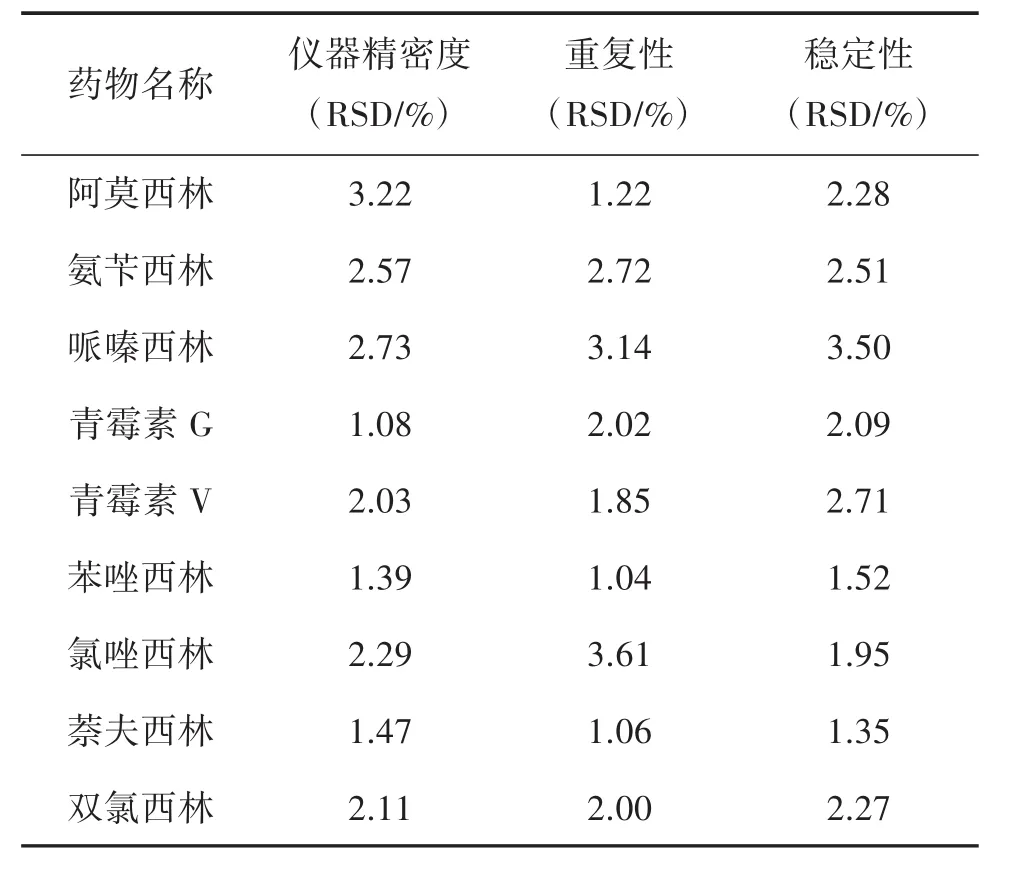
表4 各藥物成分的精密度、重復性、穩定性結果(n=6)
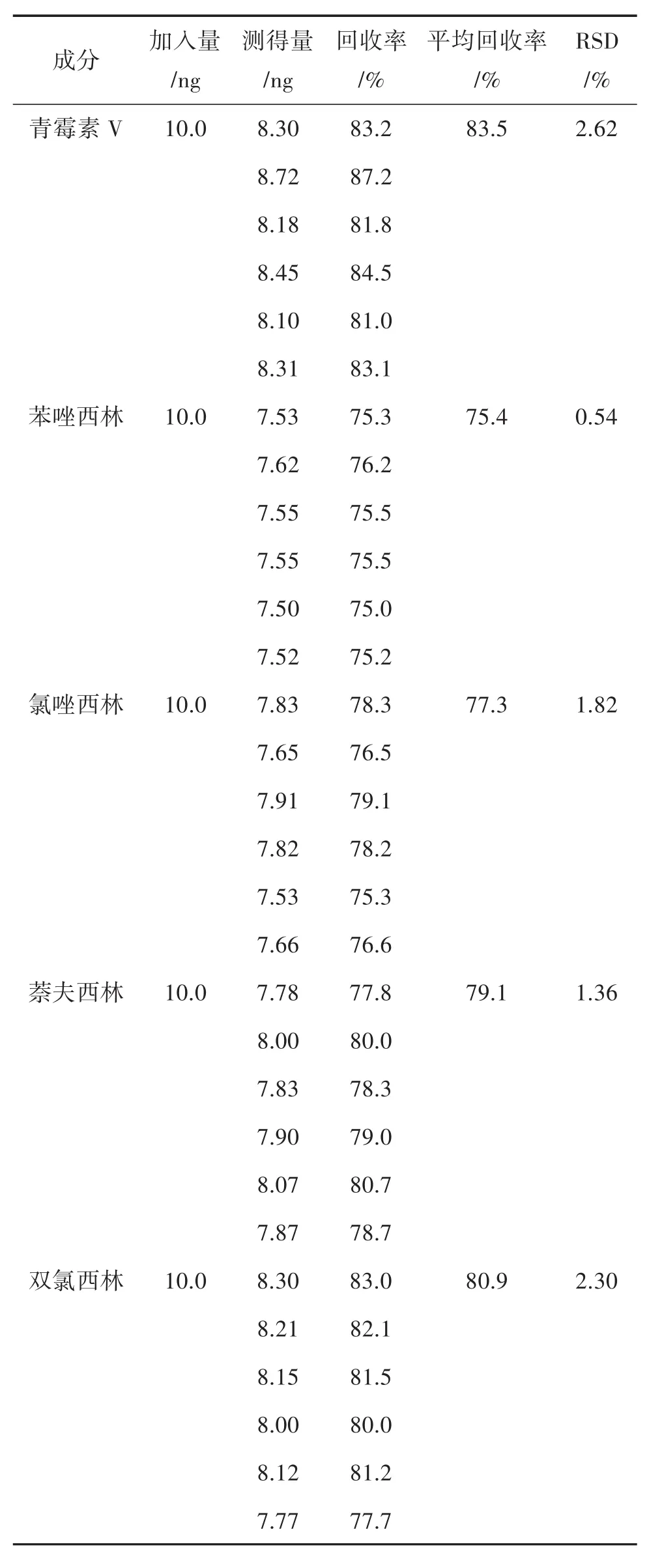
2.5 準確度試驗 精密稱取6份陰性樣品,每份約2.0 g,加對照品溶液,添加量為 10.0 ng,按“2.2.2”項下方法制備成供試品溶液,按“2.1”項條件分別進樣測定。結果見表5。
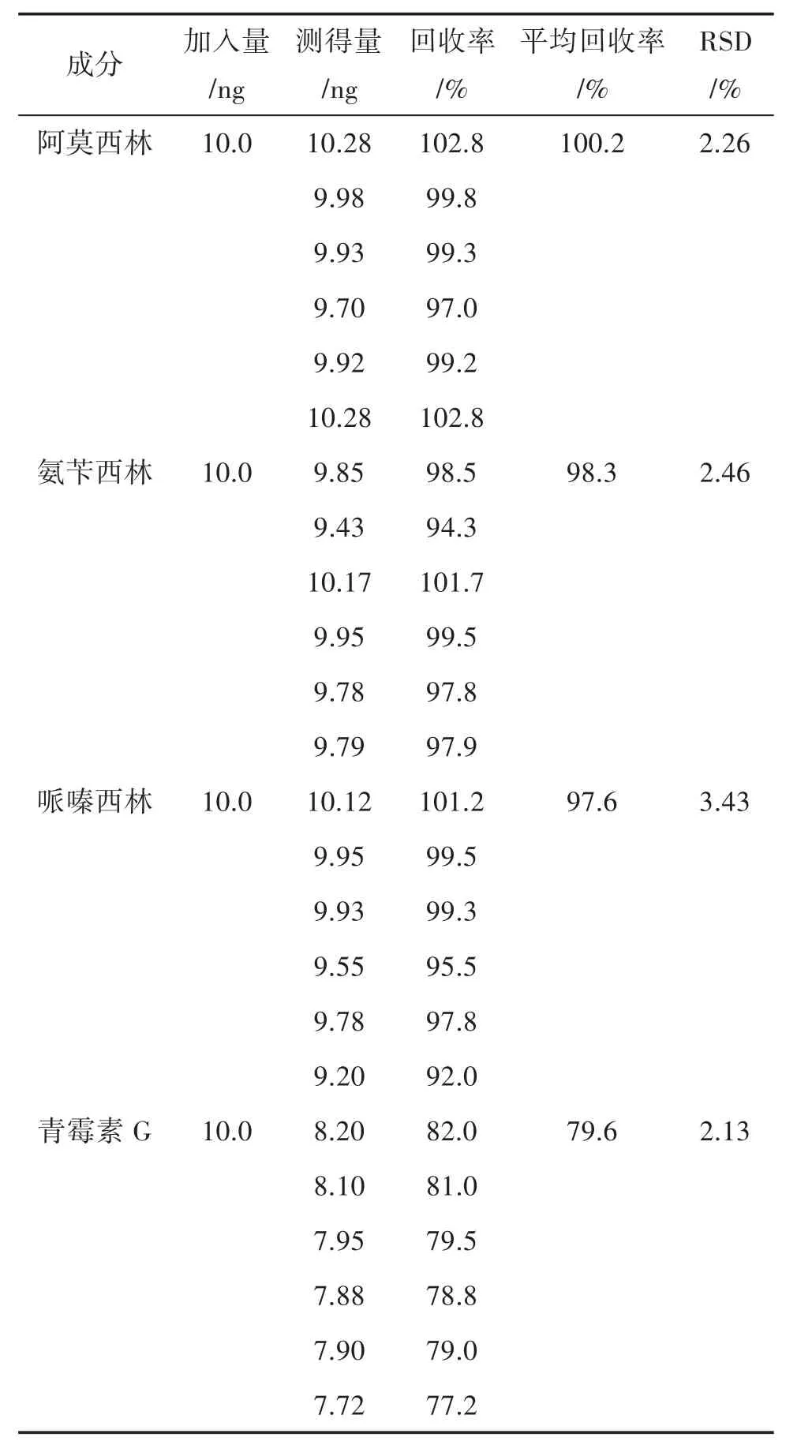
表5 各藥物成分加樣回收率試驗結果(n=6)
續表5
2.6 實際樣品的檢測 利用建立的方法,對30批樣品進行檢測,結果在30批樣品中,有1批樣品檢出雙氯西林,含量為0.193 mg·kg-1,其他樣品均未檢出。對照品溶液(A)和陽性供試品溶液(B)多反應監測(MRM)色譜圖見圖1。
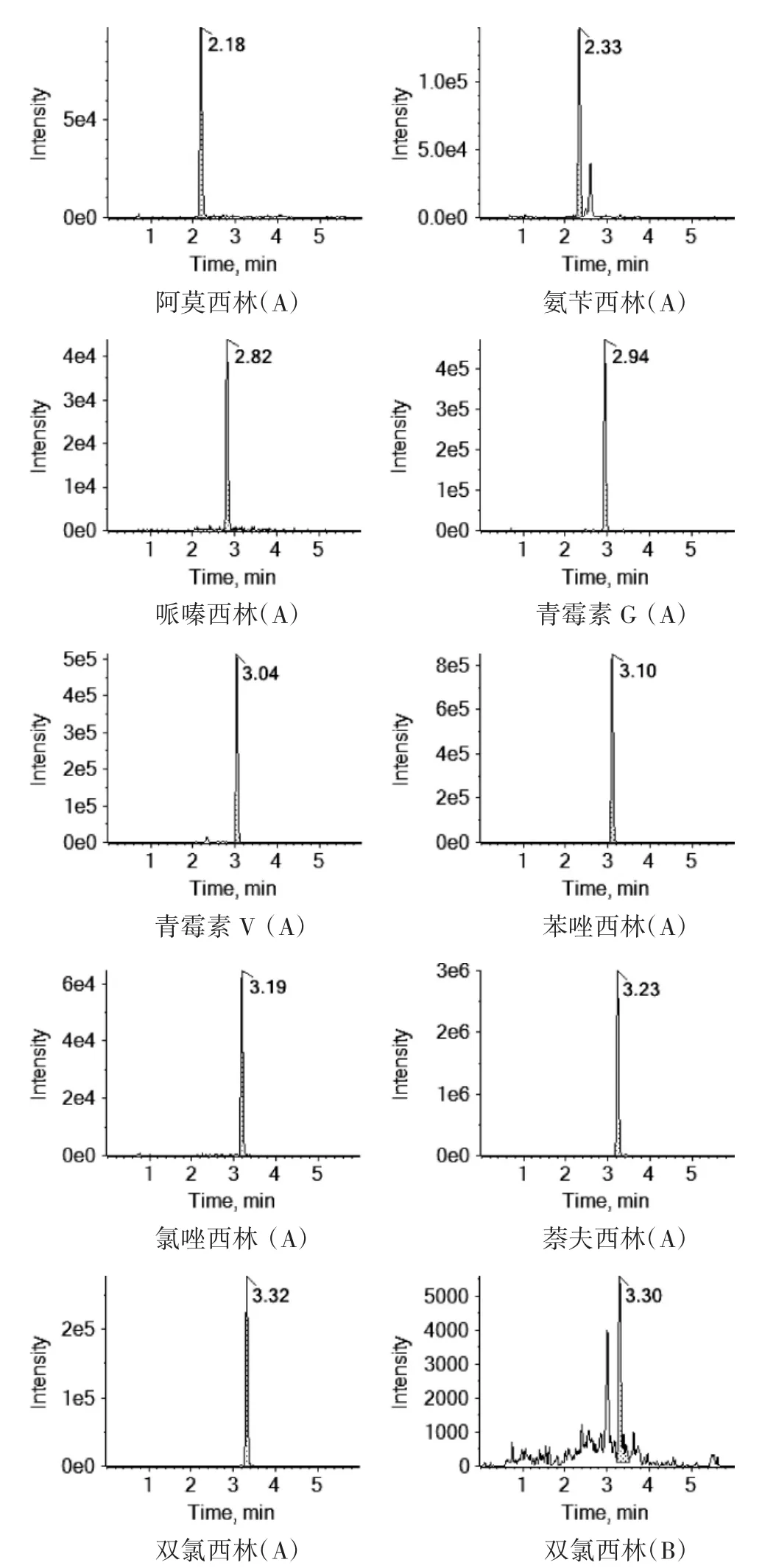
圖1 對照品溶液(A)和陽性供試品溶液(B)多反應監測(MRM)色譜圖
3 討論
3.1 色譜條件的優化 本試驗比較了流動相體積分數為0.1%的甲酸水溶液-0.1%甲酸甲醇溶液、0.1%的甲酸水溶液-甲醇溶液、0.1%的甲酸水溶液-0.1%甲酸乙腈溶液及0.1%的甲酸水溶液-乙腈溶液對目標物的分離效果。結果表明,流動相體積分數為0.1%的甲酸水溶液-乙腈溶液時,目標物離子化效率高,色譜峰形好。
3.2 前處理方法的優化 本方法比較了水、甲醇和乙腈,作為提取溶劑進行直接提取的提取效率,結果用水提取,乙腈萃取提取效率最好,但由于樣品基質復雜,基質干擾效應明顯,難于滿足回收率要求。本文選擇了QUECHERS鹽包萃取凈化法,通過優化PSA、GCB和C18用量比例,達到了最優凈化效果。
3.3 中藥丸劑抗生素殘留檢測的思考 中藥丸劑抗生素殘留,除了人為添加外,主要由蜂蜜殘留而引入。目前蜂蜜中抗生素的檢測已有報道。由于蜂蜜基質相對中藥更單一,對實驗的基質干擾更小,建議加強對中藥丸劑輔料蜂蜜的抗生素殘留進行檢測控制。
4 小結
本試驗建立了超高效液相色譜-串聯質譜法同時檢測中藥丸劑中9種青霉素類抗生素殘留的分析方法。該方法具備靈敏度高、重復性好、分析時間短、取樣量小等優點,可為檢測中藥丸劑中抗生素殘留提供參考。

