中性粒細胞與淋巴細胞比值聯合多因素對重癥肺炎死亡風險的預測價值分析
潘朝勇 汪興玲 曾匯霞
重癥肺炎(Severe pneumonia,SP)是肺部感染惡化的表現。隨著我國城市化的快速發展,空氣質量降低,老齡化人口比例加重,伴發基礎疾病增多均增加肺部感染高發的風險。有報道我國人群SP 發病率為10%~30%[1],有90%需要入住重癥加重護理病房(ICU)[2]。SP 病情進展快,居感染性疾病死亡原因的首位[3]。單一炎癥指標對SP 病情嚴重程度和預后的評估價值有限,近年來PCT、白細胞介素-6(IL-6)和Toll 樣受體-4(TLR-4)逐漸應用于SP 病情評估,而IL-6 和TLR-4 檢測費用昂貴,基層醫院難以開展和推廣。近年來多項研究報道了NLR 的診斷效能,它能夠用于不穩定型心絞痛患者冠狀動脈病變的嚴重程度以及臨床風險評估[4];可以作為小兒支氣管哮喘輔助診斷[5];更是膿毒癥并發急性腎功能損害的獨立危險因素[6];NLR<5,可以區分病毒性或支原體性和細菌性肺炎[7]。而文獻查詢NLR 聯合多因素對SP 死亡的預測價值報道較少,本研究探討NLR 聯合多因素對SP 患者死亡風險的預測價值。
1 資料與方法
1.1一般資料 回顧性分析2018 年1 月~2021 年6 月就診于肇慶市第二人民醫院呼吸與危重癥醫學科的258 例SP 患者的臨床資料,依據住院28 d 預后情況分為死亡組(81 例)和存活組(177 例)。納入標準:①所有患者診斷標準均符合中國醫師協會急診醫師分會 2019 年制定的《中國急診重癥肺炎臨床實踐專家共識》SP 的診斷標準[3];②年齡>18 歲;③入住ICU時間>48 h。排除標準:①合并嚴重肝腎功能不全者;②合并免疫功能低下或免疫抑制者;③合并血液系統疾病者;④臨床資料不完整者;⑤近期使用可能會影響外周血細胞計數相關藥物者;⑥非肺部感染者。本研究符合醫學倫理學標準,獲得醫院倫理委員會審批,所有指標和治療均獲得患者和家屬的知情同意。倫理審批文號20210730。
1.2方法 回顧性分析兩組患者的性別、年齡、糖尿病、高血壓、腦梗死、冠心病、有吸煙史及入ICU 24 h的NLR、C 反應蛋白(CRP)、PCT、丙氨酸氨基轉移酶(ALT)、尿素氮(BUN)、血肌酐(Scr)、血乳酸、呼吸頻率(RR)、平均動脈壓(MAP)、氧合指數(PaO2/FiO2)、使用血管活性藥物比例、APACHE Ⅱ評分、PSI 評分。
1.3統計學方法 采用 SPSS20.0 和MedCalc19.2 統計學軟件對研究數據進行統計分析。計量資料符合正態分布以均數±標準差()表示,采用t 檢驗;偏態分布采用四分位數[M(P25,P75)]表示,采用非參數檢驗。計數資料以率(%)表示,采用χ2檢驗。采用多因素Logistic 回歸分析篩選SP 28 d 死亡的獨立危險因素。制作ROC 曲線,以AUC 描述NLR 聯合多因素對SP 28 d 死亡的預測效能。P<0.05 表示差異有統計學意義。
2 結果
2.1兩組臨床資料比較 258 例SP 患者28 d 的死亡率為31.4%(81/258)。兩組患者性別、糖尿病、高血壓、腦梗死、冠心病、有吸煙史及入院24 h 的CRP、BUN、Scr、ALT、RR、PaO2/FiO2、MAP、血乳酸比較差異無統計學意義(P>0.05)。死亡組患者年齡大于存活組,入ICU 24 h 的NLR、PCT、APACHE Ⅱ評分、PSI 評分、使用血管活性藥物占比高于存活組,差異均具有統計學意義(P<0.05)。見表1。
表1 兩組臨床資料比較[n(%),,M(P25,P75)]
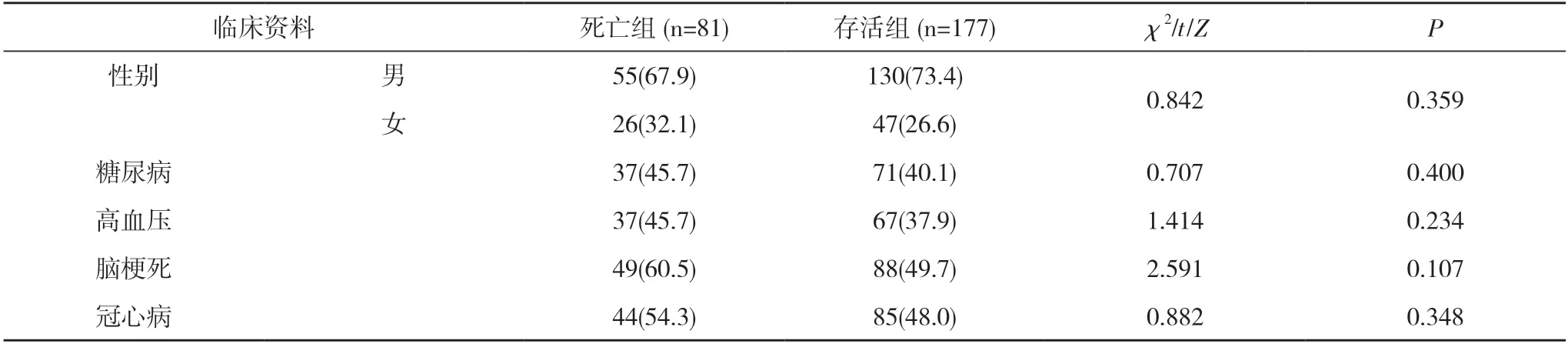
表1 兩組臨床資料比較[n(%),,M(P25,P75)]
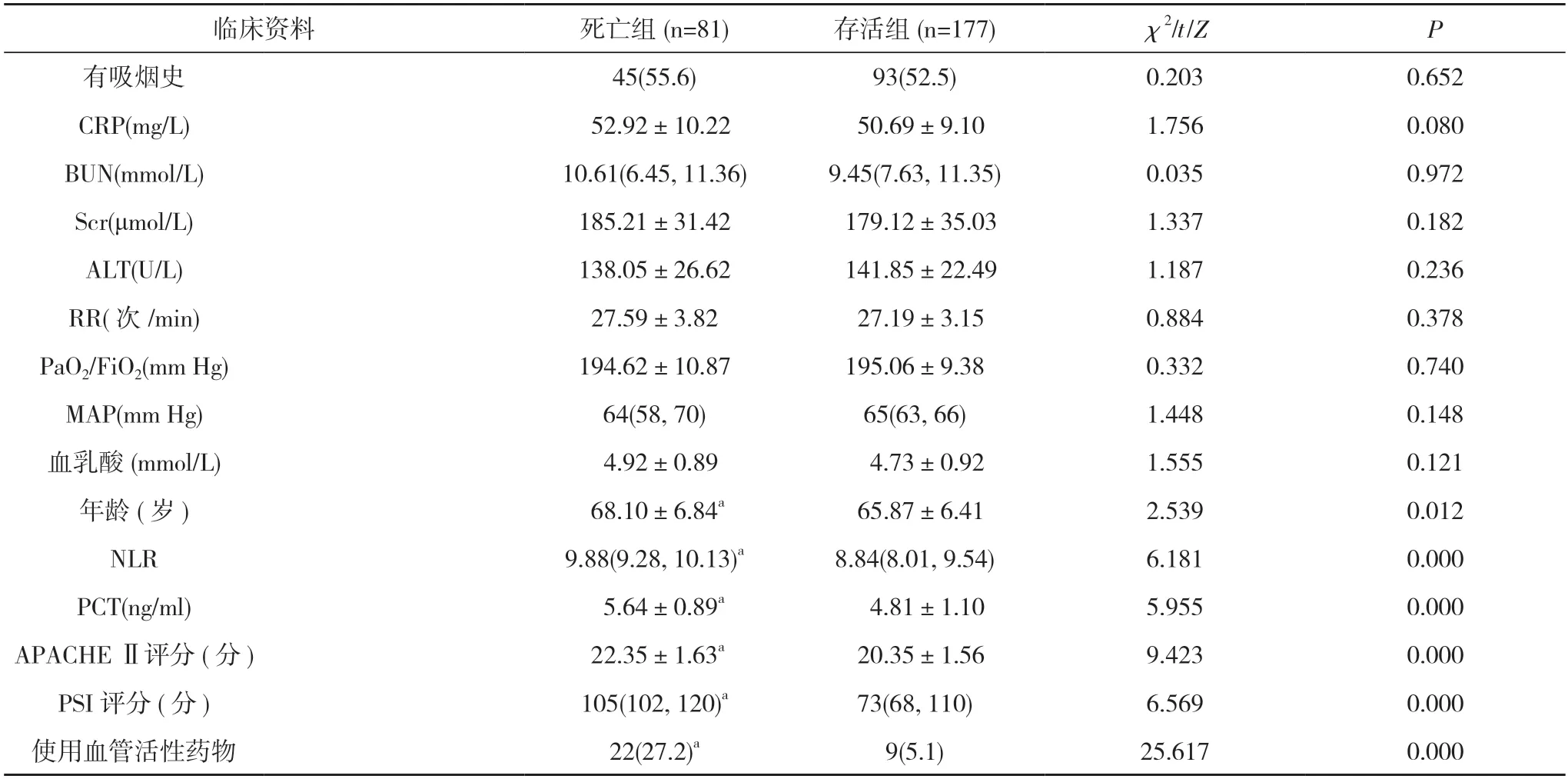
續表1
2.2SP 患者死亡危險因素的多因素Logistic 回歸分析多因素Logistic 回歸分析顯示:NLR、APACHE Ⅱ評分、PSI 評分、PCT 高為SP 患者死亡的獨立危險因素(P<0.05)。見表2。
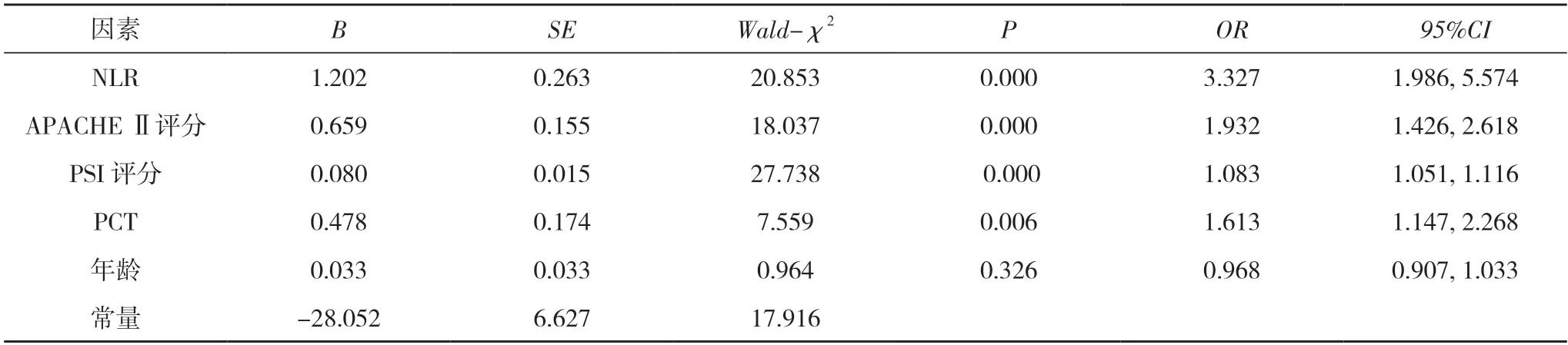
表2 SP 患者死亡危險因素的多因素Logistic 回歸分析
2.3NLR、PCT、APACHE Ⅱ評分、PSI 評分對SP 患者死亡風險的預測價值 NLR、APACHE Ⅱ評分、PSI評分、PCT 預測SP 患者死亡的截斷值分別為9.31、21.5 分、97.5 分、5.55 ng/ml;NLR 聯合多因素對SP患者死亡的預測價值最大,AUC 為0.940,均大于單一NLR、APACHE Ⅱ評分、PSI 評分、PCT 的0.740、0.806、0.755、0.762,差異有統計 學意義(P<0.05)。NLR 聯合多因素預測SP 死亡的靈敏度為92.60%,特異度為81.90%。見表3。
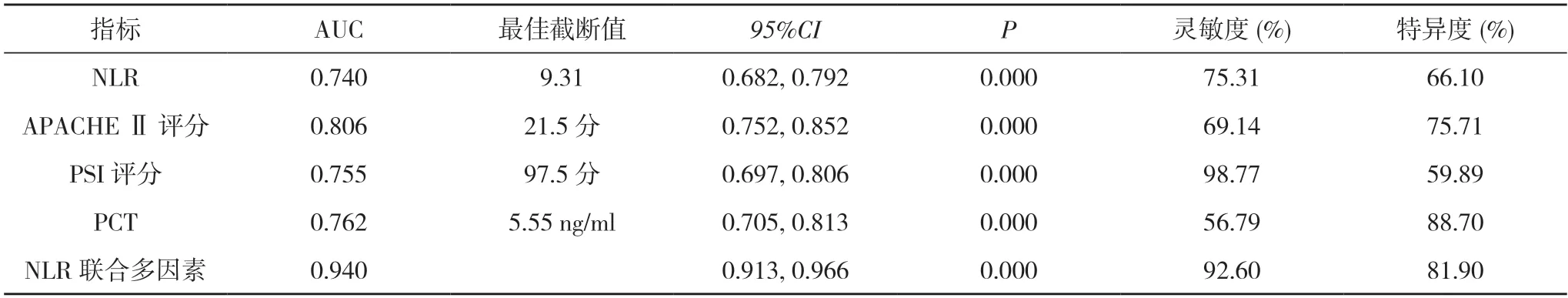
表3 NLR、PCT、APACHE Ⅱ評分、PSI 評分對SP 患者死亡的預測價值
3 討論
SP 的病理生理改變是患者對病原體侵襲作出的復雜防御反應:①病原體的內外毒素直接損害肺上皮細胞和肺組織。②病原體引發的間接損傷,表現為中性粒細胞增多和滲出到肺組織,引發肺組織化膿性溶解,還激活單核巨噬細胞系統,釋放多種炎癥因子,如白細胞介素-1(IL-1)和腫瘤壞死因子(TNF),二者繼續促進和加重粒細胞從骨髓儲存庫釋放并游走到SP 的炎癥部位[8-10];粒細胞和巨噬細胞繼續釋放趨化因子,加重多種炎癥細胞在肺間質、肺泡內的浸潤,引起肺部炎癥的瀑布樣反應;此時肺泡毛細血管膜受損,分泌表面活性物質的Ⅱ型肺泡上皮細胞受損,造成肺泡和肺組織水腫,最終出現急性呼吸窘迫綜合征,引發SP 的不良預后[11-15]。本研究中SP 患者的死亡率為31.4%,與文獻報道類似[16]。SP 病情輕重一方面取決于病原體的性質和強度;另一方面取決于患者粒細胞和淋巴細胞的反應狀態。粒細胞和淋巴細胞是SP 疾病發生發展的主要參與者,文獻報道NLR 用于痛風[17]、慢性阻塞性肺疾病[18]等慢性炎性疾病預后的評估。本研究結果提示,SP 死亡組入院24 h 的NLR 高于存活組,差異具有統計學意義(P<0.05)。分析原因為:死亡患者更嚴重的感染應激刺激機體釋放更多的兒茶酚胺類物質和皮質醇激素,加速淋巴細胞凋亡,導致NLR 增大;同單一白細胞或中性粒細胞的指標比較,NLR 對SP 引發全身炎癥反應綜合征病情嚴重程度的判斷更有效。本研究結果中NLR 預測SP 患者死亡的AUC 為0.740,低于劉九玉等[19]報道的0.840 和梁歡等[20]報道的0.791,是因為本研究納入的引發SP 的病原體除細菌外,還有其他的病原體,其他病原體引發SP 中NLR 升高的幅度不大,對診斷的效能有影響,但其AUC>0.7,能夠預測SP 的預后。
APACHE Ⅱ評分、PSI 評分和PCT 在國內SP 患者的病情評估和預后中均有廣泛應用,本研究中,NLR聯合多因素預測SP 死亡的AUC 0.940 大于單一NLR、APACHE Ⅱ評分、PSI 評分、PCT 的0.740、0.806、0.755、0.762,差異有統計學意義(P<0.05)。也高于許紹珍等[1]報道的NLR 僅聯合PCT 的AUC 0.881,提示NLR 聯合多因素預測SP 死亡的效能更高;其靈敏度為92.60%,特異度為81.90%,實踐中可以更多應用NLR 聯合多因素來評估SP 的死亡風險。
綜上所述,NLR 聯合APACHE Ⅱ評分、PSI 評分、PCT 等多因素對SP 患者死亡風險有較高的預測價值,值得應用。

