鴨2型腺病毒和鴨圓環病毒雙重PCR方法的建立
王新港,王彥輝,周 欣,丁麗萍,陳圓圓,李厚偉,張先鋒*
(河南普華基因科技有限公司,河南 鄭州 450002)
鴨2型腺病毒(Duck adenovirus 2,DAdV-2)病和鴨圓環病毒(Duck circovirus,DuCV)病是嚴重影響我國水禽養殖的兩種病毒性疾病。雛鴨階段兩種疾病的發病路和死亡率高。鴨腺病毒感染主要表現為精神萎靡、沉郁和消瘦,排淺黃白色的糞便。病理變化為肝臟腫大并有白色針尖狀壞死點灶,腎臟及脾臟腫大充血,胰腺有白色點狀壞死。而鴨圓環病毒常呈潛伏感染,并入侵鴨的免疫系統,導致機體的免疫功能下降,對多種條件性病原抵抗力減弱,使其更易遭受其他致病因素的侵襲。而一旦發生混合感染(如鴨流感病毒、鴨腺病毒、鴨大腸桿菌等混合感染),感染鴨的死亡率就會大大提升。目前上述兩種疾病已廣泛流行于廣東、福建、浙江等水禽養殖密集地區,給養鴨業造成了巨大的經濟損失。
上述兩種病原均為DNA 病毒,引起的臨床癥狀具有一定的相似性,易發生混合感染,極大地增加了臨床鑒別診斷的難度。而常規的診斷方法,如動物實驗、免疫學和病毒分離培養,在臨床診斷中存在診斷時間長、敏感性低以及操作繁瑣等缺點,在臨床中不易于快速診斷上述兩種疾病。因此,建立一種快速、準確、靈敏的檢測方法來診斷和監控上述兩種病原,確保養鴨業的健康發展尤為重要。
筆者基于前期臨床調查和研究的基礎上,進行了DAdV-2 和DuCV 雙重PCR 方法的建立,并對建立的雙重PCR 方法對鴨群中鴨圓環病毒和鴨腺病毒2 型進行鑒別診斷,驗證了該方法的可靠性和穩定性。對鴨群中鴨圓環病毒和鴨腺病毒2 型流行病學調查及防控提供了可靠的檢測手段,具有重要的臨床應用價值。
1 材料與方法
1.1 試驗儀器與試劑盒
核酸提取試劑盒購自天根生化科技(北京)有限公司;PCR儀、臺式離心機、微量移液器、無菌操作臺、電泳儀、凝膠成像儀由河南普華基因科技有限公司提供。
1.2 陽性病料、菌毒株及臨床樣品
試驗用陽性病料:含有鴨圓環病毒的陽性病料由河南普華基因科技有限公司鑒定和保存。
試驗用菌毒株:鴨腺病毒2型、鴨瘟病毒、鴨病毒性肝炎Ⅰ型、鴨呼腸孤病毒、鴨坦布蘇病毒、鴨細小病毒、鴨大腸桿菌、鴨疫里默氏桿菌、鴨源禽多殺性巴氏桿菌均由河南普華基因科技有限公司鑒定和保存。臨床樣品均來自2019-2020年不同省份送檢疑似病料,共計83份。
1.3 方法
1.3.1 引物設計與合成
根據GenBank上已報道的DAdV-2和DuCV的全基因組序列,對不同毒株基因組的比對和分析,篩選其較為保守的核酸片段,應用Primer5.0 引物設計軟件設計了兩對針對上述兩種病毒的特異性引物,并通過NCBI(https://www.ncbi.nih.gov/)對兩對引物進行在線分析。最終篩選出兩對引物(表1),引物由生工生物工程(上海)股份有限公司合成。兩對引物能夠特異性地擴增出598bp(DAdV-2)和297bp(DuCV)的特異性片段。

表1 PCR引物信息序列
1.3.2 菌毒株核酸提取
待測樣品核酸的提取:選取疑似發病動物無菌采集其內臟組織(肝臟和脾臟)約5 g,在超凈操作臺用手術剪刀將上述病料組織剪碎,用PBS按照5∶1(W/V)進行稀釋后,放置-80 ℃反復凍融三次,上述待測樣品及對照菌毒株按照病毒基因組提取試劑盒(TIANamp Virus DNA/RNA Kit)進行核酸的提取,提取后核酸置-70 ℃保存備用。
1.3.3 雙重PCR擴增
在前期單一PCR 研究的基礎上將相同濃度的DAdV-2和DuCV DNA混合后作為雙重PCR模板,對雙重PCR反應條件,包括引物終濃度、反應體積進行優化,以確定最佳反應體系及最佳反應條件。擴增產物于1.5%瓊脂糖凝膠中進行電泳鑒定。
1.3.4 雙重PCR特異性實驗
在雙重PCR 擴增優化基礎上,采用建立的雙重PCR方法分別對鴨病毒性肝炎Ⅰ型、鴨呼腸孤病毒和鴨坦布蘇病毒、鴨腺病毒2 型、鴨圓環病毒、番鴨細小病毒、鴨瘟病毒、鴨大腸桿菌、鴨疫里默氏桿菌和鴨源禽多殺性巴氏桿菌的陽性模板及ddH2O 進行擴增,同時設陰性對照,驗證所建立雙PCR方法的特異性。
1.3.5 雙重PCR敏感性實驗
利用分光光度計分別測定DAdV-2 和DuCV 的DNA濃度,用滅菌雙蒸水對其10倍濃度梯度稀釋,將各稀釋度DNA作為模板進行PCR擴增,檢測最小檢出量。
1.3.6 雙重RT-PCR方法的臨床應用
對河南普華基因科技有限公司研發中心于2019-2020年采集的83份疑似病死鴨內臟作為臨床檢測樣品處理后,保存樣品核酸,用單一PCR和已經建立的雙重PCR方法分別對樣品核酸進行檢測,通過對兩種方法檢測結果的比較,來評價建立的雙重PCR方法的臨床應用效果。
2 結果與分析
2.1 雙重PCR的建立
2.1.1 雙重PCR反應體系及反應條件優化
在反應條件不變的條件下(94 ℃90 s,94 ℃20 s,54 ℃30 s,72 ℃20 s,30個循環,最后一個循環72 ℃延伸5 min),將相同濃度的DAdV-2 和DuCV 提取的DNA 混合后作為雙重PCR模板,對雙重PCR反應條件進行優化。
引物濃度篩選:選取20 pmol/μL、10 pmol/μL、5 pmol/μL、1 pmol/μL、0.5 pmol/μL共計5個不同的引物濃度梯度進行PCR擴增,進行引物濃度篩選。
反應體系體積的篩選:在引物濃度為確定條件下,分別選擇12.5 μL、25 μL和50 μL的反應體系進行擴增。
考慮到經濟性和操作簡便性,最終選擇的雙重PCR反應體系為:2 5BR. BTUFS. JY12.5 μl,兩對上、下游引物各0.5 μl(10 pmol/μL),cDNA 模板各1 μl,ddH2O 補足至
25 μL。
2.1.2 雙重PCR特異性試驗
擴增結果顯示,只有DAdV-2和DuCV的混合DNA模板和DAdV-2、DuCV 的單一DNA 模板擴增出與目的片段大小相符的條帶。對擴增出的DuCV 病毒的PCR 擴增產物進行基因測序,并對擴增產物序列與參考引物序列進行生物信息學軟件分析,兩者核苷酸同源性達到96%以上,分析結果證實PCR擴增產物為DuCV病毒。
2.1.3 雙重PCR敏感性試驗
利用分光光度計分別測定DAdV-2 和DuCV 的DNA濃度分別為67 ng、52 ng,用滅菌雙蒸水對其10 倍比梯度稀釋,取10-1~10-5稀釋度進行檢測,將各稀釋度DNA作為模板進行PCR 擴增,檢測最小檢出量。兩種病毒DNA 混合物擴增結果表明,該方法對DAdV-2和DuCV的DNA最小檢出量分別為0.67 pg和5.2 pg。
2.2 雙重PCR臨床應用
臨床樣本檢測結果見表2,由表2 可知,本試驗雙重PCR 檢測結果與單一PCR 檢測結果的吻合率達到100%。對擴增出DAdV-2的陽性產物進行基因測序,并與參考引物序列進行生物信息學軟件分析,兩者核苷酸同源性達到98%以上,分析結果證實PCR擴增產物為DAdV-2病毒。
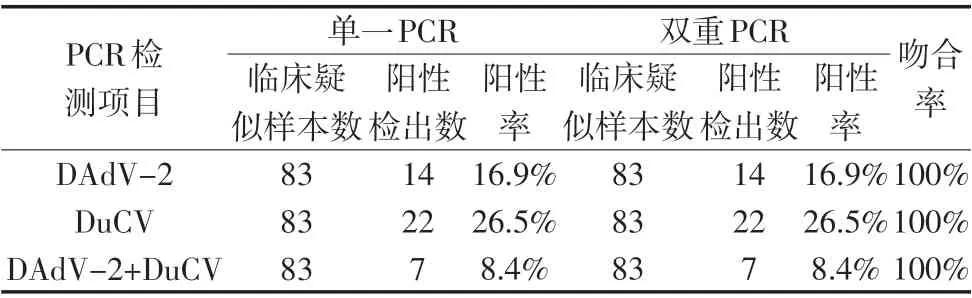
表2 臨床樣品檢測結果
3 討論
PCR是實驗室常用檢測方法之一,其具有快速、靈敏、成本低、操作簡單等優點;該方法不僅能快速確定病毒種類,還能檢測病毒的早期感染和潛伏感染。但是檢測時如果使用擴增單種病毒的引物對待測樣品進行鑒別,則可能需要準備多份樣品擴增多次才能確定感染的病毒類型,不僅在實際操作中需要增加檢測次數,另外還會引起交叉感染。雙重PCR 是在單一PCR 基礎上建立起來的,其優點在于通過一次PCR 的反應,可以同時檢測并鑒別兩種病原,在臨床中具有重要的應用價值。
該試驗建立的同時檢測DAdV-2 和DuCV 雙重PCR方法,通過一系列的試驗驗證,對DAdV-2和DuCV的核酸最小檢出量分別為0.67 pg 和5.2 pg。對臨床樣品的檢出率與單一PCR方法吻合度達到了100%。
該試驗建立的同時檢測DAdV-2 和DuCV 雙重PCR方法具有方便、快捷、敏感、特異性強及可重復性等特點,可大大節省兩種病原的檢測時間,對PRRSV和GETV的檢測、混合感染的診斷、公共衛生及流行病學調查等具有重要學術意義和應用價值。□

