糖尿病足難治性潰瘍實施網狀中厚皮片移植聯合改良VSD技術治療的應用價值
王雨辰,黃志敏,陳凱
福建省老年醫院,福建福州 350000
糖尿病足潰瘍是因患者下肢遠端神經異常和不同程度血管病變導致,引發該病主要始動因素為患者感覺性神經病變及合并過高的機械應力,長時間下反復應力作用于一個特定區域,導致潰瘍形成[1]。另外,運動神經病變在糖尿病足潰瘍中也起到一定作用,患者足內在肌攣縮可使得患者形成臨床較為典型的爪狀趾畸形,該部位容易形成潰瘍[2]。糖尿病足作為致殘率較高的慢性并發癥之一,具有治療時間較長、潰瘍創面治療較難且容易遷延不愈等特點[3]。而中厚皮片移植作為當下臨床治療該病的常規手段,雖具有耐磨度高、美觀度好等特點,由于術前潰瘍無法反復清創,使得皮片移植后存活度并不高,手術治療效果較低[4]。相關研究表明,VSD技術利用生物半透膜對于患者手術創面進行全面封閉,且不局限于患者患肢創面形狀及潰瘍深度等的影響,引流效果較好[5]。另外在常規中厚皮片基礎上形成的網狀皮片對于引流可起到更加充分的作用,顯著避免患者皮片下出現積液繼發感染,使得患者遭受二次傷害。現選取2019年3月—2021年3月福建省老年醫院收治的150例糖尿病足難治性潰瘍患者,現報道如下。
1 資料與方法
1.1 一般資料
選擇來本院就診的糖尿病足難治性潰瘍患者150例,以1:1比例分布法分為對照組與觀察組,各75例。兩組一般資料對比,差異無統計學意義(P>0.05),具有可比性,見表1。
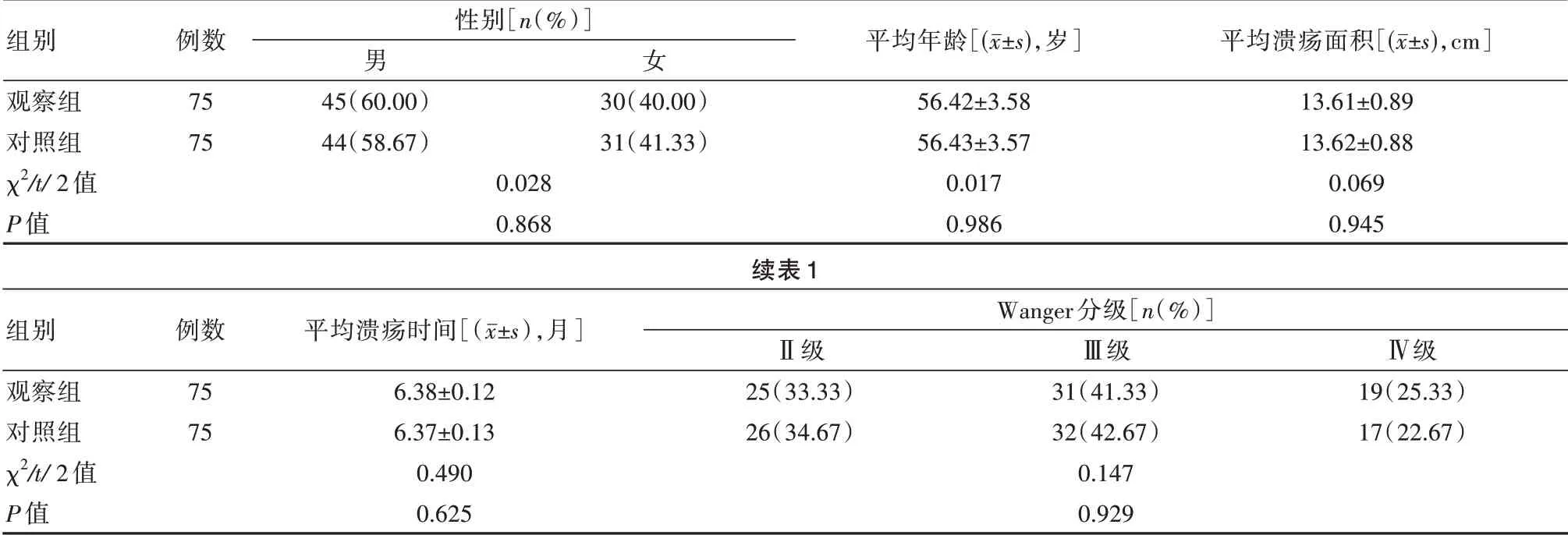
表1 兩組患者一般資料比較
1.2 納入與排除標準
納入標準:①患者經本院實驗室及影像學檢查確診為糖尿病足難治性潰瘍,符合《糖尿病足介入綜合診治臨床指南》[6]相關標準;②潰瘍出現>1個月,Wanger分級為Ⅱ~Ⅳ級;影像學顯示患者患肢主干血管并未完全狹窄;③具備植皮要求。排除標準:①合并心、肝、腎、腦等重要器官功能不全及惡性腫瘤者;②下肢主動脈血管閉塞或血管畸形者;③下肢呈大面積壞死,需給予截肢者。
1.3 方法
手術治療前兩組患者均給予服用降壓藥螺內酯(國藥準字H13022194;規格:20 mg),2次/d,20 mg/次。
1.3.1 對照組實施常規中厚皮片移植治療,對患者潰瘍創面及周圍組織使用生理鹽水進行消毒并清除壞死組織及分泌物后,以碘伏敷料覆蓋,取患者大腿內側合適組織為薄中厚皮,刮除患者潰瘍創面水腫的肉芽組織,將準備好的移植皮片植于創面并完成加壓和包扎,定期清除積液、換藥,拆線時間根據患者具體情況而定。
1.3.2 觀察組實施網狀中厚皮片移植聯合改良VSD技術治療,治療效果如下:①消毒及清創操作同于對照組,完畢后結合患者患肢潰瘍創面形狀及面積剪裁VSD敷料,使其緊密覆蓋至患者潰瘍創面,另外VSD敷料具體大小需大于患者潰瘍創面面積1~2 cm,以用于放置引流管及沖洗管,縫合敷料用以固定,利用生物半透膜封閉創面。②將引流管另一端連接負壓吸引裝置持續對患者進行負壓引流,壓力維持在125~450 mmHg,定時檢查VSD裝置,引流是否通暢,創面是否完全密閉,間隔12 h后停止負壓引流,使用沖洗管加入雙氧水和含0.3%碘伏(用量均為50~100 mL)進行灌洗,1次/d。③治療后7 d拆除VSD裝置,查看患者創面新生肉芽組織生長情況,對于積液和分泌物較多患者可以再次執行清創和VSD,若患者潰瘍部位肉芽組織符合皮片移植標準,于患者大腿內側取薄中厚皮,去除皮下多余脂肪,并將皮片戳至呈網狀,覆蓋于患者創面之上,完成縫合。完成后繼續使用VSD敷料覆蓋創面,利用生物半透膜封閉創面,繼續行負壓引流,1周后拆除VSD裝置,查看患者創面恢復情況。
1.4 觀察指標
觀察并記錄兩組患者皮片存活率、術后換藥次數、創面愈合時間、住院時間、空腹血糖及餐后1 h血糖。其中皮片存活率計算公式=(總移植皮片面積-未存活皮片面積)/總移植皮片面積×100.00%;血糖水平:空腹血糖<5.1 mmol/L;餐后1 h血糖<10.0mmol/L。
潰瘍愈合、肉芽組織生長情況:潰瘍面積縮小率=(治療前潰瘍面積-治療后潰瘍面積)/治療后潰瘍面積×100.00%;肉芽組織覆蓋率=肉芽組織覆蓋面積/創面面積×100.00%。
疼痛程度:選擇數字評價量表(Numerical Rating Scale,NRS)[7],分值0~10分,分值越高代表痛感越強。
瘢痕情況:選擇溫哥華瘢痕評分量表(Vancouver Scar Scale,VSS)[8],使用玻片按壓患者瘢痕2 s,查看并記錄其顏色變化、柔軟度及血管分布情況,分值0~15分,分值越高表示修復效果越差。
1.5 統計方法
采用SPSS 26.0統計學軟件處理數據,計量資料符合正態分布,以(±s)表示,組間差異比較采用t檢驗。P<0.05為差異有統計學意義。
2 結果
2.1 兩組患者臨床指標比較
觀察組皮片存活率顯著高于對照組,術后換藥次數、創面愈合時間、住院時間、空腹血糖及餐后1 h血糖低于對照組,差異有統計學意義(P<0.05)。見表2。
表2 兩組患者臨床指標比較(±s)
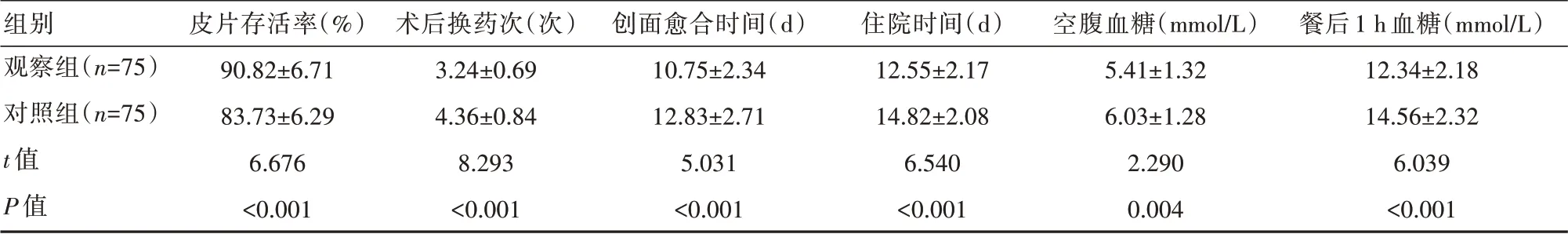
表2 兩組患者臨床指標比較(±s)
組別觀察組(n=75)對照組(n=75)t值P值皮片存活率(%)90.82±6.7183.73±6.296.676<0.001術后換藥次(次)3.24±0.694.36±0.848.293<0.001創面愈合時間(d)10.75±2.3412.83±2.715.031<0.001住院時間(d)12.55±2.1714.82±2.086.540<0.001空腹血糖(mmol/L)5.41±1.326.03±1.282.2900.004餐后1 h血糖(mmol/L)12.34±2.1814.56±2.326.039<0.001
2.2 兩組患者潰瘍愈合、肉芽組織生長情況比較
觀察組患者治療后2周和4周潰瘍面積縮小率及肉芽組織覆蓋率均顯著高于對照組,差異有統計學意義(P<0.05)。見表3。
表3 兩組患者潰瘍愈合、肉芽組織生長情況比較[(±s),%]
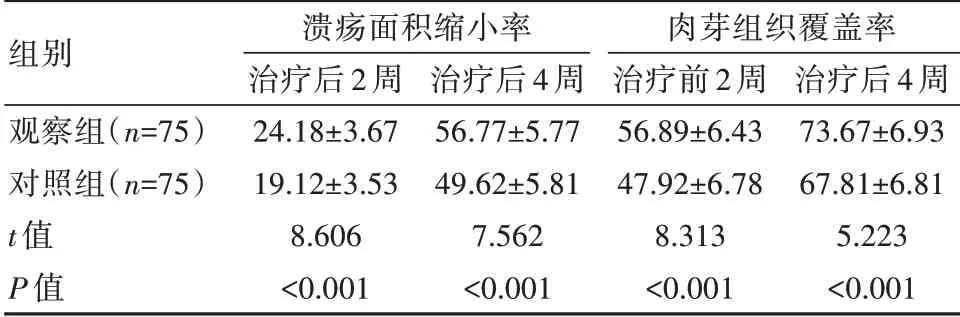
表3 兩組患者潰瘍愈合、肉芽組織生長情況比較[(±s),%]
組別觀察組(n=75)對照組(n=75)t值P值潰瘍面積縮小率治療后2周24.18±3.6719.12±3.538.606<0.001治療后4周56.77±5.7749.62±5.817.562<0.001肉芽組織覆蓋率治療前2周56.89±6.4347.92±6.788.313<0.001治療后4周73.67±6.9367.81±6.815.223<0.001
2.3 兩組患者NRS及VSS評分比較
觀察組患者治療1個月及2個月后NRS及VSS評分均顯著低于對照組,差異有統計學意義(P<0.05)。見表4。
表4 兩組患者NRS及VSS評分比較[(±s),分]
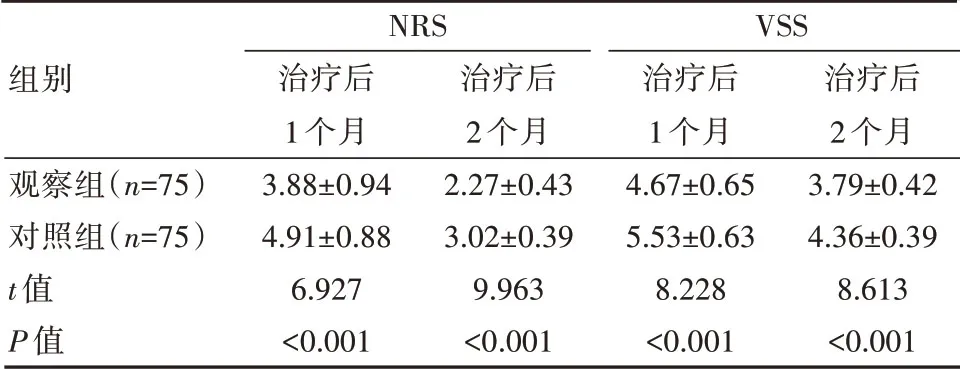
表4 兩組患者NRS及VSS評分比較[(±s),分]
組別觀察組(n=75)對照組(n=75)t值P值NRS治療后1個月3.88±0.944.91±0.886.927<0.001治療后2個月2.27±0.433.02±0.399.963<0.001 VSS治療后1個月4.67±0.655.53±0.638.228<0.001治療后2個月3.79±0.424.36±0.398.613<0.001
3 討論
糖尿病足為糖尿病最為嚴重的慢性并發癥之一,患者機體長期處于高血糖狀態下,引發患者下肢足部神經末梢血管病變,血液灌流量顯著減少,末梢局部組織缺氧、缺血導致組織壞死,長時間下壞死組織持續存在,致使細菌滋生從而出現足部潰瘍[9]。故對于糖尿病足潰瘍患者的治療關鍵節點為及時清除創面壞死組織和消毒,控制感染程度,改善血液灌流盲區等[10]。常規中厚皮片移植為目前臨床主要治療糖尿病足潰瘍的方法之一,封閉創面可有效降低感染發生率,但受制于傳統加壓和包扎,無法及時引流出術后患者創面分泌物和積液,而積液積壓容易浸潤創面,影響愈合和肉芽新發。而改良后的VSD技術聯合網狀中厚皮片移植治療,可顯著彌補常規治療下的短板,提高患者治療效果[11]。
本研究結果顯示,觀察組臨床指標、潰瘍面積縮小率、肉芽組織生長情況、NRS及VSS評分均顯著優于對照組(P<0.05)。這是因為改良VSD技術不僅可以借助引流管和負壓引流裝置可及時導出患者積液,促進潰瘍創面及周圍組織的血流供應,還可以及時灌洗消毒,保障引流通暢,減少厭氧菌滋生,顯著降低感染概率[12]。而將常規的中厚皮片使用尖頭刀制作成網狀結構,有利于對患者創面積液及分泌物等的引流,最大化避免了積液存留增加細菌自身和感染發生率,同時增加患者皮片移植適配度[13]。因此,網狀中厚皮片移植聯合改良VSD技術治療優勢為:①及時引出積液及分泌物,保障創面下基底潔凈,減少細菌滋生和侵襲,生物半透膜為患者創面創造完全封閉環境,盡可能減少患者換藥次數,減少了創面與空氣接觸的機會,避免了外界灰塵和細菌等附著在患者創面表面,減少感染風險[14]。②改良后VSD技術保障網狀中厚皮片移植時的受力均勻,與患者創面貼合度更高,這為創面肉芽新發和血管生長創造了更好的條件,故此皮片存活率和愈合情況也更高,疼痛程度和瘢痕情況在愈合較好的前提下影響較低[15]。
綜上所述,網狀中厚皮片移植聯合改良VSD技術治療,效果更加可觀,能顯著改善患者臨床指標,提高潰瘍創面恢復速度和恢復效果,降低痛感,減少瘢痕面積,在保障了治療效果的同時提高美觀度。

