流動注射褪色光度法測定水樣中的亞硝酸鹽
李 輝,李 華
(綿陽師范學院資源環境工程學院,四川 綿陽 62100)
亞硝酸鹽是水中常見的污染物之一,在pH值較低的酸性條件下,亞硝酸鹽很容易與胺類和酰胺類物質發生化學反應,并生成亞硝酸胺類的致癌物質[1],還可以將人體正常的血紅蛋白(低價血紅蛋白)氧化成高價血紅蛋白,導致人體缺氧甚至中毒死亡[2]。生活污水中含氨有機物的分解是水中亞硝酸鹽的主要來源,木材制漿、清潔劑、化肥等工業廢水和農田排水也會將亞硝酸鹽帶入水系[3]。目前,世界上越來越多的國家充分認識到監測與分析水中亞硝酸鹽的重要性,很多國家都立法規定水中亞硝酸鹽的濃度限值。因此,相關技術人員研發簡單、快速、靈敏度高、綠色環保的亞硝酸鹽分析方法就顯得越來越重要。
通過查閱文獻發現,亞硝酸鹽測定方法有很多種[4-8],但這些方法都有靈敏度不高,所用試劑具有毒害性、容易造成二次污染等缺點。目前廣泛使用的方法是分光光度法,我國國家標準使用的是《N-(1-萘基)-乙二胺光度法》(GB/T 7493-87)。而該方法的顯色劑具有致癌性,所以可以在酸性條件下,先使雙氧水和偏釩酸銨生成有色產物,再利用亞硝酸鹽使其生成的有色產物褪色,并結合流動注射分析技術建立一種簡單、快速、綠色、選擇性好的亞硝酸鹽分析方法。
1 實驗部分
1.1 主要儀器
HYY3-1營養鹽自動分析儀;信號處理及計算機系統;多通道電子蠕動泵;UV-2800紫外可見分光光度計;AT2000電子天平。
1.2 試劑
實驗所用試劑主要包括;亞硝酸鹽氮儲備液(1 000 mg/L):稱取0.492 9 g的NaNO2,用去離子水溶解后移入100 mL容量瓶中并用去離子水定容至刻度;0.1 mol/L的偏釩酸銨;0.025%(體積分數)雙氧水;6 mol/L硫酸。R:分別移取16.7 mL和6 mol/L的硫酸,20 mL的0.1 mol/L偏釩酸銨,24 mL的0.025%(體積分數)雙氧水于100 mL容量瓶中,用去離子水定容至刻度。去離子水為推動液(C)。以上試劑均為分析純,實驗用水為去離子水。
1.3 實驗方法
流動注射分析流路圖見圖1。開啟營養鹽自動分析儀、多通道電子蠕動泵和計算機,載流C與顯色液R在蠕動泵的推動下混合,混合液經檢測器D,可以在顯示器上觀察到一條基線,當基線平穩后,轉換儀器為分析狀態,進樣環中的樣品和顯色液R混合,雙氧水與偏釩酸銨形成的有色產物在反應圈中被亞硝酸鹽褪色。在一定波長處,產物的吸光度與計算機采集的峰高相對應,根據峰高可定量分析亞硝酸的含量。
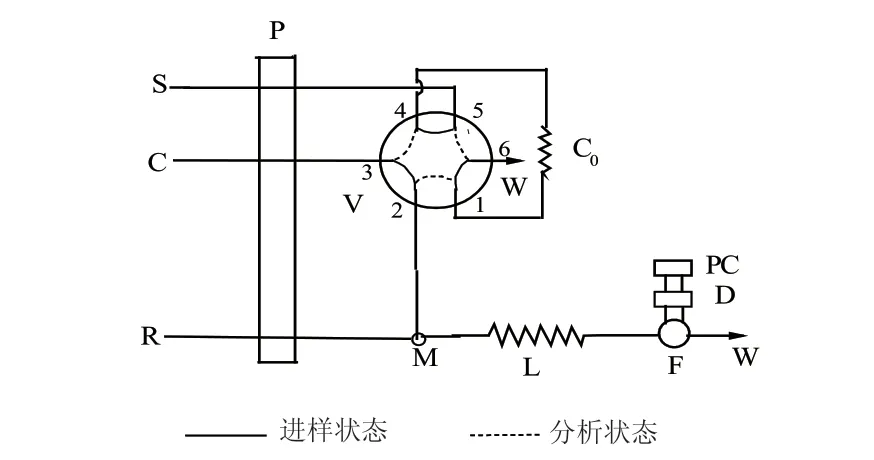
圖1 流動注射流路圖
2 結果與討論
2.1 最佳波長的確定
在酸性環境中,雙氧水與偏釩酸銨反應生成有色產物,亞硝酸鹽能使有色產物褪色,褪色的程度與亞硝酸鹽的含量具有相關性。在兩支10 mL的比色管中分別加入0.0 μg和5 μg的NO2
--N標準溶液,然后加入4 mL的R1和4 mL的R2,用去離子水定容至10 mL,反應10 min后用UV-2800紫外-可見分光光度計上在波長400 nm~800 nm可見光波長內,以去離子水為參比掃描試劑空白,以試劑空白為參比掃描反應產物。掃描結果表明,試劑空白在波長450 nm左右處有最大吸收,反應產物在波長470 nm左右處有最大吸收,因此選擇470 nm處測定波長,波長掃描圖如圖2所示。
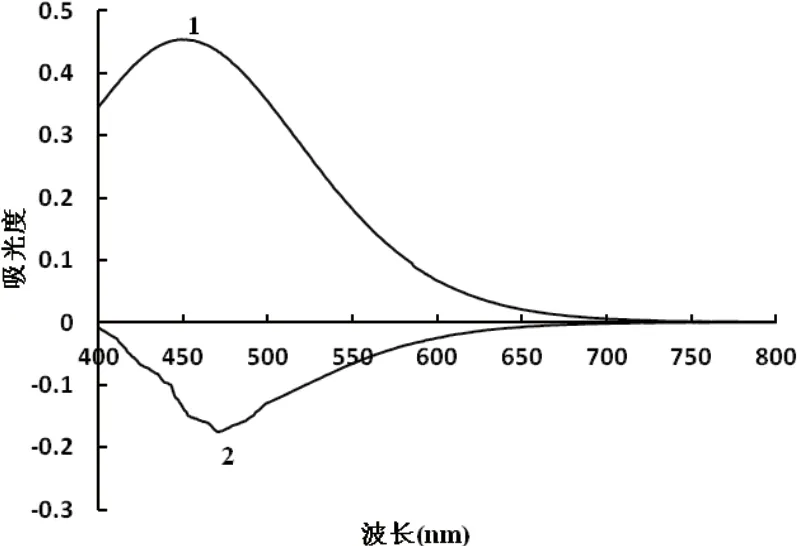
圖2 波長掃描圖
2.2 顯色體系的優化
2.2.1 硫酸濃度的影響
顯色體系的酸度對峰高的測定具有一定影響。本實驗研究了硫酸濃度在0.125~1.25 mol/L時不同酸度對應的峰高。結果發現,在硫酸濃度為0.125~1.0 mol/L范圍內,峰高隨著酸濃度的增加而升高,此后增加酸濃度反而使得峰高降低,因此,選擇硫酸濃度為1.0 mol/L 。
2.2.2 H2O2濃度的影響
考查了H2O2濃度在0.003%~0.007%范圍內對峰高的影響。結果表明,當H2O2濃度在0.003%~0.006%時,隨著H2O2濃度的增加峰高升高,此后增加H2O2濃度反而使得峰高降低,因此,選擇H2O2濃度為0.006%。
2.2.3 偏釩酸銨的影響
考查了偏釩酸銨濃度在0.012~0.044 mol/L范圍內對峰高的影響。結果顯示,當偏釩酸銨濃度在0.012~0.020 mol/L時,峰高隨偏釩酸銨濃度的增加而增高,當偏釩酸銨濃度高于0.020 mol/L時,峰高隨著偏釩酸銨濃度的增加逐漸降低。因此,選擇偏釩酸銨的濃度為0.020 mol/L。
2.3 流路體系的優化
2.3.1 泵管的優化
對于一定的流動注射體系來說,各個流路的流速不同對體系的靈敏度和單個樣品的分析時間有著不同程度的影響,所以可以通過改變各個流路的泵管直徑來控制各種液體的流動速度。實驗結果顯示,當推動液C流速為0.75 mL/min、顯色液R流速為0.30 mL/min和試樣S流速為0.55 mL/min時,流動注射體系測定的靈敏度最高。
2.3.2 反應管長度的影響
反應管長度影響反應時間從而影響測定峰高。本實驗測定了反應管長度在0.5~5.0 m時所對應的峰高。結果表明,反應管在0.5~4 m時,峰高隨著反應管長度的增加而升高,當反應管長度大于4 m后,峰高隨著反應管長度的增加而降低,因此反應盤管長度應選擇4.0 m。
2.3.3 進樣環體積的影響
進樣環體積影響每次樣品的進樣量從而影響測定峰高。本實驗測定了進樣環的體積為200~500 μL范圍所對應的峰高。實驗結果顯示,在進樣環體積為200~400 μL范圍內,峰高隨著進樣環體積的增加而升高,當體積大于400 μL后,峰高反而隨著體積的增加而略微降低,因此進樣環體積應選擇400 μL。
2.4 共存離子的影響
在確定了最佳實驗條件后,用1 mg/L的NO2-標準溶液代替水樣,加入以下水樣中常見的離子進行干擾實驗。結果表明,下列倍數的離子對實驗結果的測定相對誤差范圍在正負5%以內:Zn2+,Al3+,Cd2+,Ca2+,K+,Na+,Cl-,NH4+,F-(1 000);As5+,Cu2+,NO3-,SO42-,Mg2+,Mn2+,Ni2+(500倍);Cr3+,S2-,Pb2+,Fe3+(100)。由此可以看出,本方法對常見離子具有抗干擾能力,能用于多種水樣中亞硝酸鹽含量的測定。
2.5 工作曲線、精密度及檢出限
配置一系列亞硝酸鹽標準溶液,在最佳實驗條件下測定不同濃度亞硝酸鹽標準溶液所對應的峰高,以濃度為橫坐標,峰高為縱坐標繪制其工作曲線。亞硝酸鹽濃度在50~2 500 μg/L范圍內線性關系良好,其工作曲線回歸方程為:H=0.056C+0.693 (R2=0.999,H:峰高,mV;C:NO2-濃度,μg/L)。對濃度為1 000 μg/L的亞硝酸鹽標準溶液重復測定13次,計算其標準偏差和方法的檢出限,結果顯示該方法的相對標準偏差為0.64%,檢出限為4.5 μg/L。
2.6 樣品分析
按照上述最佳實驗條件,用本實驗建立的方法和國標法測定了河水、湖水和工業廢水中亞硝酸鹽的含量,同時進行了加標回收實驗,實驗結果見表1。
由表1可以看出,本方法與國標法測定不同水樣中亞硝酸鹽含量的結果接近,本方法加標回收率為97.9%~101.1%之間。因此本法的適用范圍較廣,可用于不同水樣中亞硝酸鹽的測定。
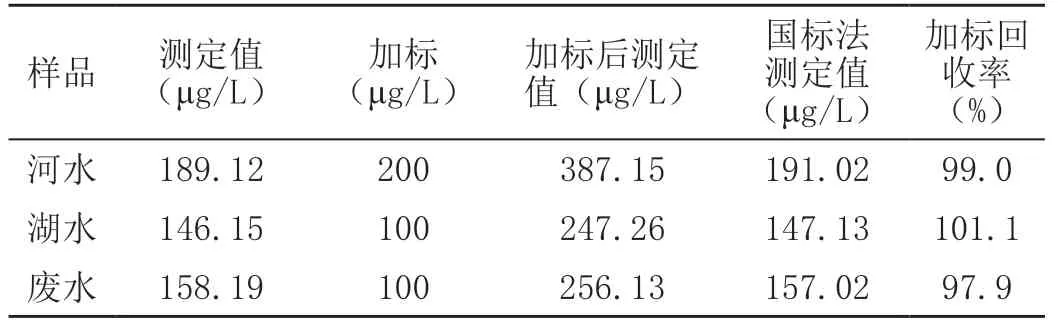
表1 不同水樣亞硝酸測定結果(n=3)
3 結論
本實驗所建立的流動注射褪色光度法測定亞硝酸鹽的新方法,簡單、快速,與其他一些測定亞硝酸鹽的方法相比[9-10],本方法不需要復雜的前處理過程,不需要嚴格的pH值和溫度控制;需要的試劑量少,且試劑無毒廉價;所用的HYY3-1營養鹽自動分析儀價格便宜、體積小、易攜帶,因而該方法可用于現場快速測定及在線自動分析。

