5種阿片受體激動劑不良反應信號的數據挖掘與分析
孫璇,張科,李正翔
疼痛是由組織損傷或潛在組織損傷引起的不愉快感覺及情感體驗,也是機體對有害刺激的一種保護性防御反應[1]。疼痛是一種令人不快的感覺和情緒上的感受,伴有實質上的或潛在的組織損傷,它是一種主觀感受[2-3]。不同個體對疼痛感受程度是不同的,同一個體在不同時期,對疼痛的反應也不盡相同。疼痛是許多疾病常見的,主要的癥狀,可引起機體發生,一系列病理生理變化和嚴重后果。痛覺是人類最原始、最普遍、最早體驗到的主觀感受,同時也是相當復雜的感覺,可發生于全身各部位、各系統器官和組織,長期的疼痛會導致抑郁癥等更為嚴重的精神疾病[4]。
阿片類受體激動劑指的是具有嗎啡效應的一類藥物。阿片類藥物主要是罌粟中提取的生物堿及體內外的衍生物,可與中樞特異性受體相互作用,從而緩解疼痛。阿片類藥物通過與阿片受體結合發揮藥理活性,阿片受體體內至少存在8種亞型。在中樞神經系統內至少存在4種亞型:μ、κ、δ、σ,每一種受體都有不同亞型。鎮痛藥能作用于阿片受體,然后作用于內源性鎮痛物質。有研究將μ-阿片受體與3種μ-阿片受體激動劑進行對接研究[5-6]。阿片類作用于受體后,引起膜電位超極化,使神經遞質釋放減少,從而阻斷神經沖動的傳遞而產生鎮痛等各種效應。在臨床上比較常見的如阿片、嗎啡、可待因等等,當然也有一些人工合成的物質,例如說哌替啶、芬太尼、美沙酮等阿片類物質,是臨床常用的鎮痛藥物,主要用來治療嚴重急性疼痛和癌痛[7]。但其非鎮痛效應,特別是影響中樞神經系統、心血管系統、消化系統便秘、易產生耐受性、成癮性等不良反應是困擾臨床用藥安全的重要因素[8],而長期應用可能出現的便秘降低了慢性疼痛病人的生活質量[9],在臨床應用中需要加強對阿片受體激動劑的不良反應監護。
美國FDA不良反應報告系統(FDA adverse event reporting system, FAERS)是一個免費公開的用于收集藥品上市后藥物不良事件信息的自發呈報數據庫,常用于開展藥品不良反應(adverse drug reaction, ADR)信號挖掘研究[10]。2022年1月本研究采用常用的信號挖掘方法報告比值比法(ROR)對阿片受體激動劑治療疼痛的相關ADR信號進行數據挖掘和分析,為臨床安全用藥提供參考借鑒[11]。
1 資料與方法
1.1 數據來源根據國內外文獻指南搜索阿片受體激動劑的類型,并鎖定5種阿片受體激動劑[11]:“morphine”(嗎啡)、“codeine”(可待因)、“pethidine”(哌替啶)、“fentanyl”(芬太尼)、“methadone”(美沙酮)。本研究數據來源于美國FAERS數據庫,該平臺允許研究人員對數據庫內的文本進行檢索、查詢和調用,可即時向公眾提供大量源于FDA數據庫的健康信息[12-13]。然后通過該平臺檢索2004年第1季度至2021年第4季度FAERS數據庫接收的嗎啡、可待因、哌替啶、芬太尼和美沙酮的ADR報告。
1.2 數據處理本研究以“嗎啡”“可待因”“哌替啶”“芬太尼”“美沙酮”為目標藥物,檢索藥物名稱包 括“morphine”“codeine”“pethidine”“fentanyl”“methadone”,依次限定目標藥物的通用名為“Methicillin”“Codeine phosphate tablet”“Pethidine hydrochloride injection”“Duragesic”“Methadone hydrochloride tablets”并進行復合檢索,得到目標藥物為懷疑及伴隨藥物的ADR報告。收集納入ADR報告中對應病人的基本信息和安全警告信號等。用SPSS 17.0軟件進行χ2檢驗,計算出P≤0.01為該ADR信號有統計學意義。
1.3 信號檢測方法目前常用的ADR信號檢測方法主要為比例失衡法,包括ROR法、比例報告比法(proportional reporting ratio, PRR)、貝葉斯置信度遞進神經網絡法(bayesian confidence propagation neural network, BCPNN)、和多項伽瑪泊松分布縮減法(multi-item gamma poisson shrinker, MGPS)等。現國際范圍內并未建立信號檢測的“金標準”。已有研究報道,PRR法和ROR法發現的信號相對較多,BCPNN和MGPS法發現的信號較少。Rothman等通過假設數據對PRR與ROR進行比較,發現ROR的檢測結果能夠進一步減少偏倚,且能夠估計相對危險度,而PRR的檢測結果會出現較大偏倚,且不能估計相對危險度。ROR是率比或危險比的一致性估計,而PRR不是,因而ROR是一種更有效、更合適的方法。因此本研究采取ROR法對嗎啡、可待因、哌替啶、芬太尼、美沙酮等5種阿片受體激動劑的ADR信號進行挖掘,其計算方法基于四表格[14-15],ROR值越大,說明該藥物造成該不良事件的風險越高,見表1。
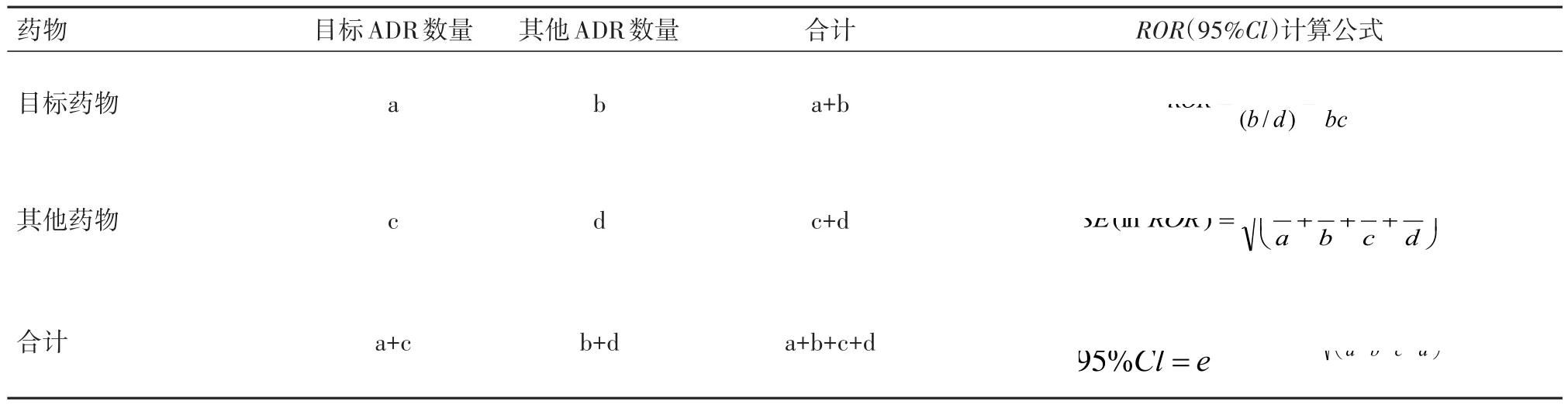
表1 比例失衡四格表和計算公式
2 結果
2.1 ADR報告的基本情況2016年第1季度至2021年第3季度阿片受體激動劑為伴隨和懷疑藥物的ADR報告有444 236份,其中嗎啡、可待因、哌替啶、芬太尼、美沙酮的ADR報告分別有165 572、79 574、9 838、145 819、43 433份。排除79 769份報告未注明病人性別外,其余報告病人為女性的有207 657份(占 46.74%)多于男性 156 810份(占35.30%)。ADR報告病人的年齡分布(年齡未知者除外),主要集中于18~60歲人群有142 955份(占32.18%)。阿片受體激動劑嗎啡、可待因、哌替啶、芬太尼、美沙酮ADR報告地所屬國家分布(未知者除外),美國占比高于其他國家為282 820份(占63.66%)。444 236份ADR報告中,嚴重的ADR報告有298 134份(占67.11%),以“死亡和住院或住院時間延長為主”,見表2。
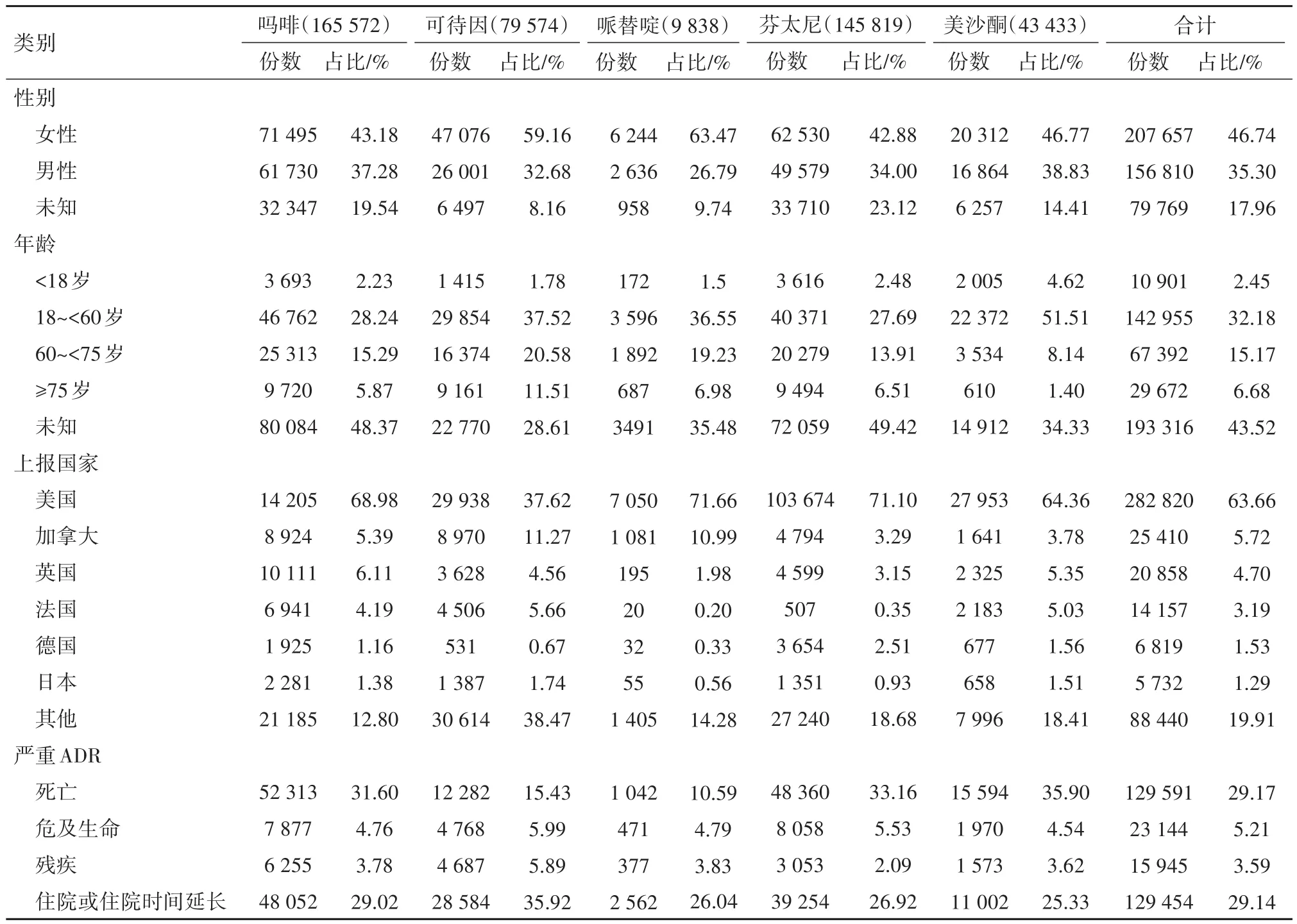
表2 阿片受體激動劑ADR報告的基本情況
2.2 5種阿片受體激動劑的ADR比較5種藥物均發生免疫系統疾病藥物過敏、各類神經系統疾病藥物依賴等以及胃腸、呼吸、心血管系統疾病、戒斷綜合征等全身性疾病等累及器官系統分類相關ADR,其中藥物過敏、藥物依賴、戒斷綜合征最為常見,均在說明書中有提及,其次是各類神經系統疾病和胃腸道系統疾病大部分在說明書中載明。由于芬太尼劑型的不同其有一些特殊的ADR見表3。

表3 阿片類藥物相關ADR上報數前20位
2.3 安全信號檢測結果分析根據累及器官分類結果顯示:神經系統相關ADR中,5種藥品均有高信號強度,嗎啡和美沙酮最強,其中嗎啡、哌替啶和美沙酮在學習障礙、發育遲緩中信號突出,可待因與芬太尼相對信號強度較低,5種藥物中嗎啡的藥物依賴性信號強度最為顯[ROR=47.57,95%CI:(46.73,48.42)];心血管系統相關ADR中,美沙酮的信號強度最為顯著,哌替啶的信號最弱;胃腸道系統相關ADR中,嗎啡在便秘、嘔吐、方面顯示陽性信號,而美沙酮未出現任何類似信號,其他藥物未出現便秘陽性信號;呼吸系統相關ADR中,嗎啡的信號最強,其中嗎啡、芬太尼、美沙酮在呼吸抑制顯示高陽性信號,嗎啡、哌替啶在急性胸部綜合征顯示高陽性信號,哌替啶未出現肺水腫陽性信號,嗎啡和美沙酮未出現上呼吸道感染陽性信號;眼部系統中,美沙酮的信號強度最顯著,其中哌替啶未出現瞳孔縮小陽性信號,其余藥物在瞳孔縮小方面的信號強度相當,哌替啶和美沙酮在新生兒視力異常方面的信號強度特別高分別為[ROR=105.69,95%CI:(69.92,159.76);ROR=239.53,95%CI:(196.63,291.80)];免疫系統中,哌替啶在藥物過敏和造影劑過敏中陽性信號最顯著,芬太尼和美沙酮未顯示此類信號,可待因未顯示感覺過敏信號;腎臟系統中,美沙酮信號最強,其中嗎啡和可待因在尿潴留顯示陽性信號,其他藥物均未顯示該信號,可待因與哌替啶在繼發性腎上腺皮質功能不全信號中未出現;全身及用藥部位癥狀中,5種藥品均有高信號強度,總體美沙酮的信號最強,其中嗎啡和美沙酮在新生兒藥物戒斷綜合征和殘疾中信號突出,在毒品轉移中信號略低,芬太尼在毒品轉移信號最顯著,美沙酮在多藥過量中信號最強[ROR=37.50,95%CI:(33.39,42.12)],具體各器官系統高危信號分布見表4。
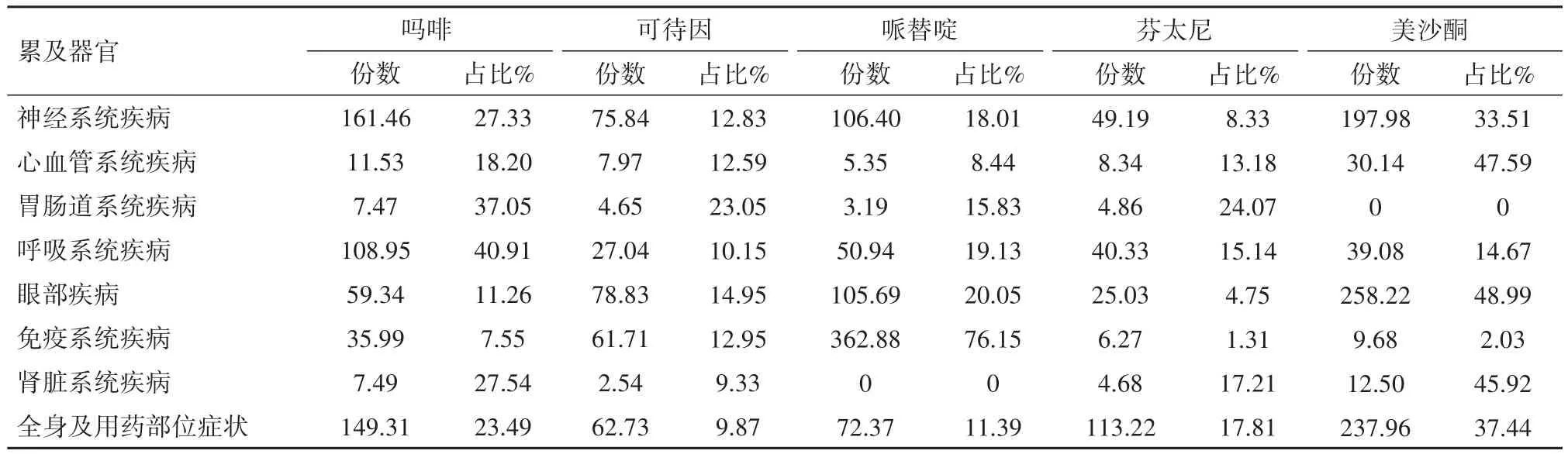
表4 阿片類藥物ADR信號累及器官分布
3 討論
此項研究采用比例失衡法中的ROR法進行信號挖掘分析,基于FAERS數據庫中5種阿片類藥物的ADR,獲得的常見ADR信號及ADR累及系統與藥品說明書大部分具有一致性,證實本研究結果真實可信。5種藥物出現ADR的主要累及系統有一定的差異性,嗎啡幾乎所有系統疾病都涉及其主要集中于神經系統、呼吸系統、胃腸道系統、眼部系統和全身及用藥部位癥狀;可待因類似嗎啡主要集中于神經系統、胃腸道系統、免疫系統和全身及用藥部位癥狀;哌替啶主要集中于神經系統、免疫系統和全身及用藥部位癥狀;芬太尼主要集中于神經系統和全身及用藥部位癥狀;美沙酮主要集中于神經系統、心血管系統、眼部系統和全身及用藥部位癥狀,其中嗎啡和美沙酮在多個累及系統中顯示高信號強度,因此在臨床使用該兩種藥物時要特別注意其相關累及系統的不良反應。嗎啡在Q-T間期延長和胃腸動力障礙、可待因在胃腸動力障礙、哌替啶在精神障礙和Q-T間期延長、芬太尼在Q-T間期延長和上呼吸道感染、美沙酮在急性胸部綜合征等累及器官下信號統計發現,表明此信號無統計學意義(P>0.01),其余信號均差異有統計學意義。ADR報告前20位且至少3藥共同的ADR信號中,嗎啡與藥物過敏、過量、藥物依賴關聯性強;可待因與藥物過敏、對各種藥劑的毒性、藥物依賴關聯性強;哌替啶與藥物過敏、藥物依賴、懷孕期間胎兒暴露關聯性強;芬太尼與過量、藥物依賴、疼痛關聯性強;美沙酮與藥物依賴、對各種藥劑的毒性、懷孕期間胎兒暴露關聯性強。本研究還檢測到了5種阿片類藥物報告前20位中學習障礙、發育遲緩、吸毒和死亡等ADR均為說明書尚未記載的,特別是學習障礙和發育遲緩提示臨床青少年使用此類藥物應警惕此類不良反應的發生,在臨床使用阿片類藥物時一定要小心、謹慎,其不僅是麻醉止疼藥同時也是毒品如若使用不當造成中毒嚴重會出現死亡。以上發現均提示在臨床使用阿片類藥物時應注意個體化給藥,監測病人用藥安全性為臨床的安全用藥提供一定的參考。
利用美國FAERS數據庫收集的超過千萬份ADR報告,數據信息量極大,可有效用于支持藥品上市后安全性風險監測及評價[16-17]。此外本研究還具有一定的局限性,由于FAERS數據庫源于自發呈報,來源比較復雜,數據庫信息量大,數據信息可能缺失較多[18-19];ROR法雖然能減少由于對照組選擇所帶來的偏倚,所得結果一致性較好,但使用ROR法本身會帶來一些不可避免的假陽性信號,部分信號還可能被遺漏,所以明確的因果關系還需進一步臨床研究證實。

