前列癃閉通片聯合諾氟沙星治療慢性前列腺炎的效果
王明珠
(商丘市中心醫院 藥劑科,河南 商丘 476000)
慢性前列腺炎(chronic prostatitis,CP)在成年男性中發病率約為10%,近年來逐漸有向年輕化發展的趨勢;CP患者主要臨床表現為疼痛、排尿異常、性功能異常等,還可誘發精神心理癥狀,嚴重影響患者生活質量[1]。目前,西醫對于CP的發病機制尚無明確闡述,故臨床對于該病無明確的診療方案,用藥單一,難以獲得令人滿意的效果。近年來,中醫中藥治療CP取得了諸多進展,口服湯藥、中藥熏洗、中藥保留灌腸等治療方式獲得了一定的治療效果,顯示出了中醫治療CP的優越性[2]。前列癃閉通片是中醫治療CP的常用藥物之一,具有益氣溫陽、活血利水之效,可治療尿頻、排尿延緩、腰膝酸軟等癥。故推測前列癃閉通片聯合諾氟沙星或可在CP的治療中獲益。基于此,本研究旨在探究前列癃閉通片聯合諾氟沙星治療CP的效果及安全性。
1 對象與方法
1.1 研究對象本研究為前瞻性隨機對照研究,病例來源于2020年10月至2021年10月在商丘市中心醫院就診的225例CP患者;按隨機數字表法將患者分為研究組(112例)與對照組(113例)。
1.2 診斷標準西醫:符合第9版《外科學》[3]中CP的診斷標準。(1)尿路感染反復發作;(2)有致病菌存在于前列腺按摩液中;(3)前列腺呈飽滿、增大、質軟、輕度壓痛,若患者病程長,則前列腺縮小、變硬;(4)每高倍視野前列腺液白細胞>10個,卵磷脂小體減少;(5)前列腺組織結構界限不清、混亂;符合上述全部標準即可診斷為CP。中醫:符合腎虛血瘀型CP的診斷標準[4]。主癥:尿頻尿急,腰膝酸軟,會陰部隱痛夜間加重。次癥:遺精,健忘,肌膚甲錯,口唇紫暗。舌脈:舌質暗紅或有瘀點,苔白,脈細澀。
1.3 入選標準納入標準:(1)符合上文診斷標準;(2)年齡20~45歲;(3)認知功能良好,可配合本研究方案的實施;(4)自愿入組,患者知情本研究且簽署知情同意書;(5)美國國立衛生研究院(National Institutes of Health,NIH)分型為Ⅲ型。排除標準:(1)合并尿路結石、尿路梗阻、前列腺增生等疾病;(2)存在藥物治療禁忌證;(3)凝血異常;(4)合并肝、腎功能異常;(5)合并自身免疫性疾病;(6)正在接受其他方案治療;(7)依從性差,無法堅持治療;(8)治療期間發生嚴重不良反應;(9)患者正在服用其他藥物,影響療效評估。
1.4 治療方法兩組患者治療期間均忌酒及辛辣刺激飲食,避免憋尿、久坐、熬夜,適當進行運動鍛煉。
1.4.1對照組 接受諾氟沙星片(吉林恒金藥業股份有限公司,國藥準字H20046234,規格:每片0.1 g)治療,每次口服諾氟沙星片2片,每日2次;同時給予患者前列腺按摩,每周1次,晚間指導患者進行熱水坐浴,每次坐浴15 min,每周2~3次;連續治療4周。
1.4.2研究組 在對照組基礎上接受前列癃閉通片(江蘇萬高藥業股份有限公司,國藥準字Z20090194,每片0.45 g)治療,每次口服4片,每日3次;連續治療4周。
1.5 評價指標
1.5.1臨床癥狀 觀察兩組患者治療前后中醫證候評分和慢性前列腺炎癥狀指數量表(NIH chronic prostatitis symptom index,NIH-CPSI)[5]評分;中醫證候參照《慢性前列腺炎中西醫結合診療指南(試行版)》[6]中中醫辨證評分表進行評分,主要觀察內容包括尿頻、尿急、腰膝酸軟而痛、會陰部隱痛、遺精、失眠健忘,將上述癥狀按照無、輕、中、重分別記為0、2、4、6分,舌脈不記分,總分為0~36分,評分越低則癥狀越輕;NIH-CPSI由9個問題組成,包含疼痛、排尿癥狀、生活質量3個方面,總分為0~43分,總分得分越低則癥狀越輕。
1.5.2炎癥因子、血液流變學 分別于治療前、治療4周時抽取兩組患者清晨7:00―8:00空腹外周肘靜脈血10 mL,裝于2支試管中,取其中1支試管,離心(3 000 r·min-1,離心半徑10 cm)10 min,取血清,采用酶聯免疫吸附法檢測腫瘤壞死因子-α(tumor necrosis factor-α,TNF-α)、超敏C反應蛋白(hypersensitive C-reactive protein,hs-CRP)、白細胞介素-8(interleukin-8,IL-8)水平,試劑盒購自重慶安納生生物工程有限公司;取另1支試管,加入肝素抗凝,應用血液流變學檢測全血高切黏度、全血低切黏度和全血還原黏度。
1.5.3安全性 比較兩組治療期間腹瀉、惡心、皮疹等不良反應發生率。

2 結果
2.1 分組情況及一般資料研究周期內,由于患者個人原因未能堅持完成整個研究、治療期間發生嚴重不良反應或服用其他藥物影響療效判斷的患者,均給予剔除,其中研究組剔除2例,對照組剔除3例,最終納入220例患者,研究組與對照組各110例。兩組在年齡、病程及體質量指數方面比較,差異無統計學意義(P>0.05),有可比性。見表1。
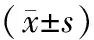
表1 兩組一般資料對比
2.2 臨床癥狀經過4周治療,相較于治療前,兩組中醫證候評分、NIH-CPSI評分均降低,且研究組更低(P<0.05)。見表2。
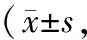
表2 兩組治療前后中醫證候評分、NIH-CPSI評分比較分)
2.3 炎癥因子經過4周治療,與治療前對比,兩組血清TNF-α、hs-CRP、IL-8水平均降低,且研究組更低(P<0.05)。見表3。
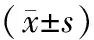
表3 兩組治療前后炎癥因子水平比較
2.4 血液流變學經過4周治療,與治療前相比,兩組全血高切黏度、全血中切黏度及全血還原黏度均降低,且研究組更低(P<0.05)。見表4。

表4 兩組治療前后血液流變學指標比較
2.5 不良反應對比兩組不良反應發生率,差異無統計學意義(P>0.05)。見表5。

表5 兩組不良反應發生率比較(n,%)
3 討論
目前,西醫主要應用抗生素、α受體阻滯劑等藥物改善CP患者尿頻、尿急等癥狀,但上述藥物不良反應較多,且長期治療容易產生耐藥性,療效欠佳。臨床實踐證明,中西醫結合治療CP有一定優勢,中醫辨證求因、對癥治療的特點能夠為CP的治療提供新的思路。CP的中醫辨證分型繁多,包括濕熱下注、濕熱瘀滯、腎虛血瘀等,其中以腎虛血瘀較為常見,約占43.60%。中醫理論認為,CP初期多因外感毒邪濕熱,蘊結于下焦,或飲食不潔,釀成濕熱,下注精室阻礙氣血運行所致;然濕熱日久纏綿難愈,則傷陰耗氣,傷及脾腎,脾腎氣虛則濕愈難化,血瘀更甚,形成腎虛血瘀的最終病理;正如《腎虛血瘀論》所云:“久病則虛,久病則瘀,虛可致瘀,瘀可致虛。虛則氣血運行不暢,瘀滯即生;瘀則機體生新不順,虛弱乃成”,故CP的治療應以滋陰補腎、活血化瘀為主[7]。
本研究采用國際公認的NIH-CPSI評分和中醫證候評分評價CP患者的臨床癥狀,發現前列癃閉通片聯合諾氟沙星片治療可改善CP患者臨床癥狀。分析其原因:前列癃閉通片中黃芪主入脾、肺經,可補中益氣,利水消腫;土鱉蟲、桃仁為活血藥,可活血,散瘀,定痛;冬葵果為利水消腫藥,具有清熱利尿、消腫之效;茯苓、桂枝可滋養經脈,助陽化氣,利水滲濕;淫羊藿可強筋補腎,治療陽痿、遺精、夜尿頻多、腰膝冷痛等腎虛癥狀;虎杖可清熱解毒,散瘀止痛;柴胡苦而微寒,有和解少陽、和解表里、疏肝升陽的作用;枳殼可破氣除痞,消積導滯,行氣化瘀;川牛膝具有逐瘀通經之效。諸藥合用,可達到活血化瘀、補腎壯陽的目的[8]。現代藥理研究指出,桂枝、茯苓可通過調控神經活性配體、受體相互作用信號通路,達到舒張血管、改善神經信號傳遞的目的,有利于改善CP患者會陰部疼痛、腰膝酸痛等癥狀[9]。川牛膝可抑制乙酰膽堿酯酶活性,提高腦內乙酰膽堿含量,從而對中樞膽堿能神經系統產生積極作用,減輕CP對患者精神系統的影響[10]。淫羊藿中的淫羊藿總黃酮可抑制由腎虛引起的體質量下降和血清睪酮水平降低,提高雄激素受體蛋白質、mRNA水平,緩解患者腰膝酸軟、遺精等腎虛癥狀[11]。而諾氟沙星作為臨床常用的抗菌藥物,可減少前列腺組織中炎癥因子分泌,加快患者臨床癥狀改善。因此,前列癃閉通片聯合諾氟沙星片治療的效果顯著,可改善CP患者臨床癥狀。
本研究還對比了兩組患者炎癥因子水平和血液流變學指標,發現前列癃閉通片聯合諾氟沙星片治療有助于減輕CP患者炎癥反應,改善血液流變學。分析其原因:前列癃閉通片中的川牛膝既能夠降低血液、血漿黏度,改善血液流變性,又可抑制白細胞介素-6、C反應蛋白等炎癥介質,減輕炎癥反應[12]。土鱉蟲可影響細胞膜外環境,使細胞膜表面受體獲得感知,從而激活相關分子活動,影響機體代謝過程,改善血液流變學[13]。桃仁可抑制血小板聚集,減少血栓形成,有利于提高血流速度,改善血液流變性[14]。柴胡中的柴胡皂苷可從抑制激酶磷酸化、阻止核因子異位2個方面抑制炎癥信號通路,降低炎癥因子水平[15]。前列癃閉通片聯合諾氟沙星片治療,再配合熱水坐浴,可進一步改善局部血液微循環,降低炎癥因子水平。此外,在安全性方面,前列癃閉通片聯合諾氟沙星片治療并未增加CP患者治療期間的不良反應發生率。
綜上所述,前列癃閉通片聯合諾氟沙星片治療CP效果顯著,可促進患者排尿異常、乏力等癥狀緩解,降低炎癥因子水平,改善血液流變學,值得推廣。

