二甲雙胍誘導鐵死亡抑制膠質瘤細胞增殖作用機制的研究
金鵬程 林 杰 朱鵬磊
膠質瘤是最常見的原發性顱內腫瘤,約占惡性腦腫瘤的81%,其5 年相對存活率不足5%[1]。最新研究發現,二甲雙胍可顯著改善膠質瘤患者的總體和無進展生存期,但其作用機制目前尚不明確[2-3]。鐵死亡是一種由鐵依賴性脂質過氧化決定的程序性細胞死亡形式,在膠質瘤中發揮抑癌作用[4]。其中膜脂過氧化物酶還原酶谷胱甘肽過氧化物酶(GPX4)利用谷胱甘肽消除磷脂過氧化物(ROS)抑制細胞鐵死亡[5]。5-、12-和15-羥二十碳四烯酸(HETE)是脂質過氧化產物,與鐵死亡中鐵蛋白的沉積有關,是鐵死亡水平的指標。鏈脂肪酸-CoA 連接酶(ACSL-4)是鐵死亡的關鍵調節因子,通過促進細胞鐵死亡在腫瘤中發揮抑癌作用[6]。本研究擬探討二甲雙胍通過誘導鐵死亡抑制膠質瘤細胞增殖的作用和可能機制。
1 實驗材料
1.1 細胞系 膠質瘤細胞系U251(TCHu 58)購自上海中科院細胞庫。U87(HTB-14)、T98G(CRL-1690)、HEB(HTX2018)均購自美國ATCC 細胞庫。
1.2 主要試劑與儀器 DMEM 培養液(Gibco,批號11320082)、胎牛血清(Gibco,批號10100147)和胰蛋白酶(Gibco,批號25200072),細胞計數試劑盒(CCK-8,Abcam,批號ab228554),丙二醛(MDA)試劑盒(Abcam,批號ab118970),ROS 試劑盒(Abcam,批號ab139476),乳酸脫氫酶(LDH)試劑盒(Abcam,批 號ab197000),5 -HETE 酶聯免疫吸附試驗(ELISA)試劑盒(FineTest,批號EU0185),12-HETE ELISA 試劑盒(FineTest,批號EU3131),15-HETE ELISA 試劑盒(FineTest,批號EU2612),流式細胞儀(BD,型號C111186),凝膠成像儀(Bio-Rad,型號VersaDoc 3000),GPX4(CST,批號59735)、ACSL-4(Abcam,批號ab155282)和甘油醛-3-磷酸脫氫酶(GAPDH)(CST,批號5174)。
2 實驗方法
2.1 細胞培養和分組 U87、U251 及T98G 膠質瘤細胞用含10%胎牛血清和青霉素-鏈霉素組合的DMEM 培養基在37 ℃和5% CO2的細胞恒溫培養箱中培養。實驗細胞按實驗設計分為對照組、二甲雙胍組或者對照組、二甲雙胍組和二甲雙胍+鐵死亡抑制劑(ferrostatin-1)處理組。
2.2 Western blot 檢測細胞蛋白表達 使用MPERTM哺乳動物蛋白提取試劑從U87 細胞中提取總蛋白,蛋白質濃度采用BCA 法測定。將等量的蛋白質提取物和2×SDS 上樣緩沖液混合并煮沸5 min。10% SDS-PAGE 分離蛋白質,然后轉移到聚偏二氟乙烯膜。將膜在室溫下用5%脫脂牛奶封閉2 h,然后與GPX4、ACSL-4 一抗在4 ℃下孵育過夜,清洗后將膜與辣根過氧化物酶綴合的二抗在室溫下孵育2 h。使用凝膠成像系統觀察并掃描蛋白質條帶。
2.3 ELSIA 檢測脂質過氧化產物水平 將PBS 清洗板2 次,每孔加入50 μL 標準品或樣品,然后向每孔中加入50 μL Biotin-labeled 抗體,輕輕敲擊板以確保充分混合,37 ℃下孵育45 min,吸出并洗滌板3次,每孔加入100 μL SABC 工作液,37 ℃孵育30 min,吸出并洗滌板5 次,加入90 μL TMB Substrate Solution,在37 ℃下孵育10~20 min,加入50 μL 終止液,讀取OD 值并計算樣品濃度。
2.4 MDA 試劑盒檢測MDA 水平 將硫代巴比妥酸液添加到樣品和標準品中,在95 ℃下孵育60 min,在冰浴中冷卻10 min,轉移到微孔板的孔中,用酶標儀分析MDA 水平。
2.5 流式檢測細胞活性氧(ROS)含量 流式細胞儀檢測細胞ROS 水平,收集處理的膠質瘤細胞,用ROS 深紅染料工作溶液染色,37 ℃下孵育細胞30~60 min。流式細胞儀監測熒光強度的變化,計算ROS含量。
2.6 CCK-8 檢測細胞活力 將U87 細胞以3000 個細胞/孔的密度接種在96 孔板上,細胞貼壁后,按照分組加入二甲雙胍或ferrostatin-1 處理48 h,每組6個復孔,更換含有CCK-8 工作液的培養基(CCK-8工作液與培養基配制比例為1∶10),每孔100 μL,37 ℃避光孵育1.5~2.0 h,用酶標儀檢測450 nm 處吸光度值。
2.7 細胞克隆形成實驗檢測細胞克隆形成能力 梯度倍數稀釋對數生長期的各組細胞懸液,取300 個細胞分別接種于10 cm 培養皿中,二甲雙胍或ferrostatin-1 處理,培養2 周。當培養皿中出現肉眼可見的克隆時終止培養。棄上清,4%多聚甲醛固定,吉薩姆染色液染色,并拍照記錄。
2.8 比色法檢測細胞LDH 水平 將U87 細胞以5000 個細胞/孔的密度接種在96 孔板上,并進行二甲雙胍或ferrostatin-1 處理,使用LDH 細胞毒性試劑盒測量LDH 水平。酶標儀測量490 nm 處的吸光度。
2.9 統計學方法 每個實驗重復3 次。應用SPSS 22.0 軟件(IBM Corp.)統計分析,所有數據符合HE分布以均數±標準差()表示,多組間比較采用單因素方差分析,兩兩比較采用LSD 檢驗。P<0.05 為差異有統計學意義。
3 結果
3.1 膠質瘤細胞鐵死亡減少 ELISA 結果顯示,與神經膠質細胞(HEB)比較,神經膠質瘤細胞U87、U251 和T98G 中的5-、12-和15-HETE 水平顯著降低(P<0.05,P<0.01,見表1);Western blot 顯示,與HEB 比較,U87、U251 和T98G 中的GPX4 表達 增高,ACSL-4 蛋白表達降低(見圖1)。
表1 HEB、U87、U251 和T98G 5-、12-和15-HETE 水平比較()

表1 HEB、U87、U251 和T98G 5-、12-和15-HETE 水平比較()
注:HEB 為人神經膠質細胞;HETE 為羥二十碳四烯酸;U87、U251、T98G 為膠質瘤細胞;與HEB 比較,aP<0.05,bP<0.01
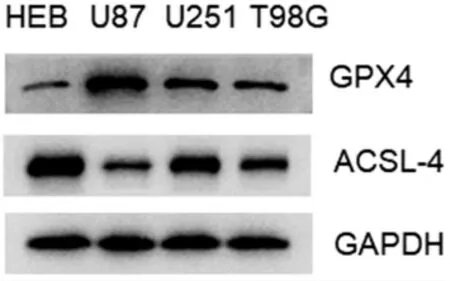
圖1 Western blot 檢測正常人神經膠質細胞HEB 和膠質瘤細胞GPX4 及ACSL-4 蛋白表達
3.2 二甲雙胍促進鐵死亡抑制膠質瘤細胞增殖 為了研究二甲雙胍對神經膠質瘤細胞的影響,以10mmol/L的二甲雙胍處理神經膠質瘤細胞系U87 0、12、24和48 h,結果表明,二甲雙胍處理U87 細胞,細胞活力呈時間梯度降低,LDH 釋放量呈時間梯度增加(P<0.05,P<0.01,見表2)。細胞克隆實驗結果表明,二甲雙胍抑制膠質瘤細胞的克隆增殖能力(見圖2A);EdU 實驗結果表明二甲雙胍抑制膠質瘤細胞增殖(見圖2B)。

圖2 二甲雙胍抑制膠質瘤細胞增殖
表2 二甲雙胍對膠質瘤細胞活力和LDH 釋放量的影響(%,)

表2 二甲雙胍對膠質瘤細胞活力和LDH 釋放量的影響(%,)
注:LDH 為乳酸脫氫酶;與0 h 比較,aP<0.05,bP<0.01
3.3 二甲雙胍通過下調GPX4 和上調ACSL-4 誘導人神經膠質瘤細胞鐵死亡 10 mmol/L 二甲雙胍處理48 h 后,U87 細胞的MDA 水平增加,細胞活力下降(見表3)。ROS 水平增加(見圖3A),GPX4 蛋白減少和ACSL-4 蛋白增多(見圖3B)。

圖3 二甲雙胍促進膠質瘤細胞鐵死亡
表3 二甲雙胍對U87 膠質瘤細胞MDA 水平和細胞活動的影響(%,)

表3 二甲雙胍對U87 膠質瘤細胞MDA 水平和細胞活動的影響(%,)
注:MDA 為丙二醛;與對照組比較,aP<0.01
3.4 鐵死亡抑制劑阻斷二甲雙胍對膠質瘤細胞的抗增殖作用 二甲雙胍處理膠質瘤U87 細胞后,細胞活力下降,MDA 水平升高(P<0.01);與二甲雙胍組比較,二甲雙胍聯合5 mmol/L 鐵死亡抑制劑ferrostatin-1 處理組U87 細胞活力升高,MDA 水平下降(P<0.05,P<0.01,見表4)。Western blot 結果表明,ferrostatin-1 抑制二甲雙胍誘導的GPX4 表達水平的降低和ACSL-4 表達水平的增加(見圖4A)。此外,ferrostatin-1 減弱二甲雙胍誘導的ROS 水平的增加(見圖4B)。與二甲雙胍處理的細胞比較,ferrostatin-1 增加二甲雙胍處理的人神經膠質瘤細胞的增殖活性,提高細胞活力和克隆形成能力(見圖4C-4D)。

圖4 鐵死亡抑制劑阻斷二甲雙胍對人神經膠質瘤細胞的抗癌作用
表4 鐵死亡抑制劑阻斷二甲雙胍對U87 細胞活動和MDA水平的影響(%,)

表4 鐵死亡抑制劑阻斷二甲雙胍對U87 細胞活動和MDA水平的影響(%,)
注:ferrostatin-1 為鐵死亡抑制劑;MDA 為丙二醛;與對照組比較,aP<0.01;與二甲雙胍組相比,bP<0.05,cP<0.01
4 討論
研究發現,二甲雙胍通過抑制細胞增殖、誘導細胞凋亡等機制在結直腸癌和乳腺癌等多種癌癥中發揮抗癌作用[7]。例如在乳腺癌中二甲雙胍通過下調細胞中的轉錄因子Sp1 使HMGA2 啟動子失活,抑制癌細胞的增殖[8]。一項Meta 分析發現,在108161 例2型糖尿病患者中二甲雙胍治療與顯著降低結直腸腫瘤風險相關[9]。膠質瘤是成人中樞神經系統發病率最高的惡性腫瘤,由于其異質性和侵襲性特征,神經膠質瘤很難完全治愈[10-11]。高血糖與膠質瘤生存率降低密切相關,是膠質瘤的不良預后因素,二甲雙胍治療可延長膠質瘤患者無進展生存期(HR=0.29,95%CI=0.11~0.78)[2,12-13]。本研究探討二甲雙胍對膠質瘤細胞增殖和鐵死亡的調控作用,結果表明二甲雙胍處理膠質瘤細胞,鐵死亡增多,細胞增殖被抑制。
鐵死亡是一種由鐵依賴性脂質過氧化決定的死亡模式,其特點為細胞中鐵依賴性脂質過氧化物(脂質ROS)的異常積累,破壞氧化還原平衡并最終導致細胞死亡,這些過程主要由細胞內GPX4 活性喪失引起[14-15]。GPX4 是一種GSH 依賴性酶,其合成增加可減少細胞內氧化應激和抑制鐵死亡,從而促進腫瘤生長[16]。ACSL-4 在脂肪酸代謝中起關鍵作用,ACSL-4 激活長鏈不飽和脂肪酸參與膜磷脂合成,引發細胞鐵死亡[17]。研究發現,二甲雙胍可增加細胞內Fe2+和脂質ROS 水平,誘導鐵死亡并抑制乳腺癌細胞的增殖[18]。機制研究發現,二甲雙胍通過上調miR-324-3p 抑制GPX4 表達誘導乳腺癌細胞鐵死亡,抑制癌細胞活力[19]。已有研究證實,二甲雙胍可抑制膠質瘤細胞增殖、遷移和侵襲,促進其凋亡,但其具體機制尚不明確[20]。本研究發現,二甲雙胍抑制膠質瘤細胞GPX4 蛋白表達,促進ACSL-4 蛋白表達,進而導致ROS 水平增加,觸發鐵死亡,抑制膠質瘤增殖。此外,本研究還發現抑制鐵死亡后,膠質瘤細胞活力升高,進一步證實二甲雙胍可能通過誘導鐵死亡來抑制膠質瘤細胞增殖。

