重組結核桿菌融合蛋白的臨床綜合評價 Δ
倪曉鳳 ,刁 莎 ,何思頤 ,焦雪峰 ,程 曉 ,陳 哲 ,劉 崢 ,曾力楠 ,康德英 ,吳 斌 ,萬朝敏 , ,應斌武 ,張 慧 ,趙榮生 ,繆麗燕 ,王 卓 ,李曉宇 0,劉茂柏 ,蔡本志 ,邱 峰 ,孫 峰 ,初乃惠 ,林明貴 ,沙巍 ,張伶俐 (.四川大學華西第二醫(yī)院藥學部/循證藥學中心/國家藥品監(jiān)督管理局藥物制劑體內(nèi)外相關性技術研究重點實驗室/出生缺陷與相關婦兒疾病教育部重點實驗室,成都 00;.四川大學華西醫(yī)院中國循證醫(yī)學中心,成都 00;.上海交通大學醫(yī)學院附屬仁濟醫(yī)院藥劑科,上海 00;.四川大學華西第二醫(yī)院兒科,成都 00;.四川大學華西醫(yī)院實驗醫(yī)學科,成都 00;.四川大學華西醫(yī)院感染管理部,成都 00;.北京大學第三醫(yī)院藥劑科,北京 00;.蘇州大學附屬第一醫(yī)院藥學部,蘇州00;.海軍軍醫(yī)大學長海醫(yī)院藥學部,上海 00;0.復旦大學附屬中山醫(yī)院藥劑科,上海 000;.福建醫(yī)科大學附屬協(xié)和醫(yī)院藥學部,福州 000;.哈爾濱醫(yī)科大學附屬第二醫(yī)院藥學部,哈爾濱00;.重慶醫(yī)科大學附屬第一醫(yī)院藥學部,重慶 000;.北京大學醫(yī)藥管理國際研究中心,北京00;.首都醫(yī)科大學附屬北京胸科醫(yī)院結核科,北京 0;.清華大學附屬北京清華長庚醫(yī)院感染科,北京 0;.同濟大學附屬上海市肺科醫(yī)院結核科,上海 00)
結核病是由結核分枝桿菌(Mycobacterium tuberculosis,MTB)感染引起的慢性傳染病,是嚴重危害人民健康的全球性公共衛(wèi)生問題。據(jù)WHO統(tǒng)計,2020年結核病已成為全球第13位死因,且在單一傳染病中位列第2位[1―2]。我國結核病負擔高居全球第2位,據(jù)2021年全球結核病報告統(tǒng)計,MTB感染人數(shù)約3.5億,新發(fā)結核病患者84.2萬,其中病死率為3.80%[2―4]。
人體感染MTB后是否發(fā)病,取決于MTB數(shù)量、毒性大小及人體免疫力。感染后約5%的感染者會在短時間內(nèi)發(fā)展為活動性結核病(active tuberculosis,ATB),而約95%的感染者體內(nèi)的MTB會進入長期潛伏狀態(tài),這又稱為潛伏性結核感染(latent tuberculosis infection,LTBI)[5]。LTBI人群龐大,已成為新發(fā)結核病的巨大源頭,因此有效識別LTBI對控制結核病具有重要意義。2015年,WHO提出將開展LTBI系統(tǒng)篩查和干預作為終止結核病的重要策略之一[6]。我國《高危人群結核分枝桿菌潛伏感染檢測及預防性治療專家共識》亦指出,加強LTBI者的主動發(fā)現(xiàn)、篩查結核病患者密切接觸者,是降低LTBI者發(fā)病率的重要措施[7]。
目前LTBI的診斷缺乏金標準,只能通過免疫學方法輔助診斷。結核菌素純蛋白衍生物(purified protein derivative of tuberculin,TB-PPD)是一種將結核菌素作為抗原來誘發(fā)機體發(fā)生遲發(fā)型變態(tài)反應的診斷藥品,具有成本低、檢測方法簡單、無需復雜的設備儀器及專門的實驗室等特點,是臨床判斷LTBI常用和傳統(tǒng)的皮膚檢測藥品。重組結核桿菌融合蛋白(recombinant Mycobacterium tuberculosis fusion protein,EC)為一種新型結核皮膚檢測藥品,由高效表達結核桿菌ESAT6-CFP10基因的大腸埃希菌,經(jīng)發(fā)酵、分離和純化后制成。EC的檢測是否較TB-PPD更具優(yōu)勢,目前尚缺乏其有效性、安全性、經(jīng)濟性、創(chuàng)新性、適宜性和可及性6個維度的研究。因此,本研究以TB-PPD為對照,對EC進行臨床綜合評價,旨在為遴選MTB感染診斷和結核病輔助診斷的皮膚檢測藥品提供證據(jù)。
1 資料與方法
1.1 專家組成員構成
專家組成員的學科專業(yè)需涵蓋臨床、藥學、護理學、診斷學及方法學,且在結核病診斷或治療領域具有臨床經(jīng)驗或研究背景;職稱為副高級及以上職稱并兼顧地域分布。
1.2 納入與排除標準
1.2.1 研究類型 本研究納入的文獻類型為臨床綜合評價相關的原始研究、指南、共識及規(guī)范等。
1.2.2 研究對象 本研究未限制納入人群的年齡、性別和種族等。
1.2.3 干預措施 在有效性、安全性和經(jīng)濟學評價中,限制干預組患者為EC,對照組患者為TB-PPD;在適宜性、可及性和創(chuàng)新性評價中,未限制干預組和對照組患者的干預措施。
1.2.4 排除標準 本研究的排除標準為:(1)無法獲取原文的文獻;(2)重復發(fā)表的文獻;(3)非中英文文獻。
1.3 文獻檢索策略
計算機檢索臨床指南數(shù)據(jù)庫(國際指南協(xié)會數(shù)據(jù)庫,英國衛(wèi)生與臨床優(yōu)化研究所數(shù)據(jù)庫,蘇格蘭、加拿大、澳大利亞、新西蘭和日本指南數(shù)據(jù)庫,中國醫(yī)脈通臨床指南庫)、Medline、the Cochrane Library、Embase、中國期刊全文數(shù)據(jù)庫、中國生物醫(yī)學文獻數(shù)據(jù)庫、萬方數(shù)據(jù)庫、維普網(wǎng)、衛(wèi)生行政部門和行業(yè)協(xié)會的官方網(wǎng)站[國家衛(wèi)生健康委(http://www.nhc.gov.cn/)、國家食品藥品監(jiān)督管理局(https://www.nmpa.gov.cn/)、中國防癆協(xié)會(http://www.cata1933.cn/)、全國團體標準信息平臺(http://www.ttbz.org.cn/StandardManage/Detail/36819/)]。中文檢索詞為“重組結核分枝桿菌融合蛋白”“重組結核桿菌融合蛋白”“宜卡”“CFP10/ESAT6”;英文檢索詞為“recombinant Mycobacterium tuberculosis fusion protein”“CFP10/ESAT6”。檢索時限均為建庫或建站起至2022年2月。
1.4 資料提取與納入文獻質量評價
由2位研究者獨立篩選文獻,提取資料并交叉核對,若有爭議,則通過討論或與第3位研究者協(xié)商解決。提取資料包括:基本信息、患者基本特征、干預措施、結局指標、偏倚風險評價等。采用SYRCLE動物實驗偏倚風險評估工具[8]評價動物實驗研究的質量;采用診斷準確性試驗質量評價工具(quality assessment of diagnostic accuracy studies,QUADAS-2)[9]評價診斷準確性研究的質量。
1.5 結局指標
1.5.1 有效性 采用系統(tǒng)評價法比較EC和TB-PPD的有效性。有效性結局指標包括:靈敏度、特異度、陽性似然比、陰性似然比。
1.5.2 安全性 安全性結局指標包括:上市前安全性為動物實驗的毒理學評價結果;上市后安全性為不良反應類型及發(fā)生率。
1.5.3 經(jīng)濟性 以MTB感染的高危人群為目標人群,基于全社會角度,使用TreeAge Pro 2011軟件,采用最小成本分析、成本-效果分析、成本-效用分析評價EC和TB-PPD的短期經(jīng)濟性;采用成本-效用分析評價長期經(jīng)濟性。藥品成本數(shù)據(jù)來自米內(nèi)網(wǎng)-中國醫(yī)藥信息數(shù)據(jù)庫(https://www.menet.com.cn/),指標參數(shù)來自有效性指標的系統(tǒng)評價結果和相關參考文獻。采用單因素敏感性分析及概率敏感性分析評估結果的穩(wěn)定性。
1.5.4 適宜性、可及性和創(chuàng)新性 采用系統(tǒng)評價法初擬評價指標,采用改良德爾菲專家咨詢法確定評價指標,根據(jù)指標內(nèi)容和性質,通過檢索文獻、查詢官網(wǎng)、查閱說明書、問卷調(diào)查等方法評價適宜性、可及性和創(chuàng)新性。
1.6 綜合評分
利用專家評分法和乘積法確定各維度及指標權重。專家組成員根據(jù)研究結果,對EC和TB-PPD在各指標下的優(yōu)劣進行評分,最終得到6個維度的綜合評分=各指標評分×各指標權重;分值越高,表示該診斷藥品在該維度越優(yōu)[10]。
1.7 分析方法
采用Meta-Disc 1.4軟件進行有效性的Meta分析;采用RevMan 5.3軟件進行安全性的Meta分析;不能進行Meta分析的數(shù)據(jù),采用描述性分析。
2 結果
2.1 有效性評價結果
共有 11 篇文獻報道了有效性[7,11―20],其中標準 2部[11―12]、指南 2 部[7,13]、專家共識 3 篇[14―16],均推薦 EC 和TB-PPD用于MTB感染檢測;1篇系統(tǒng)評價的結果顯示,我國EC的靈敏度為 86.06%[95%CI(82.39%,89.07%)][17];3篇隨機對照試驗(randomized controlled trial,RCT)經(jīng)Meta分析合并后的結果顯示,不區(qū)分人群時,EC和TB-PPD的靈敏度、陰性似然比比較,差異均無統(tǒng)計學意義(P>0.05);EC的特異度、陽性似然比、診斷比值比、陽性預測值、陰性預測值均顯著優(yōu)于TB-PPD(P<0.05)[18―20]。結果見表1(詳細結果見本團隊已發(fā)表的文獻[21])。

表1 不區(qū)分人群時EC和TB-PPD有效性的Meta分析結果
2.2 安全性評價結果
1 篇專家共識[14]、4 篇 RCT[18―20,22]報道了安全性。結果顯示,EC和TB-PPD最常見的不良反應為注射部位瘙癢和疼痛,程度多為輕度,且未有嚴重不良反應發(fā)生(詳細結果見本團隊已發(fā)表的文獻[21])。
2.3 經(jīng)濟性評價結果
2.3.1 短期經(jīng)濟性 最小成本分析結果顯示,針對靈敏度及其衍生效果指標(實際發(fā)現(xiàn)患者例數(shù)、避免新發(fā)患者例數(shù)、漏診率),EC組患者的成本(98元)顯著低于TBPPD組(136.78元),EC組更經(jīng)濟。成本-效果分析結果顯示,針對特異度及其衍生效果指標(誤診率),EC組患者的篩查總成本為980 000元、誤診率為5.88%,TB-PPD組患者的篩查總成本為1 367 800元、誤診率為59.27%;EC與TB-PPD相比,增量成本-效果比(incremental costeffectiveness ratio,ICER)為7 263.53元/%,即每減少1%誤診率,EC組患者可減少7 263.53元,EC屬于絕對優(yōu)勢方案。敏感性分析結果顯示,上述結果穩(wěn)定。成本-效用分析(1年)結果顯示,EC組患者的總成本為579.049 0元、質量調(diào)整壽命年(quality-adjusted life year,QALY)為0.991 5,TB-PPD組患者的總成本為1 539.267 0元、QALY為0.986 5。與TB-PPD組相比,EC組患者的成本更低、QALY更高,增量成本-效用比(incremental costutility ratio,ICUR)為-192 043.6元/QALY,即每增加1個QALY,EC組患者可減少192 043.6元,EC屬于絕對優(yōu)勢方案。敏感性分析結果顯示,上述結果穩(wěn)定(另文待發(fā)表)。
2.3.2 長期經(jīng)濟性 成本-效用分析(以我國人均預期壽命年,即77年[23])結果顯示,EC組患者的總成本為7 607.532 3元、QALY為9.464 5,TB-PPD組患者的總成本為15 430.520 5元、QALY為9.399 2;與TB-PPD組相比,EC組患者的成本更低、QALY更高,ICUR為-119 800.738 1元/QALY,即每增加1個QALY,EC組患者可減少119 800.738 1元,EC屬于絕對優(yōu)勢方案。敏感性分析結果顯示,上述結果穩(wěn)定(另文待發(fā)表)。
2.4 創(chuàng)新性、適宜性和可及性評價結果
共確定24項指標,其中創(chuàng)新性指標6項,包括臨床創(chuàng)新性3項和產(chǎn)業(yè)創(chuàng)新性3項;適宜性指標9項,包括技術適宜性4項和使用適宜性5項;可及性指標9項,包括價格指數(shù)1項、可負擔性3項和可獲得性5項。結果見表2。

表2 創(chuàng)新性、適宜性和可及性評價指標及評價方法
2.4.1 創(chuàng)新性 EC和TB-PPD均是我國結核病防治的重要手段。EC的抗原為MTB特異性抗原,不易發(fā)生交叉反應[24]。TB-PPD的抗原為與卡介苗和非MTB相同或相似的抗原,易發(fā)生交叉反應[25]。EC屬于國家1類新藥,并獲國內(nèi)發(fā)明專利授權(專利號:ZL201510617780.9);TB-PPD為我國改良研發(fā)而非自主研發(fā)產(chǎn)品[26]。
2.4.2 適宜性 EC和TB-PPD標簽標注均完整。EC有3種規(guī)格(最小0.3 mL),適用于6個月及以上嬰兒、兒童及65周歲以下成人;TB-PPD有2種規(guī)格(最小1.0 mL),適用于嬰兒、兒童及成人。EC藥品說明書詳細列舉了不良反應類型及發(fā)生率、藥物相互作用、臨床試驗、藥理毒理信息;TB-PPD藥品說明書中未詳細列舉上述信息。EC用西林瓶包裝,于2~8 ℃避光儲存;TB-PPD用安瓿包裝,于2~8 ℃避光儲存。同時使用EC和TB-PPD的6家醫(yī)院的調(diào)查問卷(共發(fā)放125份,共回收問卷125份,有效回收率為100%)結果顯示,與TB-PPD相比,EC結果判讀更容易、不良反應更易識別、處理難度更低、患者配合程度更高。
2.4.3 可及性 我國EC價格低于國際參考價格[27],而TB-PPD價格高于國際參考價格[28]。根據(jù)國家統(tǒng)計局發(fā)布的《2021年居民收入和消費支出情況》[29],EC藥品支出占城市和農(nóng)村家庭年人均可支配收入比例分別為0.21%、0.52%,TB-PPD分別為0.29%、0.72%。TB-PPD已納入《國家基本藥物目錄(2018年版)》和《國家醫(yī)療保險目錄(2018年版)》,EC未納入。
2.5 各維度評價指標的綜合評分結果
確定有效性、安全性、經(jīng)濟性、創(chuàng)新性、適宜性和可及性的權重分別為18.09%、17.97%、15.84%、15.37%、16.55%、16.19%。EC的靈敏度、特異度、陽性似然比、陰性似然比、診斷比值比、曲線下面積(area under the curve,AUC)、陽性預測值、陰性預測值、不良反應類型、不良反應發(fā)生率、短期經(jīng)濟性、長期經(jīng)濟性、臨床創(chuàng)新性、產(chǎn)業(yè)創(chuàng)新性、技術適宜性、使用適宜性、價格指數(shù)評分均高于TB-PPD;兩藥的可負擔性評分一致,EC的可獲得性評分低于TB-PPD。結果見表3。
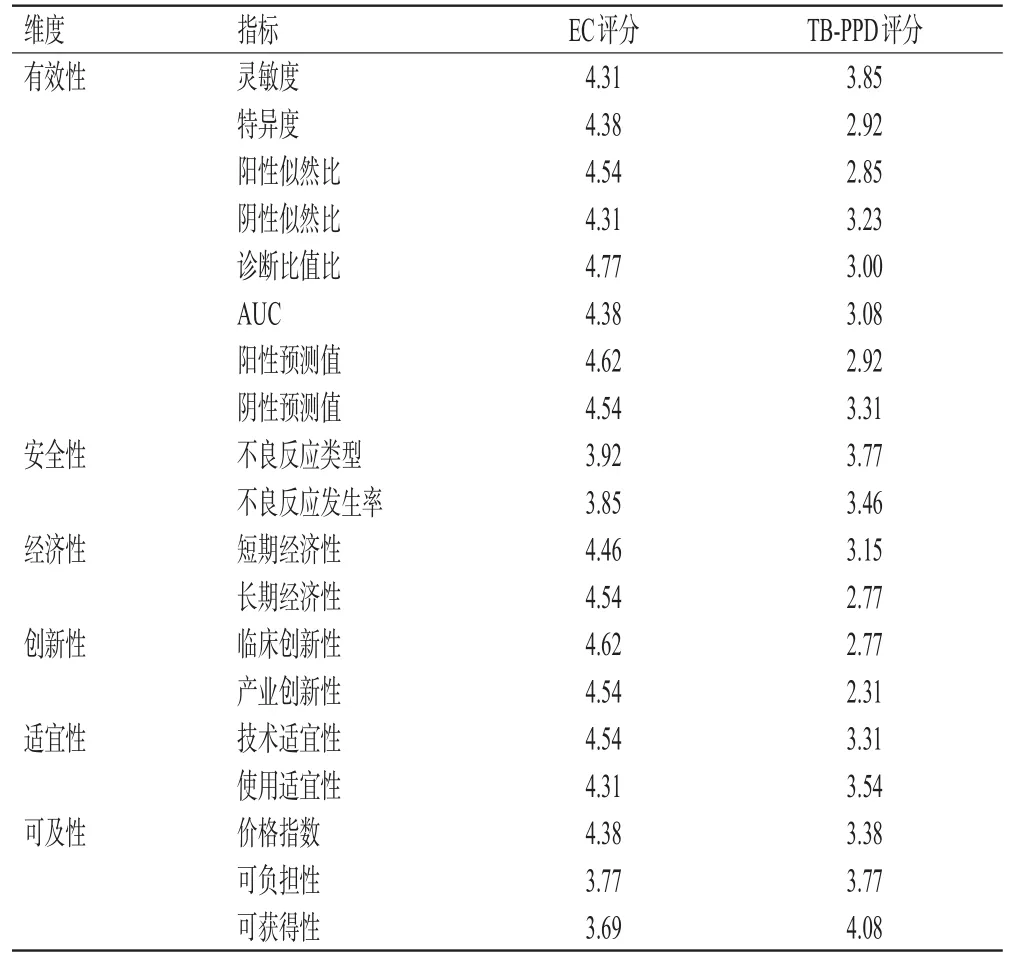
表3 EC和TB-PPD的各維度評價指標的評分結果
考慮權重后,EC的有效性(0.81 vs. 0.57)、安全性(0.70 vs. 0.57)、經(jīng)濟性(0.71 vs. 0.48)、創(chuàng)新性(0.70 vs.0.39)、適宜性(0.73 vs. 0.57)、可及性評分(0.64 vs. 0.61)及其綜合評分(4.29 vs. 3.27)均高于TB-PPD。結果見圖1。

圖1 EC和TB-PPD各維度的綜合評分結果
3 討論
在有效性方面,EC在特異度方面表現(xiàn)出一定優(yōu)勢,可有效減少因接種卡介苗或感染非MTB導致的假陽性概率。在安全性方面,EC與TB-PPD的安全性類似,均未見嚴重不良反應發(fā)生。在經(jīng)濟性方面,由于EC和TBPPD作為診斷藥品的特性,故分為短期經(jīng)濟性評價和長期經(jīng)濟性評價,短期經(jīng)濟性僅考慮診斷效果,以直接評價診斷效果的靈敏度、特異度等及1年成本-效用為結局指標;長期經(jīng)濟性考慮診斷藥品的本質是幫助患者及時接受治療,診斷效果不同會導致患者接受診療的時間和轉歸不同,因此通過長期經(jīng)濟性評價可獲得因診斷藥品效果不同引起的全生命周期治療轉歸差異。由于LTBI診斷暫無金標準,目前僅依賴于檢測試劑結果判斷機體是否感染MTB,這仍存在一定的誤差。因EC靈敏度與TB-PPD相似,但EC特異度優(yōu)于TB-PPD,故使用EC后被誤診的患者更少,因誤診導致的治療成本更低,QALY更高,同時因EC具有較低的假陽性率而顯示出了更低的成本與更高的健康收益,從而EC表現(xiàn)出更具經(jīng)濟性。在創(chuàng)新性、適宜性方面,由于EC屬于國家1類新藥并獲得專利證書,加之 EC的藥品說明書描述更全面、產(chǎn)品最小規(guī)格更接近單次人均用量,因此EC更具有創(chuàng)新性和適宜性。在可及性方面,EC的價格雖然更低,也在大多數(shù)基層醫(yī)療機構使用,但據(jù)全國醫(yī)藥經(jīng)濟信息網(wǎng)抽樣調(diào)查顯示,二級及以上醫(yī)療機構配備EC的僅1家,提示EC的可獲得性不足[30]。
綜上所述,EC作為國家1類新藥,可用于MTB感染診斷、輔助結核病臨床診斷,與TB-PPD均屬于皮膚檢驗藥品,具有無需抽血、無需儀器設備、操作便捷等特點;與TB-PPD相比,EC的有效性、安全性、經(jīng)濟性、創(chuàng)新性、適宜性和可及性均更優(yōu);但值得注意的是,EC應進一步改善可及性維度下的可獲得性。本研究的局限性為:僅基于現(xiàn)有證據(jù)評價EC相較于TB-PPD的有效性、安全性、經(jīng)濟性、創(chuàng)新性、適宜性和可及性,因研究數(shù)量有限,尚無法針對不同人群開展亞組分析,無法開展基于原始研究的經(jīng)濟學評價,也無法獲取TB-PPD的產(chǎn)能、生產(chǎn)和配送等數(shù)據(jù),故所得結果存在一定局限性,后續(xù)尚待高質量的原始研究進一步證實。

