全麻下機器人輔助STN-DBS治療高齡帕金森病的經驗分享
孫衛進 王澍 關宇光 趙萌 王雄飛 潘軍紅 唐重陽 馬皓偉 程子章 張小英 騰鵬飛 欒國明

【摘要】 目的 分析探討高齡(>80歲)帕金森病(PD)患者全麻下機器人輔助雙側丘腦底核腦深部刺激植入術(STN-DBS)的安全性及有效性。方法 納入2020年6月—2021年6月于首都醫科大學三博腦科醫院接受全麻下機器人輔助雙側STN-DBS治療的3例高齡PD患者,回顧性分析其臨床資料、手術過程并隨訪評估術后6、12個月的臨床癥狀(UPDRS-III開、關期評估運動癥狀、LEDD評估用藥情況、H-Y分期評估癥狀嚴重程度)、神經心理預后(HAMA評估焦慮情緒、HAMD評估抑郁情緒)、認知預后(WAIS評估智力認知)及生活質量(ADL評估生活質量)。結果 3例高齡PD患者STN-DBS手術順利,無嚴重術中或術后并發癥,術后靶點驗證植入誤差均在0.7 mm以內。術后6個月及12個月評估時,運動癥狀、癥狀嚴重程度、焦慮抑郁情緒、生活質量均較前有顯著改善,術后用藥量顯著減少,神經認知功能無顯著變化;6個月隨訪數據與12個月數據基本無顯著差異。結論 全麻下機器人輔助STN-DBS對高齡PD患者有較好的臨床療效,手術安全性基本可控,術后患者運動癥狀、藥物減量、神經心理、生活質量均有顯著改善且神經認知功能總體無影響。但應同時注意高齡患者一般狀況,根據患者個體狀況,對高齡PD患者選擇進行STN-DBS治療。
【關鍵詞】 帕金森病;高齡;腦深部電刺激術;安全性;療效
【中圖分類號】 R742.5 【文獻標志碼】 A 【文章編號】 1672-7770(2023)02-0125-06
Abstract: Objective To analyze the efficacy and safety of robot-assisted bilateral deep brain stimulation of the subthalamic nucleus(STN-DBS) under general anesthesia in elderly(>80 years old) patients with Parkinson's disease(PD). Methods 3 elderly PD patients who underwent robot-assisted bilateral STN-DBS under general anesthesia in Sanbo Brain Hospital, Capital Medical University from June 2020 to June 2021 were collected. Clinical characteristics, surgical procedures, symptom outcomes at 6 and 12 months after the surgery(UPDRS-III “on” and “off” score to assess motor symptoms, LEDD to assess medication dose, H-Y stage to assess symptom severity), neuropsychological outcomes(HAMA to assess anxiety, HAMD to assess depression), cognitive outcomes(WAIS to assesses intelligence and cognition), and quality of life(ADL to assess quality of life) were analyzed retrospectively. Results There were no serious intraoperative or postoperative complications, and the implantation deviations were all within 0.7 mm. 6 months and 12 months after the surgery, motor symptoms, symptom severity, anxiety, depression, and quality of life were all significantly improved, the postoperative medication dose was significantly reduced, and there was no significant change in neurocognitive function. There was no significant difference between the 6-month and 12-month follow-ups. Conclusions Robot-assisted STN-DBS under ?general anesthesia has good efficacy and acceptable safety for elderly PD patients. Postoperative motor symptoms, medication dose, neuropsychology, and quality of life all improved significantly. However, the general condition of elderly patients should be given more attention. STN-DBS for them should be performed according to their individual condition.
Key words: Parkinson's disease; Elderly; Deep brain stimulation; Safety; Efficacy
基金項目:國家重點研發計劃項目(2018YFC2000700,2021YFC2401203)
作者單位:100093 北京,首都醫科大學三博腦科醫院神經外科(孫衛進,王澍,關宇光,趙萌,王雄飛,潘軍紅,唐重陽,馬皓偉,程子章,欒國明),神經內科(張小英),腦磁圖(騰鵬飛);北京市臨床醫學研究癲癇病重點實驗室(關宇光,欒國明);北京腦重大疾病研究院癲癇研究所(關宇光,欒國明)
通信作者:欒國明,關宇光
帕金森病(Parkinson's disease,PD)是危害中老年人常見的神經系統退行性疾病[1],隨著人均壽命的延長,PD發病率和患病人群逐年升高。PD發病后,早期藥物治療可在一定程度上控制癥狀,但一般5~8年后(中晚期)會出現藥物作用減退、開關現象、異動癥等并發癥,藥物逐步無法有效控制癥狀。腦深部電刺激(deep brain stimulation,DBS)已經成為治療PD的公認有效治療方法,目前多采取雙側丘腦底核腦深部刺激植入術(deep brain stimulation of the subthalamic nucleus,STN-DBS)開展針對PD的治療。但是手術的適應年齡仍然具有爭議,目前大部分研究及功能神經外科中心認為手術適應年齡在75歲以下[2-3],部分研究認為也可對80歲以下PD患者進行STN-DBS治療[4]。但目前對于高齡(>80歲)PD患者是否應采用STN-DBS治療,以及手術療效的利弊仍存在爭議,既往研究十分有限,尚缺乏進一步研究分析其安全性和有效性。本研究回顧性分析2020年6月—2021年6月就診于首都醫科大學三博腦科醫院的3例高齡PD患者的臨床資料,以期為高齡PD患者STN-DBS治療的療效及安全性提供參考。此外,本研究進一步探討了全麻下使用機器人輔助開展STN-DBS電極植入的新技術方法特點,為該技術的進一步推廣應用提供臨床經驗。現報告如下。
1 資料與方法
1.1 一般資料 共納入3例接受全麻下機器人輔助STN-DBS治療的高齡(手術時年齡>80歲)PD患者。3例患者均具有PD的典型癥狀,符合2016年中國PD診斷標準[5]。目前患者癥狀使用多種藥物均難以有效控制且出現藥物副作用,經首都醫科大學三博腦科醫院運動障礙病中心多學科討論評估后均具有DBS手術指征,并排除了手術禁忌證,一般情況滿足全身麻醉標準及手術標準。患者一般情況及術前基線資料見表1。
1.2 植入靶點 選擇丘腦底核(subthalamic nucleus,STN)經驗坐標參考區間,AC-PC中點旁開12~16 mm,AC-PC中點后2~3 mm,AC-PC平面下4~6 mm。根據MR可見靶點位置,結合經驗坐標,確定手術靶點。
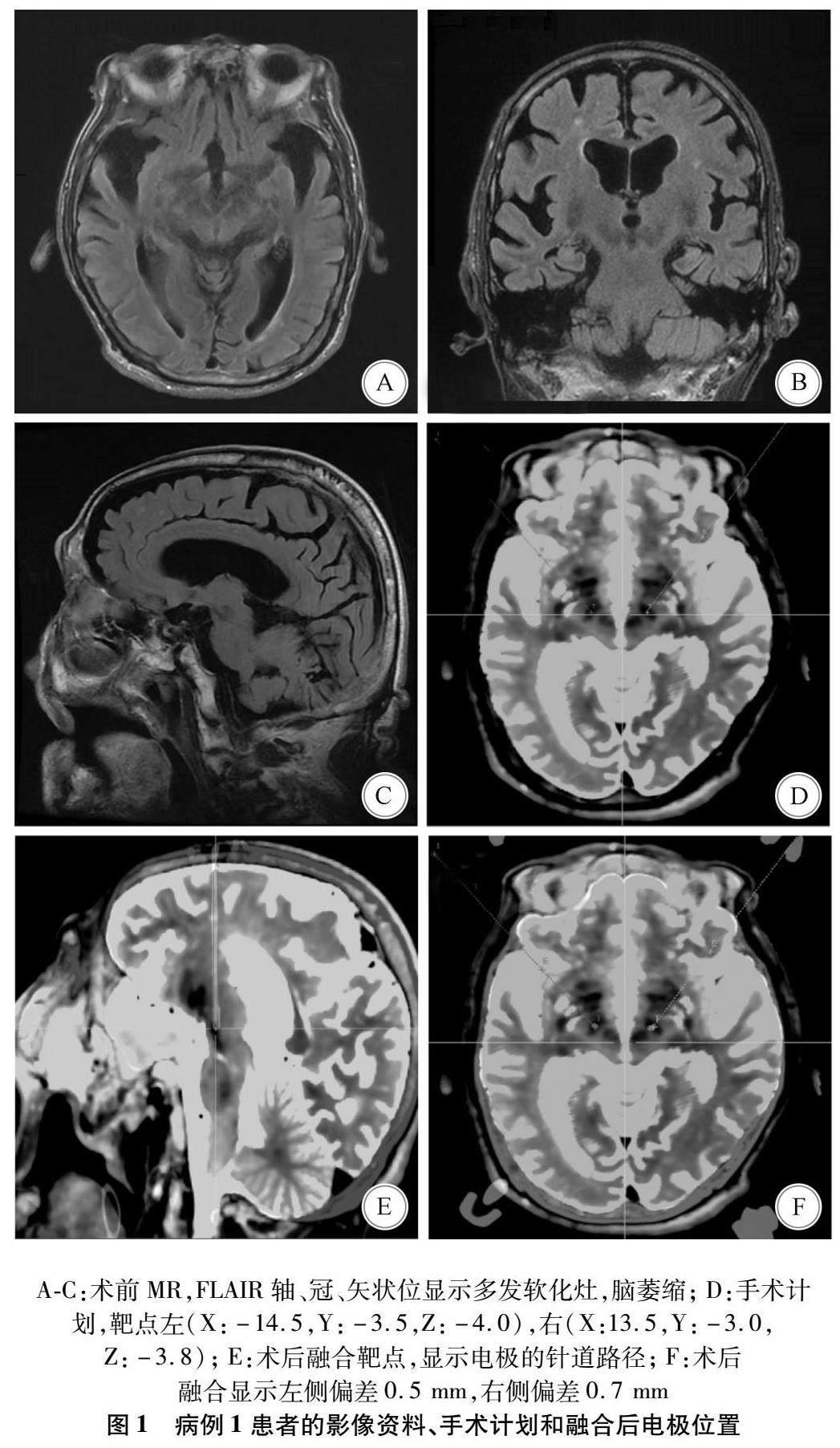
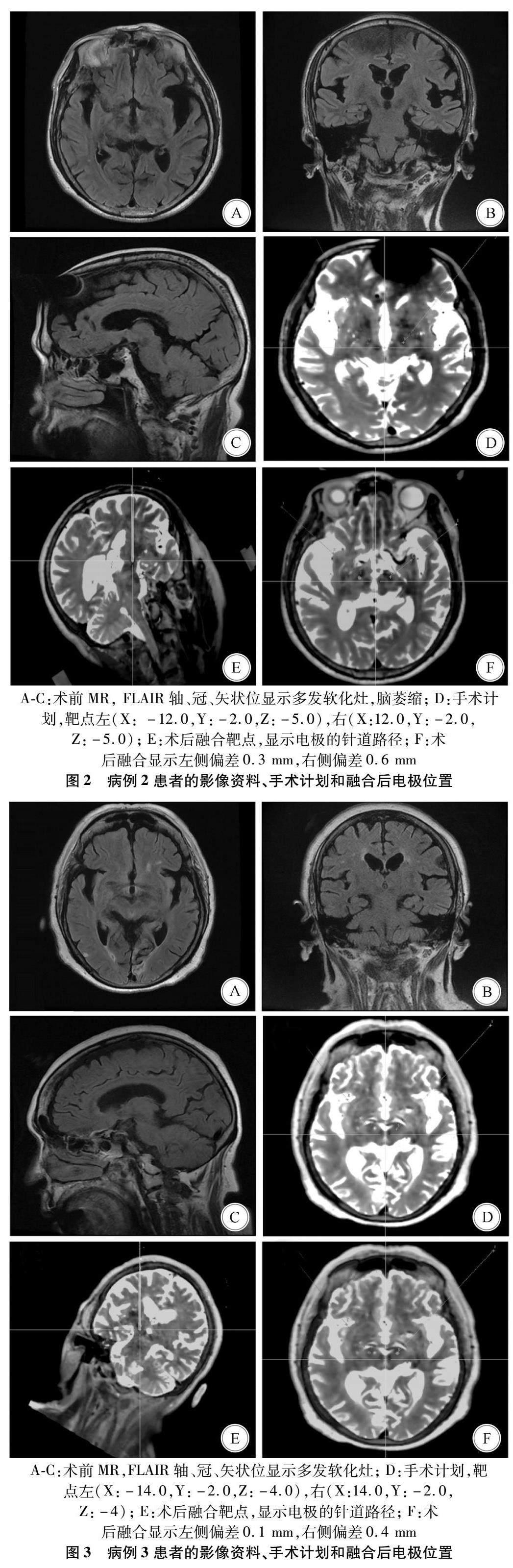
1.3 手術方法 常規行頭部核磁共振(矢狀位T1WI 平掃和增強掃描、T2WI 平掃,層厚1 mm、層間距為零)檢查;術前局麻下將5個骨性標記固定于顱骨,行薄層增強CT(層厚 1 mm、層間隔為零)掃描;將磁共振和增強CT融合,設計手術計劃,確定植入靶點及路徑;全麻下行機器人(ROSA ONE,法國MedTech公司)輔助STN-DBS電極植入,首先進行ROSA機器人引導注冊;隨后引導下切開頭皮顱骨鉆孔,模擬靶點驗證;按照計劃植入雙側STN-DBS電極(L301,北京PINS公司)至預定靶點位置,3例患者均未進行術中電生理監測,隨后縫合頭皮;行薄層頭部CT(層厚 1 mm、層間隔為零)檢查,將手術計劃與CT融合以復查確認靶點,并排除術后出血;重新消毒鋪單,行鎖骨下脈沖發生器植入;術后1周左右出院,繼續原有抗帕金森藥物;術后4周開機,并根據患者癥狀調整抗帕金森藥物使用。3例患者的影像資料、手術計劃和融合后電極位置見圖1—3。
1.4 術后程控 術后程控原則以改善患者運動癥狀為主,并盡可能減少刺激引起的不良反應。每次隨訪時,根據患者癥狀調整藥物用法用量。術后1個月左右開機,開機頻率為130 Hz,脈寬為60 μs,電壓1.0 V;根據患者癥狀主要先以調整電壓為主,脈寬頻率調整為輔。若出現不良反應,則根據病因、癥狀調整參數和藥物,以對其進行處理。
1.5 評價指標 術后6個月、術后12個月進行相關量表評分,記錄不良反應及處理,并對抗帕金森藥物使用情況進行記錄分析。主要隨訪評估量表包括臨床癥狀(UPDRS-III開、關期評分評估運動癥狀、LEDD評估用藥情況、H-Y分期評估癥狀嚴重程度)、神經心理預后(HAMA評估焦慮情緒、HAMD評估抑郁情緒)、認知預后(WAIS評估智力認知)及生活質量(ADL評估生活質量)。
1.6 統計學方法 本研究受限于樣本量有限,主要采取描述性分析方式,對患者術前術后量表評分進行評估及比較分析。患者基線數據及隨訪數據使用IBM SPSS 28.0軟件存儲。
2 結 果
2.1 手術情況 患者術前通過ROSA ONE系統設計植入靶點坐標,并進行術中注冊,STN-DBS植入手術過程中,患者一般情況均穩定良好,無術中出血,術后靶點驗證植入誤差均在0.7 mm以內,病例3左側STN-DBS電極植入誤差僅為0.1 mm,手術用時在70 min以內,所有患者在術中均一次植入成功,未二次調整植入靶點。患者靶點位置、電極植入誤差及手術時間見表2。
2.2 手術并發癥 本研究未出現出血、梗死、切口愈合不良、感染、排斥反應等手術相關并發癥;術后病例2出現陣發性房顫,給予藥物對癥治療后自動復律,考慮與麻醉相關。其余患者無嚴重未緩解的手術相關并發癥。
2.3 術后程控 本研究經過術后1個月、6個月及12個月的隨訪程控三次,3例患者脈寬及頻率均保持60 μs及130 Hz,僅對電壓進行了相應調整。在程控過程中,無嚴重持續性程控相關不良反應發生。患者術后隨訪程控參數見表3。
2.4 術后隨訪及預后 3例患者術后6個月及12個月評估時,運動癥狀、癥狀嚴重程度、焦慮抑郁情緒、生活質量均較前有顯著改善,術后用藥量顯著減少,神經認知功能無顯著變化;6個月隨訪數據與12個月數據基本無顯著差異。3例患者術后隨訪預后及改善率見表4。
3 討 論
隨著生活水平的改善和醫療技術的進步,年齡不再是選擇DBS手術的決定因素,越來越多的高齡PD患者接受并選擇DBS手術[6]。DBS對于一些藥物難治性PD病例,憑借其安全、微創、可調控等優勢,成為重要的治療方式。雖然DBS的手術靶點有很多,但目前常用的手術靶點主要有兩個,STN和蒼白球內側部(globus pallidus interior,GPI)。STN通常是年輕患者最常見的靶點,術后有顯著減少用藥量的可能性[7]。STN靶點的刺激相對于GPI需要更小幅度的電壓,有效減少電池耗電量[8]。也有研究表明,一些高齡患者選擇了STN改善了臨床癥狀[6]。由于臨床試驗通常招募一些相對年輕的患者,所以在文獻中缺乏證據支持高齡患者在STN或GPI之間的選擇[9]。本研究中,為了改善患者運動癥狀及減少藥物使用,經過多學科術前討論結合患者及家屬意愿,3例高齡患者選擇進行了STN-DBS治療,術后患者運動癥狀改善,生活質量提高,且安全性良好;術后12個月隨訪時運動癥狀UPDRS-Ⅲ(開期)改善率為41.7%~48.1%、UPDRS-Ⅲ(關期)評分改善率為46.1%~55.0%;癥狀嚴重程度H-Y分期改善率37.5%~50.0%;用藥情況LEDD改善率23.5%~40.9%;神經心理HAMA改善率57.9%~71.4%、HAMD改善率50.0%~67.4%;生活質量方面ADL改善率:42.9%~60.0%;認知功能WAIS無明顯變化,提示對于高齡PD患者,STN-DBS術后運動癥狀、癥狀嚴重程度、焦慮抑郁情緒、生活質量均較前有顯著改善,術后用藥量顯著減少,神經認知功能無顯著變化,這一結論與此前針對一般人群的相關研究類似[10-11],并且患者6個月隨訪與12個月隨訪時的運動癥狀、癥狀嚴重程度、用藥情況、生活質量進行對比均無顯著變化,均較術前有顯著改善,提示STN-DBS療效穩定,患者的癥狀及生活質量有顯著且穩定的改善。在患者癥狀明顯改善、用藥明顯減少,生活質量明顯提升之后,焦慮抑郁情緒評分也有顯著下降,這與患者癥狀改善后情緒的改善有關,且既往研究提示DBS治療本身也可改善PD相關情緒癥狀,體現出DBS治療獨特的優勢[12-13]。
既往傳統STN-DBS手術多在局部麻醉下進行,并結合術中微電極電生理記錄用于指導電極植入的位置,結合術中的刺激實驗最終確定電極的位置。電生理監測在局麻下采集信號更為明顯,但由于麻醉深度影響,在全麻下信號采集有限,目前多數中心全麻STN-DBS手術應用術中CT驗證電極植入位置的準確性,不進行術中電生理監測。此外,術中電生理監測用時較長,患者耐受程度及術中體驗不佳,并延長手術用時,有進一步增加腦脊液流失從而導致電極偏倚等其他術中風險。既往研究根據刺激靶點驗證和開機測試效果評估,認為全麻手術下單純依靠解剖靶點植入電極的精度和效果與局部麻醉下術中電生理監測無顯著差異[14-15]。相關研究表明兩種麻醉方式下電極位置的準確性均是可靠的,其臨床結果和并發癥沒有顯著差異[16]。高齡患者更容易接受全麻手術,減輕患者的焦慮疲勞和疼痛刺激,提高了患者手術的舒適感和體驗感。根據本研究3例高齡患者進行全麻下STN-DBS手術,術中無神經電生理監測,手術過程及術后麻醉恢復順利,提示全麻下STN-DBS對高齡PD患者安全性良好。但同時也應注意到,高齡患者的一般狀況及基礎疾病的相關問題是否滿足全麻手術條件以及耐受手術,應根據不同患者的個體情況選擇是否進行手術;還應發揮多學科優勢,關注神經外科、神經內科、神經影像、麻醉科等相關專家的術前多學科討論,也有助于協助判斷不同狀況的PD患者是否應接受STN-DBS手術治療。
本研究中采取了機器人輔助STN-DBS植入的方式,機器人的機械臂穩固性高,植入過程避免人為因素導致的晃動,相關文獻顯示機械臂的動作幅度小于0.1 mm,電極植入誤差平均約0.5 mm[17]。如有必要,術中可在多維平面上輕松調整靶點的位置(幅度在0.5~2 mm)。影響電極植入準確性的另一個因素是顱內積氣,腦脊液的丟失和氣體進入顱骨會導致不同程度的腦組織位移,從而影響電極植入的準確性[18]。機器人引導的手術可以減少重復操作和植入時間,從而減少腦脊液丟失和顱內積氣,保證了電極植入的準確性。本研究中,3例高齡患者應用ROSA ONE機器人輔助電極植入,電極誤差在0.1~0.7 mm之間,誤差范圍低于相關文獻報道的基于框架定位STN-DBS的平均誤差[10]。
關于手術并發癥問題,DBS治療的總體并發癥發生較少且較輕微,研究發現16%的患者可能會出現術中并發癥,例如氣道管理困難、精神錯亂、高血壓、肺栓塞,而通常這些并發癥是可控的,不良預后很少見;最嚴重的并發癥是中風、顱內出血、癲癇發作[9]。然而一項對1 757例DBS患者的回顧性分析研究表明,75歲以上的PD患者施行DBS手術后的并發癥發生率并不高于其他患者[19]。國內多項研究報道,75歲以上的PD患者進行DBS治療未見上述并發癥[6,20]。本研究3例80歲以上的高齡PD手術患者的研究中,發現其中1例患者出現了陣發性房顫,進行藥物對癥治療后迅速好轉,其余患者未見其他嚴重未緩解的手術相關并發癥。總體來說,高齡PD患者行DBS治療后可取得良好的臨床療效,手術安全性高,并發癥發生率并未有顯著上升。
全麻機器人輔助STN-DBS對高齡PD患者仍有較好的臨床療效,手術安全性基本可控,術后患者運動癥狀、藥物減量、神經心理、生活質量均有顯著改善且神經認知功能總體無影響。但應同時注意高齡患者一般狀況,根據患者個體狀況,對高齡PD患者進行STN-DBS治療。
[參 考 文 獻]
[1]羅備,閻俊,劉衛國,等.帕金森病運動癥狀的長時程連續性監測與評估的研究進展[J].臨床神經外科雜志,2021,18(1):113-116.
[2]Deuschl G,Schade-Brittinger C,Krack P,et al.A randomized trial of deep-brain stimulation for Parkinson's disease[J].N Engl J Med,2006,355(9):896-908.
[3]Okun MS,Fernandez HH,Wu SS,et al.Cognition and mood in Parkinson's disease in subthalamic nucleus versus globus pallidus interna deep brain stimulation:the COMPARE trial[J].Ann Neurol,2009,65(5):586-595.
[4]Tagliati M,Pourfar MH,Alterman RL,et al.Subthalamic nucleus deep brain stimulation in Parkinson disease patients over age 70 years[J].Neurology,2005,65(1):179-180.
[5]劉軍.中國帕金森病的診斷標準(2016版)[J].中華神經科雜志,2016,49(4):268-271.
[6]金海,陶英群,鞏順,等.丘腦底核腦深部電刺激術治療高齡帕金森病[J].中國微侵襲神經外科雜志,2021,26(4):152-154.
[7]孟凡剛,陳玲,劉鈺曄,等.中國帕金森病腦深部電刺激療法專家共識(第二版)解讀[J].中華神經外科雜志,2021,37(5):439-442.
[8]Odekerken VJJ,Van Laar T,Staal MJ,et al.Subthalamic nucleus versus globus pallidus bilateral deep brain stimulation for advanced Parkinson's disease(NSTAPS study):a randomised controlled trial[J].Lancet Neurol,2013,12(1):37-44.
[9]Azevedo P,Aquino CC,Fasano A.Surgical management of Parkinson's disease in the elderly[J].Mov Disord Clin Pract,2021,8(4):500-509.
[10]王澍,趙萌,王軍,等.不同麻醉方式下帕金森病腦深部電刺激術療效對比分析[J].中國現代神經疾病雜志,2020,20(12):1057-1065.
[11]郭松,任志偉,胡永生,等.帕金森病丘腦底核腦深部電刺激術后的長期隨訪研究[J].臨床神經外科雜志,2021,18(2):125-130.
[12]杜婷婷,陳潁川,朱冠宇,等.基于大腦形態學特征的機器學習方法預測帕金森病患者的抑郁癥狀[J].臨床神經外科雜志,2021,18(2):121-124,130.
[13]朱冠宇,陳潁川,杜婷婷,等.帕金森病患者腦深部電刺激術后焦慮改善率的影響因素研究[J].臨床神經外科雜志,2021,18(4):399-403.
[14]Mirzadeh Z,Chapple K,Lambert M,et al.Parkinson's disease outcomes after intraoperative CT-guided“asleep”deep brain stimulation in the globus pallidus internus[J].J Neurosurg,2016,124(4):902-907.
[15]Ostrem JL,Ziman N,Galifianakis NB,et al.Clinical outcomes using ClearPoint interventional MRI for deep brain stimulation lead placement in Parkinson's disease[J].J Neurosurg,2016,124(4):908-916.
[16]Wang J,Ponce FA,Tao J,et al.Comparison of awake and asleep deep brain stimulation for Parkinson's disease:a detailed analysis through literature review[J].Neuromodulation,2020,23(4):444-450.
[17]邱暢,董文文,章文斌.神經外科手術導航系統發展概述與展望[J].臨床神經外科雜志,2022,19(3):352-355.
[18]Liu LN,Mariani SG,De Schlichting E,et al.Frameless ROSA robot-assisted lead implantation for deep brain stimulation:technique and accuracy[J].Oper Neurosurg (Hagerstown),2020,19(1):57-64.
[19]DeLong MR,Huang KT,Gallis J,et al.Effect of advancing age on outcomes of deep brain stimulation for Parkinson disease[J].JAMA Neurol,2014,71(10):1290-1295.
[20]趙市偉,張睿,史有才,等.丘腦底核電刺激術對75歲以上帕金森病患者療效[J].立體定向和功能性神經外科雜志,2019,32(1):13-17.
(收稿2022-06-26 修回2022-08-19)