實驗性自身免疫性腦脊髓炎小鼠模型的構建*
謝文娟,趙雅妮,龍雪麟,李淑蓉,蘇炳銀△,譚泓琳△
1.成都醫學院 發育與再生四川省重點實驗室(成都 610500);2.成都醫學院 組織學與胚胎學教研室(成都 610500);3.成都醫學院 病理與病理生理學教研室(成都 610500)
多發性硬化癥(multiple sclerosis, MS)是一種中樞神經系統自身免疫性脫髓鞘疾病,常累及腦、脊髓和視神經,其主要病理特征包括脫髓鞘、軸突損傷及神經炎癥[1]。MS發病年齡在20~40 歲,是青壯年致殘的主要疾病之一[2]。目前,MS的病因和發病機理尚未明確,由于MS患者的腦組織標本不易獲取,限制了對該疾病的基礎和臨床研究,因此構建合適的動物模型十分必要。
目前常用的MS模型包括實驗性自身免疫性腦脊髓 炎(experimental autoimmune encephalomyelitis,EAE)、銅螯合劑-新銅試劑等毒素誘導的脫髓鞘模型和小鼠腦脊髓炎病毒模型,其中EAE模型與人類疾病十分相似,因此在科研中應用廣泛,其原理是給動物體內注射某些抗原物質,引起機體免疫系統識別異常,從而導致髓鞘、軸突等結構的免疫性損傷。髓鞘少突膠質細胞糖蛋白(myelin oligodendrocyte glycoprotein,MOG)雖然只占髓鞘總蛋白的0.05%左右,但由于其在少突膠質細胞膜上表達,因此具有很強的免疫原性[3]。MOG35-55是MOG細胞膜表面致腦炎的抗原決定簇之一,其敏感小鼠品系為C57BL/6J小鼠[4],該品系在國內常見且遺傳背景清晰。
本研究以MOG35-55作為抗原兩次免疫C57BL/6J小鼠,同時注射百日咳毒素(pertussis toxin, PTX)制備EAE模型,通過臨床癥狀評分和組織病理學檢測分析模型是否構建成功,以期為進一步研究MS的發病機制、病理過程及藥物開發提供實驗基礎。
1 材料與方法
1.1 實驗動物
SPF級8 周齡C57BL/6J雌性小鼠,體重18~20 g,20 只,購于成都達碩實驗動物有限公司,按隨機數字表法分為EAE組和對照組,每組10只。所有小鼠按照SPF級標準飼養,環境要求如下:室內溫度18 ℃~29 ℃,相對濕度40%~70%,氣流速度≤0.18 m/s,新鮮空氣換氣次數10次/h,潔凈度10000級,氨濃度15 mg/m32,光照度150~300 Lux,噪聲≤60 dB。實驗小鼠正常進食、飲水,定期更換墊料、飲水等。
1.2 試劑與儀器
MOG35-55多肽由上海生物工程有限公司合成(貨號:T510219),經質譜分析純度> 97%;卡介苗滅活凍干粉購自上海晶諾生物科技有限公司(貨號:GOMY0147);不完全弗氏佐劑(incomplete Freund's adjuvant, IFA)購自上海sigma-Aldrich公司(貨號:F5506);PTX購自上海sigma-Aldrich公司(貨號:P7208);髓鞘堿性蛋白抗體(anti-myelin basic protein, Anti-MBP)購自美國Millipore公司(貨號:NE1019);小膠質細胞特異性標志物抗體(Anti-Iba1)購于上海Abcam公司(貨號:ab178847);Anti-Mouse IgG(貨號:31160)、Anti-Rabbit IgG(貨號:31210)購自美國Invitrogen公司;牛血清白蛋白(bovine serum albumin,BSA)購自安徽biosharp生物科技有限公司(貨號:BS114);曲拉通X-100(Triton X-100)購自上海生工生物工程股份有限公司(貨號:A600198);Black-Gold Ⅱ染色試劑盒購自上海sigma-Aldrich公司(貨號:AG105)。
倒置熒光顯微鏡購自日本Olympus公司(型號:BX-63);脫色搖床購自太倉市華利達實驗設備有限公司(型號:ZD-9556);冰凍切片機購自美國Thermo公司(型號:CM1950)。
1.3 試劑配制
抗原乳劑:將100 mg卡介苗滅活凍干粉加入到10 mL IFA中,使之成為完全弗式佐劑(complete Freund's adjuvant,CFA);4 mg MOG35-55多肽溶于1.33 mL 磷酸鹽緩沖液(phosphate buffer saline,PBS),即配制濃度為3 g/L的多肽液;MOG35-55多肽液(3 g/L)與CFA按1∶1比例混合,用注射器反復推拉乳化,制成“油包水”的抗原乳劑。PTX溶液:50 μg PTX溶于1 mL PBS,配制成50 mg/L的PTX儲備液,使用濃度為1 mg/L。
1.4 EAE 的構建
EAE組小鼠在雙側腹股溝及后肢分4 點皮下注射,每點注射50 μL乳劑。于首次免疫后0、48 h腹腔注射PTX (1 mg/L)200 μL,6 d后在相同部位注射相同劑量抗原乳劑加強免疫。對照組小鼠在雙側腹股溝及后肢分4 點皮下注射不含MOG35-55多肽的CFA,其余實驗方法均與EAE組相同。
1.5 神經功能評分
建模后,根據Kelero等[5]提出的神經功能評分標準,課題組成員每天觀察兩組小鼠行為學變化,并對小鼠的神經功能進行評分(表1)。

表1 小鼠神經功能評分(分)
1.6 組織取材與檢測
1)取材:在EAE組小鼠癥狀較嚴重時(免疫后第19 天),腹腔注射4%水合氯醛對小鼠進行麻醉,使用消毒滅菌后的手術器械,快速打開小鼠胸腔,充分暴露心臟,經左心室灌注1×PBS充分洗凈組織中的血液,觀察肝臟顏色變白后改用4%多聚甲醛灌注,充分固定后立即取出小鼠的大腦和脊髓組織,放入4%多聚甲醛液中進行后固定,固定好的組織進行梯度脫水,OCT包埋并冰凍切片(20 μm)。2)免疫組織化學染色:切片置于PBS復水,隨后滴加封閉液(5% BSA + 1.5% Triton X-100+1×PBS)于37 ℃孵育60 min;滴加Anti-MBP、Anti-Iba1 抗體(1∶500), 4 ℃孵育過夜;PBS清洗3 次后,滴加DyLight 488 標記的山羊抗兔二抗(1∶200),室溫孵育1.5 h;PBS清洗3 次后,使用含DAPI的抗熒光淬滅劑進行封片,熒光顯微鏡下觀察及拍照。3)Black Gold染色:切片復水后放入60 ℃Black Gold Ⅱ染色液染色到合適深淺的顏色,染色時間15~20 min,采用95%、75%酒精進行梯度脫水,二甲苯透明,中性樹脂封片。
2 結果
2.1 兩組小鼠神經功能評分比較
EAE組小鼠在首次免疫后第12天開始發病,在第19天癥狀最為顯著,隨后病情有所緩解,發病率為100%。EAE組小鼠首先出現尾部張力下降,接著出現尾部癱瘓拖垂、步態搖擺、后肢無力、后肢癱瘓等癥狀。對照組小鼠在首次免疫后第14天左右出現短暫的尾巴無力癥狀(圖1)。
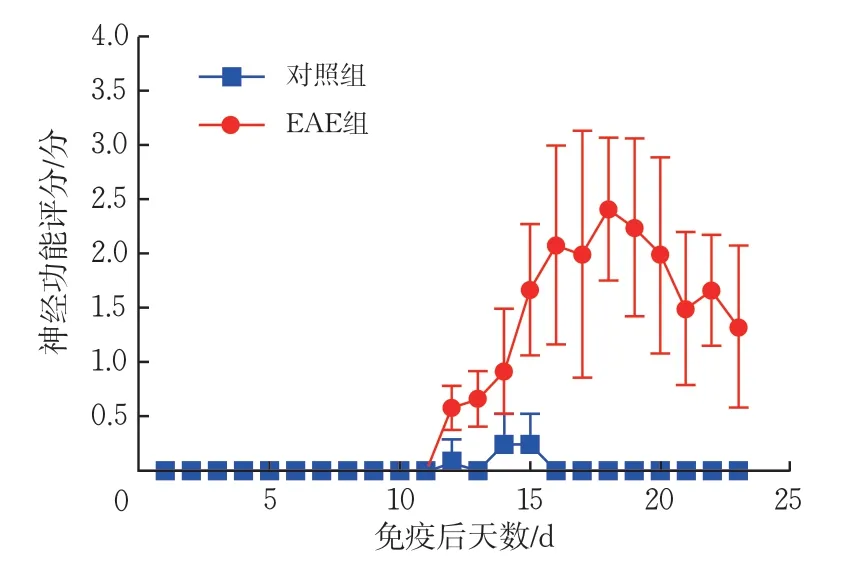
圖1 兩組小鼠神經功能評分比較
2.2 兩組小鼠脫髓鞘情況比較
Black Gold髓鞘染色結果顯示,EAE組小鼠脊髓白質著色比對照組淺,脊髓灰質的絲狀著色明顯減少(圖2A~B),同時EAE組小鼠大腦胼胝體區域著色相比對照組更淺(圖2C~D)。MBP的免疫熒光染色結果顯示,EAE組小鼠脊髓和大腦的MBP著色較對照組淺(圖3),提示EAE組小鼠脊髓和腦組織發生了脫髓鞘。
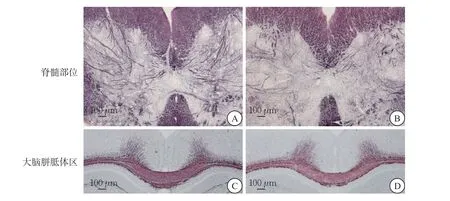
圖2 兩組小鼠脊髓組織Black Gold染色

圖3 兩組小鼠MBP免疫熒光染色
2.3 兩組小鼠小膠質細胞增殖情況比較
免疫熒光染色結果顯示,與對照組相比,EAE組小鼠脊髓和大腦皮層區域的小膠質細胞數量明顯增多,同時伴隨小膠質細胞胞體增大、突起增多等形態學改變(圖4),提示EAE組小鼠脊髓和腦組織的小膠質細胞處于增殖活化狀態。
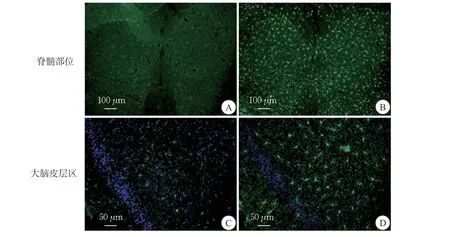
圖4 兩組小鼠Iba-1 染色
3 討論
MS的病因和發病機制目前尚未明確,認可度較高的理論是由于病毒或某些抗原物質觸發了機體自身免疫反應,從而損害髓鞘及其包裹的神經元軸突,基于該理論建立了不同的EAE模型,目前所制備的動物模型還不穩定,需要進一步探索。
本研究采用的抗原物質是MOG35-55多肽,與其他髓鞘蛋白相比,如MBP、髓鞘蛋白脂質蛋白(myelin proteolipid protein,PLP)等,MOG因在少突膠質細胞膜表面表達而具有很強的免疫原性,并且MBP的敏感小鼠品系是B10.PL和PL小鼠[6],PLP的敏感小鼠品系是SJL和SWXJ小鼠[7-8],這些品系在國內不易獲得,而MOG的敏感小鼠品系C57BL/6J,是常見的實驗小鼠品系。在構建EAE模型時,通常會加入強效佐劑CFA,增強抗原的免疫反應強度并延長免疫反應時間[9],刺激大量吞噬細胞攝取和呈遞抗原以及CD4+T細胞的增殖活化[10],提高模型成功率。而PTX具有破壞血腦屏障的作用,使外周反應性T細胞得以進入中樞神經系統分泌相關細胞因子,促進炎癥反應發生[10-11]。目前大多數EAE模型構建只進行1 次免疫誘導,本研究采用MOG35-55和CFA的混合乳劑兩次加強誘導C57BL/6J小鼠,并對注射部位進行了調整,在小鼠雙側腹股溝和下肢分4 點進行皮下注射,于首次免疫后0、48 h腹腔注射PTX破壞血腦屏障,然后根據小鼠的行為學表現進行神經功能評分,并進行組織病理學檢測,發現EAE組小鼠在免疫后第12 天開始發病,第19 天癥狀最為嚴重(神經功能評分<3.5 分),表明該方法構建的EAE模型穩定,且發病率為100%。本研究中對照組小鼠在免疫后第14 天左右出現短暫的尾巴無力癥狀,推測是由CFA中的結核分枝桿菌及注射的PTX引發的炎癥所造成的。脫髓鞘是MS主要的病理特征。本研究中Black Gold髓鞘染色和MBP免疫熒光染色結果表明,EAE組小鼠的脊髓和大腦胼胝體均出現脫髓鞘,并且大腦胼胝體的脫髓鞘要遲于脊髓,原因可能與免疫部位位于腹股溝和后肢有關。膠質細胞活化是MS常見的一個病理學特征,與中樞神經系統炎性損傷密切相關[12]。本研究發現,EAE組小鼠脊髓和大腦的小膠質細胞增殖活化,提示小膠質細胞參與了脫髓鞘和神經變性。活化的小膠質細胞在EAE發病過程中扮演著雙重角色:一方面,小膠質細胞活化會增強抗MOG的自身免疫反應,參與炎癥級聯反應,加重髓鞘脫失和軸突損傷;另一方面,小膠質細胞能吞噬、清除崩解的髓鞘碎片,并招募少突膠質細胞前體細胞到達脫髓鞘部位進行髓鞘修復,促進髓鞘再生[13-14]。
綜上所述,本研究建立的EAE模型發病率為100%,EAE組小鼠表現為平衡失調及運動功能障礙,脊髓和腦組織均發生髓鞘脫失及小膠質細胞活化,符合MS的臨床表現及病理特征,因此本研究采用MOG35-55兩次免疫C57BL/6J小鼠成功構建了EAE模型。該方法的優點在于易于誘導,能模擬出MS的典型特征(脫髓鞘和炎癥損傷),且發病率高、病程穩定,但該模型也存在一定的局限性。EAE模型是人工誘導的免疫應答,以CD4+T細胞反應為主,而MS患者發生的免疫反應以CD8+T細胞和B細胞介導為主。此外,EAE誘導的脫髓鞘主要是軸突損傷后的繼發性脫髓鞘,原發性脫髓鞘較少,故該模型與人類MS存在一定差異,仍需進行大量研究以建立更好的MS模型,為后續藥物開發奠定基礎。

