心血管疾病重癥患者全死因死亡的危險因素分析*
劉志玄,王 羽 ,張換想,隋曉芳,邱洪斌,張藝瀠△
1.佳木斯大學 公共衛生學院(佳木斯 154007);2.佳木斯大學附屬第一醫院 健康管理體檢中心(佳木斯 154007)
心血管疾病(cardiovascular disease,CVD)病死率較高,給社會及個人帶來巨大壓力[1]。CVD主要包括高血壓、缺血性心臟病、慢性風濕性心臟病及腦血管病等[2]。目前CVD的檢測率較低,患者缺乏系統性、持續性的預防與管理[3-5],因此本研究擬探討CVD重癥患者全死因死亡的危險因素,以期為CVD的預防與治療提供參考依據。
1 資料與方法
1.1 臨床資料
選取2002—2012年美國重癥監護醫學信息庫數據庫中含有血清鐵檢測指標的5830例CVD重癥患者為研究對象,該數據庫的建立和使用已通過美國機構倫理審查委員會批準(Record ID:10014897)。1)納入標準:入住ICU且含有血清鐵指標者;對于多次入住ICU者,選取首次入院時的記錄信息。2)排除標準:年齡<18歲;ICU住院時間<24 h;入院后24 h內死亡者;妊娠、分娩、產褥期者;關鍵變量缺失者;住院期間使用鐵補充劑治療者。經篩選后,最終納入CVD重癥患者5779例,根據研究結局將其分為存活組(n=5032)和全死因死亡組(n=1626);根據血清鐵濃度按照四分位數法將其分為4組:G1組(50~210 μg/L,n=1473)、G2組(210~350 μg/L,n=1471)、G3組(350~590 μg/L,n=1398)、G4組(>590 μg/L,n=1437)。由于數據庫隱私性的考慮,89 歲以上患者的年齡被掩蓋,這部分患者年齡中位數為91.4 歲[6]。
1.2 資料收集
一般資料包括年齡、性別、體重等;合并癥主要包括轉移癌、實體瘤、外周血管病等;實驗室指標主要包括患者入院24 h測得的血紅蛋白、白蛋白、紅細胞、總鐵結合力、血清鐵、轉鐵蛋白等數據;治療方法有24 h通氣治療和腎替代療法。
1.3 隨訪
本研究共隨訪6 個月,記錄納入患者的生存狀況,分析CVD重癥患者全死因死亡的危險因素。
1.4 統計學方法
采用 IBM SPSS Statistics 22.0 統計軟件進行數據分析,偏態分布的定量資料采用M(P25,P75)表示,組間比較采用秩和檢驗;定性資料采用例數(%)表示,組間比較采用χ2檢驗。采用Cox回歸分析各指標與CVD重癥患者全死因死亡的關系,并繪制K-M生存分析曲線圖。檢驗水準α除特別說明外均設定為0.05。
2 結果
2.1 兩組一般資料比較
納入患者中,存活組年齡中位數為67歲,全死因死亡組年齡中位數為71歲。與存活組比較,全死因死亡組年齡、紅細胞分布寬度、總膽紅素、白細胞、轉鐵蛋白、血清鐵、簡化急性生理學評分、序貫器官衰竭評分更高,體重、血紅蛋白、紅細胞、血氧飽和度、總鐵結合力、舒張壓更低,更易發生實體瘤和外周血管病(表1)。
表 1 兩組一般資料比較[,n(%)]
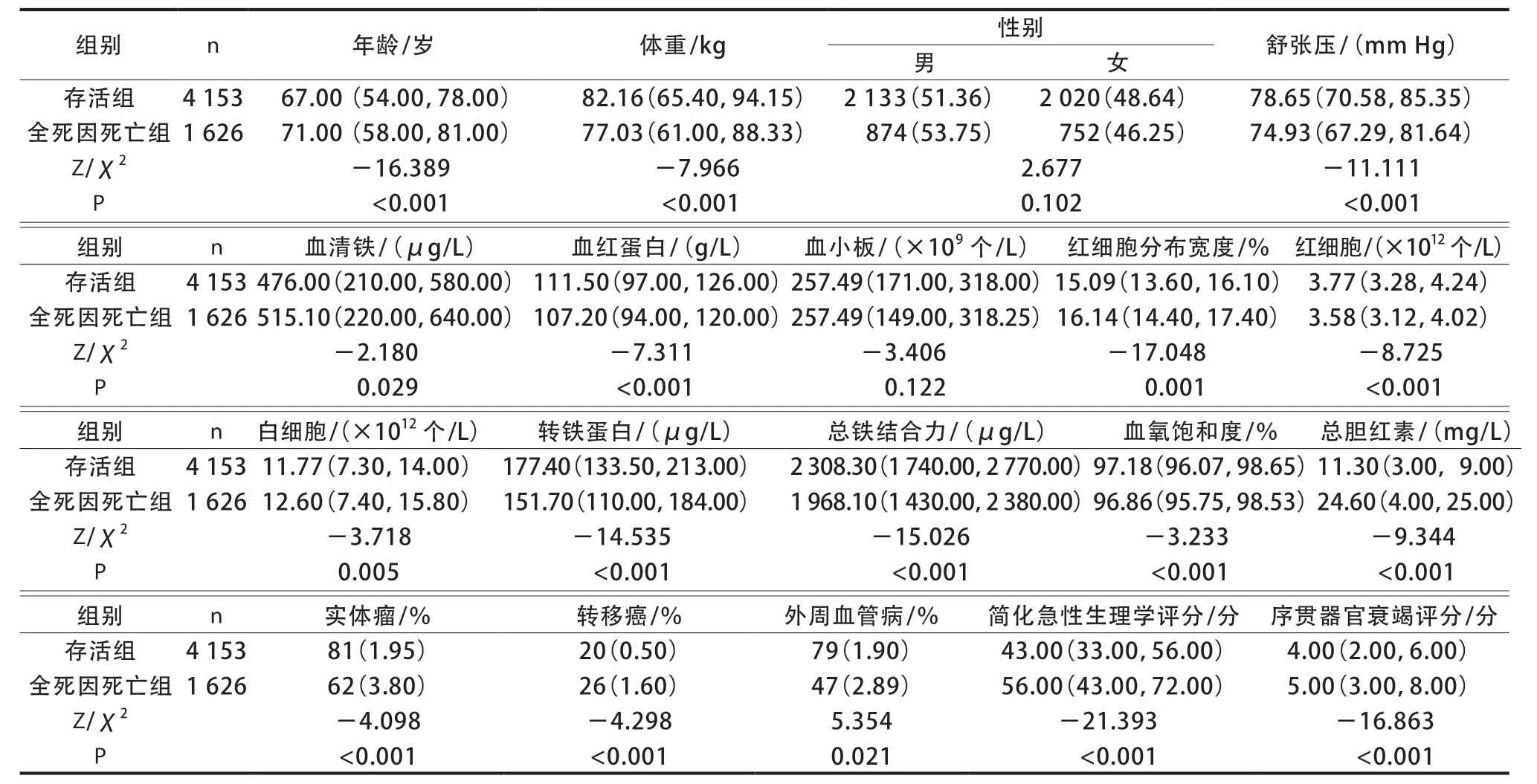
表 1 兩組一般資料比較[,n(%)]
注:1 mm Hg=0.133 kPa。
組別n年齡/歲體重/kg性別舒張壓/(mm Hg)男女存活組415367.00 (54.00,78.00)82.16(65.40,94.15) 2133(51.36) 2020(48.64)78.65(70.58,85.35)全死因死亡組162671.00 (58.00,81.00)77.03(61.00,88.33)874(53.75)752(46.25)74.93(67.29,81.64)Z/χ2-16.389-7.9662.677-11.111 P<0.001<0.0010.102<0.001組別n血清鐵/(μg/L)血紅蛋白/(g/L)血小板/(×109 個/L) 紅細胞分布寬度/% 紅細胞/(×1012 個/L)存活組4153 476.00(210.00,580.00)111.50(97.00,126.00)257.49(171.00,318.00)15.09(13.60,16.10) 3.77(3.28,4.24)全死因死亡組1626 515.10(220.00,640.00)107.20(94.00,120.00)257.49(149.00,318.25)16.14(14.40,17.40) 3.58(3.12,4.02)Z/χ2-2.180-7.311-3.406-17.048-8.725 P 0.029<0.0010.1220.001<0.001組別n 白細胞/(×1012 個/L)轉鐵蛋白/(μg/L)總鐵結合力/(μg/L)血氧飽和度/%總膽紅素/(mg/L存活組4153 11.77(7.30,14.00) 177.40(133.50,213.00) 2308.30(1740.00,2770.00)97.18(96.07,98.65)11.30(3.00, 9.00全死因死亡組1626 12.60(7.40,15.80) 151.70(110.00,184.00) 1968.10(1430.00,2380.00)96.86(95.75,98.53)24.60(4.00,25.00 Z/χ2-3.718-14.535-15.026-3.233-9.344 P 0.005<0.001<0.001<0.001<0.001組別n實體瘤/%轉移癌/%外周血管病/%簡化急性生理學評分/分 序貫器官衰竭評分/分存活組415381(1.95)20(0.50)79(1.90)43.00(33.00,56.00)4.00(2.00,6.00)全死因死亡組162662(3.80)26(1.60)47(2.89)56.00(43.00,72.00)5.00(3.00,8.00)Z/χ2-4.098-4.2985.354-21.393-16.863 P<0.001<0.0010.021<0.001<0.001
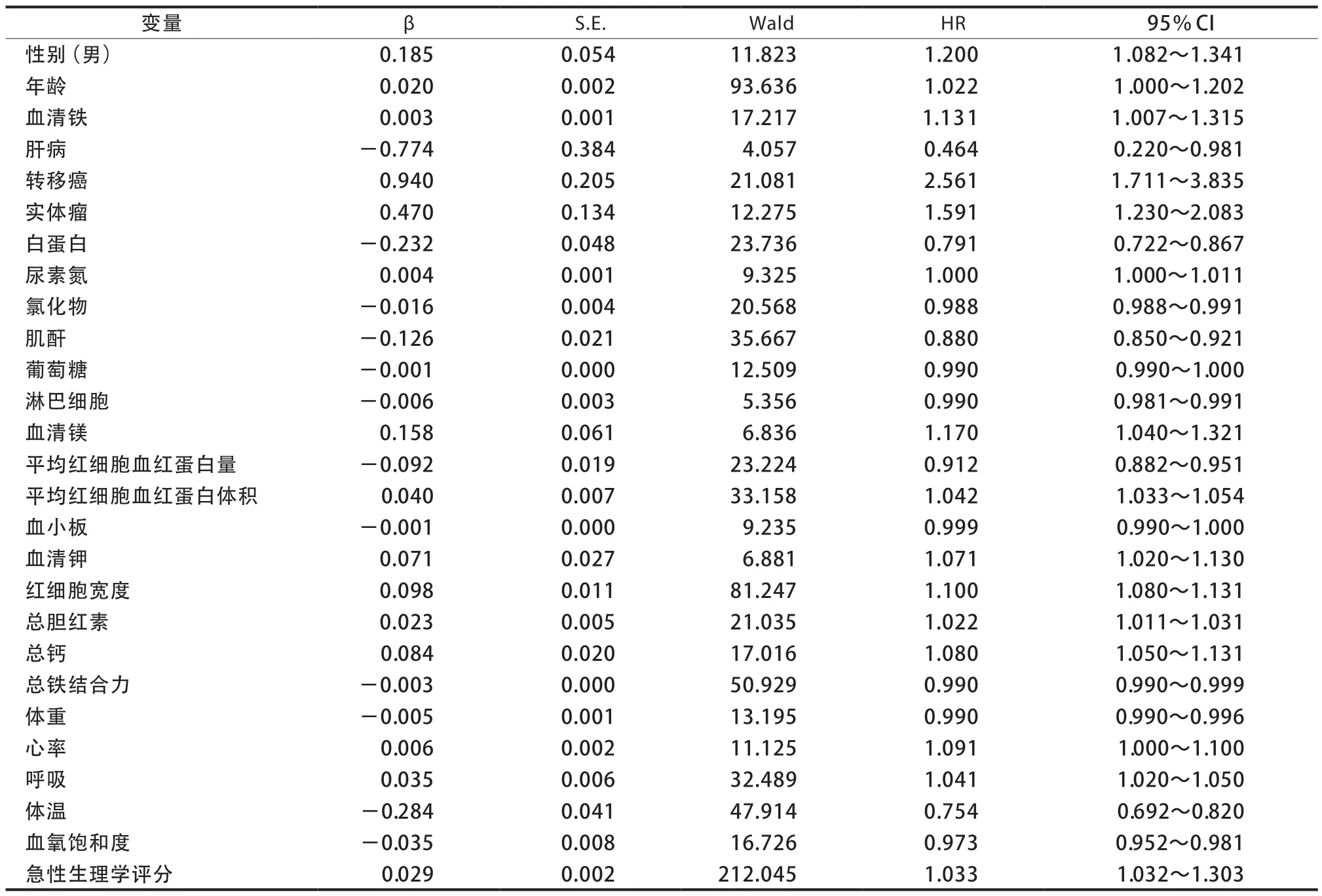
表2 CVD重癥患者全死因死亡Cox回歸分析
2.2 血清鐵濃度與CVD 重癥患者生存率的關系分析
K-M生存分析顯示,與G1 組比較,G4 組存活率更低,差異有統計學意義(P=0.008);CVD重癥患者隨著血清鐵濃度增加,其死亡風險增高,生存率下降(圖1)。
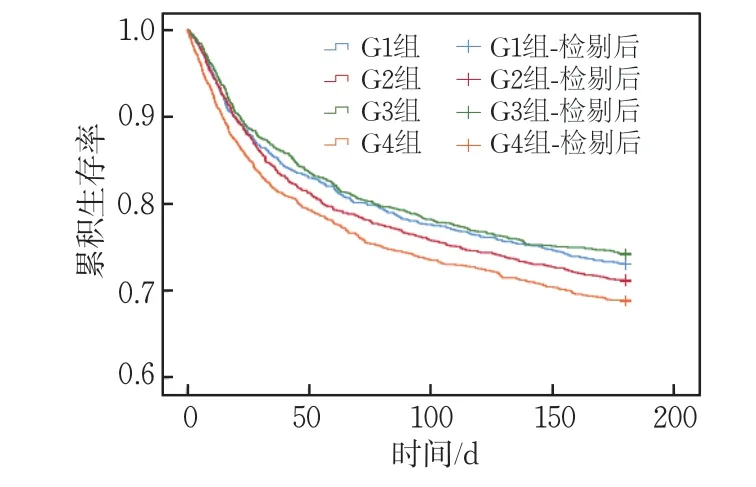
圖1 K-M生存分析曲線
2.3 CVD 重癥患者全死因死亡的Cox 回歸分析
納入患者基線資料、治療方法、合并癥及相關實驗室指標中具有統計學意義的指標,調整混雜因素年齡、性別、肝病、轉移癌、實體瘤、白蛋白、血氧飽和度、葡萄糖等混雜因素,采用向前步進似然比法進行統計分析,結果顯示,男性CVD重癥患者發生全死因死亡的風險高于女性(HR=1.200,P=0.001);年齡高于50歲發生CVD全死因死亡的風險更高(HR=1.022,P<0.001);血清鐵濃度是影響CVD重癥患者全死因死亡的危險因素(HR=1.131,95%CI:1.007~1.315),合并轉移癌、實體瘤是CVD重癥患者全死因死亡的危險因素;而白蛋白、總鐵結合力、氯化物、肌酐、葡萄糖是其保護因素(表 2)。
2.4 血清鐵濃度與CVD 重癥患者全死因死亡的Cox 回歸分析
納入患者基線資料、治療方法、合并癥及相關實驗室指標,調整年齡、性別、白蛋白、葡萄糖等混雜因素進行Cox回歸分析,結果顯示,與G1 組比較,G4 組發生全死因死亡的風險更高(HR=1.333,95% CI:1.051~1.541)(表3)。

表3 血清鐵濃度與CVD重癥患者全死因死亡的Cox回歸分析
3 討論
鐵是人體必需的微量元素,也是血紅蛋白、多種酶的組成部分,在機體發育過程中起重要作用。多項研究[5-8]證實,鐵負荷過量可誘發動脈粥樣硬化,同時也會形成一定的心肌毒性。有研究[9]發現,CVD重癥患者體內脂質氧化依賴組織內鐵的濃度,動脈粥樣硬化斑塊內鐵水平較高,這可能是CVD的危險因素之一。本研究發現,CVD重癥患者隨著血清鐵濃度增高,其死亡風險升高,與相關研究[10-13]結果一致。
本研究結果顯示,CVD重癥患者的白細胞濃度、總膽紅素水平、血清鐵水平、紅細胞分布寬度增加,合并外周血管病、實體瘤時發生心血管死亡風險增高,該結果與相關研究[14-16]結果一致。本研究結果顯示,與存活組比較,全死因死亡組年齡較大,表明高齡是CVD重癥患者發生全死因死亡的危險因素。有研究[17-20]顯示,血清鐵水平與CVD的發病率相關,在60 歲以上人群中表現得更明顯,其原因可能是由于老年人隨著年齡的增長睡眠質量下降,吸煙、飲酒、熬夜等不良生活習慣均會影響脂質代謝,從而誘發高血壓、高血脂的發生,進一步加劇CVD的患病風險,與本研究結果一致,血清鐵水平可能對CVD的風險分層具有預測價值[21]。
本研究結果顯示,男性CVD重癥患者發生死亡的風險較高。研究[22]表明,CVD病死率有明顯的性別差異,男性高于女性。CVD的發生與患者不良生活習慣、飲食因素等密切相關。有研究[23]顯示,吸煙、飲酒等不良生活行為習慣會加劇CVD的發生發展。研究[24]表明,吸煙可增加患腦卒中風險,少量飲酒對缺血性心肌病具有保護作用,過量飲酒可加重CVD患病風險[25]。血清鐵水平升高會增加中國男性人群發生CVD的風險[26]。在冠心病患者中,血清鐵濃度≥200 μg/L的男性發生動脈粥樣硬化的風險是健康男性的4 倍[27]。研究[28]發現,通過血清鐵濃度評估,高濃度鐵是伊朗男性人群過早發生冠心病的獨立危險因素。有研究[25]表明,月經停止后,女性人群體內血清鐵水平比絕經前高3倍。有研究[29-31]表明,在女性人群中,血清鐵水平表現為一定的保護作用。研究[32]發現,血清鐵水平與女性冠心病風險呈負相關。
本研究納入樣本充足,實驗室指標豐富,但還存在一定不足,如未選擇健康人群作為對照,今后需進一步深入研究。
綜上所述,CVD患者血清鐵濃度越高發生全死因死亡風險越高,此外,男性、高齡等為CVD危險因素,而白蛋白、總鐵結合力等為保護因素。目前我國已進入老齡化社會,為提高老年人群生活質量,老年人應定期監測血清鐵濃度,以預防心腦血管疾病的發生。

