晚期強直性脊柱炎致髖關節強直行全髖關節置換的療效分析*
梁一鳴,李 彪,楊 毅,劉俊洪,曾 鑫,李楠曦
(昆明醫科大學第一附屬醫院骨科,云南 昆明 650032)
強直性脊柱炎(ankylosing spondylitis,AS)是一種血清學陰性反應的結締組織疾病,多發于中青年,男性比例高達75%。發病部位多為骶髂關節,并以此為軸心向上蔓延至脊柱或下肢大關節,導致受累部位出現纖維性變化或骨性強直融合[1]。AS累及髖關節患者約占AS患者人群的19%~36%,晚期常致脊柱“竹節樣”改變[2]、髖關節強直融合,嚴重影響患者的活動、工作能力和生活質量。AS早期的治療方法為藥物治療,晚期則需手術治療[3],人工全髖關節置換術(total hip arthroplasty,THA)是改善AS晚期致髖關節強直及功能障礙的主要外科治療手段[4]。本科室2019年6月-2022年12月期間對上述AS致髖關節強直融合的9例患者(13髖)行THA手術均取得良好療效,現報告如下。
1 方法
1.1 一般資料
納入昆明醫科大學第一附屬醫院自2019年6月-2022年12月因晚期強直性脊柱炎累及髖關節致完全融合而需行全髖關節置換術的患者共9例(13側髖),其中7例男性,2例女性;年齡在21~72歲之間,平均41.08±15.86歲;左側8髖,右側5髖。所有患者術前實驗室檢查均示HLA-B27(+)。
1.2 納入及排除標準
納入標準:(1)合并髖關節功能嚴重受損,擬接受THA手術的成年患者;(2)實驗室檢查人類白細胞抗原(human leukocyte antigen-B27,HLA-B27)為陽性;(3)影像學檢查示BASRI-hip評分雙側骶髂關節炎≥2級或單側骶髂關節炎3~4級合并髖關節間隙變窄、骨性融合表現;(4)患者及家屬均對病情及治療方案知情同意,術后定期復查;(5)治療方案通過醫院倫理委員會批準。排除標準:(1)合并或既往存在嚴重心腦血管疾病、肝腎功能、呼吸功能嚴重受損或其他原因導致無法承受麻醉及術后康復治療者;(2)術側髖關節既往創傷、手術或處于感染中者。(3)隨訪丟失者。
1.3 治療方法
本研究中所有手術均由同一主刀醫生及其團隊完成。雙側髖關節強直融合患者在一側術后間隔1~3個月行對側手術。
手術:麻醉成功后取側臥位,注意保護患者固有脊柱曲度,所有患者均采用后外側入路,以大粗隆外緣為中心,作一長約12cm弧形切口,逐層切開皮膚及股骨外側闊筋膜張肌,鈍性分離臀大肌,顯露并切開關節囊,根據軟組織攣縮狀況予以松解。分別在股骨小粗隆上方1.5cm處及股骨頭與股骨頸交界處以45°以擺鋸平行兩刀截除股骨頸,根據術前影像學檢查及術中殘存解剖結構(卵圓窩處存在的較薄脂肪)確定髖臼位置,將骨性髖臼銼磨至合適深度及直徑,然后以前傾角約10°,外展角約45°,安放人工髖臼假體。將股骨近端前傾15°開口,并使用股骨髓腔銼將其磨至適當大小,安裝股骨側假體及相應型號的人工股骨頭,復位后屈曲內外旋髖關節,檢查是否有脫位情況,并確保活動良好。用可吸收性縫合線逐層縫合術后刀口,最后連續皮內縫合。在手術當天及術后第1d全身應用頭孢或其他廣譜抗生素預防感染,術后24h內拔除引流管,每天監測體溫,并口服依托考昔+肌注鹽酸曲馬多注射液鎮痛,同時每日口服利伐沙班,以預防血栓產生。在術后第1d,建議開始踝泵鍛煉和股四頭肌等長回縮鍛煉。
1.4 評價標準
在術前和24.08±5.95個月的隨訪時,對各項評分進行統計,以反映其臨床表現和治療效果。
1.4.1 患髖屈曲活動度
使患者仰臥于平板床面,在最大屈髖屈膝位時,將量角器軸心定位于人體外側股骨大轉子位置處,定位臂與床面保持平行,移動臂與股骨長軸保持平行,以此來測定患者髖關節屈曲活動度。
1.4.2 髖關節功能Harris評分
滿分為100分,≥ 90者為優秀,80~89分為良好,70~79分為一般,<70分為差。
1.4.3 視覺模擬評分(VAS)
受試者可以按照自身疼痛情況進行自我主觀打分,2~4分表示輕度疼痛,5~7分表示中等疼痛,8~9分則表示嚴重疼痛。
1.3.4 疾病活動性評價指數(ASDAS)
包括患者背痛、晨僵、患者整體感覺和周圍關節病變等,聯合CRP計算得分。ASDAS-CRP=患者總體評價×0.1+晨僵時間×0.06+外周關節腫脹或疼痛×0.07+腰背痛×0.12+Ln(CRP+1)×0.58。ASDAS<1.3代表疾病處于非活動期,2.1分是疾病活動度低與高的分界線,3.5分以上提示疾病處在極高活動度期。
1.3.5 巴氏強直性脊柱炎功能指數(BASFI)
在臨床上用于評價AS患者的綜合功能情況和治療后的改善情況,分為0~10分,分值越低代表患髖的綜合功能及療效越好。
1.3.6 強直性脊柱炎生活質量問卷(ASQOL)
一種通過專門針對AS患者對18個問題的主觀評分以評價其生活質量的評分表。分值高者代表生活質量越差。
1.5 統計學方法
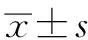
2 結果
2.1 患髖屈曲活動度
末次隨訪與術前對比,患髖屈曲活動度明顯改善,結果具有統計學意義(P<0.001),見表1。
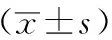
表1 患髖術前及末次隨訪屈曲活動度對比結果
2.2 各項評分術前及末次結果對比 Harris評分見表2*1、VAS評分見表2*2、ASDAS評分見表2*3、BASFI評分見表2*4及ASQOL評分見表2*5
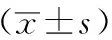
表2 患者各項評分術前與末次隨訪對比結果
末次隨訪平均分較術前平均分明顯改善,差異均具有統計學意義(P<0.001)。其中 Harris提示患者經手術治療后髖關節功能較術前改善明顯,但末次隨訪平均分值仍處于Harris功能評分中功能一般的范圍[14]。VAS評分提示患者經手術治療后髖關節疼痛較術前改善,但仍存在疼痛。本組患者在AS活動性及生活質量上均較術前有明顯改善。
3 典型病例
患者劉某某,51歲,男性,術前骨盆正位片示患者雙側骶髂關節融合、雙髖關節骨性強直融合(BASRI-hip4級)見圖1a,分兩次行一期THA,術后復查骨盆正位片示雙側人工髖關節對合良好,假體無斷裂、松動、脫位等征象見圖1b。術后復查患髖屈曲活動度約75°見圖1c,術后可脫離拐杖自行行走見圖1d。
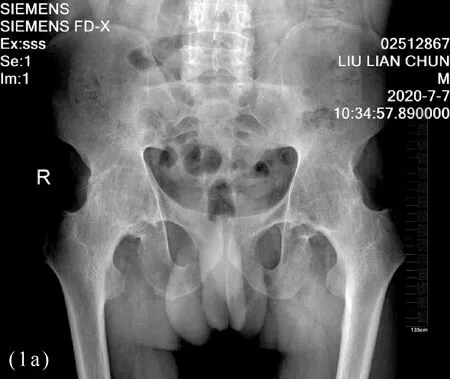
圖1a 患者劉某因髖關節強直行THA術前術后骨盆正位片對比
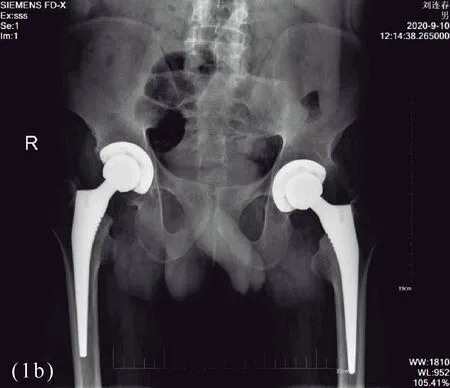
圖1b 患者劉某因髖關節強直行THA術前術后骨盆正位片對比
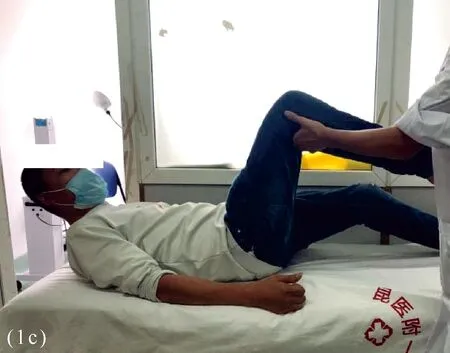
圖1c 患者術后屈曲功能

圖1d 患者術后可無輔助自主行走
4 討論
髖關節強直作為AS累及髖關節病變的最終末期改變,對患者生活質量、工作能力等影響巨大,THA是目前針對此類型患者改善髖關節功能、糾正髖關節強直的最佳治療方案[5,6]。
手術技術結合本組患者實際情況及主刀醫生習慣,本研究均采用后外側入路,以二次截骨法進行截骨,這種截骨方式可以避免截骨時手術視野受限引起的骨性髖臼損傷。本研究選擇使用生物型人工假體搭配高交聯聚乙烯-陶瓷或陶瓷-陶瓷對合界面,以滿足AS患者一般起病年齡低,假體使用壽命較高的需求,同時兼顧可能存在的翻修保留骨量。
術中體位擺放與假體安放角度與常規行THA患者不同,AS患者終末期通常合并脊柱融合后凸畸形,骨盆存在后傾骨盆及腰椎在屈髖動作下代償較正常人明顯受限,術前擺放患者體位時應注意側臥位下患者顱骨中心即耳道與股骨頭連線平行于手術床長軸,以保證患者處于功能位下進行手術,使髖臼側假體在植入時角度更加符合患者個體情況,從而降低假體磨損率、松動率和脫位率。本組患者以約前傾5~10°,外展45°安放髖臼側假體,以15°前傾安放股骨側假體。
圍手術期的藥物管理非甾體類抗炎藥物對THA患者術后消炎鎮痛效果顯著[7],同時聯合手術部位低劑量放療起到預防異位骨化的作用。生物制劑是目前AS靶向性及療效俱佳的保守治療方案[8],但對需行THA的患者存在術口愈合延遲、感染風險增高、血栓形成等風險,應考慮將術期安排在生物制劑治療周期末以降低其并發癥發病率。由于上述藥物所致的免疫功能減低[9],本研究患者術后予以應用廣譜抗生素以減少術后感染的發生率。
通過本研究發現,本組患者經手術治療后髖關節活動度、Harris評分及VAS疼痛評分等指標均有改善,結果具有統計學意義。隨訪期內均未出現假體脫位、松動、界面磨損、感染等情況,但本組患者術后Harris髖關節評分僅恢復至評分系統中的良好水平,部分患者術后仍存在疼痛或其他不適。根據臨床觀察及既往文獻報道[10],分析造成這一結果的原因可能包括髖關節長期強直致周圍軟組織攣縮、肌力減弱、脊柱骨盆矢狀面失衡、髖臼側及股骨側放置位置及角度等原因。同時應充分加強對AS患者的宣教,術后定期復查與AS活動性相關指標,動態調整患者術后康復理療和藥物治療方案[11],以控制或延緩AS病程和對全身各系統的影響。
5 不足與展望
由于此類患者個體差異較大,術前測量手段欠精準,未來可考慮在術前對患者CT數據運用三維重建技術進行建模,并在模型上實施模擬手術,對模擬手術后的模型進行有限元分析[12],施加載荷后觀測應力集中、磨損等遠期情況,以實現較為精準的術前規劃。之后,可考慮為患者個體化定制手術方案[13]、3D打印導板或假體[14]、使用計算機導航技術,實現精準化手術。

