經臍部單孔腹腔鏡術結合卵巢托底縫合重建術治療小兒卵巢成熟性畸胎瘤的效果
郭立華,李驥,王磊,孫權,張謙
(鄭州大學第一附屬醫院 小兒外科,河南 鄭州 450052)
兒童卵巢腫瘤較少見,總發病率為10萬分之2.6[1-3],卵巢成熟性畸胎瘤是一種生長緩慢但可能發生惡性轉變的腫瘤,是最常見的良性青春期前卵巢腫瘤[3]。卵巢成熟性畸胎瘤一旦發現后,應積極治療,避免出現急性扭轉、破裂及惡性變。既往應用常規三孔腹腔鏡于腹腔鏡下治療小兒卵巢成熟性畸胎瘤,2019年6月至2022年6月,鄭州大學第一附屬醫院小兒外科應用經臍部單孔腹腔鏡術結合卵巢托底縫合重建術治療小兒卵巢成熟性畸胎瘤,現報告如下。
1 對象與方法
1.1 研究對象
選取2017年1月至2022年6月在鄭州大學第一附屬醫院小兒外科接受微創手術治療的41例小兒卵巢成熟性畸胎瘤患兒,年齡2個月~14歲,中位年齡為82.0(63.5,123.0)個月。選取標準:術前檢查考慮囊性為主的卵巢成熟性畸胎瘤。排除標準:術前有腹部手術史;考慮存在腹腔及盆腔粘連;術前檢查提示實性成分為主的卵巢腫瘤或者惡性腫瘤;有麻醉及手術禁忌證。2例以陣發性腹痛急診入院,39例以發現腹部包塊入院,其中25例包塊巨大者有輕微腹痛癥狀,其中2例發現血尿并尿頻6 d,行CT檢查發現左下腹部囊性占位,左側輸尿管及膀胱受壓。41例術前均接受超聲和平掃加增強CT掃描檢查,提示卵巢囊性占位,囊內有少許實性及鈣化組織,41例患兒中左側28例,右側13例,無雙側病例。瘤體大小:3 cm×3 cm×4 cm~12 cm×12 cm×14 cm。全部患兒甲胎蛋白、人絨毛膜促性腺激素、乳酸脫氫酶、癌胚抗原、雌二醇和睪酮檢查均在正常范圍。41例患兒術前診斷均考慮為卵巢成熟性畸胎瘤,且均囊性成分為主,其中2例急腹癥急診入院患兒經急診綠色通道、醫生陪同行急診超聲及CT檢查后,考慮為卵巢囊性畸胎瘤合并蒂扭轉,行急診手術,其余患兒完善檢查后,均接受限期手術。本研究經鄭州大學第一附屬醫院醫學倫理委員會審批通過,倫理審批號:2021-KY-0908-002。2017年1月至2019年5月的19例患兒接受傳統腹腔鏡術治療,作為三孔組,2019年6月至2022年6月的22例患兒接受經臍部單孔腹腔鏡手術結合卵巢托底縫合重建術,作為經臍單孔組。兩組患兒一般資料比較差異無統計學意義(P>0.05)。見表1。

表1 兩組患兒一般資料比較
1.2 手術方法
1.2.1經臍單孔組
全部患兒接受靜脈吸入復合全麻并氣管插管或者喉罩。取平臥位,于臍部正中縱行切口,長約3 cm,依次切開臍部各層入腹,插入1個單孔腹腔鏡手術端口切口牽開器(30 mm),該牽開器由遠端環、近端環和圓柱形連接套筒組成。單孔腹腔鏡手術臍部端口有3個接入端口(1個10 mm端口和2個5 mm端口)以及2個進氣口。建立人工氣腹,壓力維持在8~12 mmHg(1 mmHg=0.133 kPa),置入2個5 mm Trocar和1個10 mm Trocar,進入30°腹腔鏡鏡頭探查,并置入2個無損傷抓鉗。調整患兒體位,頭低腳高位,使腹腔內腸管向頭端下移,便于充分暴露病灶,使卵巢腫瘤向頭端移動接近臍部。探查盆腔,探查子宮、雙側附件,辨認附件有無扭轉及壞死,辨認對側附件有無病變。若卵巢腫瘤合并扭轉,先立即鏡下進行復位,復位后觀察卵巢顏色變化,若血運恢復正常或明顯改善均給予保留。明確腫瘤來源,了解腫瘤大小、部位,了解腫瘤與盆腔內組織及器官有無粘連。患兒腫瘤均起源于卵巢,呈囊腫樣物。若瘤體巨大,腔鏡監視下,于單孔鞘管內進入一穿刺針,于囊腫卵巢門對側的部位穿刺進針,抽吸出黃色清亮囊液至囊腫變癟,抓鉗鉗夾瘤體囊壁至臍部下方,若瘤體較小,抓鉗直接鉗夾瘤體至臍部下方,而后直視下穿刺抽吸出囊液,取出3個Trocar,撤除氣腹,保留臍部切口牽開器,將卵巢腫瘤自端口切口牽開器內提出臍孔切口外,直視下用電刀切開卵巢皮質較薄處少許,可見卵巢部分實質被壓迫呈薄片狀,沿卵巢內部畸胎瘤表面小心剝離腫瘤,完整剝除瘤體,卵巢腺體血供豐富,需徹底止血,可應用雙極電凝止血,盡可能減少對殘余卵巢皮質、髓質的熱損傷,盡可能保護殘余的卵巢腺體及卵泡組織。過薄的卵巢皮質也需保留,應用5-0可吸收縫線于卵巢腔內髓質的基質組織由一端至另一端逐排橫行連續托底縫合,特別是出血及滲血處,不可貫穿縫合達皮質,避免損傷卵巢皮質,充分止血并消滅卵巢內的無效腔,避免術后卵巢腔內出血及形成血腫,將顯著膨大的卵巢腔一定程度縮小,重建卵巢。卵巢腔內不應放置止血紗布,避免吸收不徹底,影響日后卵泡生成及排卵。5-0可吸收縫線連續鎖邊或間斷縫合卵巢白膜切緣后將其還納入盆腔,重新建立氣腹,進鏡觀察2~3 min,確認殘留卵巢組織無出血及明顯滲血,退鏡并關閉氣腹,2-0可吸收縫線間斷縫合臍部腹白線,5-0可吸收縫線間斷縫合臍部切口。見圖1。

A為腹腔穿刺針經單孔鞘管內進入抽吸瘤體囊腔內囊液減壓;B為瘤體自臍孔的切口保護器內牽拉出并直視下剝除瘤體;C為5-0可吸收縫線于卵巢剩余皮質內由一端至另一端逐排橫行連續托底縫合,充分止血,消除無效腔并重建卵巢;D為重建后的卵巢還納入盆腔。
1.2.2三孔組
患兒取平臥位,于臍部正中縱行切開長約2 cm,依次切開臍部各層入腹,置入12 mm Trocar,建立人工氣腹,壓力維持在8~12 mmHg,進入30°腹腔鏡鏡頭探查,分別于平臍左右旁開3 cm取一長6~7 mm切口,直視下分別置入2個5 mm Trocar,腹腔內探查步驟同經臍單孔組,于瘤體表面卵巢組織最薄處將卵巢被膜及實質切開1~2 cm,提起卵巢組織,分離鉗分離瘤體,完整剝除并止血,將瘤體裝入取物袋,從臍部切口取出,必要時適當延長臍部切口。
1.3 觀察指標
本研究的術中及術后觀察指標包括手術時間、術中出血量、切口長度、術后出血例數以及住院時間。手術時間為開始切皮至縫合結束所用時間。術中出血量為估算的腹腔內操作和腹壁切口以及經臍部腹腔外操作的出血量總和。經臍單孔組切口長度為臍部單切口長度,三孔組切口長度為臍部切口加臍部兩側切口的總長度。住院時間為住院第1天至出院前1天的共計時間,出院當天不計算為住院天數。
1.4 統計學處理
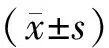
2 結果
2.1 術中基本情況
本組19例患兒順利完成傳統腹腔鏡卵巢腫瘤剔除術,22例患兒順利完成經臍部單孔腹腔鏡術結合卵巢托底縫合重建術,兩組無術中并發癥,未中轉開放手術。經臍單孔組均于臍部切口外直視下剝除瘤體及卵巢托底縫合重建,術中未發生卵巢漏斗韌帶及固有韌帶的撕裂出血,有6例年齡偏大患兒因臍部至盆腔距離延長,臍部切口暴露困難,故向下方延長5~10 mm后,將卵巢腫瘤牽拉至臍部切口外。2例卵巢畸胎瘤合并蒂扭轉,術中先行扭轉卵巢復位,復位后觀察卵巢血運顏色變化,1例血運明顯改善,1例有所改善,剝除瘤體并保留殘余卵巢。
2.2 術后基本情況
經臍單孔組術后切口基本隱藏于臍隱窩內,外觀較美觀,術后早期無并發癥發生,術后無卵巢血腫形成,無腹腔積血積液等并發癥。三孔組3例術后出現腹腔內出血,其中1例出血量較大,該患兒術后1 d出現腹痛、發熱及貧血癥狀,急查床旁超聲顯示患側卵巢體積增大,卵巢腔內巨大血腫形成,并有腹腔積液,立即給予輸血、補液及止血藥物,經積極治療,3 d后患兒病情穩定。兩組術后病理結果均為卵巢成熟性畸胎瘤。
2.3 圍手術期相關指標
兩組患兒手術時間、術后出血例數以及住院時間比較差異無統計學意義(P>0.05),術中出血量和切口長度比較差異有統計學意義(P<0.05),見表2。

表2 兩組術中及術后情況比較
2.4 隨訪結果
術后隨訪6~66個月,復查時所有患兒均接受彩超檢查,未見瘤體復發。術后3個月,32例彩超顯示雙側卵巢未見明顯異常,患側卵巢大小及血供均與正常側類似,9例患側卵巢體積較對側偏大,回聲增強,血供輕度減少。術后6個月復查超聲,41例卵巢全部顯示,大小及血運均已基本恢復正常,2例合并卵巢蒂扭轉的患兒術后未見卵巢萎縮及壞死,超聲可見卵泡回聲。
3 討論
根據細胞來源的不同卵巢腫瘤主要分為生殖細胞腫瘤、性索-間質腫瘤和上皮性腫瘤,成人以上皮性腫瘤為主,但是兒童以生殖細胞腫瘤為主,90%的兒童卵巢腫瘤被歸為良性腫瘤[4]。卵巢畸胎瘤來源于具有分化功能的生殖細胞,由外胚層、中胚層、內胚層3個胚層組織構成。卵巢畸胎瘤按照病理組織學類型分為成熟性、交界性、未成熟性,其中成熟性畸胎瘤是最常見的良性腫瘤,所占比率為95%[5]。本研究41例病理結果均診斷為卵巢成熟性畸胎瘤。
小兒卵巢成熟性畸胎瘤多表現為腹部巨大囊性包塊,一部分患兒體檢時發現,一部分患兒可出現并發癥,如卵巢腫瘤扭轉、壓迫腸管、壓迫輸尿管、瘤體破裂、血性腹膜炎等。故小兒卵巢成熟性畸胎瘤一旦發現需完善檢查,明確診斷后應積極手術切除。合理開展治療的關鍵是術前準確判斷卵巢腫瘤的性質,腫瘤性質的判斷也直接影響患兒預后[6]。如果術前判斷為良性腫瘤,可采取微創手術完整剝除腫瘤,最大程度保留患側卵巢組織,有利于最大限度保留生育能力。如果為惡性腫瘤,則需徹底切除腫瘤及卵巢,最大限度避免腫瘤破潰,探查腹腔進行手術并進行分期評估,惡性卵巢腫瘤的首選術式仍然是開放手術[7]。術前一定要結合超聲、CT或MRI以及腫瘤標志物鑒別卵巢腫瘤的良惡性,可根據術前診斷選擇合適的手術方式。腫瘤標志物在兒童卵巢良惡性腫瘤評估中具有重要的診斷價值,對判斷療效及預后有重要意義,同時腫瘤標志物也與卵巢腫瘤類型有一定相關性[8]。絕大部分卵巢成熟性畸胎瘤患兒的腫瘤標志物指標在正常范圍內。以實質成分為主的卵巢腫瘤惡性概率較高,囊性腫瘤則良性居多,但文獻報道有約22%的卵巢惡性腫瘤也可能不含實質成分[9]。CT和MRI對腫瘤內特殊成分的識別有助于診斷卵巢成熟性畸胎瘤,如鈣化的骨骼、毛發、脂肪等成分。因此采用腹腔鏡手術治療兒童卵巢腫瘤,一定要掌握好手術指征,排除卵巢惡性腫瘤。
本研究早期應用常規三孔腹腔鏡于腹腔鏡下治療小兒卵巢成熟性畸胎瘤,因瘤體普遍較大,小兒腹腔空間相對成人較小,操作空間受限,發現與開放手術相比,鏡下剝除瘤體、止血及縫合相對困難,卵巢為腺體組織,血供豐富,鏡下精細縫合重建卵巢要求較高的微創手術水準,難度明顯大于開放手術。有些病例鏡下操作困難,尚需要在腹壁上增加輔助操作孔,進一步增加了腹壁的切口創傷。2019年6月至2022年6月,團隊應用經臍部單孔腹腔鏡術結合托底縫合卵巢重建術治療22例小兒卵巢成熟性畸胎瘤,術中操作難度降低,手術安全性增加,也具備較好的切口微創美容效果,同時獲得良好的手術效果。小兒腹腔和盆腔相對較淺,卵巢蒂相對較長,卵巢腫瘤活動度大且游離無粘連,小兒臍部相對較大,臍部腹壁相對較薄,青春期前小兒卵巢位于真性骨盆以上,即位于腹腔內,與臍部距離較短,以上獨特的解剖因素使單孔腹腔鏡輔助下經臍部將卵巢成熟性畸胎瘤提出切口外剝除成為可能。臨床治療中發現年齡偏大患兒及肥胖腹壁脂肪較厚患兒經臍部提出卵巢腫瘤的難度加大,需要向臍環下方適當延長切口。術中牽拉卵巢腫瘤時務必要輕柔用力,避免暴力強行牽拉,引起卵巢固有韌帶撕裂或斷裂,出現卵巢血管損傷及出血。經臍部單孔腹腔鏡操作通道內進入穿刺針抽吸腫瘤囊腔內液,避免了經腹壁進入穿刺針,減少了創傷及污染的概率,同時穿刺減壓,使瘤體囊腔縮小后能從臍部提出。本組22例手術中,于臍孔外直視下剝除瘤體與卵巢重建時,術者與助手均使用頭戴式手術放大眼鏡,清晰地辨別瘤體與卵巢實質的交界,徹底剝除瘤體,并最大程度地保留卵巢實質及功能。術中可選用雙極電凝代替常規電刀止血,但需要盡可能降低殘留卵巢實質的熱損傷,避免過度損傷卵巢的皮質及髓質。與三孔組相比,經臍單孔組手術時間較短,切口長度較小,術中出血量較少,術后出血的并發癥更低,其中切口長度及術中出血量有差異,手術時間、術后出血、并發癥例數無差異,但是經臍單孔組的手術時間更短,術后出血例數更少。
卵巢為腺體組織,髓質與卵巢門相連,含有豐富的血管、神經、淋巴管及疏松結締組織。卵巢血運極其豐富,總結3例術后出血的經驗教訓,術中務必在不過多損傷卵巢實質的同時精細徹底止血。為了預防術后出現卵巢腔內出血,本研究應用5-0可吸收縫線于卵巢腔內剝離創面由一端至另一端逐排橫行連續托底縫合,縫合深度僅達髓質,尚未貫穿縫合達皮質,最大程度保護卵巢皮質,止血并消除無效腔,最大程度上避免了術后出現卵巢腔內出血及血腫形成的可能,同時,也在一定程度上縮小了異常膨大的卵巢腔體積,有利于卵巢術后的形態及功能的恢復。
國內外有較多關于單孔腹腔鏡治療兒童卵巢成熟性畸胎瘤報道,但未見關于托底縫合重建卵巢的研究報道。沈剛等[10]研究顯示,22例患者接受單孔腹腔鏡兒童卵巢囊腫蒂扭轉復位術及經臍部腹腔外囊腫剝除術后隨訪3~36個月,超聲檢查無卵巢萎縮及囊腫復發。賽愷等[11]應用單孔腹腔鏡于腹腔鏡下治療24例小兒良性卵巢畸胎瘤,手術均成功,無復發。黃華等[12]報道經臍單通道腹腔鏡輔助治療9例小兒卵巢囊腫,效果滿意,無復發。Lee[13]報道采用快速防滲漏臍部單切口腹腔鏡輔助切除術治療7名育齡期及3名青少年女性巨大卵巢囊腫,未發生腫瘤內容物腹腔內滲漏及術后并發癥。Pecorelli等[14]發現采用腹腔鏡輔助經下腹部小切口行無滲漏體外引流治療卵巢大型囊性腫瘤是一種安全可行的方法。腹腔鏡輔助經臍部單切口手術集合了腹腔鏡技術和傳統開放手術操作的優勢,將腔鏡探查診斷與傳統手術操作整合于單一切口,避免了盲目的開放式剖腹手術,也減少了腹腔內切除瘤體可能導致的瘤體破潰及腹腔感染的可能性,直視下操作更加精準,同時又具有腔鏡手術切口小、損傷小、出血少、術后恢復快、切口疼痛輕及切口感染率低的優點。但是需掌握手術指征,對于既往有盆腔手術史、腹腔粘連嚴重者,卵巢蒂扭轉壞死與周圍組織粘連嚴重、卵巢組織質地脆易破潰及出血者,術前卵巢實性腫瘤或術前考慮為卵巢惡性腫瘤者,過度肥胖患兒,不建議行腹腔鏡輔助經臍部切除術式。
本研究41例卵巢腫瘤均未接受卵巢切除術,盡可能多地保留卵巢實質,其中2例卵巢腫瘤合并扭轉的患兒復位后,卵巢血運明顯改善和有所改善,在完整切除瘤體的基礎上,最大限度保留了卵巢殘余實質。術后6個月復查超聲顯示卵巢體積及血運基本恢復正常。目前國內外研究都普遍認為在確保卵巢腫瘤最佳切除和遠期預后的基礎上,應最大限度保留卵巢組織,重視卵巢腫瘤患兒術后遠期的生育和激素功能,減少性激素異常和不育的發生[4,6,15]。Yasui等[16]報道的大規模人群隊列研究表明,卵巢切除術對女性生育能力以及心理和激素健康具有重要的長期不利影響。
4 結論
與傳統腹腔鏡術相比,經臍部單孔腹腔鏡術結合卵巢托底縫合重建術治療小兒卵巢成熟性畸胎瘤的手術操作難度降低,術后出血發生率降低,安全可靠,效果確切,同時也具備較好的切口微創美容效果。

