Rapidplan優化模塊在胸上段食管癌容積旋轉調強計劃中的應用
劉曉男,戚文慧,程秀艷,劉曉,李兵,毛榮虎
(鄭州大學附屬腫瘤醫院/河南省腫瘤醫院 放療科,河南 鄭州 450008)
治療計劃設計是放射治療的核心,其通過計劃系統模擬患者體內的劑量分布,預測和評估實際治療中的情況,有助于放射治療的安全性和有效性,并最大程度地減少對正常組織的影響。醫療人員的經驗和技術水平不同,不同級別的醫院和不同的物理師(劑量師)針對同一病例設計的放療計劃在質量上存在較大差異。這可能會降低部分患者的腫瘤控制率或增加不必要的正常組織并發癥的概率。為了解決這一問題,醫生采用“基于經驗放療”或“基于模型放療”的放療計劃設計方案,利用技術手段提高放療計劃的質量。其中,瓦里安Eclipse V15.5計劃系統的Rapidplan模塊是一種基于先驗知識的機器學習方法,通過提取和分析模型庫中靶區和危及器官的空間位置信息以及劑量分布信息預測放療計劃。研究表明,Rapidplan模塊在頭頸、肺、乳腺、肝、前列腺等部位已初步應用[1-5],并能達到或者超過傳統人工設計的計劃,降低物理師經驗水平等主觀因素對計劃的影響。國內關于食管癌自動計劃的研究較少。本研究使用Rapidplan優化模塊建立了胸上段食管癌容積旋轉調強放療計劃的訓練模型,并利用該模型對另外10例胸上段食管癌患者的容積旋轉調強放療計劃進行了測試。通過比較人工制定的放療計劃和經過Rapidplan優化模塊自動優化的放療計劃,探索Rapidplan優化模塊在胸上段食管癌容積旋轉調強放療計劃中的可行性和潛在優勢。
1 對象與方法
1.1 研究對象及模型庫創建
選擇2018年1月至2020年6月在河南省腫瘤醫院瓦里安Truebeam加速器上接受容積旋轉調強(volumetric modulated arc therapy,VMAT)治療的50例胸上段食管癌患者作為研究對象。依據國際輻射單位與測量委員會52和62號報告的勾畫標準,給予腫瘤計劃靶區(planning target volume,PTV)60 Gy/30f的處方,治療計劃均經過嚴格的審核并執行。創建Eclipse Rapidplan模型數據庫,并將50例計劃逐一導入。所有計劃均為3個全弧VMAT計劃,2個弧照射整個靶區,并設置240°~300°和60°~120°不出束,另外1個弧小機頭旋轉90°只照射鎖骨上部分。
1.2 模型訓練
在模型庫訓練過程中,基于病例的危及器官和靶區的空間位置關系以及劑量分布,劑量體積直方圖(dose and volume histogram,DVH)預測模型會將靶區和危及器官之間的空間位置關系分割成葉片漏射區、射野外、射野內、射野內和靶區重合等不同區域。在建立各個危及器官的預測模型時,通過提取和計算這些不同區域的體積、DVH和幾何預期劑量來完成。模型訓練完成后,通過查看各個危及器官(organ-at-risk,OAR)和靶區的模型分析報告,以及一些統計學圖表(如回歸曲線、殘差表曲線)來評估模型庫的質量。在統計曲線中,對出現的幾何和劑量異常值以及擬合強影響點進行嚴重程度、原因分析和處理。幾何異常值的產生可能與靶區或危及器官的形狀、體積是否明顯異于其他患者以及肺在呼氣末或吸氣末的位置等因素有關。劑量異常值的產生可能與對危及器官的限制過于嚴格或過于松散,以及臨床要求與其他病例存在較大差異等因素有關。在對模型庫中的離群值進行綜合分析和處理后,需要對模型庫進行再訓練,以達到各個危及器官擬合優度較高的模型。
1.3 模型獨立驗證測試
隨機選取10例未納入模型訓練的胸上段食管癌患者,靶區勾畫和處方與模型訓練時采用的訓練集保持同樣的標準,劃分為人工計劃(traditional manual plan,RG)和經Rapidplan優化的計劃(Rapidplan automatic optimization plan,RP)。兩組計劃的布野條件、射線能量、治療機器,治療技術和處方一致。
1.4 計劃評估和比較
靶區:滿足100%的處方劑量覆蓋95%的PTV,通過適形指數(conformity index,CI)和均質性指數(homogeneity index,HI)2個參數進行評價RP計劃和RG計劃的優劣。CI的計算公式為:
式中:ICI為適形指數,Vt,ref為參考等劑量線面所包繞的靶區體積,Vt為靶區體積,Vref為參考等劑量線面所包繞的體積。CI值范圍是 0~1,值越接近1,表示適形度越好。
HI的計算公式為:
式中:IHI為均質性指數,D2為PTV 2%體積接受的劑量,D98為PTV 98%體積接受的劑量,D50為PTV 50%體積接受的劑量。HI越接近于0,均勻性越好。
危及器官:比較RP計劃和RG計劃的脊髓外擴結構(脊髓外擴0.4 mm)最大點劑量(Dmax),左右肺和總肺的體積劑量指標(V5、V10、V20、平均劑量)和心臟的平均劑量(Dmean)。
1.5 統計學方法
將RP計劃和RG計劃導入MIM系統中,將兩組計劃的DVH數據信息導出。將兩組計劃每個參數的絕對體積劑量轉化為相對體積劑量。根據相對體積劑量信息繪制RP計劃和RG計劃的DVH圖。采用SPSS 22.0統計軟件,兩組數據采用配對t檢驗的方法,結果用均數±標準差表示,P<0.05表示有統計學差異。
2 結果
2.1 靶區劑量學
RP計劃和RG計劃均能滿足臨床要求。與RG計劃相比,RP計劃靶區的CI提高,HI降低,差異有統計學意義(P<0.05)。兩種計劃的D2和D50差異無統計學意義(P>0.05),D98的差異有統計學意義(P<0.05)。靶區的具體劑量學指標見表1、圖1。

A、B、C為RG計劃;D、E、F為RP計劃。
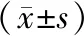
表1 RP計劃和RG計劃的靶區劑量學比較
2.2 危及器官的劑量學
與RP計劃相比,RG計劃在左肺、右肺、肺總的V5、V10、V20、Dmean和心臟的Dmean差異無統計學意義(P>0.05)。脊髓外擴結構的Dmax差異有統計學意義(P<0.05)。見表2。
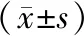
表2 RP計劃和RG計劃的危及器官的劑量學比較
2.3 計劃的優化和執行效率
RP計劃在優化時調整的次數較少,在第一步和第二步保持優化2次,優化時間平均為(15.3±2.7)min,RG計劃在優化時調整次數相對較多,對于靶區和脊髓的Dmax花費更多的時間,平均優化時間為(20.2±3.2)min。兩組計劃的優化時間差異有統計學意義(P<0.05)。兩組計劃的MU數差異無統計學意義(P>0.05),執行效率相當。見表3。

表3 RP計劃和RG計劃的MU數比較
2.4 RP計劃與RG計劃DVH圖
RP計劃與RG計劃在臨床靶區(clinical tumor volume,CTV)、PTV、左肺、右肺、總肺和心臟的劑量體積曲線差異無統計學意義,脊髓外擴結構的Dmax及其高劑量區的體積差異有統計學意義。見圖2。兩組計劃左肺、右肺、總肺和心臟的具體劑量體積指標(V5、V10、V20)差異無統計學意義。見圖3。

圖2 RP計劃和RG計劃DVH圖

圖3 RP計劃和RG計劃的危及器官具體DVH指標
3 討論
多個平臺上的實驗數據表明,基于模型的放療計劃不僅可以幫助物理師及時發現并改進欠佳的計劃,還可以實現半自動計劃設計,提高工作效率[6-8]。高水平醫院可以利用其優質的放療計劃來訓練成熟的模型,并將其移植到其他醫院的同類型計劃系統中[9-10],為后者的治療提供患者個體化優化參數基準值,從而協助改進計劃質量。這樣不僅可以縮小醫院及物理師之間計劃設計質量差異,還可以使更多的患者受益。
本研究的結果顯示,RP計劃在靶區和其他危及器官受量相當的情況下,降低了脊髓外擴結構的受量。在計劃效率方面,RP計劃的優化時間更短。原因在于RP計劃采用的Rapidplan優化是基于解剖結構和先驗知識的AI方法。在優化時提供了模板庫給予的OAR預測區間進行參考,而模板庫的計劃都是經過挑選的優質計劃,集中了不同物理師的共同智慧,對危及器官的優化按照區間的下限為目標進行優化,能夠避免因為物理師經驗不足而導致的計劃質量不高,在計劃質量相當的情況下,能夠更快達到優化目標。
本研究中RP計劃的HI稍差于RG計劃,主要是因為D2相當的情況下,D98不如RG計劃。總結發現,RG計劃的Dmax有幾例大于110%,而RP計劃均小于110%,可能是由于RG計劃沒有刻意壓Dmax導致PTV的D98略好于RP計劃。RP計劃脊髓外擴結構的Dmax降低,這種現象的原因在于脊髓的劑量限制相對容易實現,物理師在滿足要求后沒有刻意再去限制其劑量。相比之下,自動計劃可以基于最相似病例的函數來對脊髓進行更嚴格的限制[11],從而更有效降低其受照劑量。心臟和肺的受量兩種計劃差異無統計學意義,這可能是因為所選研究病例為胸上段食管癌,靶區下界在隆突處,涉及心臟層面較少,未增加計劃優化的難度,無論是RP計劃還是RG計劃都沒有以較高權重限制心臟的體積劑量。而左右肺由于兩種計劃均在左右側規避60°的弧度進行照射,肺的受照射區域受到同樣的限制,且由于靶區較短,規避照射之后肺的限制條件相對容易實現。
Fogliata等[12]研究表明,將Rapidplan應用于肺癌和前列腺癌計劃優化時,可降低周圍正常組織的受照量,提高臨床計劃的通過率。Hussein等[13]研究也表明,在優化盆腔放療計劃時,Rapidplan比人工臨床計劃效果更好。Hansen等[14]將自動計劃應用于頭頸部腫瘤計劃設計,發現在無人工干預的情況下,94%的自動計劃質量超過或類似于人工計劃。本研究的結果與這些研究類似,即在保證靶區和其他危及器官受量相當的情況下,通過降低脊髓的受照劑量,進一步提高了治療的安全性和有效性。
本研究中RP計劃和RG計劃在優化時均采用了一樣的規避角度,下一步的研究方向為當RP計劃不規避或者少規避一定的弧度數,能否依靠優質計劃建立的模板庫來實現與規避較大弧度數的RG計劃相當的靶區劑量分布和危及器官體積劑量。另外,本研究的研究對象是胸上段食管癌,靶區相對全段食管癌小。全段食管癌的計劃難度較大,危及器官相對更難以實現,如能建立優質的模板庫實現自動計劃,將有更大的臨床意義,這也是未來的研究目標。
4 結論
模板庫的Rapidplan模塊在優化胸上段食管癌VMAT計劃時,能夠高效完成臨床要求。因此,在優化胸上段食管癌VMAT計劃時,推薦使用Rapidplan模塊自動優化,但在建立模板庫的時候,要挑選優質的人工計劃來訓練模型。

