某院113 例小分子蛋白激酶抑制劑不良反應分析*
戴 麗,王鳳玲,邢海燕,汪星輝,孟祥云
(安徽省合肥市第二人民醫(yī)院,安徽 合肥 230011)
蛋白激酶是細胞生命活動的重要信號使者,參與細胞增殖、凋亡、神經傳導等生理過程[1],現(xiàn)已成為新型抗腫瘤藥物研發(fā)的重要靶點。截至2021年,美國食品和藥物管理局(FDA)已批準68 種小分子蛋白激酶抑制劑[2],我國也自主研發(fā)并上市多個小分子蛋白激酶抑制劑[3]。由于小分子蛋白激酶抑制劑上市時間較短,缺乏基于真實世界的藥品上市后安全性評價,若產生嚴重藥品不良反應(ADR),可導致停藥甚至危及生命[4-5],故應重點關注其ADR。本研究中分析了我院小分子蛋白激酶抑制劑ADR 發(fā)生的規(guī)律及特點,為臨床合理應用提供參考。現(xiàn)報道如下。
1 資料與方法
收集我院2018 年1 月至2021 年12 月上報國家藥品不良反應監(jiān)測中心且關聯(lián)性確認為肯定、很可能、可能的ADR 報告,篩選出小分子蛋白激酶抑制劑的報告113 份。采用回顧性研究方法,按藥品主要作用靶點分類,對患者的性別、年齡、原患疾病、藥品品種、ADR 累及系統(tǒng)/器官、臨床表現(xiàn)、治療及轉歸等進行統(tǒng)計與分析。ADR 關聯(lián)性評價標準和嚴重程度分級均以《藥品不良反應報告和監(jiān)測管理辦法》[6]為依據。
2 結果
2.1 患者性別與年齡分布
共納入113份ADR 報告,涉及患者113例。其中,男63 例(55.75%),女50 例(44.25%);年齡30~87 歲,平均(67.8±13.7)歲。詳見表1。
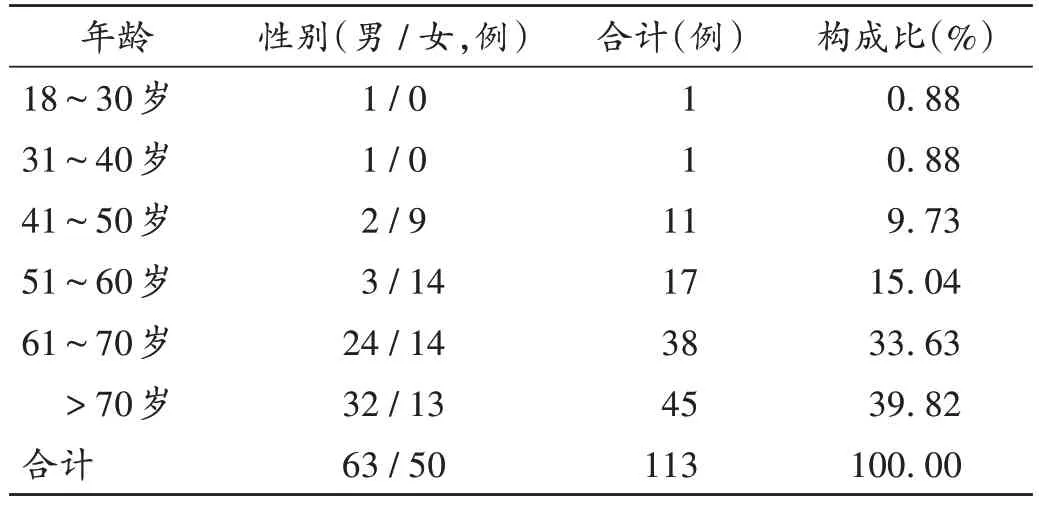
表1 患者年齡與性別分布(n=113)Tab.1 Age and gender distribution of patients(n=113)
2.2 ADR 報告主體
113 份ADR 報告中,醫(yī)師上報93 份(82.30%),藥師上報18份(15.93%),護士上報2份(1.77%)。
2.3 小分子蛋白激酶抑制劑用藥情況
113 份ADR 報告中,呼吸系統(tǒng)腫瘤用藥42 份,消化系統(tǒng)腫瘤用藥39 份,生殖系統(tǒng)腫瘤用藥8 份,乳腺癌用藥7份,血液系統(tǒng)腫瘤用藥3份,泌尿系統(tǒng)腫瘤用藥2份,其他腫瘤用藥12 份。小分子蛋白激酶抑制劑超適應證用藥27 例(23.89%),其中阿帕替尼24 例(21.24%)。詳見表2。

表2 小分子蛋白激酶抑制劑超適應證用藥統(tǒng)計Tab.2 Statistics on off-label use of small molecule protein kinase inhibitors
2.4 引起ADR 的小分子蛋白激酶抑制劑品種及相關ADR 發(fā)生情況
113 份ADR 報告中,共涉及9 種小分子蛋白激酶抑制劑。其中,血管內皮細胞生長因子受體(VEGFR)抑制劑70 份,表皮生長因子受體(EGFR)抑制劑40 份,布魯頓酪氨酸激酶(BTK)抑制劑2份,BCR-Ab1抑制劑1份。詳見表3。

表3 引起ADR的小分子蛋白激酶抑制劑品種及相關ADR發(fā)生情況(n=113)Tab.3 Varieties of small molecule protein kinase inhibitors those induced ADRs and the incidence of related ADRs(n=113)
2.5 ADR 發(fā)生時間
113 例患者中,91 例(80.53%)的ADR 發(fā)生在用藥后1個月內,其中2例(1.77%)發(fā)生在用藥后30 min內;12 例(10.62%)發(fā)生在用藥后1~3 個月;9 例(7.96%)發(fā)生在用藥后4~6 個月;1 例(0.88%)發(fā)生在用藥后6~9個月。
2.6 ADR 累及系統(tǒng)/器官與臨床表現(xiàn)
113 例患者發(fā)生ADR 121 例次,小分子蛋白激酶抑制劑相關ADR 累及多個系統(tǒng)/ 器官,以皮膚及其附件損害(27.27%)最常見,臨床主要表現(xiàn)為皮疹、瘙癢、手足綜合征等;其次為消化系統(tǒng)(23.97%),臨床主要表現(xiàn)為肝功能損傷、腹瀉、惡心嘔吐等。詳見表4。
2.7 ADR 關聯(lián)性評價、程度分級及預后與轉歸
113 份ADR 報告中,關聯(lián)性評價為可能33 份,很可能73 份,肯定7 份。93 例患者經停藥或對癥處理后痊愈或好轉;14例患者因出院后隨訪失聯(lián),轉歸情況不詳;6例患者耐受ADR 故未停藥,繼續(xù)觀察后未見好轉。小分子蛋白激酶抑制劑致新的或嚴重ADR見表5。

表5 小分子蛋白激酶抑制劑致新的或嚴重ADRTab.5 New and severe ADR induced by small molecule protein kinase inhibitors
3 討論
3.1 患者基本情況分析
113例小分子蛋白激酶抑制劑致ADR患者中,男性多于女性,與全球腫瘤發(fā)病率的趨勢一致[7],可能與男性化學治療時ADR 的發(fā)生率高于女性有關[8];以不低于61 歲的老年患者為主(73.45%),老年患者各臟器功能衰退,影響藥物的代謝與排泄,易致藥物在體內蓄積,增加ADR 的發(fā)生風險。因此,臨床藥師需加強此類患者的用藥監(jiān)護。
3.2 ADR 報告主體
該院ADR 上報主體為藥師的占比為15.93%,低于《國家藥品不良反應監(jiān)測年度報告(2022 年)》中藥師上報率25.8%的水平。未報、漏報ADR 的原因可能為ADR無上報的必要性及醫(yī)護人員發(fā)現(xiàn)ADR未與臨床藥師商討有關。因此,增加臨床藥師的人員配備和在臨床的工作時間,鼓勵臨床藥師密切監(jiān)測患者用藥后的反應,以盡早發(fā)現(xiàn)ADR并提供處理意見。
3.3 超適應證合理性分析
《新型抗腫瘤藥物臨床應用指導原則(2022 年版)》[9]規(guī)定,抗腫瘤藥物使用須遵循藥品說明書。但腫瘤治療缺乏有效治療標準,尤其是腫瘤晚期在常規(guī)治療失敗后,臨床超藥品說明書用藥可延緩疾病進展,超藥品說明書用藥現(xiàn)象普遍存在[10]。我院小分子蛋白激酶抑制劑超適應證用藥27 例(23.89%),且以阿帕替尼為主。國家藥品監(jiān)督管理局(NMPA)批準阿帕替尼的適應證包括晚期胃腺癌或胃食管結合部腺癌、肝細胞癌。《原發(fā)性肺癌診療指南(2022年版)》[11]未建議阿帕替尼用于非小細胞肺癌,僅文獻[12 - 13]報道阿帕替尼治療非小細胞肺癌。但循證醫(yī)學證據級別較低,臨床應慎用。同時,檢索發(fā)現(xiàn)阿帕替尼治療乳腺癌、卵巢癌、結直腸癌等惡性腫瘤均為單中心回顧性研究[14-16],有待開展更大樣本的臨床試驗進一步評價其療效及安全性。我院阿帕替尼超適應證用藥現(xiàn)象普遍,與國內其他醫(yī)療機構報道的臨床應用情況類似[17-18],可能與其抗腫瘤機制和廣泛的Ⅱ/Ⅲ期臨床試驗研究相關。醫(yī)院今后應加強超適應證用藥的管理,限制無循證醫(yī)學證據的超適應證用藥行為,保障患者用藥安全。
113 份ADR 報告中涉及9 種抗腫瘤藥物,以阿帕替尼為主,可能與該院收治的患者多為胃癌有關,也可能與患者多線治療后超適應證給藥有關[18]。阿帕替尼作為靶向藥物口服制劑,患者依從性高,且治療費用低。因此,醫(yī)師在臨床治療中應提高安全用藥意識,降低用藥風險;臨床藥師應加強藥學監(jiān)護,提高患者的治療依從性和用藥安全性。
3.4 ADR 發(fā)生時間
本研究中納入的小分子蛋白激酶抑制劑相關ADR多發(fā)生于用藥后1 個月內(80.53%),與文獻[19]的研究結果一致;未見患者在用藥12個月以后發(fā)生ADR。另外,2例患者在用藥后30 min內發(fā)生ADR。因此,建議臨床醫(yī)師和藥師在患者用藥后應密切監(jiān)測ADR 的發(fā)生情況,對于長期應用小分子蛋白激酶抑制劑發(fā)生ADR 的情況仍需作進一步研究以確認。
3.5 ADR 累及系統(tǒng)/器官
皮膚毒性反應是不同靶點小分子蛋白激酶抑制劑的常見ADR,如VEGFR 抑制劑可誘發(fā)手足綜合征[20];EGFR 抑制劑常引發(fā)皮疹、瘙癢等[21]。皮膚毒性反應的機制目前尚不明確,可能與正常皮膚組織中存在的VEGFR,EGFR 等藥物作用靶點被抑制進而影響細胞分化、表皮生長、創(chuàng)面愈合有關[22]。多數皮膚相關的ADR呈劑量依賴性和自限性,治療方案依據皮疹的嚴重程度制訂,輕癥對癥治療,重癥給予減量或停藥[23]。本研究中發(fā)現(xiàn)1例嚴重的皮膚ADR。80歲左肺腺癌男性患者應用阿帕替尼聯(lián)合卡瑞利珠單抗治療5 d 后,全身皮疹面積占體表面積的50%~60%,發(fā)生嚴重皮疹伴瘙癢后入院治療,停用阿帕替尼及卡瑞利珠單抗,給予糖皮質激素和抗過敏藥物等對癥治療,10 d后皮疹基本消退。因此,應用小分子蛋白激酶抑制劑治療時,臨床藥師要加強用藥宣教,囑患者注意避光防曬,保持皮膚干凈與潤濕。
消化系統(tǒng)反應也是小分子蛋白激酶抑制劑常見的ADR,臨床主要表現(xiàn)為肝功能損傷、腹瀉、惡心嘔吐等,可能與此類藥物多為口服制劑有關[24]。本研究中收集12 例次肝功能損傷,均為輕型,可能與臨床已廣泛關注肝毒性,特別是舒尼替尼、拉帕替尼等藥品說明書均已將肝毒性作為黑框警示有關。因此,臨床應用小分子蛋白激酶抑制劑治療前及治療過程中均應密切監(jiān)測肝功能,及時發(fā)現(xiàn)異常并給予干預,可減少和避免嚴重的肝臟毒性事件發(fā)生。
3.6 新的及嚴重ADR
1份吉非替尼引起流淚異常的ADR,目前其藥品說明書及文獻報道中均未提及。該患者患左肺腺癌,2019 年1 月29 日起給予CP 方案(培美曲塞+順鉑)2 個周期后無法耐受,同時基因檢測結果顯示EGFR 基因21 外顯子突變,3月17日調整治療方案為口服靶向藥物吉非替尼(0.25 g、每天1 次);7 月1 日再次入院時患者訴服用吉非替尼1~2 h 后流淚不止,無其他不適,繼續(xù)服用吉非替尼,流淚較前無明顯改善;臨床藥師根據我國ADR關聯(lián)性評價方法[25],分析流淚異常與吉非替尼可能有關。查閱文獻[26],發(fā)現(xiàn)1 例被診斷為EGFR 基因突變的肺腺癌的86 歲女性患者,接受2 個月的吉非替尼(0.25 g、每天1次)治療后出現(xiàn)雙側角膜神經營養(yǎng)潰瘍,一側已穿孔,可能與角膜緣和結膜上皮基底細胞中的EGFR 被抑制進而抑制上皮細胞的遷移和增殖導致眼毒性有關[27]。眼毒性罕見但可造成不可逆的損傷,極大地降低了患者的生活質量,故用藥過程中應重點關注。
2份嚴重ADR報告為伊布替尼致Ⅳ級血小板減少。伊布替尼引發(fā)血小板減少非常常見(≥20%),一項真實世界研究報道,伊布替尼單藥治療慢性淋巴細胞白血病引發(fā)Ⅲ- Ⅳ級血小板減少達6.76%[28]。可能的機制為伊布替尼選擇性抑制血小板信號傳導進而影響血小板對血管性血友病因子的黏附功能[29]。臨床應用伊布替尼時患者出血發(fā)生率較高,故臨床藥師應密切監(jiān)測患者的凝血功能和出血體征,輕度出血予對癥處理和保護措施,同時告知患者在服藥期間避免應用魚油、維生素E等抑制血小板的藥物。
隨著小分子蛋白激酶抑制劑在臨床的廣泛應用,其ADR 逐漸顯現(xiàn),臨床應用初期應重點監(jiān)測患者的皮膚及其附件損害、消化系統(tǒng)損害等,同時還要警惕新的ADR 的發(fā)生。本研究結果顯示,多數小分子蛋白激酶抑制劑所致ADR 是可預防和控制的,經停藥或對癥處理后可痊愈或好轉。因此,臨床藥師應加強宣教,做到早識別、早干預,以提高患者治療的依從性和有效性,保障患者用藥安全。

