懷菊花總黃酮富集純化工藝優(yōu)化及其抗炎活性、成分組成研究
鄧曉顏王小蘭李 孟張 莉李玉賢*鄭曉珂馮衛(wèi)生
(1.河南中醫(yī)藥大學(xué)藥學(xué)院,河南 鄭州 450046;2.河南省中藥開(kāi)發(fā)工程技術(shù)研究中心,河南 鄭州 450046)
懷菊花為菊科植物菊Chrysanthemum morifoliumRamat.的干燥頭狀花序,具有清熱解毒、清肝明目功效,為河南道地藥材四大懷藥之一[1]。課題組前期對(duì)懷菊花及其莖葉化學(xué)成分進(jìn)行研究,發(fā)現(xiàn)大量黃酮類(lèi)化合物[2-3],并對(duì)其抗炎活性進(jìn)行篩選[4-5]。
中藥具有多成分、多靶點(diǎn)、多途徑的特點(diǎn),其有效部位是發(fā)揮療效的物質(zhì)基礎(chǔ),故如何富集以增強(qiáng)臨床療效是相關(guān)研究的關(guān)鍵[6]。黃酮作為懷菊花主要成分,具有抗氧化[7]、降血壓[8]作用,并且菊花清熱解毒功效與抗炎作用有一定相關(guān)性[9],活性成分主要為黃酮[10],故對(duì)其富集純化有助于挖掘藥材更多藥用價(jià)值。
目前,關(guān)于懷菊花總黃酮的研究主要集中在提取工藝、含量測(cè)定方面[11-12],鮮有涉及純化方面。因此,本實(shí)驗(yàn)采用AB-8 型大孔吸附樹(shù)脂[13]對(duì)懷菊花總黃酮進(jìn)行富集純化,響應(yīng)面法優(yōu)化工藝,并通過(guò)氧化型低密度脂蛋白(ox-LDL) 誘導(dǎo)的HUVECs增殖細(xì)胞模型來(lái)評(píng)價(jià)抗炎活性,HPLC 法來(lái)分析成分組成,以期為綜合開(kāi)發(fā)該成分提供科學(xué)依據(jù)。
1 材料
1.1 儀器 DZTW 型調(diào)溫電熱套(上海力辰邦西儀器科技有限公司);NVP-1000 型隔膜真空泵、OSB-2000 型旋轉(zhuǎn)蒸發(fā)儀、A-1000S 型水流抽氣機(jī)、FDU-2110 型冷凍干燥機(jī)、CA-1116A 型冷卻水循環(huán)裝置(上海愛(ài)朗儀器有限公司);SHH.W21.420型智能恒溫水箱(北京市長(zhǎng)風(fēng)儀器儀表公司);EVOLUTION300 型紫外可見(jiàn)分光光度計(jì)(美國(guó)賽默飛世爾科技公司);BSA224S 型電子天平[賽多利斯科學(xué)儀器(北京) 有限公司];Forma 3111 細(xì)胞培養(yǎng)箱 (美國(guó)Thermo Fisher Scientific 公司);TS100 倒置顯微鏡 (日本Nikon 公司);Milli-Q Advantage A10 超純水儀(美國(guó)Millipore 公司);全波長(zhǎng)酶標(biāo)儀(美國(guó)BioTek 公司);Centrifuge-5804R小型高速低溫冷凍離心機(jī)(德國(guó)Eppendorf 公司);SW-CJ-2FD 超凈工作臺(tái)(蘇州安泰空氣技術(shù)有限公司)。
1.2 試劑與藥物 蘆丁對(duì)照品(批號(hào)B20771,上海源葉生物科技有限公司)。亞硝酸鈉、硝酸鋁(天津市風(fēng)船化學(xué)試劑科技有限公司);氫氧化鈉(成都市科隆化學(xué)品有限公司)。AB-8 型吸附樹(shù)脂(滄州寶恩吸附材料科技有限公司)。ox-LDL (批號(hào)YB-002-1,廣州奕源生物科技有限公司);IL-1β、IL-6、TNF-α ELISA 檢測(cè)試劑盒 (批號(hào)KE00021,KE00139,KE00154,武漢三鷹生物科技有限公司);CCK-8 (批號(hào)CA1210)、青霉素-鏈霉素-慶大霉素混合溶液(批號(hào)P1410) (北京索萊寶科技有限公司);DMEM (批號(hào)2338234,美國(guó)Gibco 公司);胎牛血清(批號(hào)20010502,杭州四季青生物工程研究所)。其他試劑均為分析純。
1.3 細(xì)胞 人臍靜脈內(nèi)皮細(xì)胞(HUVECs),由河南中醫(yī)藥大學(xué)第一附屬醫(yī)院李強(qiáng)老師惠贈(zèng)。
1.4 藥材 懷菊花購(gòu)自河南綠禾藥業(yè)有限公司,經(jīng)河南中醫(yī)藥大學(xué)藥學(xué)院董誠(chéng)明教授鑒定為菊科植物菊Chrysanthemum morifoliumRamat 的干燥頭狀花序。
2 方法與結(jié)果
2.1 總黃酮含量測(cè)定
2.1.1 粗提物制備 參考文獻(xiàn)[14] 報(bào)道,稱取藥材20 g,以料液比1 ∶25 加入70%乙醇500 mL,加熱回流提取2 次,每次2 h,合并提取液,減壓回收乙醇,濃縮液冷凍干燥,即得,提取率為55.2%。
2.1.2 線性關(guān)系考察 精密稱取蘆丁對(duì)照品5 mg,70%乙醇溶解并定容至25 mL 量瓶中,分別精密量取0.5、1.5、2.5、3.5、5.5、7.5 mL 至25 mL 量瓶中,依次加入顯色劑亞硝酸鈉、硝酸鋁后定容,以70%乙醇為空白對(duì)照,在510 nm 波長(zhǎng)處測(cè)定吸光度。以蘆丁質(zhì)量濃度為橫坐標(biāo)(X),吸光度為縱坐標(biāo) (A) 進(jìn)行回歸,得方程為A=11.621X+0.003 3 (r=0.999 0),在0.004 0~0.060 0 mg/mL 范圍內(nèi)線性關(guān)系良好。
2.1.3 測(cè)定方法 精密量取“2.1.1” 項(xiàng)下濃縮液2.5 mL 至25 mL 量瓶中,70%乙醇超聲溶解并定容,得到樣品溶液,量取10 mL 至25 mL 量瓶中,按“2.1.2” 項(xiàng)下方法顯色,測(cè)得總黃酮含量為14.015 mg/mL。
2.2 純化工藝優(yōu)化 在單因素試驗(yàn)基礎(chǔ)上,采用Box-Behnken 響應(yīng)面法。
2.2.1 大孔吸附樹(shù)脂預(yù)處理 參考文獻(xiàn)[15] 報(bào)道,采用95%乙醇浸泡樹(shù)脂24 h 以上,充分溶脹后將漂浮雜質(zhì)除去,濕法裝柱,95%乙醇沖柱至沖洗液無(wú)白色混濁,大量蒸餾水沖洗至無(wú)醇味。
2.2.3 單因素試驗(yàn) 以上樣質(zhì)量濃度、上樣液pH值、上樣量、乙醇解吸體積分?jǐn)?shù)、水除雜體積、乙醇解吸體積為影響因素,考察它們對(duì)純化工藝的影響。(1) 上樣質(zhì)量濃度,稱取6 份預(yù)先處理好的AB-8 型樹(shù)脂10 g,濕法裝柱,70%乙醇將濃縮液稀釋定容為含總黃酮0.12、0.36、0.56、0.67、0.83、1.46 mg/mL 的上樣液各25 mL,分別量取7 mL上樣,收集流出液;(2) 上樣液pH 值,分別配制pH 值為2、3、4、5、6、8 的0.56 mg/mL 總黃酮溶液,上樣,收集流出液;(3) 上樣量,配制pH 值為4 的0.56 mg/mL 總黃酮溶液,上樣2 BV,分別在0.4、0.8、1.2、1.6、2 BV 收集過(guò)柱液;(4) 乙醇解吸體積分?jǐn)?shù),配制pH 值為4 的0.56 mg/mL 總黃酮溶液,上樣0.9 BV,4 BV 蒸餾水除雜,分別用70%、80%、90%、95% 乙醇各2 BV 解吸,收集解吸液;(5) 水除雜體積,配制pH 值為4 的0.56 mg/mL 總黃酮溶液,上樣,分別用2、3、4、5、6 BV 蒸餾水除雜,2 BV 80%乙醇解吸,收集解吸液;(6) 乙醇解吸體積,配制pH 值為4 的0.56 mg/mL 總黃酮溶液,上樣,4 BV蒸餾水除雜,分別用0.5、1、2、3、4 BV 80%乙醇解吸,收集解吸液,結(jié)果見(jiàn)圖1。
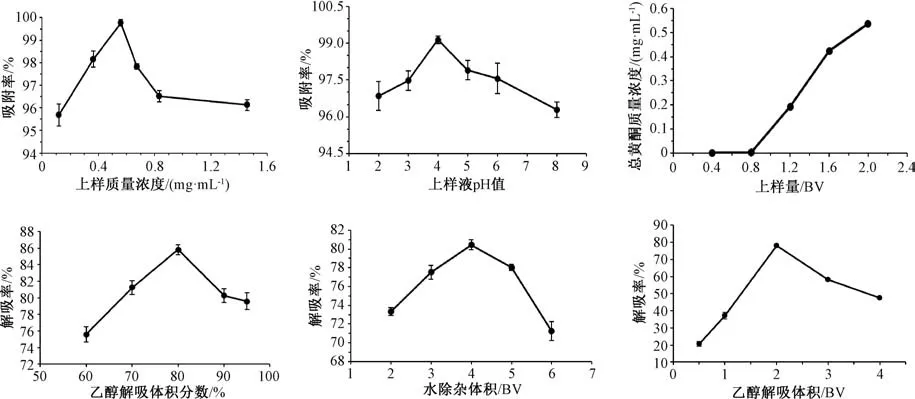
圖1 單因素試驗(yàn)結(jié)果Fig.1 Results of single factor tests
由此可知,吸附率、解吸率都隨著各影響因素增加先升后降,當(dāng)上樣液質(zhì)量濃度為0.56 mg/mL,pH 值為4 時(shí),樹(shù)脂吸附飽和,吸附率達(dá)到最大。前期報(bào)道,當(dāng)流出液中總黃酮質(zhì)量濃度達(dá)到上樣液體積分?jǐn)?shù)的10%時(shí),即達(dá)到泄漏點(diǎn)[16],而本實(shí)驗(yàn)發(fā)現(xiàn),上樣1.2 BV 時(shí)已超過(guò)泄漏點(diǎn),故選取接近泄漏點(diǎn)的0.9 BV 作為最優(yōu)上樣量。另外,用4 BV水除雜,2 BV 80%乙醇解吸時(shí),總黃酮解吸完全并不被稀釋,解吸率達(dá)到最大。最終,分別選擇80%、2 BV、4 BV 作為乙醇解吸體積分?jǐn)?shù)、乙醇解吸體積、水除雜體積的響應(yīng)面中心點(diǎn)。
2.2.4 Box-Behnken 響應(yīng)面法 結(jié)合單因素試驗(yàn)結(jié)果,選擇乙醇解吸體積分?jǐn)?shù)(A)、乙醇解吸體積(B)、水除雜體積(C) 作為影響因素,解吸率(Y) 作為評(píng)價(jià)指標(biāo),設(shè)計(jì)三因素三水平試驗(yàn),具體見(jiàn)表1,結(jié)果見(jiàn)表2。
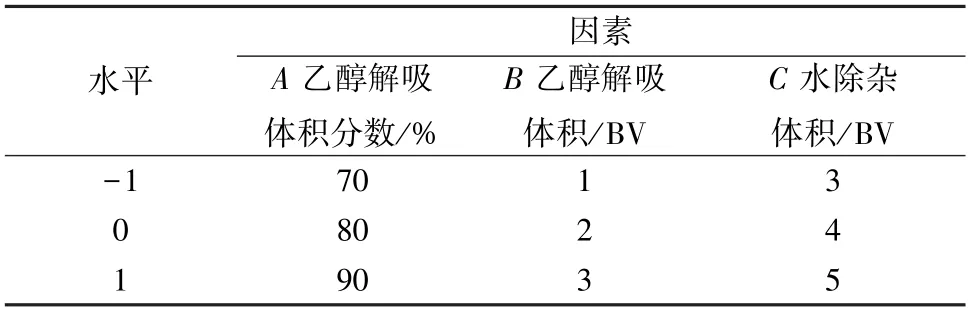
表1 因素水平Tab.1 Factors and levels
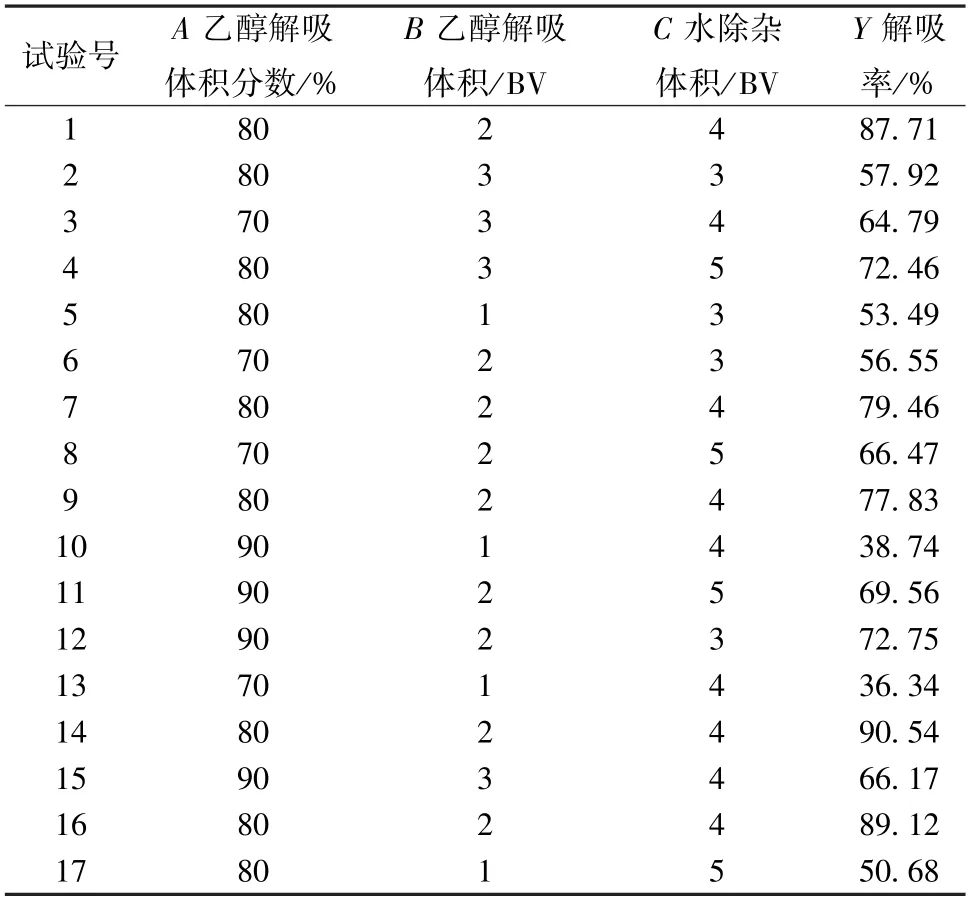
表2 試驗(yàn)設(shè)計(jì)與結(jié)果Tab.2 Design and results of tests
采用Design-Expert 11.0 軟件對(duì)表2 數(shù)據(jù)進(jìn)行二次多項(xiàng)式擬合,得方程為Y=84.93+2.88A+10.26B+ 2.31C-0.256 3AB-3.28AC+ 4.34BC-12.86A2-20.56B2-5.74C2,結(jié)果見(jiàn)表3。由此可知,模型P<0.01,具有高度顯著性;失擬項(xiàng)P>0.05,表明是由隨機(jī)誤差引起的殘差[17];確定系數(shù)R2=0.933 2,AdjustedR2=0.847 3,表明模型擬合程度較好,響應(yīng)值變化有84.73%來(lái)源于影響因素;因素B、A2、B2有極顯著影響(P<0.01);各因素影響程度依次為B>A>C。
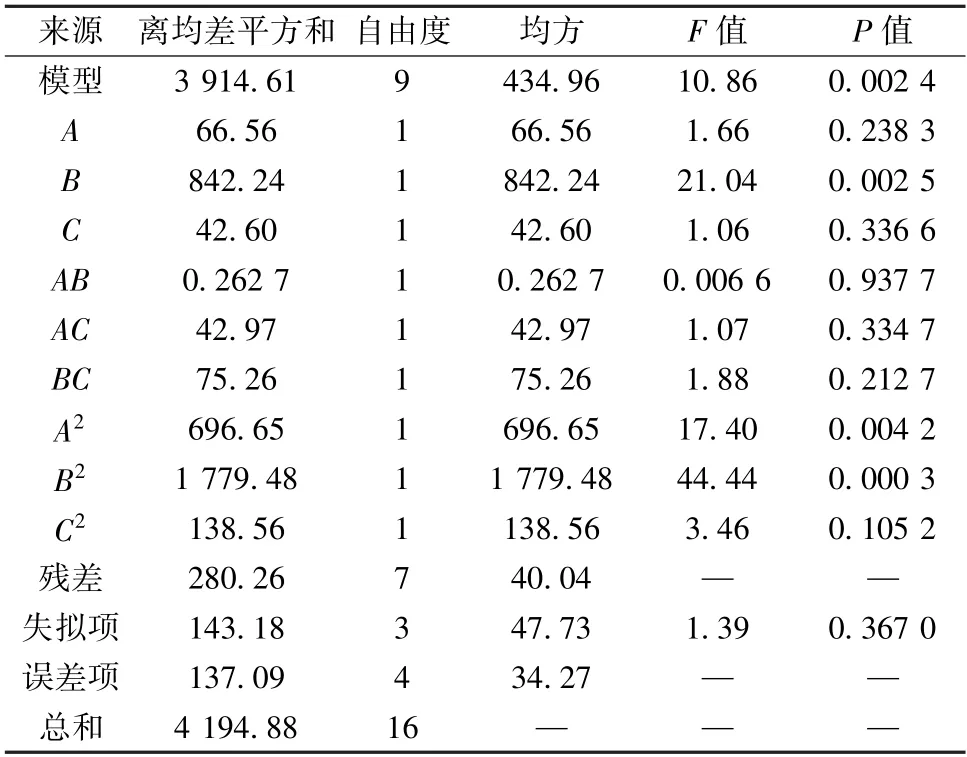
表3 方差分析Tab.3 Analysis of variance
響應(yīng)面分析見(jiàn)圖2[18-19]。由此可知,因素B對(duì)解吸率的影響最大,A次之,C最小,與表2 結(jié)果一致;各因素交互項(xiàng)影響程度依次為BC>AC>AB。
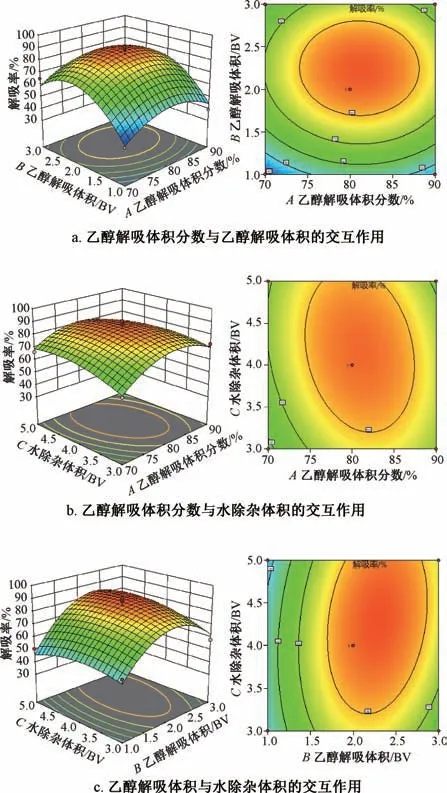
圖2 各因素響應(yīng)面圖Fig.2 Response surface plots for various factors
2.2.5 驗(yàn)證試驗(yàn) 按“2.2.4” 項(xiàng)下結(jié)果,得到最優(yōu)純化工藝為乙醇解吸體積分?jǐn)?shù)80.73%,乙醇解吸體積2.28 BV,水除雜體積4.28 BV,考慮到實(shí)際可操作性,將其調(diào)整為乙醇解吸體積分?jǐn)?shù)80%,乙醇解吸體積2 BV,水除雜體積4 BV。按優(yōu)化工藝進(jìn)行3 批驗(yàn)證試驗(yàn),測(cè)得平均解吸率為84.93%,與預(yù)測(cè)值86.80%接近;純化前總黃酮純度為11.74%,而純化后升至52.71%,表明該工藝穩(wěn)定可靠。
2.3 抗炎活性研究
2.3.1 細(xì)胞培養(yǎng)、分組及給藥 HUVECs 細(xì)胞復(fù)蘇后,用含10%胎牛血清的DMEM 高糖培養(yǎng)基進(jìn)行培養(yǎng),設(shè)定溫度為37 ℃ (含5% CO2),分為對(duì)照組(正常培養(yǎng)基培養(yǎng)48 h)、ox-LDL 組(正常培養(yǎng)基培養(yǎng)24 h 后,150 μg/mL ox-LDL 處理24 h)、給藥組(500 μg/mL 總提物及25、50、100 μg/mL總黃酮含藥培養(yǎng)基培養(yǎng)24 h 后,150 μg/mL ox-LDL 處理24 h),每組6 個(gè)復(fù)孔。
2.3.2 總黃酮對(duì)細(xì)胞增殖的影響 將HUVECs 細(xì)胞懸液接種于96 孔板(密度4.0×104/孔),細(xì)胞貼壁后更換無(wú)血清的培養(yǎng)基培養(yǎng)24 h 使其生長(zhǎng)同步化,分組并給藥24 h 后取上清液,加入100 μL新鮮培養(yǎng)基,再加入10 μL CCK-8 孵育4 h,在全波長(zhǎng)酶標(biāo)儀540 nm 波長(zhǎng)處檢測(cè)吸光度,計(jì)算細(xì)胞增殖率[20],公式為增殖率=(實(shí)驗(yàn)組吸光度/對(duì)照組吸光度) ×100%,結(jié)果見(jiàn)圖3。由此可知,與對(duì)照組比較,ox-LDL 組細(xì)胞增殖率降低(P<0.01);與ox-LDL 組比較,總提物、總黃酮組細(xì)胞增殖率升高(P<0.05,P<0.01),并且總黃酮組呈一定劑量依賴性。
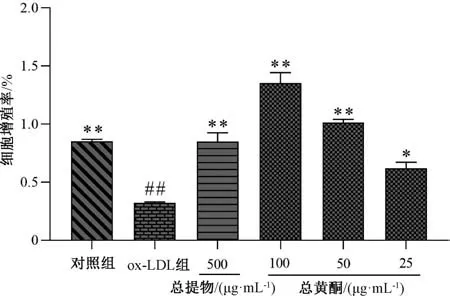
圖3 懷菊花總黃酮對(duì)ox-LDL 誘導(dǎo)HUVECs 細(xì)胞增殖率的影響Fig.3 Effect of total flavonoids from Huai Chrysanthemum on proliferation rate of HUVECs cells induced by ox-LDL
2.3.3 總黃酮對(duì)炎癥因子水平的影響 將“2.3.2”項(xiàng)下細(xì)胞上清液在4 ℃下離心5 min 后,按照ELISA 試劑盒說(shuō)明書(shū)檢測(cè)IL-1β (圖4A)、IL-6(圖4B)、TNF-α (圖4C) 水平,結(jié)果見(jiàn)圖4。由此可知,與對(duì)照組比較,ox-LDL 組IL-1β、IL-6、TNF-α 水平升高(P<0.05,P<0.01);與ox-LDL組比較,總提物、100 μg/mL 總黃酮組IL-1β、IL-6 水平降低(P<0.05,P<0.01),總提物、不同劑量總黃酮組TNF-α 水平降低(P<0.05,P<0.01)。
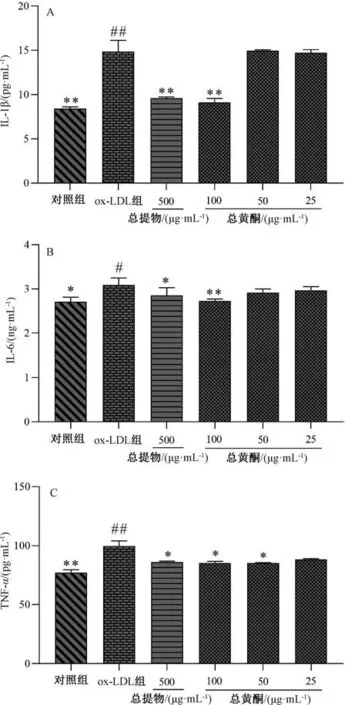
圖4 懷菊花總黃酮對(duì)ox-LDL 誘導(dǎo)HUVECs 細(xì)胞炎癥因子水平的影響Fig.4 Effects of total flavonoids from Huai Chrysanthemum on inflammatory factor levels in HUVECs cells induced by ox-LDL
2.4 成分組成分析 采用HPLC 法。
2.4.1 色譜條件 Symmetry C18色譜柱(4.6 mm×250 mm,5 μm);流動(dòng)相乙腈 (A)-0.2% 磷酸(B),梯度洗脫 (0~5 min,11%~16% A;5~15 min,16%A;15~18 min,16%~19%A;18~30 min,19%A;30~35 min,19%~22% A;35~55 min,22%A;55~57 min,22%~28% A;57~70 min,28%A;70~95 min,28%~80%A);體積流量1.0 mL/min;柱溫30 ℃;檢測(cè)波長(zhǎng)270 nm;進(jìn)樣量10 μL。
2.4.2 對(duì)照品溶液制備 取各對(duì)照品適量,置于10 mL 量瓶中,甲醇超聲溶解,定容,制成分別含101 μg/mL 木犀草苷、201 μg/mL 異綠原酸A、107 μg/mL 芹菜素-7-O-葡萄糖苷、759.05 μg/mL香葉木素-7-O-葡萄糖苷、796 μg/mL 木犀草素、663.48 μg/mL 金合歡素-7-O-葡萄糖苷、832 μg/mL芹菜素、762 μg/mL 香葉木素、855 μg/mL 金合歡素的貯備液,分別取0.5 mL,甲醇稀釋1 倍,過(guò)0.22 μm 微孔濾膜,即得。
2.4.3 供試品溶液制備 取純化后的總黃酮凍干粉約1 mg,置于錐形瓶中,加1 mL 甲醇溶解,搖勻,過(guò)0.22 μm 微孔濾膜,即得。
2.4.4 結(jié)果分析 取對(duì)照品、供試品溶液適量,在“2.4.1” 項(xiàng)色譜條件下進(jìn)樣測(cè)定,通過(guò)比對(duì)色譜峰保留時(shí)間、紫外最大吸收波長(zhǎng)結(jié)合相關(guān)文獻(xiàn)確認(rèn)成分,結(jié)果見(jiàn)圖5,共發(fā)現(xiàn)9 種成分,包括8 種黃酮、1 種有機(jī)酸,分別為木犀草苷、芹菜素-7-O-葡萄糖苷、香葉木素-7-O-葡萄糖苷、木犀草素、金合歡素-7-O-葡萄糖苷、芹菜素、香葉木素、金合歡素、異綠原酸A。
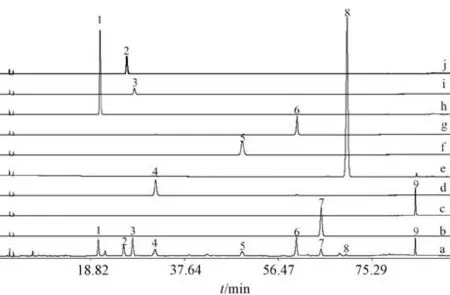
圖5 各成分HPLC 色譜圖Fig.5 HPLC chromatograms of various constituents
3 討論與結(jié)論
在純化工藝中,上樣液濃度大、黏性增加、雜質(zhì)增多、pH 過(guò)高或過(guò)低均會(huì)造成黃酮存在形式發(fā)生變化,從而影響大孔吸附樹(shù)脂吸附,并且在除雜、解吸時(shí)其用量過(guò)大也會(huì)將吸附上的黃酮解吸下來(lái)而造成損失。純化前,懷菊花總提物凍干粉呈偏黑褐色,易吸潮而變黏稠;純化后,它呈偏黃棕色,吸濕性降低,總黃酮純度明顯提高。
在前期研究基礎(chǔ)上,本實(shí)驗(yàn)采用ox-LDL 誘導(dǎo)HUVECs 細(xì)胞損傷模型,評(píng)價(jià)懷菊花總提物及其總黃酮對(duì)HUVECs 細(xì)胞的保護(hù)作用。結(jié)果顯示,總黃酮可通過(guò)降低細(xì)胞炎性因子分泌來(lái)保護(hù)內(nèi)皮細(xì)胞,具有潛在的抗動(dòng)脈粥樣硬化活性,但其藥效和作用機(jī)制還有待通過(guò)體內(nèi)藥理實(shí)驗(yàn)作進(jìn)一步研究。
目前,關(guān)于懷菊花所含成分含量測(cè)定的報(bào)道大多只涉及2020 年版《中國(guó)藥典》 規(guī)定的3 種指標(biāo)成分[21](綠原酸、木犀草苷、3,5-O-二咖啡酰基奎寧酸),僅王月茹[22]測(cè)定了其他5 種黃酮含量。本實(shí)驗(yàn)采用HPLC 法指認(rèn)了懷菊花總黃酮中8 種黃酮、1 種有機(jī)酸,數(shù)量多于目前相關(guān)文獻(xiàn)所發(fā)表,可為該藥材開(kāi)發(fā)利用提供參考依據(jù),具有一定實(shí)際意義。
- 中成藥的其它文章
- 吸入粉霧劑制劑處方組成的研究進(jìn)展
- 雷公藤多苷片對(duì)類(lèi)風(fēng)濕關(guān)節(jié)炎合并間質(zhì)性肺病患者的臨床療效
- 基于網(wǎng)絡(luò)藥理學(xué)和細(xì)胞實(shí)驗(yàn)探討桂枝茯苓丸對(duì)卵巢癌的作用
- 鳶尾苷元通過(guò)miR-449a 調(diào)控JAK/STAT 信號(hào)通路對(duì)人牙齦成纖維細(xì)胞增殖及凋亡的影響
- 紫草素對(duì)體外模擬糖尿病并發(fā)抑郁癥環(huán)境大鼠海馬神經(jīng)元凋亡的影響
- 大孔吸附樹(shù)脂分離純化白子菜總黃酮工藝優(yōu)化

