基于網絡藥理學和分子對接技術研究黃芩治療糖尿病腦病的作用
高書春,杜卓琦,馬世平,鄧雪陽
(中國藥科大學,江蘇 南京 211198)
糖尿病是一種常見的代謝疾病,受遺傳和環境因素等影響,發病率逐年增高[1]。糖尿病腦病是指糖尿病導致的中樞神經系統病變,這種使大腦在結構、神經生理及認知功能等方面發生病理改變是糖尿病最常見的并發癥之一[2]。阿爾茨海默病是一種慢性神經退行性疾病,以記憶缺失逐漸進展為癡呆特征的神經退行性疾病[3]。糖尿病作為認知功能障礙的獨立危險因素之一,與阿爾茨海默病關系密切[4]。目前糖尿病腦病的治療仍以控制血糖為主,然而療效有限,而西藥治療可能會導致低血糖,誘發或加重神經病變[5]。
糖尿病屬中醫學“消渴癥” 范疇[6-7],阿爾茨海默病屬“呆病”[7],無論是糖尿病還是阿爾茨海默病,其病因繁多,病情表現反復,暫無根治辦法,因此探索中藥多成分、多靶點的治療機制就顯得尤為重要。黃芩具有清熱燥濕、瀉火解毒、止血、安胎的功效,可用于糖尿病的治療[8],因此認為黃芩治療糖尿病腦病具有臨床應用價值。網絡藥理學以網絡為基礎,結合藥理學并涉及多層次、多方向的數據分析,在分子、細胞、生物過程及通路等方面解析藥物與疾病靶點之間多成分、多靶點、多通路的結果,這也與中醫藥的整體觀相同[9]。
1 材料與方法
1.1 黃芩活性成分篩選 通過中藥系統藥理學數據庫與分析平臺 (TCMSP,https://tcmspw.com/tcmsp.php)[10]檢索黃芩的化學成分,根據黃芩ADME 性質,以口服生物利用度 (oral bioavailability,OB) ≥30%,類藥性 (druglikeness,DL) ≥0.18 進行篩選[11],然后獲得其相關靶點蛋白,并根據相關文獻及PharmMapper 庫(http://lilabecust.cn/pharmmapper/index.html)、SwissTargetPrediction庫(http://swisstargetprediction.ch/) 進行補充,并篩選符合糖尿病和阿爾茨海默病的靶點。利用UniProt 庫(https://www.uniprot.org/)、DrugBank 庫(https://go.drugbank.com/) 查詢靶點蛋白對應的基因名,將黃芩活性化合物對應的靶點蛋白進行統一規范。
1.2 糖尿病和阿爾茨海默病靶點篩選 在OMIM 庫(https://www.omim.org/)、GeneCards 庫 (https://www.genecards.org/)、Therapeutic Target Database (http://db.idrblab.net/ttd/) 及DrugBank庫 (https://go.drugbank.com/) 中,以“diabetes mellitus” 為關鍵詞檢索糖尿病的潛在靶點,以“Alzheimer’s disease” 為關鍵詞檢索阿爾茨海默病的潛在靶點,依據潛在靶點與疾病的高相關性以及后續的網絡分析,對所得靶點按relevance score 值等由大到小,以4 倍中位數為閾值進行篩選[12],合并糖尿病和阿爾茨海默病的疾病靶點。
1.3 構建黃芩活性成分-靶點網絡 將靶點與黃芩活性成分導入Cytoscape3.7.2 軟件(https://cytoscape.org/) 構建“活性成分-靶點” 網絡。
1.4 構建黃芩-糖尿病-阿爾茨海默病靶點的PPI 網絡 將黃芩、糖尿病和阿爾茨海默病的靶點導入VENNY2.1(https://bioinfogp.cnb.csic.es/tools/venny/index.html)在線繪制韋恩圖,得到交集靶點,并將交集靶點上傳至STRING11.0 (https://string-db.org/),得到蛋白質互作網絡 (protein-protein interaction networks,PPI),并將該PPI 網絡信息保存為TSV 文件,導入Cytoscape3.7.2 中詳細繪制PPI 互作網絡并進行網絡拓撲分析,根據degree 值篩選關鍵靶點[13]。
1.5 GO 功能與KEGG 通路富集分析 將黃芩-糖尿病-阿爾茨海默病交集靶點上傳至Metascape 庫[14](http://www.metascape.org/gp/index.html#/main/step1) 中進行基因本體(gene ontology,GO) 與京都基因與基因組百科全書(Kyoto encyclopedia of genes and genomes,KEGG) 富集分析,獲得KEGG 通路結果及GO 富集分析中分子功能(molecular functions,MF)、細胞組成(cellular components,CC)、生物過程 (biological processes,BP)[15],用GraphPad Prism 7 軟件進行可視化。
1.6 構建黃芩成分-疾病靶點-通路網絡 將上述得到的核心通路和交集靶點、藥物成分導入到Cytoscape3.7.2 軟件中,構建“藥物-成分-疾病靶點-通路” 網絡圖,利用內部工具Network Analyzer 對黃芩活性成分及交集靶點進行拓撲學分析。
1.7 分子對接 利用TCMSP 獲得主要活性成分的mol2 結構,在PDB (http://www.rcsb.org/) 數據庫中檢索核心靶點的三維結構,利用Auto Dock Tools 1.5.6 軟件對蛋白3D 結構進行去水、加氫并計算電荷,保存為pdbqt 格式;同法將活性成分的mol2 結構轉為pdbqt 格式。最后用Auto Dock Tools 1.5.6 軟件進行分子對接,并用Pymol 2.4.1 進行可視化。
2 結果
2.1 黃芩活性成分的篩選及成分-靶點網絡的構建 經過檢索TCMSP 庫,篩選獲得黃芩活性成分36 種,進一步查詢對應靶點,去重后獲得黃芩重要的活性成分22 種,見表1,其中僅黃芩中存在的成分為黃芩新素、黃芩黃酮Ⅱ、紅花素、二氫奧洛昔林、5,8,2'-三羥基-7-甲氧基黃酮、5,7,2,5-四羥基-8,6-二甲氧基黃酮,而2,6,2',4'-四羥基-6'-甲氧基查爾酮因未查到靶點信息而舍去。篩選得到作用靶點146 個。黃芩成分-靶點網絡中有節點164 個,見圖1。
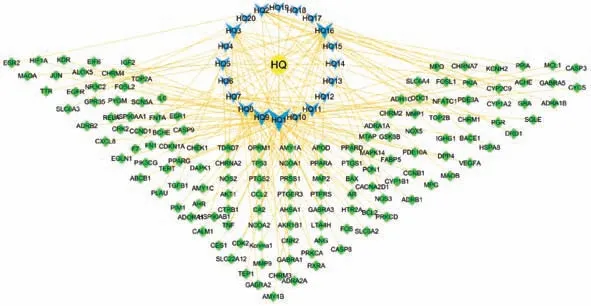
圖1 黃芩化合物-靶點網絡圖

表1 黃芩活性成分的基本信息
2.2 糖尿病和阿爾茨海默病靶點的獲取 糖尿病靶點主要來自于GeneCards 庫,獲得靶點6 134 個,其Relevance Score 值的4 倍中位數為7.9,score>7.9 的靶點有1 299 個,再與OMIM 等庫合并,去重后獲得1 125 個糖尿病潛在靶點;同理獲得阿爾茨海默病靶點9 553 個,score>5.06 的靶點有2 391 個,合并去重后獲得1 144 個糖尿病潛在靶點。
2.3 黃芩-糖尿病-阿爾茨海默病靶點的PPI 網絡構建 將上述獲得的146 個黃芩靶點,1 125 個糖尿病靶點,1 144個阿爾茨海默病靶點導入Venny2.1 繪制Venn 圖,見圖2。

圖2 黃芩、糖尿病、阿爾茨海默病靶點交集Venn 圖
將交集靶點上傳至STRING 11.0 (因為存在1 個游離靶點,故實際得到的PPI 網絡中靶點為60 個) 進行處理,接著導入Cytoscape 3.7.2 軟件中詳細繪制PPI 互作網絡,見圖3。STRING 數據分析可知節點數60 個,邊數630 條,平均節點度值20.7,預測的邊數248。在Cytoscape 中用內部工具NetworkAnalyzer 進行拓撲學分析,篩選度值前二十的靶點 (degree >28),分別為AKT1、IL-6、VEGFA、TNF、CASP3 JUN、TP53、FOS、EGFR、HSP90AA1、PTGS2、MMP9、NOS3、ESR1、CYCS、FN1、MAPK14、PPARG、CXCL8、CCL2。

圖3 黃芩、糖尿病、阿爾茨海默病交集靶點的PPI 網絡
2.4 核心靶點的GO 功能與KEGG 通路富集分析 將黃芩、糖尿病、阿爾茨海默病交集靶點經Metascape 庫分析后,得到KEGG 通路258 條,GO 富集分析中分子功能(MF) 101條、細胞組成(CC) 76 條、生物過程(BP) 1 413 條。根據P值篩選得到KEGG 通路排名前二十的通路,見圖4,主要涉及AGE-RAGE 信號介導的糖尿病并發癥通路(AGERAGE signaling pathway in diabetic complications)、IL-17 信號通路(IL-17 signaling pathway)、MAPK 信號通路(MAPK signaling pathway)、TNF 信號通路(TNF signaling pathway)、磷脂酰肌醇3 激酶-蛋白激酶B 信號通路 (PI3K-Akt signaling pathway)、C 型凝集素受體信號通路(C-type lectin receptor signaling pathway)、胰島素抵抗通路 (insulin resistance) 等。

圖4 交集靶點KEGG 通路富集分析
GO 富集分析中,MF 主要涉及核受體活性 (nuclear receptor activity)、轉錄輔激活因子結合 (transcription coactivator binding)、類固醇激素受體 (steroid hormone receptor activity)、蛋白質結構域特異性結合(protein domain specific binding)、脂質結合(lipid binding) 等,見圖5A。CC 主要涉及囊腔(vesicle lumen)、分泌顆粒腔(secretory granule lumen)、胞質泡腔(cytoplasmic vesicle lumen)、膜微區(membrane microdomain)、膜區(membrane region)、受體復合物(receptor complex) 等,見圖5B。BP 主要涉及脂多糖的反應(response to lipopolysaccharide)、活性氧代謝過程(reactive oxygen species metabolic process)、細胞對脂質的反應 (cellular response to lipid)、氧化應激反應(response to oxidative stress)、心血管系統發育(cardiovascular system development)、MAPK 級聯的調節(regulation of MAPK cascade)、跨膜受體蛋白酪氨酸激酶信號通路 (transmembrane receptor protein tyrosine kinase signaling pathway) 等,見圖5C。

圖5 交集靶點GO 功能富集分析
2.5 黃芩成分-疾病靶點-通路網絡構建 經Cytoscape3.7.2軟件構建“藥物成分-疾病靶點-通路” 網絡圖,見圖6。經分析后可知,平均度值為7,度值靠前的成分主要是漢黃芩素、黃芩素、β-谷甾醇、金合歡素、降穿心蓮黃酮、紅花素、二氫奧洛昔林、5,8,2'-三羥基-7-甲氧基黃酮等,其中紅花素、二氫奧洛昔林、5,8,2'-三羥基-7-甲氧基黃酮等為黃芩中獨有的成分。度值靠前的靶點主要是AKT1、IL-6、JUN、MAPK14、FOS、TNF、PRKCA、VEGFA 等。

圖6 黃芩成分-疾病靶點-通路網絡
2.6 分子對接驗證 將漢黃芩素、金合歡素、黃芩素、紅花素、二氫奧洛昔林、黃芩黃酮Ⅱ、5,7,2,5-四羥基-8,6-二甲氧基黃酮、降穿心蓮黃酮等活性成分與核心靶點VEGFA、AKT1、TNF、MAPK14、IL-6 進行對接,對接結果見表2。由此可知,黃芩是通過多成分、多靶點以不同活性結合,進一步驗證了關鍵活性成分與核心交集靶點的相互作用。部分結果可視化后見圖7,其中氫鍵以虛線顯示,結合位點以不同顏色在蛋白質與分子之間顯示。
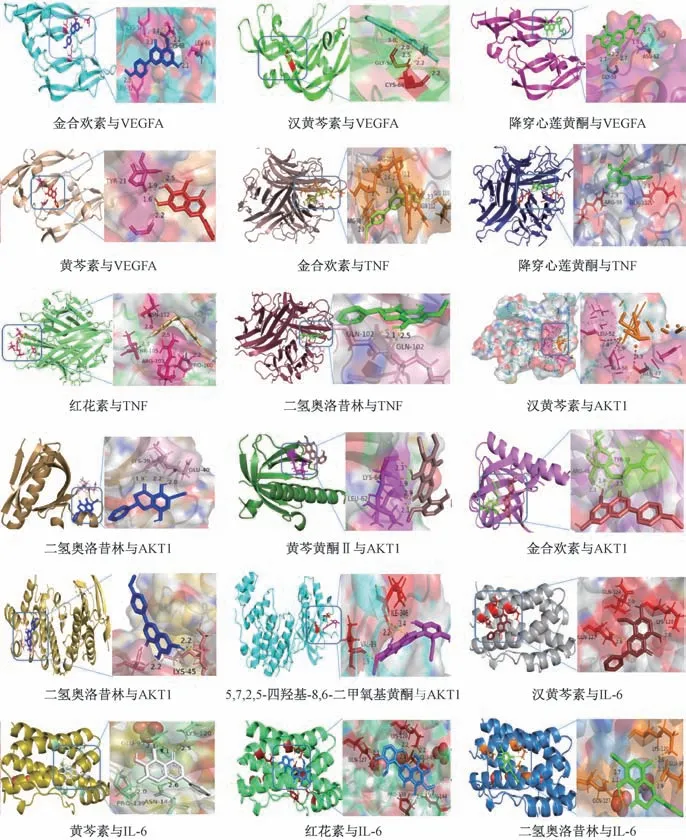
圖7 黃芩活性成分與核心靶點的對接
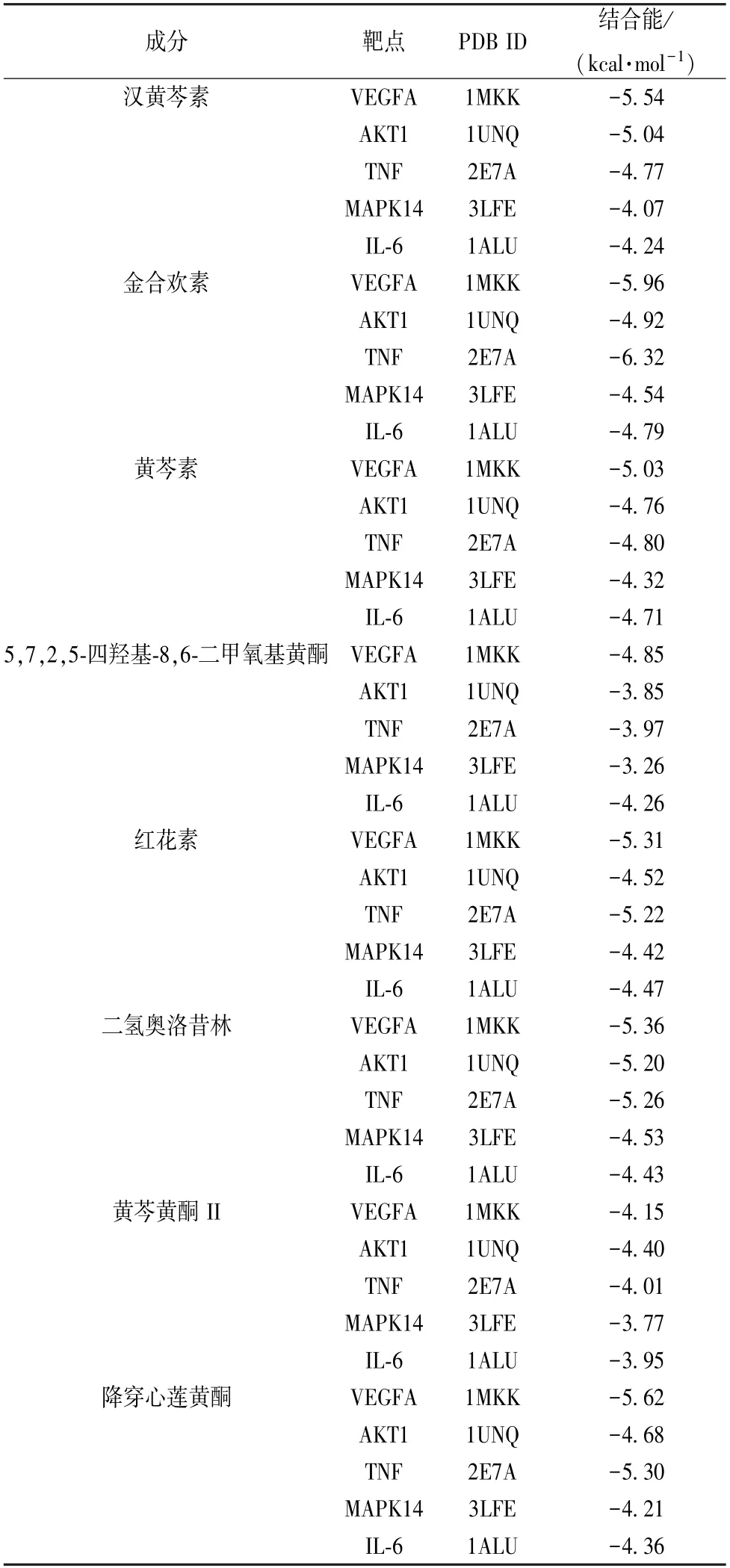
表2 黃芩活性成分與核心靶點的分子對接結果
3 討論
黃芩性寒,味苦,具有瀉火除煩之功效,是歷代醫家治療神志病及消渴病的常用中藥。課題組前期研究發現黃芩及其活性成分具有顯著的神經保護活性,及抗氧化、抗神經細胞凋亡等作用[16-18]。因此,本研究結合網絡藥理學和分子對接技術系統地探索黃芩治療糖尿病腦病的分子機制。
本研究對活性成分-靶點的研究中得到僅黃芩中存在的成分為黃芩新素、黃芩黃酮Ⅱ、紅花素、二氫奧洛昔林、5,8,2'-三羥基-7-甲氧基黃酮、5,7,2,5-四羥基-8,6-二甲氧基黃酮、2,6,2',4'-四羥基-6'-甲氧基查爾酮,在相關實驗研究中均有報道證實。Guo 等[19]研究發現漢黃芩素能減輕神經炎癥,其作用機制與緩解Aβ 蛋白導致的認知功能喪失有關[20]。黃芩素還可抑制小膠質細胞活化,減少炎癥,減輕氧化應激和細胞凋亡[21-22]。漢黃芩素可以通過AKT/GLUT4 途徑發揮降血糖作用,以改善胰島素抵抗[23]。目前研究發現紅花素提取自黃芩莖葉總黃酮,其可以抑制Aβ 蛋白引起的神經元凋亡,改善胰島素抵抗[24-26]。崔曉燕等[27]研究發現黃芩提取物在海馬和皮質中可促使乙酰膽堿的合成,以此改善阿爾茨海默病表現出的學習記憶障礙。
本研究通過構建活性成分-靶點網絡、PPI 網絡及疾病-靶點-通路網絡,經網絡拓撲分析,篩選出一部分重要的靶點,度值靠前的成分主要是漢黃芩素、黃芩素、β-谷甾醇、金合歡素、降穿心蓮黃酮、紅花素、二氫奧洛昔林、5,8,2'-三羥基-7-甲氧基黃酮等,其中紅花素、二氫奧洛昔林、5,8,2'-三羥基-7-甲氧基黃酮等為黃芩中獨有的成分。度值靠前的靶點主要是AKT1、IL-6、JUN、MAPK14、FOS、TNF、PRKCA、VEGFA 等,其在基礎研究中均得到驗證,說明這些靶點對糖尿病腦病的重要性。在糖尿病中,一方面AKT1 的過表達可促進葡萄糖的吸收,另一方面AKT 可抑制胰高血糖素的分泌,其機制與改善胰島素抵抗有關[28-29]。在阿爾茨海默病中,AKT1 磷酸化表達的增加被認為與淀粉樣蛋白負荷增加有關[30];腫瘤壞死因子和IL-6 在葡萄糖和脂質代謝、心血管功能中起重要作用;IL-6 的升高被認為與炎癥、胰島素抵抗和β 細胞功能障礙的發展有關[31];慢性應激和Aβ 蛋白會破壞小膠質細胞的活性,導致IL-6 進一步釋放[32];MAPK14 參與了自噬過程,抑制MAPK14 的活性一定程度上可以緩解病癥,也可通過靶向調節MAPK14 表達來減少Aβ 蛋白沉積以減輕病癥[33-34]。目前研究發現血管內皮生長因子(VEGF) 的變異與糖尿病、阿爾茨海默病發生的風險增加有關,還可能與其他神經系統疾病有關[35-36]。
本研究通過KEGG 富集通路分析,得出黃芩治療糖尿病腦病的主要通路涉及AGE-RAGE 信號通路、IL-17 信號通路、MAPK 信號通路、TNF 信號通路、PI3K-Akt 信號通路等。AGE-RAGE 信號通路中AGE 與受體RAGE 結合,誘導促炎性細胞因子、ROS 的產生,影響神經元和神經膠質細胞的活力[37],通過抑制AGE-RAGE 通路和隨后的氧化應激、炎癥,可以預防糖尿病導致的神經系統病變[38-39]。IL-17 和TNF 信號通路主要是通過誘發炎癥級聯通路的激活導致糖尿病神經系統病變,現階段普遍認為通過抑制IL-17 和TNF 可以有效治療糖尿病及其相關并發癥[40-41]。PI3K-Akt信號通路被認為是胰島素作用的主要介質,在阿爾茨海默病患者腦中已觀察到PI3K 亞基表達降低,此外胰島素可以通過PI3K-Akt 信號通路增強神經元生長,而胰島素活性的恢復有望成為治療糖尿病及其并發癥認知障礙的靶點[42-43]。
綜上所述,本研究通過網絡藥理學分析得出,黃芩可能通過漢黃芩素、黃芩素、金合歡素、降穿心蓮黃酮、紅花素、二氫奧洛昔林等多成分,通過多靶點,以AGERAGE、IL-17、TNF、MAPK、PI3K-Akt 及胰島素抵抗等多種信號通路,影響糖尿病涉及的炎癥、氧化應激、胰島素活性等多種方式,來緩解并發癥阿爾茨海默病,并利用分子對接來驗證關鍵活性成分和核心靶點的相互作用。本研究結果為黃芩治療糖尿病腦病提供了一定的理論指導和方向,但仍需進一步開展相關的藥理學實驗,進一步驗證和闡明黃芩治療糖尿病腦病的作用機制。

