晚期食管癌PD-1/PD-L1免疫檢查點抑制劑療法的Cochrane Meta分析
許雨柔 鄒宜豐 蔡寧 范佳慧 陳興棟 索晨△
(1復旦大學公共衛生學院流行病學系 上海 200032; 2復旦大學公共衛生安全教育部重點實驗室 上海 200032;3復旦大學人類表型組研究院遺傳工程國家重點實驗室 上海 200438; 4復旦大學泰州健康科學研究院 泰州 225300;5復旦大學義烏研究院 義烏 322000)
食管癌(esophageal cancer,EC)是常見的消化道惡性腫瘤之一,其全球發病率具有廣泛的地理差異,中國處于“食管癌帶”的高發病率地區[1]。根據GOLOBOCAN估計的全球癌癥發病率和死亡率,2020年食管癌的發病率為604 127例,為第八高發的惡性癌癥;死亡544 076例,在癌癥死亡率中排第六[2]。食管癌分為兩種主要的亞型:食管鱗狀細胞癌(esophageal squamous cell carcinoma,ESCC)和食管腺癌(esophageal adenocarcinoma,EAC)。目前,食管癌的治療主要包括內窺鏡治療、手術、放療和化療,但總體預后并不樂觀[3]。近幾年,隨著生物免疫治療的發展,免疫檢查點抑制劑在黑色素瘤、非小細胞肺癌及腎癌等實體瘤的治療取得了突破性進展,腫瘤的免疫治療進入了新時代[4]。這些免疫檢查點抑制劑也嘗試用于食管癌,針對食管癌的免疫治療研究初顯成效[5]。目前,免疫檢查點抑制劑以程序性細胞死亡蛋白-1[6](programmed death-1,PD-1/PD-L1)抑制劑和細胞毒性T淋巴細胞相關抗原4(cytotoxic T lymphocyte-associated antigen-4,CTLA-4)抑制劑為主[7],但有關療效的系統評價較少,其安全性和毒性仍存在質疑。本研究旨在評價現有PD-1/PD-L1免疫檢查點抑制劑療法對接受手術、放療或化療的食管癌患者的療效和毒性,比較不同的治療策略的療效及安全性,為臨床醫師和腫瘤學研究者提供全面的循證指南,為相關的臨床研究、臨床治療過程中藥物選擇提供參考。
資料和方法
資料選擇
研究類型 隨機對照試驗(randomized controlled trials,RCTs),處于Ⅱ期或Ⅲ期的雙臂臨床試驗。
研究對象 診斷為組織學或細胞學的晚期食管癌、先前接受過手術、化療、放療等傳統治療的成人患者。
干預類型 對照組采用常規化療方案治療;試驗組在對照組干預措施基礎上加用或直接使用免疫檢查點抑制劑免疫治療。
結局指標 主要結局指標:總體生存率(overall survival,OS);次要結局指標:無進展生存期(progression-free survival,PFS)、總體療效評價、與免疫相關的反應、與治療相關的不良反應(treatment-related adverse events,TRAEs)。
文獻檢索策略計算機檢索Embase、PubMed、CENTRAL及其他來源檢索庫,查詢食管癌免疫療法的相關研究,主要包括免疫檢查點抑制劑治療,包括會議論文及學位論文,語種不限,檢索時限為建庫至2022年11月20日。檢索詞包括食管癌的相關詞匯(esophageal neoplasms,esophageal cancer,esophageal carcinoma,esophagus cancer,esophagus carcinoma)、免疫療法(chemical therapy,chemotherapy,chemotherapeutic,chemotherapy combined,immune therapy,immunization therapy,immunotherapy,PD-1 inhibitors,PD-L1 inhibitors)以及研究類型(clinical trials, randomized controlled trials,RCTs)。本研究在Cochrane Library的注冊號:501519050617405596。
文獻篩選與資料提取利用NoteExpress文獻管理軟件篩選文獻、提取資料并進行核對,排除標準:(1)只有摘要而無正文的文獻;(2)無法提供所需數據的文獻;(3)書籍、信件、專家意見、病例報告、動物試驗相關文獻。盡量與原作者聯系補充缺乏的資料,制定并填寫數據提取表。提取內容包括第一作者姓名、發表日期、研究類型、研究對象年齡及性別、腫瘤分期、化療方案、免疫細胞劑量及結局指標等信息。
文獻質量評價納入的RCTs研究參考Cochrane協作網對偏倚風險評價條目[8]的設定,獨立評估每項研究的偏倚風險:使用隨機數字表、計算機隨機、拋硬幣、洗撲克或信封、抽簽、擲骰子時給1分;中心化分配、同一外觀、連續編號的藥物容器、不透明的信封給藥給1分;采用盲法給1分;沒有丟失結局數據、采用傾向性分析給1分;無選擇性結局報告給1分;研究表現出沒有其他偏倚來源給1分;根據每項評分得出總得分。
統計學分析采用RevMan5.4軟件進行Meta分析。納入研究結果間的異質性采用χ2檢驗(檢驗水準α=0.10)。若各研究間無統計學異質性(P>0.10,I2<50%),采用固定效應模型進行分析;若各研究間存在統計學異質性(P<0.10,I2>50%),則采用隨機效應模型進行分析,或采用亞組分析與敏感性分析處理、解釋其異質性來源。采用危險比(hazard ratio,HR)和95%CI評估RCTs的OS和PFS,客觀緩解率(objective response rate,ORR)、疾病控制率(disease control rate,DCR)和與治療相關的不良事件用風險比(risk ratio,RR)及其95%CI來評估。采用Stata16.0進行Egger檢驗、Begg檢驗,以評估研究的發表偏倚。
結 果
文獻篩選結果初步檢索相關文獻329篇,其中檢索數據庫及檢索文獻數具體如下:Embase(n=108)、PubMed(n=58)、CENTRAL(n=176)以及其他檢索庫(n=15)。通過NoteExpress文獻管理軟件刪重98篇,通過閱讀標題摘要和關鍵詞排除無關文獻、非臨床試驗及已注冊的protocol文獻155篇,對剩余的98篇文獻進行全文閱讀,篩除85篇(包含27篇綜述報告,7篇重復臨床試驗,37篇論文摘要,8篇病理討論,以及6篇非單一干預)的文獻。對符合標準的13篇文獻進行深入閱讀,最終納入10篇文獻[7-16],包含6 497個實驗對象。納入文獻的研究主要為免疫檢查點抑制劑的相關臨床試驗,包括帕勃利珠單抗(Pembrolizumab)、納武單抗(Nivolumab)、卡瑞利珠單抗(Camrelizumab)、特瑞普利單抗(Toripalimab)等。具體篩選過程見圖1。

圖1 納入文獻篩選流程圖Fig 1 Flow chart of the study identification process
納入文獻的基本特征和風險偏倚評估結果納入研究的基本特征見表1,10篇文獻中的RCTs研究共包含受試對象6 497人。RCTs研究的風險偏倚由RevMan5.4進行評估,本次Meta分析中包含的10項研究在隨機序列生成以及對受試者及研究人員的盲法使用方面均為低風險,1項研究在對結果評估的盲法使用風險較高,1項研究未報告完整的結局數據。總體來說,納入的研究質量評估的風險偏低(圖2)。

表1 納入文獻研究的一般特征Tab 1 Basic characteristics of the eligible studies

圖2 由RevMan評估的納入RCT研究的風險偏倚圖Fig 2 Risk of bias graphed by RevMan to review authors' judgements about each risk of bias item presented as percentages across all included studies
Meta分析結果
總體生存率 總體生存率(overall survival,OS)的數據來自10篇文獻[7-16]的研究,各研究間的OS異質性低(I2<50%),采用固定效應模型。用HR作為效應指標,Meta分析結果顯示,免疫干預組的OS優于對照組,即接受PD-1/PD-L1免疫檢查點抑劑處理組的患者死亡風險明顯低于接受傳統手術、放化療的晚期食管癌患者,且差異有統計學意義(HR=0.75,95%CI:0.71~0.80,P<0.000 1;H:I2=48%,P=0.05)(圖3)。對不同因素進行亞組分析的結果如圖4所示,在性別、種族、PD-L1表達、癌癥的組織學特征以及有無遠處轉移、有無吸煙亞組間的OS均有顯著差異(P<0.05);男性、亞洲人群、有遠轉移、組織學特征為鱗癌以及目前吸煙的患者中,免疫療法的OS更高;PD-L1腫瘤陽性評分(tumor proportion score,TPS)≥1%的患者OS優于TPS<1%的患者(HR:0.66vs.0.85,P組內<0.001),同樣的優勢在TPS≥10%及CPS≥10%亞組內也能觀察到。在不同類型的免疫抑制劑療法中,相對于傳統化療療法,Toripalimab顯示出最佳的OS優勢,其次是Sintilimab和Camrelizumab,但其亞組內差異無統計學意義(P亞組=0.061)。
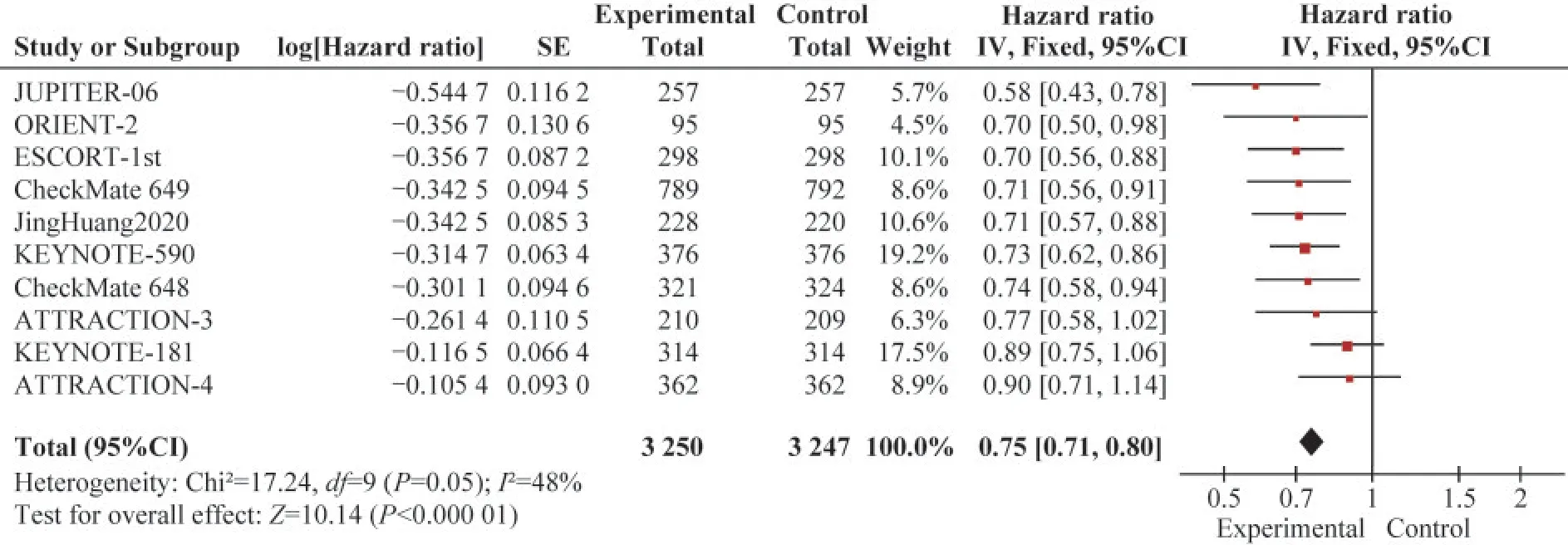
圖3 總體生存率的Meta分析森林圖Fig 3 Forest plot of comparison of overall survival intervention
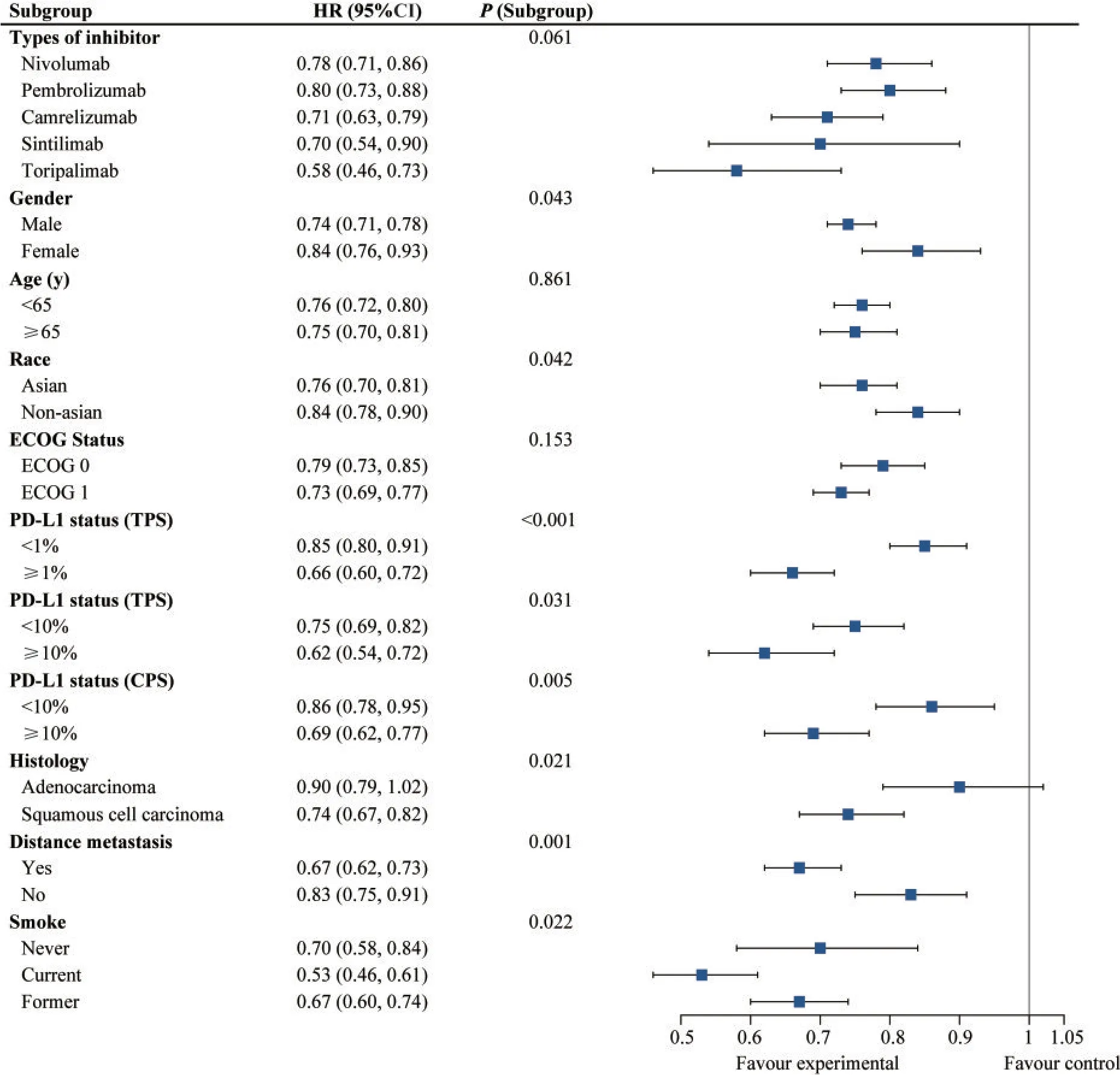
圖4 總體生存率的亞組分析Fig 4 Subgroups analysis of overall survival
無進展生存期 PFS的數據來自10篇文獻[7-16]的研究結果,各研究間的PFS異質性較高(I2>50%,P<0.001),因此采用隨機效應模型。采用HR作為效應指標,Meta分析結果顯示,免疫抑制劑治療組的患者總體PFS顯著優于對照組,說明免疫治療組食管癌病情惡化風險低于對照組(HR=0.77,95%CI:0.66~0.90,P=0.000 8; H:I2=90%,P<0.001)(圖5)。
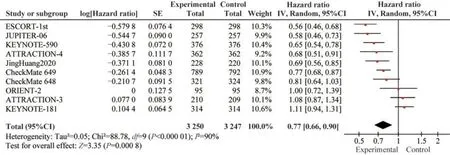
圖5 無進展生存期的森林圖Fig 5 Forest plot of comparison of progression-free survival intervention
總體療效評價 總體療效由ORR和DCR來評價,分別納入8個研究[9,11-13,15-18]和5個研究[7,10-13]的數據。采用RR作為效應指標,Meta分析結果顯示,免疫治療組的患者ORR高于對照組,差異有統計學意義(RR=1.28,95%CI:1.16~1.40,P<0.000 1;H:I2=49%,P=0.06)(圖6A),各研究間異質性較低,采用固定效應模型;免疫治療組的患者DCR高于對照組,且納入研究的異質性低,差異有統計學意義(RR=1.07,95%CI:1.02~1.12,P=0.003;H:I2=28%,P=0.24)(圖6B)。
安全性比較 安全性分析結果如表2所示,在TRAEs比較中,對于任何級別的不良反應(RR=0.97,95%CI:0.96~0.99,P<0.001)和≥3級的不良反應(OR=0.98,95%CI:0.94~1.02,P=0.22)發生率,免疫抑制劑療法組均低于對照組,僅前者差異有統計學意義;然而,相比于傳統療法,免疫療法組患者發生嚴重不良反應(RR=1.67,95%CI:1.51~1.86,P<0.001)、因不良反應引起治療中止(RR=1.09,95%CI:1.00~1.19,P=0.049)的可能性更高;在與不良反應相關的死亡風險中,兩組差異無統計學意義。與對照組相比,免疫療法組發生免疫相關的不良反應發生風險較高(RR=2.45,95%CI:2.16~2.78,P<0.001)。

表2 與治療及免疫相關的不良反應的Meta分析結果Tab 2 Results of Meta-analysis of treatment-related and immune-related adverse events
敏感性分析和發表偏倚分析 在總體療效分析中,逐個剔除研究后,發現剔除Keynote-181研究后,疾病控制率的異質性(I2)從67%下降為0,提示該研究結果為敏感性來源,因此在DCR的分析中不納入該研究的結果。總體生存分析和安全性評價中,逐個剔除研究后,結果未發生逆轉且變化小,提示Meta分析結果穩健,敏感性較小。繪制報道PFS、ORR以及TRAEs的文獻發表偏倚漏斗圖,顯示對稱性欠佳,考慮與樣本納入量較少有關。進一步進行Begg檢驗和Egger檢驗,結果顯示,對于OS以及PFS,Egger檢驗結果分別為P=0.762及P=0.013,提示PFS的分析結果受發表偏倚影響可能性較高;對于總體療效以及安全性比較,Begg檢驗結果提示分析結果受發表偏倚影響的可能性較小(表3)。

表3 Begg檢驗和Egger檢驗的P值Tab 3 P values of Begg’s and Egger's tests
討 論
食管癌的發病因素眾多,除了地域因素,還與患者年齡、性別、種族生活環境及飲食習慣有關[19]。多數患者早期無明顯臨床表現,部分患者首次就診時已進展至中晚期[20]。手術、放療和化療是食管癌患者的常規治療手段,但其效率不高,且有較大的毒性副反應,患者常因難以耐受痛苦而中斷治療,使得食管癌預后較差。相比而言,食管癌的免疫治療安全性強,且療效顯著[21]。
本研究探討的免疫檢查點抑制劑是針對相應的免疫檢查點研發的單抗類藥物,可阻斷表達免疫檢查點的腫瘤細胞對免疫細胞的抑制作用[22]。納入研究中的免疫檢查點抑制劑主要包括PD-1/PDL1抑制劑,T細胞表面的PD-1與高表達在腫瘤細胞表面的PD-1配體(PD-L1或PD-L2)結合后可使PD-1通路持續激活,進而抑制T細胞對腫瘤細胞的殺傷作用,因此抑制PD-1通路可以阻斷這一通路,恢復部分T細胞的功能,加強機體對腫瘤的自身免疫[23]。目前針對食管癌中PD-1/PD-L1通路開展的臨床研究以PD-1抑制劑Pembrolizumab和Nivolumab為代表,近年來以國產新型PD-1單抗如Sintilimab[24]、Atezolizumab[25]等開展的臨床研究也顯示出了較好的療效,可提高晚期食管癌患者的疾病控制率,改善患者的免疫功能和生活質量[26]。
盡管不同臨床試驗中,免疫檢查點抑制劑對晚期食管癌患者的有效性和安全性有不同的結論,但本次Meta分析結果顯示,通過對結果及統計量的合并,PD-1/PD-L1抑制劑的免疫檢查點抑制劑療法和/或聯合放化療,無論是一線治療還是化療后進展的二線治療,均能有效提高食管癌的OS、PFS、ORR和DCR,且具有可管理的安全性。與國內外的研究相比,目前對于食管癌的免疫療法Meta分析文獻較少,在Wang等[27]的研究中,PD-1/PD-L1抑制劑療法已顯示在晚期食管/胃食管交界癌患者中具有一定的抗腫瘤療效和可控的安全性,且PD-L1過表達且用了抑制劑的患者的ORR更高;Yang等[28]的研究也顯示,以PD-1/PD-L1為靶點治療晚期食管胃管癌患者延長了部分患者的生存期,但與單純化療相比,免疫療法表現出更高的治療毒性。本研究在一定程度上對食管鱗癌及腺癌患者免疫療法的有效性和安全性的臨床證據進行了補充和完善。
總體生存期的亞組分析結果表明,PD-1/PDL1抑制劑對總體生存期的顯著改善在不同特征的患者中有差異。PD-L1的表達作為腫瘤免疫療法的療效生物標志物,是治療預后及臨床反應的較好預測指標[29],本研究顯示,不論是根據TPS還是CPS作為亞組進行分析,PD-L1高表達的患者均表現出較高的總體生存期,與既往結果一致[5,28]。性別和年齡是已知與免疫反應療效相關的因素[30],本研究發現男性食管癌患者接受免疫療法后具有更高的OS,這與Fabio等[31]的研究結論相同,可能是由于性激素調節的差異,男性和女性對外來及自身抗原的免疫反應不同,且在先天性及適應性免疫反應方面表現出差異[30]。在免疫療法的種族差異方面,本研究發現亞洲人相比于非亞洲人有更優的OS,Peng等[32]針對PD-1抑制劑的研究中也觀察到了相同的結果,一種可能的解釋是亞洲與非亞洲患者之間存在T細胞功能和病理特征的差異[33]。此外,腫瘤的組織學特征、有無遠處轉移以及患者的吸煙情況也在亞組分析中顯示出差異,提示應根據不同患者的具體特征評估PD-1/PD-L1抑制劑療法的療效和預后。總體而言,PD-1/PD-L1抑制劑治療的生存獲益在本研究中得到進一步證實。
安全性評價中,免疫抑制劑在任何級別的TRAEs發生更少,但因治療導致的嚴重不良反應、治療中止以及與免疫相關的不良反應在免疫干預組中顯示出更高的發生風險。許多研究表明,抗PD-1/抗PD-L1抗體的免疫相關不良事件是由于T細胞抑制的自我耐受性受損,不良反應一般可控,但在某些情況下也可能是致命的[34],因此在治療過程中密切關注患者的不良反應十分重要。考慮到免疫治療的安全性與樣本量及患者個體耐受力差異等因素有關,需要納入大樣本的具體數據進行評估。通過漏斗圖、Egger檢驗、Begg檢驗法對納入文獻的發表偏倚進行檢測,結果表明無明顯發表偏倚;敏感性分析表明,本次Meta分析的結果較為穩健。
本研究的優勢在于納入了國內外實施完善的RCTs,對晚期食管癌免疫抑制劑療法的總體療效及安全性進行了合并分析,并在亞組分析中考慮了患者的特征,如年齡、性別、吸煙史以及PD-L1表達等影響療效的重要因素。本研究有一定的的局限性:(1)各研究中化療方案不盡相同,可能會影響結果一致性;(2)僅納入關于PD-1/PD-L1抑制劑的試驗進行分析,對于免疫檢查點療法的研究結果一定程度上缺乏推廣意義;(3)免疫療法存在特定的不良反應,本研究的安全性評價中并未分析不同免疫相關反應的發生率。
本研究顯示,以PD-1/PD-L1免疫檢查點抑制劑為主的食管癌免疫療法可以提高食管癌的治療療效和總體生存水平,顯示出優于傳統化療的安全性,但可能存在一定的免疫毒性。本研究對臨床實踐具有一定指導意義,但納入的研究和病例數有限,所得結論需要更進一步的臨床數據及分析支持。
作者貢獻聲明許雨柔 論文構思和撰寫,文獻檢索,數據整理和分析。蔡寧,鄒宜豐 檢索策略制定。范佳慧 文獻質量篩選,論文修改。陳興棟,索晨 可行性分析,論文指導和修訂。
利益沖突聲明所有作者均聲明不存在利益沖突。

