前列地爾治療感染性休克合并急性呼吸窘迫綜合征的效果觀察
段文文 秦 超
鄭州大學第五附屬醫院重癥醫學科,河南省鄭州市 450000
感染性休克是因病原微生物入侵引起的膿毒癥而導致的循環衰竭和細胞代謝異常的嚴重全身障礙疾病,可引起多器官功能障礙綜合征(MODS),其中以急性呼吸窘迫綜合征(ARDS)最為常見,病死率可高達48%~75%[1],嚴重威脅患者生命安全。目前臨床治療該疾病已形成完整的體系。但是隨著研究的深入發展[2],發現微循環障礙是ARDS發生的重要機制,而常規治療中往往忽略改善微循環障礙致使病情恢復緩慢,難以達到令人滿意的治療效果。前列地爾是一種具有高生物活性的PGE1類物質,具有擴張血管等生理藥理作用,將其用于該類患者中可能會更有效,故我院對此進行探討,結果如下。
1 資料與方法
1.1 一般資料 前瞻性選取2020年9月—2022年2月我院收治的109例感染性休克合并ARDS患者作為觀察對象。納入標準:(1)符合感染性休克診斷標準[3];(2)伴有ARDS;(3)患者家屬均簽署書面知情同意書。排除標準:(1)伴有嚴重凝血功能障礙者;(2)對本研究所用藥物過敏者;(3)伴有嚴重心腦血管疾病者。將所納入的患者按照隨機數字表法分為常規組和聯合組。常規組54例,男29例,女25例;年齡32~74歲,平均年齡(54.76±15.34)歲;APACHE Ⅱ評分23~31分,平均APACHE Ⅱ評分(25.31±4.25)分。聯合組55例,男31例,女24例;年齡33~75歲,平均年齡(55.21±14.98)歲;APACHE Ⅱ評分23~32分,平均APACHE Ⅱ評分(25.54±4.39)分。兩組基線資料對比無統計學差異(P>0.05),具有可比性。我院倫理委員會已對本研究予以審核批準。
1.2 方法 常規組予以常規治療:根據基礎藥敏試驗予以敏感抗生素進行抗感染治療;采用呼吸機進行輔助呼吸;予以營養支持治療。聯合組給予前列地爾注射液(南陽普康藥業,國藥準字H41024186,規格:100μg)治療,泵以2.5μg/h的速度泵注,10μg/次,1次/d。兩組患者均連續治療10d。
1.3 觀察指標
1.3.1 肺血管通透性:治療前以及治療10d后,采用脈搏指示連續心排血量監測技術檢測肺血管外肺水指數(EVLWI)、肺血管通透性指數(PVPI)。
1.3.2 免疫功能:治療前以及治療結束后,抽取5ml肘部空腹靜脈血采用流式細胞儀檢測誘導性T細胞/輔助性T細胞(CD4+)、抑制性T細胞/細胞毒性T細胞(CD8+)以及CD4+/CD8+水平。
1.3.3 腸道黏膜屏障功能:治療前以及治療結束后,采用酶學分光光度法檢測D-乳酸、二胺氧化酶,采用鱟試劑比濁法檢測內毒素水平。
1.3.4 不良反應發生情況:治療期間,統計兩組患者各種不良反應的發生率,包括血壓驟降、惡心嘔吐、頭痛、刺痛、心動過緩。
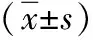
2 結果
2.1 兩組肺血管通透性對比 治療前兩組患者肺血管通透性各指標對比無統計學差異(P>0.05);治療10d后兩組肺血管通透性各指標均低于治療前,且聯合組低于常規組(P<0.05),見表1。
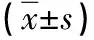
表1 兩組肺血管通透性對比
2.2 兩組免疫功能對比 治療前兩組免疫功能各指標對比無統計學差異(P>0.05);治療10d后,CD4+、CD4+/CD8+高于治療前,且聯合組高于常規組,CD8+均低于治療前,且聯合組低于常規組(P<0.05),見表2。
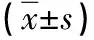
表2 兩組免疫功能對比
2.3 兩組腸道黏膜屏障功能對比 治療前兩組患者D-乳酸、二胺氧化酶以及內毒素對比差異均無統計學院意義(P>0.05);治療10d后兩組D-乳酸、二胺氧化酶以及內毒素均低于治療前,且聯合組低于常規組(P<0.05),見表3。
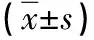
表3 兩組腸道黏膜屏障功能對比
2.4 兩組不良反應發生率對比 治療期間,兩組不良反應總發生率對比差異無統計學意義(χ2=1.682,P=0.194>0.05),見表4。

表4 兩組不良反應發生率對比[n(%)]
3 討論
ARDS是感染性休克最常見的并發癥,當感染發生后體內大量的炎癥因子釋放,可對肺血管內皮細胞造成不同程度的損傷,繼而激活機體的凝血系統,致使血液黏膜滯度升高,因此中性粒細胞肺部浸潤積聚以及肺血管通透性增加為感染性休克并ARDS的主要特征[4]。因此抗炎以及保護血管內皮功能為臨床治療該疾病的主要方式。目前通常采用抗炎、抗凝等作為主要治療方式。既往研究[5]發現微循環障礙為感染性休克并ARDS的主要機制,而常規治療中對微循環治療較為薄弱,故難以達到令人滿意的效果。前列地爾是一種天然前列腺素類物質,具有改善微循環的作用,將其用于該類患者中可能會彌補常規治療方式的不足。
EVLWI是可以反映肺泡、肺間質內液變化程度的特異性量化指標,其水平上升提示肺泡—毛細血管屏障功能障礙,另外EVLWI的升高與ARDS患者病死率增加相關。在膿毒癥休克患者中EVLWI水平呈顯著上升趨勢,當患者發生ARDS時,肺泡釋放大量的細胞因子,進而刺激巨噬細胞合成炎癥因子,導致肺泡上皮細胞發生壞死、凋亡,降低內皮細胞的功能,增加肺通透性,最終使得EVLWI水平異常上升增高。PVPI是反映ARDS病情嚴重程度的有效指標[6]。本文中,聯合組EVLWI及PVPI均低于常規組(P<0.05),說明前列地爾治療感染性休克合并ARDS患者可改善肺血管通透性。可能的原因是首先常規治療方案中通過抗感染等一系列治療措施有效控制炎癥水平,減輕炎性浸潤,減輕對肺泡—毛細血管屏障功能障礙的損害,降低血管通透性。其次前列地爾通過降低組織中內皮素含量,防止血管過度收縮,對炎癥細胞的黏附和聚集進行抑制,減輕炎性浸潤,進一步降低血管通過性,以達到改善肺血管通透性的目的。
Th1/Th2細胞比例以及功能的失調是感染性休克并ARDS患者免疫調節紊亂的主要表現。本文中,聯合組免疫功能各指標均優于常規組(P<0.05),說明前列地爾治療該類患者可更好地調節免疫功能。可能的原因是首先前列地爾可抑制前列腺素受體2蛋白激酶A信號,對T細胞的功能進行調節,改善機體的免疫功能。其次前列腺素E1是構成前列地爾的主要成分,該物質具有抑制血小板積聚、改善血液紅細胞變形等作用,因此可對機體的微循環進行調節,從而更好地減輕機體炎癥反應,降低炎性物質對免疫功能的影響,從而加快免疫功能的恢復。另外本文中,聯合組不良反應總發生率為12.73%,略高于常規組的5.56%,但組間對比差異無統計學意義(P>0.05),說明將此藥物用于該類患者的治療中不增加不良反應發生率,與王建國等[7]的結論一致,可能同本研究所納入樣本量小而產生的偏倚性有關。
胃腸道是感染性休克后影響最早、病變最嚴重的器官之一,以腸黏膜屏障功能損傷為主。D-乳酸、二胺氧化酶以及內毒素均可經通透性增加的腸道進入血循環,形成內毒素血癥,進而誘發或加重全身炎性反應。本文中,聯合組D-乳酸、二胺氧化酶以及內毒素均低于常規組(P<0.05),說明前列地爾治療該類患者可減輕對腸道黏膜屏障功能的影響。可能的原因是前列地爾作為天然前列腺素類藥物,可增加體內的cAMP的含量,增加機體對Ca2+的吸收,降低Ca2+的含量,從而發揮抑制血小板聚集,改善血液循環,增加腸黏膜血液灌注量,以此達到改善腸黏膜屏障功能障礙的作用[8]。
綜上所述,將前列地爾用于感染性休克合并ARDS患者中可改善肺血管通透性,調節免疫功能,減輕對腸道黏膜屏障功能的影響,且不會增加不良反應發生率。

