不同年齡病理性近視脈絡膜新生血管患者黃斑形態和微循環指標比較
劉 坤, 徐清怡, 朱 俊, 陳 放
(1. 江蘇省建湖縣人民醫院 眼科, 江蘇 鹽城, 224700;2. 揚州大學附屬蘇北人民醫院 眼科, 江蘇 揚州, 225001)
病理性近視脈絡膜新生血管(PM-CNV)是可以導致中心視力突然喪失的嚴重影響患者視力的病理性近視(PM)并發癥之一[1]。研究[2]表明, 50歲以下的脈絡膜新生血管(CNV)患者中, PM-CNV是最常見的病因。老年PM-CNV患者可能同時具有老年性黃斑變性和PM的臨床病理生理特征[3], 故老年PM-CNV患者的治療方案與青年患者是否應該有所區別值得進一步探討。本研究對PM-CNV患者進行常規眼科檢查和光學相干斷層成像(OCT)、光學相干斷層掃描血管成像(OCTA)檢查,比較不同年齡層PM-CNV患者的基本特征、患眼黃斑形態和微循環指標水平,現將結果報告如下。
1 資料與方法
1.1 一般資料
采用橫斷面研究方法分析2019年12月—2022年11月在江蘇省蘇北人民醫院確診PM-CNV的70例患者(均為單眼發病,共納入70眼)的臨床資料,根據年齡的不同將患者分為≤50歲組18例(18眼)和>50歲組52例(52眼)。納入標準: ① 有高度近視病史,等效球鏡度數(SE)≥-6.0 D或眼軸≥26.5 mm者; ② OCTA檢查提示CNV存在者。排除標準: ① 既往接受過光動力療法,或有玻璃體腔注射抗血管內皮生長因子(VEGF)藥物治療史及玻璃體視網膜手術史者; ② 存在其他可引起CNV的眼部疾病(老年黃斑變性、血管樣條紋、中心性滲出性脈絡膜視網膜病變、炎癥性疾病等)者; ③ 存在其他影響視力的眼部疾病(糖尿病性視網膜病變、青光眼、視網膜靜脈阻塞、葡萄膜炎等)者; ④ 屈光介質混濁導致OCT、OCTA圖像質量不佳或嚴重影響視力者。≤50歲組患者平均年齡(38.22±9.59)歲,男9例、女9例; >50歲組患者平均年齡(65.04±9.70)歲,男16例、女36例。2組患者性別構成比較,差異無統計學意義(P=0.142)。本研究遵循《赫爾辛基宣言》要求,且獲得蘇北人民醫院倫理委員會批準(倫理批號2022ky131)。
1.2 方法
記錄所有患者的年齡、性別、患病眼別,均給予裂隙燈檢查(日本Topcon株式會社)、OCT與OCTA檢查(美國Optovue公司RTVue XR)和最佳矯正視力(BCVA)、眼軸(IOL-Master眼科光學生物測量儀,德國Zeiss公司)、SE檢查。
檢查方法: ① BCVA檢查采用國際標準視力表,并轉換為LogMAR視力進一步統計分析。② 眼軸測量由同一檢查者完成,每只眼進行5次測量后取平均值。③ OCT檢查指標由3位經驗豐富的眼科技師手動測量取平均值,記錄并分析黃斑中心凹下外層視網膜結構,主要包括Bruch膜、嵌合體帶完整性,黃斑中心凹1 mm×1 mm范圍內連續則視為完整,若不連續則視為不完整。④ OCTA掃描范圍為以中心凹為中心的3 mm×3 mm區域,自動去除眼球運動偽影,每次掃描后仔細校對分層是否正確,若遇到機器不能正確分層的情況,由2位經驗豐富的眼科技師手動調整錯誤分區。設備自動測量得到黃斑區淺層及深層毛細血管網血流密度,在Flow工具中,選擇脈絡膜毛細血管層,以黃斑中心凹為中心對半徑1.0 mm的圓形區域自動化測量血流面積,脈絡膜毛細血管血流密度(CC-VD)為血流面積與選中圓形區域面積的比值。手動選取CNV后,設備自動測量CNV面積、CNV血流面積,機器自動將黃斑區劃分為直徑分別為1 mm和3 mm的內環和外環,中心凹為內環以內區域,旁中心凹為內環、外環之間的區域,根據CNV相對中心凹的位置將CNV位置定義為中心凹下及中心凹外。黃斑中心凹視網膜厚度(CMT)為黃斑中心凹1 mm范圍內界膜到視網膜色素上皮(RPE)層的平均垂直距離,中心凹下內層視網膜厚度(IRT)為黃斑中心凹1 mm范圍內界膜到內叢狀層的平均厚度,中心凹下外層視網膜厚度(ORT)為黃斑中心凹1 mm范圍內從內核層到RPE層的平均厚度,中心凹下脈絡膜厚度(SFCT)為Bruch膜下10 μm至鞏膜內表面的垂直距離; 視網膜淺層毛細血管血流密度(SCP-VD)為內界膜至內叢狀層上10 μm區域內的血流密度; 視網膜深層毛細血管血流密度(DCP-VD)為內叢狀層上10 μm至外叢狀層上10 μm區域內的血流密度。
1.3 統計學分析

2 結 果
2.1 眼科常規檢查結果
≤50歲組患者平均LogMAR BCVA為(0.56±0.35), >50歲組為(0.69±0.34), 差異無統計學意義(P=0.164); ≤50歲組患者SE為-11.88(-17.00, -9.19)D, >50歲組為-12.00(-15.00, -9.63) D, 差異無統計學意義(P=0.556); ≤50歲組患者平均眼軸為28.70(26.93, 30.16) mm, >50歲組為28.74(27.86, 29.76) mm, 差異無統計學意義(P=0.587)。
2.2 黃斑形態指標水平比較
≤50歲組CMT、ORT均小于>50歲組,但差異無統計學意義(P=0.106、0.134); ≤50歲組IRT大于>50歲組,但差異無統計學意義(P=0.797); ≤50歲組SFCT大于>50歲組患者,差異有統計學意義(P<0.001)。見表1。
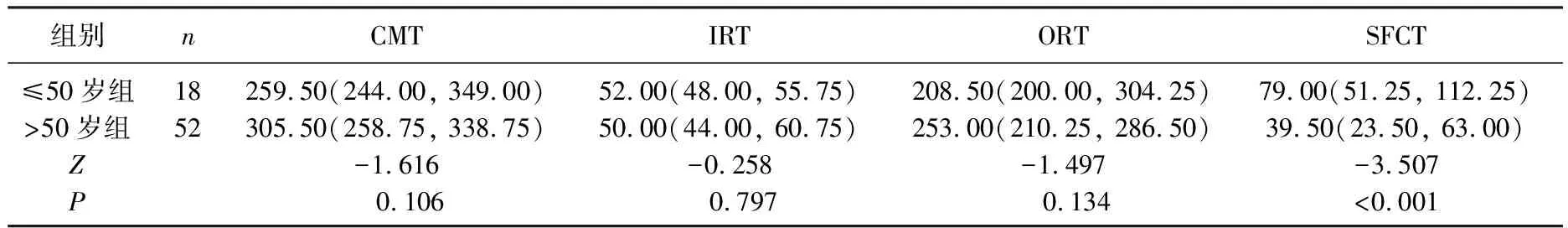
表1 2組黃斑區視網膜厚度比較[M(P25, P75)] μm
黃斑中心凹下外層視網膜結構觀察結果顯示, ≤50歲組嵌合體完整者7例(占38.89%), >50歲組嵌合體完整者19例(占36.54%), 差異無統計學意義(P=0.859); ≤50歲組Bruch膜完整者14例(占77.78%), >50歲組Bruch膜完整者37例(占71.15%), 差異無統計學意義(P=0.586)。
2.3 黃斑區微循環指標水平比較
≤50歲組的SCP-VD高于>50歲組,差異有統計學意義(P=0.001); 2組DCP-VD、CC-VD比較,差異無統計學意義(P=0.384、0.348)。見表2。

表2 2組黃斑區微循環指標水平比較 %
2.4 CNV相關指標水平比較
≤50歲組CNV面積、CNV血流面積分別為0.43、0.39 mm2, >50歲組則分別為0.38、0.29 mm2, 2組比較差異無統計學意義(P=0.326、0.242)。≤50歲組中, CNV位于中心凹下11例、中心凹外7例; >50歲組中, CNV位于中心凹下35例、中心凹外17例。2組CNV位置比較,差異無統計學意義(P=0.633)。
3 討 論
PM是全球常見的致盲眼病之一,其并發癥CNV會造成嚴重的視力損害[1]。PM-CNV的發病機制尚未完全明確,既往研究[4]認為PM患者眼軸不斷增長造成Bruch膜破裂,促血管生長因子與抗血管生長因子之間的平衡被打破,繼而誘導CNV形成。然而有研究[5]發現CNV也可以出現在正常眼軸的高度近視患者中,而這些患者普遍存在黃斑區循環缺血及局部脈絡膜組織萎縮,提示包含脈絡膜結構的黃斑形態結構及微循環異常可能參與PM-CNV的形成。OCT、OCTA能以無創方式提供視網膜和脈絡膜斷層結構及分層血流信息,并能定量評估視網膜及脈絡膜毛細血管網密度[6], 因此本研究基于OCT、OCTA檢查對PM-CNV患者黃斑區視網膜形態、微循環指標水平及CNV相關指標水平進行分析。
西歐地區的一項研究[7]顯示,年齡小于50歲的CNV患者中, PM-CNV約占62%, 且PM是西歐地區CNV患者最常見的致病因素。中國一項針對青年CNV患者的研究[8]顯示, PM位列青年CNV病因第2位,可見PM-CNV在青年患者中發病率很高。隨著時間的推移, PM的高發病率必將導致老年PM-CNV患者數量不斷增加,而老年PM-CNV的病因更加復雜,預后結局可能比青年PM-CNV患者更差。比較不同年齡PM-CNV患者黃斑形態與微循環指標水平的差異,或可為PM-CNV的發病機制與治療策略研究提供更多的臨床依據。本研究結果顯示, >50歲組PM-CNV患者的SFCT小于≤50歲組,差異有統計學意義。近年來較多研究[5, 9]發現高度近視患者的脈絡膜厚度顯著小于視力正常人群,脈絡膜厚度減小可能提示脈絡膜循環不良,可導致患者視功能受損甚至視力喪失,因而脈絡膜厚度與BCVA顯著相關。脈絡膜厚度可間接反映脈絡膜供血情況, PM-CNV患者中,老年患者的脈絡膜厚度較年輕患者更小,提示老年PM-CNV患者脈絡膜循環水平更差,甚至可能存在更嚴重的脈絡膜缺血情況。
相關研究[10]提出,脈絡膜循環的血流動力學改變是CNV出現的原因之一,脈絡膜變薄會引起脈絡膜缺血,促進VEGF分泌,進而促進新生血管產生。本研究中, >50歲組的樣本量顯著多于≤50歲組, >50歲組患者的SFCT顯著小于≤50歲組,提示SFCT與PM、年齡存在相關性,即老年患者脈絡膜厚度更小,脈絡膜缺血更嚴重,并發PM-CNV的概率更高。
研究[11]發現, 2年隨訪期間內發生近視性黃斑病變進展的患者,其基線SFCT較無黃斑病變進展患者更薄,并提出SFCT是近視黃斑病變進展的獨立預測因子。因此, SFCT間接反映了脈絡膜供血情況,脈絡膜變薄是評價脈絡膜缺血的生物標志物,是近視黃斑病變發展的一個重要的潛在危險因素,提示老年PM-CNV患者的脈絡膜循環不良可能更傾向于發生黃斑病變的進展,進而導致預后較青年患者差。但值得注意的是, >50歲組患者SFCT更低,但>50歲組患者脈絡膜毛細血管血流密度與≤50歲組比較差異無統計學意義。由此提示, SFCT可能較微循環指標可以更先一步提示患者脈絡膜循環水平下降,更早一步對患者預后進行預測。
黃斑是體內代謝最活躍的組織之一,在許多疾病狀態的早期即受到缺氧條件的影響。由于高需氧量,黃斑具有多個周圍毛細血管叢,其完整性和功能依賴于這些毛細血管叢的健康。本研究中, ≤50歲組患者SCP-VD顯著高于>50歲組,但2組DCP-VD無顯著差異,提示>50歲患者的淺層視網膜微循環相較≤50歲患者損害更重,但深層視網膜微循環則無顯著差異。PM患者的視敏度會隨著DCP-VD的降低而顯著降低, SCP-VD則對視敏度無顯著影響,提示DCP-VD與PM患者視功能損害有關。深層視網膜毛細血管叢嵌于內核層和外叢狀層,有助于為光感受器內節段提供氧氣[12]。PM患者的脈絡膜變薄,脈絡膜毛細血管喪失,因此DCP-VD降低可能導致光感受器缺氧和營養缺乏,進而造成視力下降。本研究中,雖然≤50歲組患者SCP-VD較>50歲組顯著更高,但2組的DCP-VD無顯著差異,故2組BCVA亦無顯著差異。有研究[13]提出,年齡與SCP-VD、DCP-VD、全視網膜平均毛細血管血流密度均呈顯著負相關。本研究中>50歲患者的SCP-VD顯著更低,可能與其年齡增長帶來的影響(如視網膜淺層毛細血管中血液流速減慢及血管阻力增加)有關。
本研究中,部分PM-CNV患者RPE與橢圓體帶之間表現為邊緣模糊,但2組嵌合體帶、Bruch膜完整性差異均無統計學意義。黃斑區外層視網膜結構改變可能由CNV產生的滲出物導致,研究[14]表明黃斑形態結構改變可以早于視覺癥狀,且多達93%的患者在治療后可以恢復正常。相關研究[15]發現,術前外層視網膜結構完整的患眼術后視力更好,因此外層結構的完整性對患者病情評估和療效預測具有重要意義。外層視網膜結構中, Bruch膜被認為參與近視的發生,其病理性改變可能是近視發展的始動因素,也是造成PM進展的要素之一[16]。研究[17]提出, Bruch膜缺損對PM-CNV患者的視力預后和治療效果有重要影響, Bruch膜形態不完整意味著預后更差,無Bruch膜缺損的患者則視力預后更好。本研究發現, >50歲患者的視網膜外層結構(嵌合體帶、Bruch膜完整性)與≤50歲患者無顯著差異,表明雖然視網膜外層結構對視力預后較為重要,但外層結構破壞的原因可能與疾病本身更為相關,與患者基線年齡則無關。

