高糖誘導人牙髓細胞鈣化的初步探究
劉瑜佳 關為群
福建醫科大學附屬協和醫院口腔科,福建省福州市 350000
糖尿病是一種以高血糖為特征的慢性多系統代謝疾病,影響許多器官和組織的結構、功能和免疫應答。通常表現為纖維化、視網膜病變、神經病變和心血管疾病等并發癥。在我國,由于糖尿病的高發生率,糖尿病相關的口腔疾病包括牙周組織病變、口腔黏膜病變、牙體、牙髓組織病變等逐漸引起人們的重視。
牙髓鈣化是牙髓組織對創傷、齲壞及牙周病等刺激的一種反應,也是一種增齡性變化[1]。關于糖尿病與牙髓鈣化之間的關系,目前的研究很少,最近的一項研究報告稱,與健康人群相比,2型糖尿病患者更容易出現牙髓鈣化并伴有牙髓結石[2],同時有動物實驗研究發現糖尿病大鼠牙髓組織中髓石的數量和大小均高于正常大鼠[3]。糖尿病患者不僅容易產生髓石,根尖周病變也經常發生[4],散在的鈣化顆粒和髓石可能阻擋根管口,從而改變了髓腔內部的解剖形態,增加臨床醫生根管治療難度,為此需要采用合適的器械和方法將髓石移除以完成良好的牙髓治療。為了探索高糖是否會對人牙髓細胞鈣化產生影響,本實驗將不同高濃度的葡萄糖分別作用于人牙髓細胞,觀察其對人牙髓細胞增殖以及鈣化結節形成的影響。
1 材料與方法
1.1 主要試劑及儀器 DMEM、胎牛血清、青霉素、鏈霉素、胰酶、MTT均購自Hyclone公司(美國),葡萄糖、DMSO、茜素紅購于Sigma公司(美國),鼠抗人角蛋白抗體、鼠抗人波形蛋白抗體、DAB顯色劑購于北京中杉金橋生物技術公司,十二烷基硫酸鈉購于北京鼎國生物有限公司,倒置顯微鏡(Nikon TS-100,日本); 高速低溫離心機(Eppendorf,美國);酶聯檢測儀(Biotek Power Wave,美國)。
1.2 人牙髓細胞原代培養 本研究經福建醫科大學附屬協和醫院醫學倫理委員會批準,獲得參與者知情同意,人牙髓組織取自于福建醫科大學附屬協和醫院口腔科因阻生或正畸需要拔除的14~20 歲新鮮健康的恒牙,拔除后置于含雙抗(100μg/ml 青霉素、100μg/ml鏈霉素)的PBS中; 無菌條件下取出牙髓組織,剪成小碎片。使用組織塊貼壁法分離培養。將獲得的細胞懸液置于37°C、5%CO2孵育箱內培養,每2d換液,當細胞融合率達到80%時傳代,取第3~5代細胞進行后續實驗。
1.3 人牙髓細胞(hDPCs)的組織來源鑒定 取處于對數生長期性能穩定、細胞單一的hDPCs,常規消化制備細胞懸液,調整細胞濃度,以每孔5 000個細胞接種于 24 孔板中,待細胞長滿板底 80%時,行細胞波形蛋白及角蛋白免疫細胞化學染色。
1.4 細胞分組及培養基配制 將hDPCs分為: 對照組(5.5mmol/L組)和實驗組(分別為15mmol/L、25mmol/L、35mmol/L、45mmol/L)。含5.5mmol/L 葡萄糖DMEM培養基是人牙髓細胞存活的最基本的營養要素,作為本實驗的對照組。根據葡萄糖濃度(mmol/L)=葡萄糖含量(mg/L)/180(葡萄糖分子量),配制出含不同濃度葡萄糖的高糖培養基。
1.5 MTT法檢測hDPCs增殖活性 將hDPCs以2×103個/孔的密度接種于96孔板內,配制含5.5mmol/L(對照組)、15mmol/L、25mmol/L、35mmol/L、45mmol/L的完全培養基,分別于培養1、3、5、7、10d,每天同一時間,每孔加入10μl MTT,置于37℃ 、CO2孵育箱培養4h后,小心吸掉上清,每孔加入100μl二甲基亞砜,置搖床上低速振蕩10min,使結晶物充分溶解。酶標儀在450nm波長下檢測各組細胞吸光度(A)值。本實驗重復3次,并記錄結果。
1.6 茜素紅染色檢測hDPCs形成鈣化結節能力 將hDPCs以1×105個/孔的密度接種于6 孔培養板內, 培養28d后茜素紅染色,顯微鏡觀察并拍照。為了量化鈣的相對量,每孔加入0.5mol/L HCl和5%十二烷基硫酸鈉(SDS)37℃反應1h。吸取200μl等量的上清液在OD 450nm處測量其吸光度值。做茜素紅標準曲線(0~10mmol/L茜素紅溶解于5%SDS),上述測得的OD值與標準曲線比較,即可獲得茜素紅濃度。
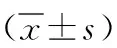
2 結果
2.1 hDPCs的形態及鑒定 牙髓組織塊原代培養1周即可見有hDPCs從組織塊周圍爬出(見圖1a),其形態為長梭形或星形,細胞核圓形或橢圓形,胞體均勻、豐滿,核仁明顯,圍繞組織塊呈放射狀或漩渦狀生長。傳代后的細胞以成纖維樣細胞為主,形態趨于一致(見圖1b)。hDPCs抗波形蛋白染色陽性(見圖2a)抗角蛋白染色陰性(見圖2b)。

a 原代培養第6天 b 原代培養第12天

a 波形蛋白陽性染色 b 角質蛋白陰性染色
2.2 不同糖濃度對hDPCs增殖活性的影響 用MTT法檢測第3代hDPCs在五種不同糖濃度培養基條件下的增殖情況見表1,從結果中可以看出:不同濃度葡萄糖(5.5、15、25、35、45mmol/L)對牙髓細胞的增殖作用具有時間依賴性,隨著時間的延長對hDPCs增殖作用逐漸增強。采用單因素方差分析,15mmol/L組僅在第5、7天有促進牙髓細胞增殖的作用,與對照組(5.5mmol/L)相比,差異有統計學意義(P<0.05);25mmol/L組在第1、3、5、7天時有促進牙髓細胞增殖的作用,與對照組(5.5mmol/L)相比,差異有統計學意義(P<0.05),并且這種增殖效應在第7天時達到最高峰(P<0.001)。35mmol/L組在第10天與對照組(5.5mmol/L)相比,可明顯促進hDPCs的增殖,與對照組(5.5mmol/L)相比,差異有統計學意義(P<0.05)。45mmol/L組在第1、3、5、7、10天與對照組(5.5mmol/L)相比,均無促進hDPCs的增殖,與對照組(5.5mmol/L)相比,差異無統計學意義(P>0.05)。

表1 不同濃度及作用時間葡萄糖刺激下hDPCs增殖活性變化
2.3 不同濃度葡萄糖對hDPCs礦化結節形成的影響 hDPCs在培養至21d時,即可看到兩組細胞均呈復層生長,并呈漩渦狀排列,在漩渦狀中心處可出現致密的礦化結節,結節中心透光性較差(見圖3a)。培養至28d時,茜素紅染色可見兩組均有紅色的礦化結節,正常對照組(5.5mmol/L)礦化結節數目少,結節較小,染色淺(見圖3b)。高糖組(15、25、35、45mmol/L)細胞鈣結節數目較多,且結節較大,染色深并伴有許多顆粒狀的致密的鈣化小點(見圖3c~f)。
將上述礦化結節通過SDS方法進行半定量分析,由圖4可以看出,濃度為15、25、35、45mmol/L的礦化沉積量均高于對照組,但僅有15和25mmol/L組與對照組相比,其差異具有統計學意義(P<0.05),尤其25mmol/L差異最為顯著(P<0.01)。

圖4 半定量檢測不同hDPCs組礦化結節情況
3 討論
近年來我國糖尿病的發病率逐年升高,與糖尿病相關的并發癥逐漸引起人們重視,高血糖是糖尿病的主要特征,研究顯示其對血管內皮細胞、牙周膜韌帶細胞、骨細胞等有明顯影響[5-7],參與糖尿病并發癥的發生。體外實驗多采用高濃度的葡萄糖干預實驗細胞,模擬糖尿病狀態下細胞的生物學行為。本實驗采用改良組織塊法成功培養出人牙髓細胞,通過免疫組織化學染色方法發現體外培養的 hDPCs 抗波形蛋白染色陽性,角蛋白染色陰性,提示細胞來源于中胚層,無上皮細胞混雜,為進一步的實驗研究奠定基礎。
牙髓細胞增殖是人牙體組織鈣化形成修復性牙本質或礦化結構的主要細胞以及生物基礎[8]。用MTT方法檢測高糖對hDPCs增殖的影響,從hDPCs增殖曲線圖中可以看出,葡萄糖在一定濃度范圍內(5.5~25mmol/L)對hDPCs的生長可以起到促進作用,并呈濃度和時間依賴性。這可能與一定范圍內高濃度的葡萄糖給予細胞的生長提供更多的能量有關,從而促進其增殖,在第7天,15和25mmol/L組細胞進入生長平臺期。隨著葡萄糖濃度的進一步提高,35mmol/L組在培養7d內與對照組相比并無明顯促進hDPCs生長的作用,從第7天起開始才顯示促進hDPCs生長,這可能開始時由于過高濃度葡萄糖影響細胞外液滲透壓對細胞增殖產生抑制作用,也有可能是因為過高濃度葡萄糖影響細胞內多種酶的活性有關[9],從而影響細胞的正常生長, Gabriella Doronzo 等人分別用5.5、15和25mmol/L濃度葡萄糖培養糖尿病模型的大鼠血管平滑肌細胞,發現高濃度葡萄糖促進大鼠平滑肌細胞的增殖,其中25mmol/L促進細胞增殖效果最為顯著[10]。這與本實驗結果大體一致,而超過一定濃度范圍的高糖則抑制hDPCs增殖,但其機制尚不完全明確,需要進一步研究。
細胞外鈣鹽沉積是牙髓細胞具有礦化能力的最直接表現,反映鈣鹽變化最直觀的表現就是礦化結節的形成[8]。通過不同條件下礦化結節大小和數量的比較,可以直觀觀察不同刺激對牙髓細胞礦化能力的影響。細胞形成礦化結節的先決條件是體外牙髓細胞呈復層生長的能力,而礦化的先決條件是細胞結節的三維結構[11]。體外持續培養hDPCs時,最初細胞以單層貼壁的方式生長,當細胞不斷增殖單層匯合后可繼續生長,此時表現為復層生長方式,繼而形成具有三維結構的細胞結節,隨后細胞外基質發生礦化,最終形成礦化結節。本實驗采用茜素紅與表面活性劑十二烷基硫酸鈉(SDS)并用的方法發現,hDPCs無論在正常或者高糖條件培養下,在第28天時可形成茜素紅染色陽性的鈣化結節,這表明hDPCs在體外培養條件下具有合成、分泌并形成礦化細胞外基質的能力。同時還發現高糖組(25、35、45mmol/L)細胞鈣結節數目較多,且結節較大,染色深并伴有許多顆粒狀的致密的鈣化小點;正常組(5.5mmol/L)鈣化結節數目少,結節較小,染色淺,這表明高糖可明顯促進hDPCs形成鈣化結節的能力。用SDS法半定量檢測礦化物沉積含量的結果顯示,高糖組25mmol/L可以顯著促進hDPCs鈣化結節的形成。這與Yuji Inagaki等[3]的結果一致,他們運用免疫組織化學染色方法觀察30周大小的糖尿病大鼠模型發現,糖尿病大鼠的牙髓組織的鈣化結節在數目和數量上都高于正常大鼠,但其機制仍不詳。另外,也有學者的研究也得出了類似的結論,發現高糖促進間充質細胞的骨向分化[12]。但是不同于Colombo和Kim的研究,他們認為高糖抑制骨細胞和牙周膜韌帶細胞的成骨分化,抑制細胞外基質鈣化結節的形成[13-14]。這可能是因為在不同的研究中,由于細胞來源的異質性,實驗條件的不同以及實驗所采用的葡萄糖刺激方式不同等因素,高糖對細胞礦化可能產生相反的作用。
綜上所述,一定濃度范圍內的高糖以濃度依賴的方式促進hDPCs的增殖及礦化。雖然目前的資料顯示高血糖影響了細胞的增殖以及礦化,但是糖尿病是非常復雜的全身系統疾病,體外模擬糖尿病高糖是否能完全代表糖尿病的機體狀態還未知。本實驗擬初步探討高糖是否會對牙髓細胞鈣化產生影響,為解決糖尿病患者的一些臨床問題提供實驗基礎,在后續的研究中我們將進一步研究高糖對牙髓細胞相關鈣化因子表達的影響。

