幽門螺桿菌感染對潰瘍性結(jié)腸炎患者反復發(fā)作的影響
郭艷麗 王 錦 李穎霞
1 鄭州頤和醫(yī)院消化內(nèi)科,河南省鄭州市 450000; 2 鄭州大學第一附屬醫(yī)院消化內(nèi)科
潰瘍性結(jié)腸炎是一種慢性腸道炎癥性疾病,主要累及結(jié)腸黏膜及黏膜下層,屬終生復發(fā)性疾病,且具有較高癌變概率。現(xiàn)階段,潰瘍性結(jié)腸炎的發(fā)病機制尚未明確,可能是由于環(huán)境、遺傳、免疫、腸道微生態(tài)等多種因素相互作用的結(jié)果。胃腸道內(nèi)營養(yǎng)豐富、消化酶種類繁多,是細菌生長代謝的理想環(huán)境,腸道微生物可為宿主提供自身無法合成的化合物,對宿主免疫功能提供支持。一般情況下,宿主對共生細菌具有良好的耐受性,但由于共生細菌數(shù)量巨大,當胃腸道穩(wěn)態(tài)發(fā)生變化時,仍然可能導致宿主發(fā)生病變。幽門螺桿菌(Hp)主要定植于胃內(nèi),與胃潰瘍、慢性胃炎等密切相關(guān)。有研究指出,采用聚合酶鏈式反應法可從糞便或腸黏膜中檢測出Hp DNA[1]。由于潰瘍性結(jié)腸炎的致病因素涉及免疫與腸道微生態(tài),因此Hp感染與潰瘍性結(jié)腸炎的關(guān)系受到高度關(guān)注。本研究觀察潰瘍性結(jié)腸炎患者Hp感染情況,并分析其對疾病反復發(fā)作的影響,以期為控制潰瘍性結(jié)腸炎發(fā)作頻率提供依據(jù)。現(xiàn)報道如下。
1 資料與方法
1.1 一般資料 納入2018年1月—2021年1月鄭州頤和醫(yī)院收治的112例潰瘍性結(jié)腸炎患者為研究對象,進行前瞻性研究。納入標準:(1)潰瘍性結(jié)腸炎符合《潰瘍性結(jié)腸炎診療指南》[2]中相關(guān)診斷標準;(2)病程超過1年;(3)肝腎功能基本正常;(4)患者或家屬簽署知情同意書。排除標準:(1)近4周接受抗生素、質(zhì)子泵抑制劑、微生態(tài)制劑、鉍制劑、柳氮磺吡啶治療;(2)既往有Hp根除治療史;(3)合并急性上消化道出血;(4)合并自身免疫性疾病;(5)合并溶血性貧血或特發(fā)性血小板減少性紫癜;(6)合并真菌性腸炎、放射性腸炎、嗜酸粒細胞性腸炎、腸結(jié)核;(7)妊娠期或哺乳期女性。
1.2 方法
1.2.1 資料收集:入院時詳細詢問患者病史,記錄患者性別、年齡、平均每日排便次數(shù)、吸煙史[吸煙指數(shù)(每日吸類支數(shù)×吸煙年限)≥200視為有吸煙史]、飲酒史(女性平均每日飲酒量>20g,男性平均每日飲酒量>40g,且飲酒時間>5年視為有飲酒史)以及是否存在腹痛、腹瀉、黏液膿血便等癥狀,隨訪1年,記錄患者1年內(nèi)潰瘍性結(jié)腸炎患者疾病發(fā)作次數(shù)。
1.2.2 Hp檢測:入院24h內(nèi)對患者進行Hp檢測,囑咐患者檢查前禁食8h、禁水6h,檢測前使用溫水漱口,用20ml溫水送服1粒尿素14C膠囊(上海欣科醫(yī)藥,國藥準字H20000228),靜坐15~20min,醫(yī)務人員取出集氣卡,指導患者用適當力度向卡內(nèi)吹氣,注意采集氣體過程中應避免倒吸,當集氣卡顏色出現(xiàn)變化時則表明采樣成功,將集氣卡插入YH04F幽門螺桿菌檢測儀(深圳市中核海得威生物科技),對采集的樣本進行檢測,嚴格按照說明書中操作流程測定,明確Hp感染情況。
1.2.3 實驗室指標檢測:入院24h內(nèi)采集患者空腹靜脈血5ml,離心(離心速度為3 000r/min)20min,取血清,采用酶聯(lián)免疫吸附法檢測血清C反應蛋白(CRP)、白細胞介素-1(IL-1)、白細胞介素-6(IL-6)、腫瘤壞死因子-α(TNF-α)水平;采用儀器法檢測血常規(guī),包括白細胞計數(shù)、中性粒細胞計數(shù)、血小板計數(shù)、血紅蛋白、紅細胞壓積;采用魏氏法檢測紅細胞沉降率。
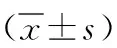
2 結(jié)果
2.1 潰瘍性結(jié)腸炎患者Hp感染情況 112例潰瘍性結(jié)腸炎患者中Hp感染21例,占18.75%。
2.2 兩組患者臨床資料比較 感染組疾病發(fā)作次數(shù)少于未感染組,差異有統(tǒng)計學意義(P<0.05);兩組性別、年齡、平均每日排便次數(shù)等資料比較,差異無統(tǒng)計學意義(P>0.05)。見表1。

表1 兩組患者臨床資料比較
2.3 兩組患者實驗室指標比較 感染組血清CRP、IL-1、IL-6、TNF-α低于未感染組,差異有統(tǒng)計學意義(P<0.05);兩組白細胞計數(shù)、中性粒細胞計數(shù)、血小板計數(shù)、血紅蛋白、紅細胞壓積、紅細胞沉降率比較,差異無統(tǒng)計學意義(P>0.05)。見表2。
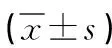
表2 兩組患者實驗室指標比較
2.4 Hp感染對疾病反復發(fā)作的影響 將潰瘍性結(jié)腸炎患者Hp感染情況作為自變量并賦值(1=感染,0=未感染),將疾病發(fā)作次數(shù)作為因變量(連續(xù)變量),經(jīng)Logistic回歸分析,結(jié)果顯示,Hp感染是潰瘍性結(jié)腸炎患者疾病反復發(fā)作的保護性因素(OR<1,P<0.05)。見表3。

表3 Hp感染對疾病反復發(fā)作的影響
2.5 潰瘍性結(jié)腸炎患者Hp感染與實驗室指標的關(guān)系 將潰瘍性結(jié)腸炎患者Hp感染情況作為自變量并賦值(1=感染,0=未感染),將實驗室指標(CRP、IL-1、IL-6、TNF-α)作為因變量(均為連續(xù)變量),經(jīng)Logistic回歸分析,結(jié)果顯示,潰瘍性結(jié)腸炎患者Hp感染與CRP、IL-1、IL-6、TNF-α水平密切相關(guān)(OR<1,P<0.05)。見表4。

表4 實驗室指標與潰瘍性結(jié)腸炎患者Hp感染的關(guān)系
3 討論
流行病學研究結(jié)果顯示,潰瘍性結(jié)腸炎發(fā)病率呈顯著增長趨勢,其原因可能是由于醫(yī)療水平進步,臨床診斷水平提高,從而提升潰瘍性結(jié)腸炎檢出率;此外,人類所處環(huán)境更加清潔,降低了機體對外界未知抗原的抵抗能力,由此引起細菌感染也可能導致其發(fā)病率的增長[3]。大多數(shù)潰瘍性結(jié)腸炎患者病情均較為穩(wěn)定,但仍有少數(shù)患者可能會發(fā)展為巨結(jié)腸或結(jié)腸癌,增加臨床治療難度,不利于患者預后。現(xiàn)階段,臨床治療潰瘍性結(jié)腸炎的方法多種多樣,但效果差強人意。近年來,有研究指出,通過增加潰瘍性結(jié)腸炎患者腸道中細菌物種豐富度可在一定程度上減輕疾病程度[4]。由此,推測人體腸道中微生物可能與潰瘍性結(jié)腸炎疾病發(fā)作存在一定關(guān)系。
人體為一個龐大的共生體,除腸道外,多個器官內(nèi)均存在多種細菌,包括益生菌、條件致病菌及致病菌,其中Hp屬條件致病菌。Hp主要定植于胃竇,可誘導體液免疫反應及炎癥反應,Hp感染后T細胞和B細胞可特異性識別胃黏膜內(nèi)黏膜相關(guān)淋巴組織,引起表面蛋白的免疫應答,還可與腸道中具有抗原相似的表面蛋白的其他細菌交叉反應。長期以來,Hp被認為是消化性潰瘍、淋巴增生性胃淋巴瘤、胃癌的危險因素,但事實上僅有少數(shù)Hp感染患者會發(fā)生上述疾病。據(jù)統(tǒng)計,不足15%Hp感染患者會發(fā)生消化性潰瘍疾病,不足1%的Hp感染患者會發(fā)生胃癌[5]。此外,在部分患者中,Hp感染還可能提供益處。近年來,越來越多的證據(jù)表明,Hp可通過免疫成分保護人體免受多種疾病侵襲[6]。本文中觀察潰瘍性結(jié)腸炎患者Hp感染情況發(fā)現(xiàn),112例潰瘍性結(jié)腸炎患者中Hp感染21例,占18.75%,低于肖一峰等[7]對健康體檢人群Hp感染的統(tǒng)計結(jié)果(46.81%);此外,本文結(jié)果還顯示,Hp感染患者潰瘍性結(jié)腸炎疾病發(fā)作次數(shù)明顯少于未感染的患者,表明Hp對潰瘍性結(jié)腸炎具有一定保護作用,可預防該癥的發(fā)生,減少發(fā)作頻次。分析其原因,Hp可促進腸系膜淋巴結(jié)生成Treg細胞,并下調(diào)Th17細胞水平,對腸黏膜Th17/Tregs與Th1/Th2細胞平衡產(chǎn)生一定調(diào)節(jié)作用,進而調(diào)控免疫機理,促使宿主免疫應答向免疫耐受方向轉(zhuǎn)換,從而遏制潰瘍性結(jié)腸炎患者疾病反復發(fā)作。進一步Logistic回歸分析,證實Hp感染是潰瘍性結(jié)腸炎患者疾病反復發(fā)作的保護性因素。根據(jù)2015年日本京都Hp根除全球共識中觀點,Hp感染患者均應接受Hp根除治療[8]。然而我國人口基數(shù)龐大,無癥狀Hp感染者眾多,普查極為困難;且隨耐藥基因轉(zhuǎn)變,耐藥性也隨之增加,Hp感染復發(fā)率居高不下。我國Hp感染處理共識中指出,針對消化性潰瘍、淋巴增生性胃淋巴瘤患者強烈建議其進行Hp根除治療,但對于胃腸道微生物群不穩(wěn)定或不成熟者應謹慎使用抗生素[9]。由此可見,臨床應謹慎對待Hp感染患者,尤其對潰瘍性結(jié)腸炎患者而言,除非合并消化性潰瘍、淋巴增生性胃淋巴瘤、具有明確胃癌家族史,否則不應立即進行Hp根除治療,以免增加疾病發(fā)作頻率。
腸黏膜局部炎癥反應在潰瘍性結(jié)腸炎中起到重要作用,而腸黏膜炎癥的發(fā)生主要是由于促炎性細胞因子與抑制性炎性介質(zhì)平衡紊亂,致使炎癥呈慢性化表現(xiàn),介導疾病反復發(fā)作。本文結(jié)果顯示,感染組CRP、IL-1、IL-6、TNF-α水平低于未感染組,表明Hp感染可降低潰瘍性結(jié)腸炎患者血清炎性細胞因子水平。且經(jīng)Logistic回歸分析,結(jié)果顯示,潰瘍性結(jié)腸炎患者Hp感染與CRP、IL-1、IL-6、TNF-α水平密切相關(guān)。Hp可誘導樹突狀細胞增殖,并參與樹突狀細胞重塑,促使其向耐受性樹突狀細胞轉(zhuǎn)化,而樹突狀細胞作為TH0細胞激活劑和強大抗原呈遞細胞,在誘導TH0細胞分化、調(diào)節(jié)適應性免疫、呈遞抗原方面具有關(guān)鍵性作用,促進TH0細胞向Tregs分化,升高轉(zhuǎn)化生長因子-β,降低IL-6水平;此外Tregs還可直接抑制多種炎性細胞因子,從而減輕潰瘍性結(jié)腸炎患者機體炎癥反應[10]。
綜上所述,Hp感染是潰瘍性結(jié)腸炎患者疾病反復發(fā)作的保護性因素,Hp感染的潰瘍性結(jié)腸炎患者疾病發(fā)作頻率更低,炎癥反應較低,建議對于Hp感染的患者應根據(jù)特定指證進行Hp根除治療,尤其對于潰瘍性結(jié)腸炎患者,需謹慎進行Hp根除治療。

