MAP新輔助化療方案聯合保肢手術對骨肉瘤患者近期療效及安全性分析
馮 晨 馮 華 溫宏麗
(1.牡丹江醫學院附屬紅旗醫院骨外科,黑龍江 牡丹江, 157011;2.牡丹江醫學院病理教研室,黑龍江 牡丹江, 157011;3.牡丹江醫學院外語教研部,黑龍江 牡丹江, 157011)
骨肉瘤是臨床常見的原發性惡性腫瘤之一,好發于青少年人群,發病率為(2 ~3)/100 萬,占惡性腫瘤的0.2%,占原發骨腫瘤的11.7%。骨肉瘤亞型一般分為傳統型骨肉瘤、毛細血管擴張型骨肉瘤、小細胞骨肉瘤、低度惡性中心骨肉瘤、繼發性骨肉瘤、骨膜骨肉瘤及高度惡性表面骨肉瘤[1]。其病灶常位于股骨下端、脛骨上端、腓骨上端等,臨床癥狀主要表現為腫脹、局部疼痛、功能障礙等,部分患者會出現病理性骨折,由于骨肉瘤有著極高惡性程度,因此極易出現預后不佳的情況,給患者生命安全造成了嚴重的威脅[2]。既往臨床上常用的治療方案多為截肢手術,但近年來研究表明,骨肉瘤患者采取截肢手術治療后,可能由于患者的腫瘤病灶在術前存在細微轉移,導使其術后出現復發,最終導致死亡[3]。隨著醫學不斷進展,目前臨床上治療骨肉瘤患者多采取保肢手術,這對患者后續康復有著重要的臨床意義,但盡管如此,許多學者也仍然擔憂患者保肢術后疾病復發。自從新輔助化療開展以來,有效提高了保肢率,研究顯示,新輔助化療雖相較以往輔助化療并不能提高生存率,但至少可使外科手術更容易進行,進而提高保肢率,并降低局部復發率[4]。本研究旨在進一步探究不同新輔助化療方案聯合保肢手術對骨肉瘤患者近期療效及安全性分析,現匯報如下。
1 資料與方法
1.1 一般資料
選取2015 年1 月—2022 年12 月牡丹江醫學院附屬紅旗醫院收治的90 例骨肉瘤患者作為研究對象,按治療方式不同將其分為A 組、B 組、C 組,每組30 例。三組患者年齡、性別等基線資料比較,差異無統計學意義(P>0.05),有可比性,見表1。在醫護人員充分說明研究的目的、方式等內容后,由患者及家屬簽訂相關文書。本研究經牡丹江醫學院附屬紅旗醫院醫學倫理委員會審批后正式啟動且本研究符合《赫爾辛基宣言》中的倫理準則[(倫)審202009006]。
表1 兩組患者基線資料比較 [(±s)/n(%)]
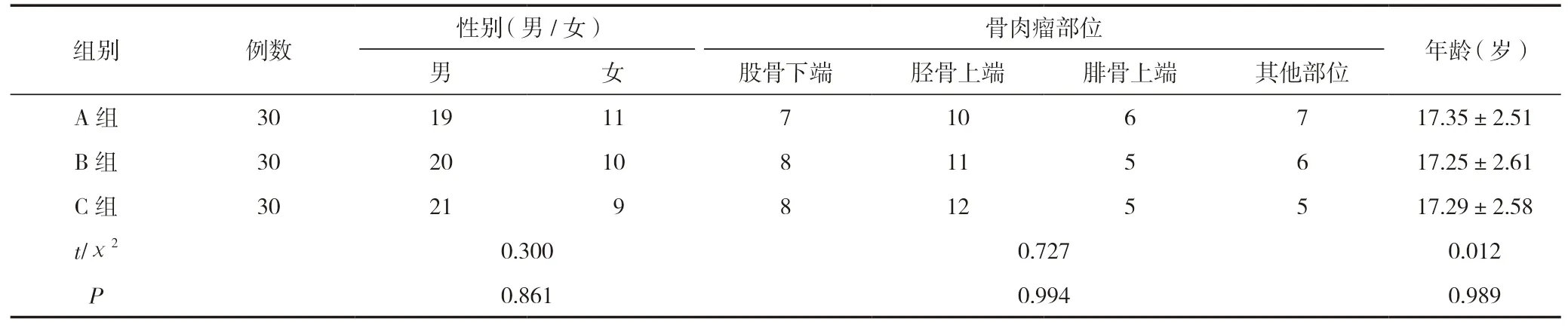
表1 兩組患者基線資料比較 [(±s)/n(%)]
?
續表1 兩組患者基線資料比較 [(±s)/n(%)]

表1 兩組患者基線資料比較 [(±s)/n(%)]
?
1.2 納入與排除標準
納入標準:①符合《經典型骨肉瘤臨床診療專家共識》[2]中的診斷標準;②各項臨床資料無缺失,且目前機體狀態良好,體力狀態(PS)評分均在0~3 分;③具有強烈的保肢意愿;④所有的骨缺損重建均采用瘤段骨滅活再植;⑤為原發性骨肉瘤且均未出現遠處轉移;⑥年齡13~25 歲。
排除標準:①患者伴隨認知障礙、精神類疾病或機體多個器官衰竭導致無法配合研究進行者;②預計生存期低于半年;③患者因自身原因或轉院治療導致中途退組者;④患者在近3 個月有過重大手術史。
1.3 方法
C 組患者給予保肢手術聯合DIA 方案治療。DIA 方案具體如下:30 mg/m2鹽酸多柔比星脂質體(生產企業:石藥集團歐意藥業有限公司,國藥準字H20163178,規格:5 mL:10 mg)、100 mg/m2順鉑(生產企業:齊魯制藥有限公司,國藥準字H37021358,規格:10 mg/瓶)、10 g/m2異環磷酰胺(生產企業:北京斯利安藥業有限公司,國藥準字H20066021,規格:0.5 g、1.0 g)。保肢手術具體流程如下:①將腫瘤部位的骨段切除:在進行手術前,患者需經核磁共振、骨掃描等各項檢查明確病灶位置。在手術的過程中,主刀醫師需距離患者腫瘤病灶邊緣4 cm 左右將病灶全部切除,手術完畢后對切除的腫瘤標本邊緣進行病理分析。②骨段移植:在患者進行手術前30 min 將需移植的骨段取出,放置室溫下回溫并采用37℃的乙醇沖洗,隨即將骨段上多余的組織清除,在髓內安裝好固定裝置后再用37 ℃的乙醇沖洗松質骨部位,采用濃度為3%的氧化氫清洗髓腔。骨骺處采用松質骨拉力螺釘與截骨面垂體固定。手術完畢后,采用石膏將患者患肢固定,持續固定6 周后,開始進行康復訓練。術后采用常規化療方案治療,1 個療程為21 d,持續治療2 個療程。
B 組患者給予保肢手術聯合MAPI 化療方案治療。MAPI方案具體如下:10~12 g/m2甲氨蝶呤(生產企業:悅康藥業集團有限公司,國藥準字H20113120,規格:0.1 g/瓶)、30 mg/m2鹽酸多柔比星脂質體(生產企業:石藥集團歐意藥業有限公司,國藥準字H20163178,規格:5 mL:10 mg)、10 g/m2異環磷酰胺(生產企業:北京斯利安藥業有限公司,國藥準字H20066021,規格:0.5 g、1.0 g)。保肢手術同C 組一致。
A 組患者給予保肢手術聯合MAP 新輔助化療方案治療。MAP 新輔助化療方案具體如下:10~12 g/m2甲氨蝶呤(生產企業:悅康藥業集團有限公司,國藥準字H20113120,規格:0.1 g/瓶)+30 mg/m2鹽酸多柔比星脂質體(生產企業:石藥集團歐意藥業有限公司,國藥準字H20163178,規格:5 mL:10 mg)+100 mg/m2順鉑(生產企業:齊魯制藥有限公司,國藥準字H37021358,規格:10 mg/瓶)。其中,在治療過程中給予A、B 組患者持續靜脈滴注氨甲蝶呤4~6 h,結束后6 h予以患者15 mg/m2亞葉酸鈣(生產企業:江蘇恒瑞醫藥股份有限公司,國藥準字H32022391,規格:0.1 g×1 瓶/盒)解救,進行肌肉注射,6 h/次,共注射12 次,每支亞葉酸鈣劑量為100 mg,按15 mg/m2計算后,將剩余的亞葉酸鈣用濃度為0.9%氯化鈉溶液稀釋后漱口。在甲氨蝶呤治療結束后24、48、72 h 分別對患者進行血藥濃度的監測,并進行250 mL 碳酸氫鈉(生產企業:浙江康恩貝制藥股份有限公司,國藥準字H20057190,規格:2 mL)靜脈滴注,2 d/次進行尿液堿化。每日用pH 試紙測試尿液,保證患者尿液呈堿性,保持每天2 000~3 000 mL 液體充分水化。以上化療方案1 個療程為21 d,治療2 個療程,MAP 新輔助化療方案進行2 個療程后開展保肢手術,具體手術過程與C 組一致。
在治療過程中對三組患者出現的不良反應如肝腎損傷、血小板降低等進行對癥處理。
1.4 觀察指標
①三組患者采取不同方案治療方式 90 d 后臨床療效比較。目前指南推薦骨肉瘤術前化療療效評估主要有5 個方面:癥狀與體征:肢體疼痛(有無改善)、皮溫(與健側對比)、肢體腫脹與表淺靜脈怒張(與化療前對比)、關節活動度(與化療前對比)、 患肢周徑(與化療前對比)。實驗室檢查:堿性磷酸酶、乳酸脫氫酶的變化。影像學檢查:X 線、CT、MRI、發射型計算機斷層掃描(ECT)變化。根據以上結果進行綜合評估,評價新輔助化療療效。按照實體瘤療效評價標準(RECIST)1.0 版進行評價。有效:患者腫瘤病灶消失且未出現新的病灶,持續時間≥28 d;穩定:患者腫瘤病灶直徑減小幅度>30%,經影像學檢查后未見淋巴結或其他部位出現腫瘤病灶轉移狀況;無效:患者腫瘤病灶直徑增長>20%,經影像學檢查后可見淋巴結或其他部位出現腫瘤病灶轉移狀況。總有效率=(有效+穩定)例數/總例數×100%。
②三組患者采取不同方案治療方式后不良反應發生情況比較。化療不良反應包括腎功能損害、血小板減少、肝功能損害、白細胞下降、末梢神經毒性及胃腸道反應。不良反應發生率=(腎功能損害+血小板減少+肝功能損害+白細胞下降+末梢神經毒性+胃腸道反應)例數/總例數×100%
③比較三組患者采取不同方案治療方式半年后肢體功能。采用骨與軟組織腫瘤外科治療后功能評定(Enneking)[5]三組患者治療后肢體功能。共包括6 個維度:活動能力、疼痛情況、運動情況、肌力、心理承受及肢體穩定性。每個維度為5 分,滿分30 分。功能分級:患者得分24~30 分為優,18~23 分為良,12~17 分為可,<12 分為差。優良率=(優+良) 例數/總例數×100%。
1.5 統計學分析
使用SPSS 23.0 軟件系統分析處理本研究所有數據,計量資料 用 (±s)表示,多組間比較采用方差分析;計數資料用[n(%)]表示,行χ2檢驗。P<0.05 表示差異有統計學意義。
2 結果
2.1 三組患者治療90 d 后臨床療效比較
治療后,A 組患者臨床總有效率顯著高于B 組、C 組,差異有統計學意義(P<0.05);B 組、C 組臨床總有效率比較,差異無統計學意義(P>0.05),見表2。
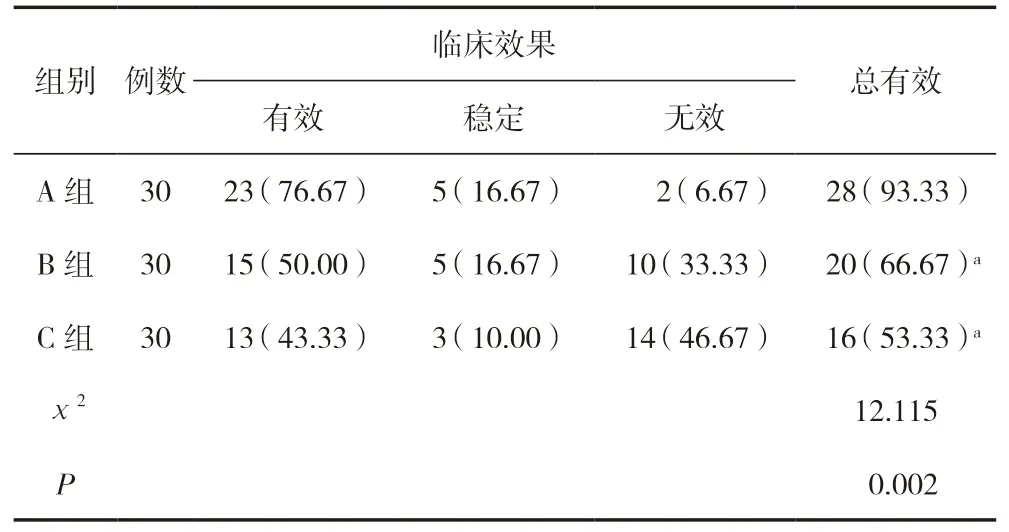
表2 三組患者治療后臨床療效比較 [n(%)]
2.2 三組患者治療后不良反應發生率比較
治療后,A 組患者不良反應發生率顯著低于B 組、C 組,差異有統計學意義(P<0.05);B 組、C 組不良反應發生率比較,差異無統計學意義(P>0.05),見表3。
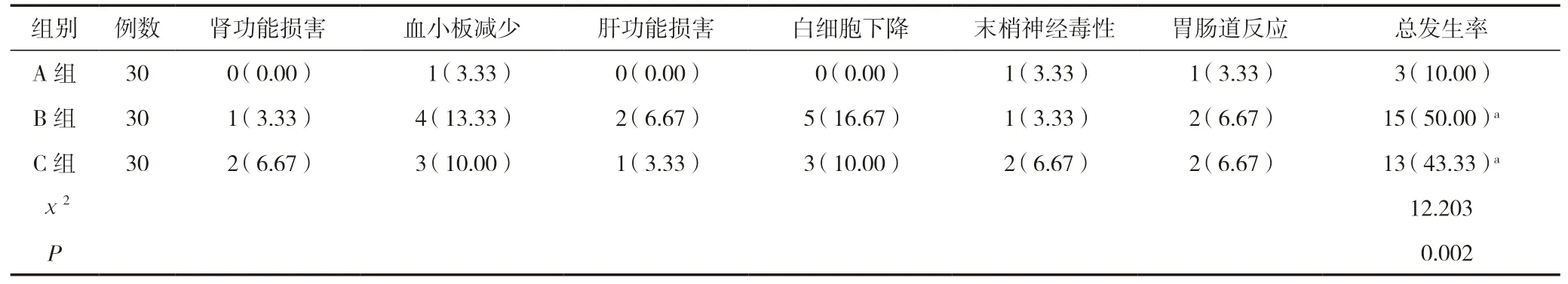
表3 三組患者治療后不良反應發生率比較 [n(%)]
2.3 三組患者采取不同方案治療方式半年后肢體功能比較
治療后,A 組Enneking 評分及優良率高于B 組、C 組,差異有統計學意義(P<0.05);B 組、C 組Enneking 評分及優良率比較,差異無統計學意義(P>0.05),見表4。
表4 三組患者采取不同方案治療方式半年后肢體功能比較 [(±s)/n(%)]
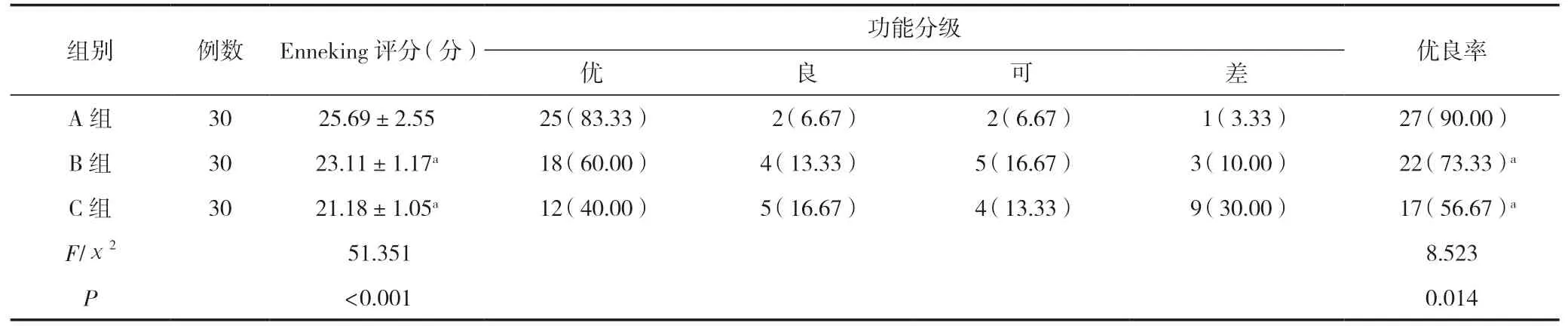
表4 三組患者采取不同方案治療方式半年后肢體功能比較 [(±s)/n(%)]
注:與A 組相比,aP<0.05。
?
3 討論
在過往臨床治療骨肉瘤患者采用的截肢手術中,雖能將惡性腫瘤病灶部位切除,但對于患者血液及組織內存在的活性腫瘤細胞卻無法徹底清除,導致疾病在后期仍然會復發,引起患者死亡。有研究顯示,單一使用截肢手術治療骨肉瘤,患者在5 年內的生存率低于20%[6]。而將手術治療與化療結合,則能顯著提升患者生存率。近年來,隨著臨床醫學飛速發展,手術技術也越來越完善,新輔助化療也開始逐漸應用于臨床,這使得患者生活質量及生存率得到了極大的改善[7-8]。新輔助化療是在患者進行手術前進行短期化療,能將影像學及其他醫學檢查不能顯示的細微轉移腫瘤病灶得以清除,消滅血液及組織內的存在的活性腫瘤細胞。且患者在進行新輔助化療的過程中,可減小腫瘤病灶直徑,減輕周圍粘連浸潤,利于后續手術將病灶切除,進一步降低手術難度[9-10]。患者在進行手術后,持續化療還能進一步抑制組織內殘留的惡性腫瘤細胞,進而鞏固治療效果,達到降低疾病復發率的目的。有研究表明,在多種惡性腫瘤的治療中,新輔助化療與手術治療相結合,其臨床有效率顯著高于單純根治性手術聯合術后化療,其中包含結直腸惡性腫瘤等[11]。
本研究采用的3 種不同新輔助化療方案作為骨肉瘤患者的化療方案。通過抑制惡性腫瘤細胞繁殖的復制、轉錄、合成等過程而產生作用,聯合化療可應對骨肉瘤患者產生的耐藥性,并在術前進行化療,抑制患者惡性腫瘤的生長,殺死部分惡性腫瘤細胞,提高手術成功率。本研究結果提示MAP 新輔助化療方案聯合保肢手術臨床治療療效最為顯著。究其原因可能為,MAP 新輔助化療方案中采用的順鉑藥物為細胞周期非特異性藥物,該藥對惡性腫瘤細胞具有良好的抑制作用[12-14]。鹽酸多柔比星脂質體能顯著干擾惡性腫瘤細胞轉錄,抑制信使RNA 合成與惡性腫瘤細胞的增殖和生長。而甲氨蝶呤則是抗葉酸類抗惡性腫瘤藥物,可通過阻止惡性腫瘤細胞合成來進一步抑制其生長。綜上所述,MAP 方案治療骨肉瘤腫瘤組織壞死率高,有效率高,保肢成功率高,近期療效顯著。與此同時,臨床極為注重藥物在應用過程中的安全性,尤其針對化療患者所使用的藥物,在選擇的同時又會對有益的細胞造成一定的傷害,利弊關系需要權衡。目前所采用的化療藥物均存在安全系數低、毒性大等問題,鑒于化療藥物耐藥性的增多,臨床不斷地加大藥物劑量,導致化療不良反應發生率相對增加。本研究所采用的MAP 新輔助化療,通過亞葉酸鈣解救、充分水化及堿化尿液等預防處理后,未出現嚴重不良反應,不良反應可耐受,安全性好,值得臨床應用[15-16]。
綜上所述,MAP 新輔助化療方案聯合保肢手術治療骨肉瘤患者取得了顯著的近期臨床療效,患者不良反應發生率低,聯合治療安全性良好,本研究為臨床治療骨肉瘤患者提供了新的依據。

