氫氧化鑭通過阻斷HIF-1α信號(hào)通路抑制慢性腎病所致的血管鈣化
崔雅婷,王琪雯,王勝男,李 剛
(1. 內(nèi)蒙古自治區(qū)呼和浩特市第一醫(yī)院藥劑科,2. 內(nèi)蒙古醫(yī)科大學(xué)藥學(xué)院藥理學(xué)教研室,內(nèi)蒙古 呼和浩特 010110)
血管鈣化可能會(huì)導(dǎo)致心血管疾病的風(fēng)險(xiǎn)增加,尤其在患有慢性腎病(chronic kidney disease,CKD)的患者中,這種風(fēng)險(xiǎn)的增加更為明顯。隨著年齡的增長,血管平滑肌細(xì)胞(vascular smooth muscle cell,VSMC)的表型變化對(duì)CKD的影響越來越明顯,其表型變化可以通過羥基磷灰石的大量沉積來實(shí)現(xiàn),這種鈣化反應(yīng)可以通過骨礦化的方式來實(shí)現(xiàn)[1-3]。此外,由于CKD會(huì)使血磷水平增加,這也會(huì)對(duì)VSMC的表型變化產(chǎn)生一定的影響[4]。CKD是一種嚴(yán)重的慢性疾病,其發(fā)生主要是因?yàn)樯眢w內(nèi)的細(xì)胞功能障礙,如貧血、微血管病變[5-6],這些因素會(huì)使人體陷入缺氧的狀態(tài),并且這種情況會(huì)對(duì)VSMC鈣化及成骨樣表型的形成產(chǎn)生重要影響。
低氧誘導(dǎo)因子1(hypoxia inducible factor 1,HIF-1)是一種轉(zhuǎn)錄復(fù)合物,可調(diào)節(jié)細(xì)胞和系統(tǒng)對(duì)氧氣可用性的穩(wěn)態(tài)反應(yīng)。HIF-1是由氧敏感的HIF-1α和組成型表達(dá)的HIF-1β亞基組成的異二聚體。其中HIF-1α的氧依賴性調(diào)節(jié)是一個(gè)多步驟的過程,包括在常氧條件下降解,但在低氧條件下穩(wěn)定,轉(zhuǎn)移到細(xì)胞核并激活。對(duì)缺氧的適應(yīng)是正常細(xì)胞發(fā)育、分化及缺血等病理環(huán)境中的關(guān)鍵事件。作為體內(nèi)平衡的中樞介質(zhì),HIF-1α可以使細(xì)胞在低氧環(huán)境中存活[7-9]。Li等[10]研究表明,2型糖尿病患者血清中HIF-1α的水平與血管鈣化呈正相關(guān)。Perrotta等[11]研究發(fā)現(xiàn),HIF-1α與狹窄血管中的新生血管生成和鈣化區(qū)域共定位。此外,還有研究發(fā)現(xiàn)高磷是一種新的HIF-1誘導(dǎo)劑和激活劑[12]。這些研究均強(qiáng)調(diào)了HIF-1在血管鈣化中的重要作用。
氫氧化鑭是一種新型鑭類化合物,白色固體,難溶于水,較容易吸收空氣中的二氧化碳,是目前本課題組研究較多的稀土配合物。課題組前期研究已經(jīng)證明,氫氧化鑭可降低血磷水平,減少血管鈣化的發(fā)生[13-14],但未對(duì)其改善血管鈣化的作用機(jī)制進(jìn)行研究。前期通過網(wǎng)絡(luò)藥理學(xué)的方法,篩選發(fā)現(xiàn)血管鈣化與缺氧有很大的相關(guān)性,并通過KEGG分析發(fā)現(xiàn)HIF-1α信號(hào)通路與血管鈣化有較強(qiáng)相關(guān)性。因此,本文研究氫氧化鑭是否通過HIF-1α通路對(duì)CKD及其并發(fā)癥血管鈣化產(chǎn)生影響,提出CKD血管鈣化治療可能的新策略,以期實(shí)現(xiàn)CKD血管鈣化新型治療藥物和靶點(diǎn)的發(fā)現(xiàn)。
1 材料
1.1 實(shí)驗(yàn)動(dòng)物Wistar大鼠,♂,6~8周齡,體質(zhì)量(200~220) g,購自北京市維通利華實(shí)驗(yàn)動(dòng)物科技公司,生產(chǎn)許可證號(hào):SCXK(京)2016-0006。大鼠飼養(yǎng)于內(nèi)蒙古醫(yī)科大學(xué)動(dòng)物實(shí)驗(yàn)中心的SPF級(jí)屏障區(qū),溫度(21~22) ℃,濕度40%~50%,適應(yīng)性飼養(yǎng)7 d后開始實(shí)驗(yàn)。動(dòng)物實(shí)驗(yàn)經(jīng)內(nèi)蒙古醫(yī)科大學(xué)醫(yī)學(xué)倫理委員會(huì)批準(zhǔn)(文件編號(hào):YKD2019019)。
1.2 藥物與試劑氫氧化鑭(批號(hào):2020年9月,純度96%),由本實(shí)驗(yàn)室合成;碳酸鑭(貨號(hào):54451-24-0)、碳酸鈣(貨號(hào):471-34-1)、腺嘌呤(貨號(hào):73-24-5),均購自Sigma-Aldrich公司;磷(Pi)測試盒(貨號(hào):C006-1-1)、鈣(Ca)測定試劑盒(貨號(hào):C004-2-1)、血肌酐(serum creatinine,Scr)測定試劑盒(貨號(hào):C011-2-1)、血尿素氮(blood urea nitrogen,BUN)測定試劑盒(貨號(hào):C013-2-1),均購自南京建成生物工程研究所;大鼠成纖維細(xì)胞生長因子23(fibroblast growth factor 23,FGF23)ELISA試劑盒(貨號(hào):F4444-B)、大鼠甲狀旁腺激素(parathyroid hormone,PTH)ELISA試劑盒(貨號(hào):F4378-B),均購自上海易利生物科技有限公司;抗酒石酸酸性磷酸酶5b(tartrate-resistant acid phosphatase 5b,TRAP-5b)ELISA試劑盒(貨號(hào):E-EL-H1551c),購于Elabscience;von Kossa染色試劑盒(貨號(hào):G1043)、EVG染液套裝(貨號(hào):G1042),均購自武漢賽維爾生物科技有限公司;抗小鼠IgG(H+L)(貨號(hào):A23910)、抗兔IgG(H+L)(貨號(hào):A23920),均購自Abbkine公司;骨形態(tài)發(fā)生蛋白2(bone morphogenetic protein 2,BMP-2)抗體(貨號(hào):sc-137087)、Runt相關(guān)轉(zhuǎn)錄因子2(Runt-related transcription factor 2,RUNX2)抗體(貨號(hào):sc-101145),均購自Santa Cruz Biotechnology公司;β-actin抗體(貨號(hào):K101527P),購自北京索萊寶科技有限公司;Lamin A抗體(貨號(hào):10298-1-AP),購自Proteintech公司;HIF-1α抗體(貨號(hào):ab32152),購自Abcam公司;NE-PERTM細(xì)胞核和細(xì)胞質(zhì)提取試劑(貨號(hào):78833),購自ThermoFisher Scientific公司;總RNA提取試劑盒(貨號(hào):DP419),購自天根生化科技(北京)有限公司;反轉(zhuǎn)錄試劑盒(貨號(hào):FSQ-101)、SYBR Green熒光定量檢測試劑盒(貨號(hào):QPK-201),均購自TOYOBO Life Science公司。
1.3 主要儀器Molecular Devices多功能酶標(biāo)儀(SpectraMax i3x,美谷分子儀器有限公司);熒光定量PCR儀(PiKoreal96,美國ThermoFisher公司);BIO-RAD基礎(chǔ)電泳儀[伯樂生命醫(yī)學(xué)產(chǎn)品(上海)有限公司];Odyssey紅外激光成像系統(tǒng)(Odyssey CLX,美國LI-COR公司);高速冷凍離心機(jī)(3-18K,Sigma公司);病理切片機(jī)(RM2016,上海徠卡儀器有限公司)。
2 方法
2.1 實(shí)驗(yàn)動(dòng)物造模、分組及給藥采用腺嘌呤建立Wistar大鼠CKD模型。在1~2周內(nèi),給予大鼠2%的腺嘌呤混懸液,每日灌胃,第3~4周隔天給予2%的腺嘌呤混懸液灌胃。最終,從大鼠的眼底靜脈叢采集血樣本,檢測血清磷、肌酐及尿素氮水平,判斷該模型是否成功構(gòu)建。模型建立成功后,大鼠隨機(jī)分為6組:模型組、氫氧化鑭(LH 0.1、0.2、0.4 g·kg-1)組、碳酸鑭(LC 0.3 g·kg-1)組、碳酸鈣(CC 0.42 g·kg-1)組,每組10只,造模成功后開始給藥,給藥時(shí)間為8周。給藥組每天給予相應(yīng)劑量的藥物灌胃,模型組每日給予生理鹽水灌胃。另隨機(jī)選擇10只Wistar大鼠作為空白對(duì)照(Control)組。
2.2 血清學(xué)指標(biāo)檢測分別通過脲酶法、肌氨酸氧化酶法、MTB法,測定血清中的BUN、Scr、Ca水平;ELISA法檢測血清中PTH、FGF23、TRAP-5b水平。
2.3 胸主動(dòng)脈病理學(xué)檢查使用4%的多聚甲醛固定大鼠的胸主動(dòng)脈,包埋切片。
2.3.1von Kossa染色 取大鼠胸主動(dòng)脈段,用石蠟包埋后,4 μm厚切片,常規(guī)脫蠟、脫水。1%硝酸銀溶液浸泡,日光下照射30 min后,將玻片浸入5%硫代硫酸鈉溶液1 min,后用堿性品紅返染。脫水、透明、封片,用光鏡觀察。
2.3.2EVG染色 將染液A、B、C依照5 ∶2 ∶2的比例配制,將其加入到染液中,并用清水清潔。然后,將染液B加倍,使其略有分離,再用清水清潔,最后通過顯微鏡觀察,將染液的濃度調(diào)節(jié)到一定范圍,使其變?yōu)樽虾谏?而背面則變?yōu)榻咏跓o的灰白色。將EVG染液E 9 mL與D 1 mL按百分比混合,制備VG染液,洗滌1~3 min(根據(jù)組織中彈力玻璃纖維的含量而定,洗滌時(shí)間過短會(huì)導(dǎo)致膠原色素變淺,而洗滌時(shí)間過長則會(huì)使彈力玻璃纖維褪色),然后迅速用清水沖洗,無水乙醇脫水,二甲苯透明,中性樹脂封片。
2.4 qPCR檢測大鼠胸主動(dòng)脈SM22α、BMP-2、Runx2、VEGF mRNA表達(dá)根據(jù)RNA提取試劑盒說明書,提取大鼠胸主動(dòng)脈RNA,逆轉(zhuǎn)錄為cDNA。然后,利用cDNA作為模板,進(jìn)行qPCR擴(kuò)增,該qPCR實(shí)驗(yàn)體系包括:cDNA模板2 μL,上、下游引物各0.8 μL,SYBR Green Realtime PCR Master Mix 10 μL,無RNase水6.4 μL。qPCR儀的工作模式是:將溫度調(diào)節(jié)到95 ℃,持續(xù)30 s;95 ℃、5 s,60 ℃、10 s,72 ℃、15 s,進(jìn)行40個(gè)循環(huán);在60 ℃延伸步驟對(duì)熒光信號(hào)進(jìn)行采集,反應(yīng)結(jié)束后,觀察熔解曲線及擴(kuò)增曲線,分析qPCR 引物的特異性。采用2-△△CT法測定樣品中目的基因的相對(duì)表達(dá)水平,選擇穩(wěn)定表達(dá)的GAPDH作為內(nèi)參。引物序列見Tab 1。

Tab 1 Primer sequences for qPCR
2.5 Western blot檢測大鼠胸主動(dòng)脈組織細(xì)胞質(zhì)和細(xì)胞核中蛋白表達(dá)取大鼠主動(dòng)脈組織50 mg,剪成細(xì)小的碎片,加入500 μL完全RIPA裂解液,冰上充分研磨、裂解。將研磨好的組織倒入離心管中,渦旋2 min,冰上靜置10 min,重復(fù)3次。4 ℃、12 000 r·min-1離心10 min,取上清液,BCA法對(duì)蛋白進(jìn)行定量。蛋白煮沸變性后,進(jìn)行SDS-PAGE電泳,轉(zhuǎn)膜,封閉后,將膜放入一抗中,4 ℃孵育過夜,洗膜后加入二抗,37 ℃避光孵育1 h。將膜放在紅外激光成像儀上進(jìn)行圖像分析,使用ImageJ v1.8.0軟件,對(duì)胞質(zhì)中BMP2、SM22α、VEGF和HIF-1α蛋白的表達(dá)水平進(jìn)行測量,使用目的蛋白與內(nèi)參β-actin的比值反映其表達(dá)量。此外,對(duì)細(xì)胞核中的HIF-1α和RUNX2蛋白的表達(dá)水平進(jìn)行測量,使用目的蛋白與內(nèi)參Lamin A的比值反映其表達(dá)量。
3 結(jié)果
3.1 氫氧化鑭可改善CKD大鼠血清學(xué)指標(biāo)如Tab 2所示,給予氫氧化鑭、碳酸鑭、碳酸鈣治療8周后,CKD大鼠的血清Pi濃度、Scr、BUN、PTH、FGF23和TRAP-5b水平均明顯下降(P<0.01),Ca濃度無明顯變化。
3.2 氫氧化鑭對(duì)CKD大鼠血管鈣化的影響如Fig 1所示,HE和von Kossa染色檢測表明,與對(duì)照組相比,模型組的胸主動(dòng)脈血管變得更加粗糙,而且其中膜出現(xiàn)了更多的黑色鈣化;給予氫氧化鑭后,CKD大鼠的血管鈣化沉積有了明顯的改善,與其他鈣化治療方法相比,碳酸鈣的療效卻很有限。大鼠胸主動(dòng)脈EVG染色結(jié)果表明,與對(duì)照組相比,模型組大鼠的主動(dòng)脈血管鈣化區(qū)域的彈性纖維明顯減少,甚至出現(xiàn)了斷裂現(xiàn)象;與模型組相比,氫氧化鑭可改善彈性纖維的斷裂,但碳酸鈣組作用不明顯。
3.3 氫氧化鑭可影響CKD大鼠胸主動(dòng)脈SM22α、BMP-2、RUNX2、VEGF mRNA表達(dá)Fig 2結(jié)果顯示,給予氫氧化鑭8周,SM22α mRNA的表達(dá)明顯升高(P<0.05),BMP-2、RUNX2和HIF-1通路的下游蛋白VEGF mRNA的表達(dá)水平明顯降低。提示氫氧化鑭治療8周,可逆轉(zhuǎn)模型組這些基因的表達(dá)異常。
3.4 氫氧化鑭可影響CKD大鼠胸主動(dòng)脈SM22α、BMP-2、RUNX2、VEGF、HIF-1α蛋白的表達(dá)為了更好地研究氫氧化鑭是否能夠抑制血管鈣化的發(fā)生和發(fā)展,需要探究其是否能夠阻斷HIF-1通路的活性,因而檢測了SM22α、BMP-2、RUNX2,以及HIF-1通路中HIF-1α、VEGF的蛋白表達(dá)情況。Fig 3結(jié)果顯示,與對(duì)照組相比,模型組BMP-2的表達(dá)量明顯增加,而血管平滑肌標(biāo)記性蛋白SM22α的表達(dá)則有所下降,說明VSMC已經(jīng)開始發(fā)生骨骼轉(zhuǎn)化。與對(duì)照組相比,模型組細(xì)胞質(zhì)內(nèi)的HIF-1α表達(dá)明顯降低,同時(shí)下游蛋白VEGF表達(dá)明顯升高;與模型組相比,給予氫氧化鑭(0.1、0.2、0.4 g·kg-1)、碳酸鑭、碳酸鈣后,CKD大鼠HIF-1α表達(dá)升高,VEGF表達(dá)降低。
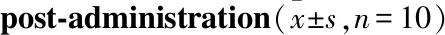
Tab 2 The serum biochemical test results of rats with chronic renal failure hyperphosphatemia at 8 weeks
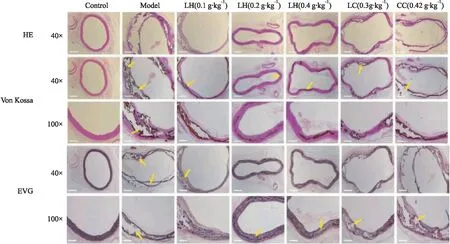
Fig 1 HE staining, von Kossa staining and EVG staining of thoracic aorta slices of rats with chronic renal failure
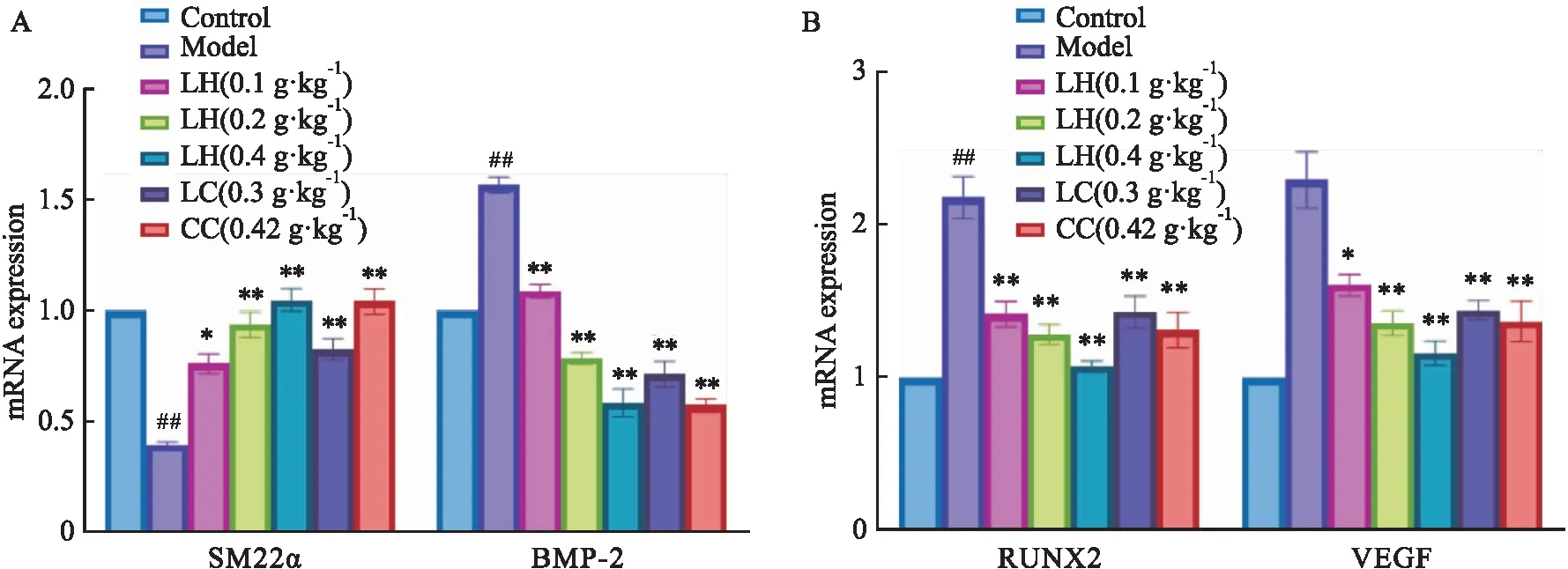
Fig 2 Effect of lanthanum hydroxide on mRNA expression of SM22α, BMP-2 (A), RUNX2
如Fig 4所示,與對(duì)照組相比,模型組血管細(xì)胞核內(nèi)RUNX2蛋白的表達(dá)量明顯增加,說明VSMC已經(jīng)開始發(fā)生骨骼轉(zhuǎn)化,給予氫氧化鑭、碳酸鑭、碳酸鈣后該蛋白的表達(dá)量降低。模型組細(xì)胞核內(nèi)HIF-1α表達(dá)明顯升高(P<0.01);與模型組相比,給予氫氧化鑭(0.1、0.2、0.4 g·kg-1)、碳酸鑭、碳酸鈣后,CKD大鼠血管胞核內(nèi)HIF-1α的表達(dá)分別降低了約24%、38%、49%、41%、23%。
4 討論
本文實(shí)驗(yàn)研究發(fā)現(xiàn),一種新型磷結(jié)合劑——?dú)溲趸|能夠有效抑制慢性腎衰血管鈣化的發(fā)生發(fā)展,并且通過血清學(xué)指標(biāo)檢測、胸主動(dòng)脈組織病理學(xué)檢查、qPCR及Western blot,證實(shí)其能夠有效阻斷HIF-1通路,從而達(dá)到抑制血管鈣化的目的。
HIF-1α是一種氧調(diào)節(jié)蛋白,對(duì)氧的濃度十分敏感,被稱為“缺氧基因的表達(dá)總開關(guān)”[15-18]。常氧條件下,HIF-1α被VHL識(shí)別后,會(huì)經(jīng)由蛋白質(zhì)的泛素化水解反應(yīng)被降解。但是,如果細(xì)胞處于缺氧的環(huán)境,則會(huì)對(duì)HIF-1α的降解產(chǎn)生阻礙,從而使其更容易與HIF-1β相互作用,促進(jìn)HIF-1靶基因的轉(zhuǎn)錄[19]。SM22α、BMP-2、RUNX2和VEGF是與細(xì)胞分化和血管生成相關(guān)的一些蛋白質(zhì)。SM22α是一種平滑肌特異性蛋白質(zhì),主要在平滑肌細(xì)胞中表達(dá),其在細(xì)胞分化和收縮中起著重要的調(diào)節(jié)作用。BMP-2是一種骨形態(tài)發(fā)生蛋白家族成員,對(duì)骨細(xì)胞分化和骨組織生成起著重要的調(diào)節(jié)作用,其被廣泛應(yīng)用于骨再生和骨修復(fù)的臨床治療中。RUNX2是一種轉(zhuǎn)錄因子,對(duì)骨細(xì)胞分化和骨組織形成起關(guān)鍵作用,是骨發(fā)育和骨再生過程中的重要調(diào)節(jié)因子[20-21]。VEGF是一種促血管生成的蛋白質(zhì),對(duì)血管發(fā)生、生長和修復(fù)具有重要作用,在組織修復(fù)和再生過程中起關(guān)鍵調(diào)節(jié)作用。這些蛋白質(zhì)在細(xì)胞分化、骨組織生成和血管生成等方面的研究,對(duì)于理解相關(guān)疾病的發(fā)生機(jī)制以及開發(fā)相關(guān)治療方法具有重要意義。TRAP-5b是一種酸性磷酸酶,也被稱為骨吸收標(biāo)記物,在骨骼系統(tǒng)中發(fā)揮重要作用,特別是在骨重塑和骨吸收過程中。TRAP-5b主要存在于成熟的骨吸收細(xì)胞(如巨噬細(xì)胞、骨吸收細(xì)胞),它參與了骨骼的正常代謝和再生。在骨吸收過程中,TRAP-5b可降解骨骼中的無機(jī)磷酸鹽和有機(jī)骨基質(zhì),促進(jìn)骨重塑和骨質(zhì)疏松。由于TRAP-5b的特定表達(dá)與骨吸收過程有關(guān),其被廣泛用作評(píng)估骨代謝活動(dòng)和骨質(zhì)疏松癥的標(biāo)志物。本研究發(fā)現(xiàn),給予氫氧化鑭治療后,抑制了高磷誘導(dǎo)的活性氧的產(chǎn)生,可明顯減少CKD大鼠胸主動(dòng)脈的鈣沉積、胞質(zhì)中BMP-2、VEGF表達(dá),以及胞核內(nèi)RUNX2、HIF-1α的表達(dá),增加SM22α的表達(dá),進(jìn)而抑制了VSMC的轉(zhuǎn)分化和鈣化[22-23]。
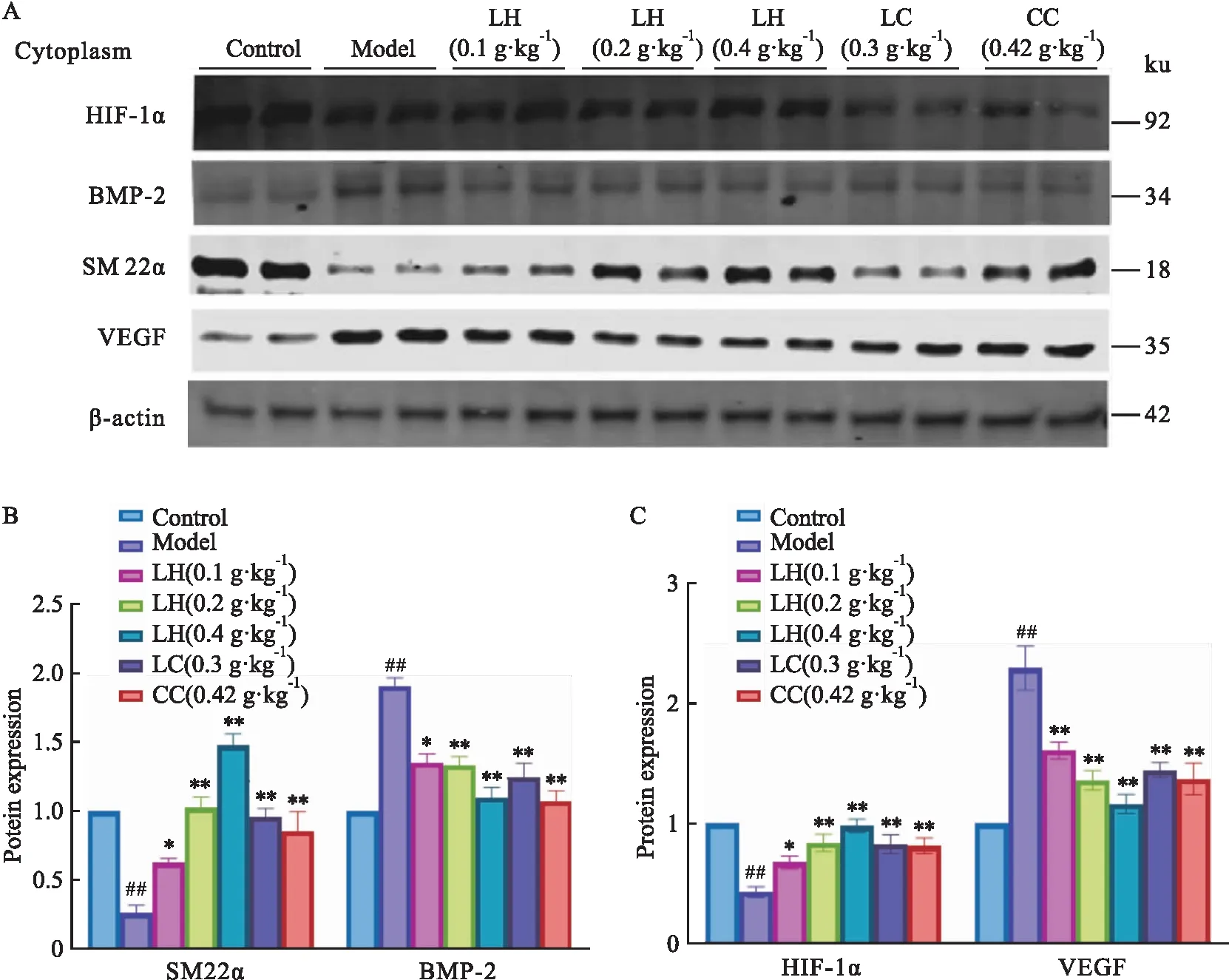
Fig 3 Effect of lanthanum hydroxide on HIF-1α, BMP-2, SM22α and VEGF expression
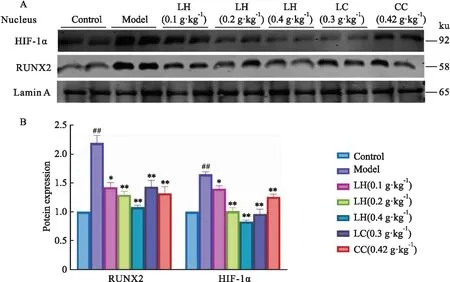
Fig 4 Effect of lanthanum hydroxide on HIF-1α and RUNX2 protein expression in nucleus of thoracic aorta of CKD n=4)
綜上所述,氫氧化鑭可抑制慢性腎衰血管鈣化的發(fā)生及發(fā)展,其可能通過阻斷HIF-1通路的激活來抑制CKD所致的血管鈣化。本研究為氫氧化鑭成為臨床候選藥物奠定了臨床前期藥理學(xué)研究基礎(chǔ)。
- 中國藥理學(xué)通報(bào)的其它文章
- 心腦舒通膠囊及有效成分對(duì)氧糖剝奪/復(fù)氧損傷腦微血管內(nèi)皮細(xì)胞屏障完整性的影響及機(jī)制研究
- 基于網(wǎng)絡(luò)藥理學(xué)和分子對(duì)接探討芪術(shù)抗癌方治療原發(fā)性肝癌的分子機(jī)制
- 高糖環(huán)境中雄激素受體對(duì)心肌成纖維細(xì)胞增殖和脂質(zhì)合成能力的影響
- 甲基化轉(zhuǎn)移酶樣蛋白3介導(dǎo)的m6A修飾參與高靜水壓誘導(dǎo)的心房肌細(xì)胞電重塑
- 卡維地洛調(diào)節(jié)ApoE-/-小鼠肝臟ACAD10、mTOR抗動(dòng)脈粥樣硬化
- ACT001通過STAT1/CIITA/MHC-Ⅱ通路發(fā)揮抗炎抗氧化活性治療膿毒癥引起的急性肺損傷