血清糖蛋白非轉移性黑色素瘤蛋白B對表皮生長因子受體擴增伴隨突變的非小細胞肺癌預后的預測作用
劉邦卿,李劍鋒,劉曉輝,張勁男,胡亞麗
(唐山市人民醫院 1. 胸外二科; 2. 頭頸外科,河北 唐山 063001)
非小細胞肺癌 (non-small cell lung cancer,NSCLC)是一種高發的惡性腫瘤[1]。表皮生長因子受體 (epidermal growth factor receptor,EGFR) 是NSCLC臨床研究中最受關注且最重要的靶點[2]。近年來,臨床相關資料表明EGFR在多種腫瘤中過表達,EGFR的擴增伴隨突變是主要的突變類型之一[3],激活EGFR能夠引起腫瘤細胞內的酪氨酸活化及其受體磷酸化,促進腫瘤細胞增殖、分化以及血管生成等過程,加速腫瘤細胞的惡性進展[4]。
研究[5-6]表明,酪氨酸激酶抑制劑 (EGFR-tyrosine kinase inhibitor,EGFR-TKI) 在EGFR基因突變的NSCLC治療中效果顯著。此外,越來越多的研究[7]表明NSCLC患者的EGFR基因突變類型和患者對EGFR-TKI的應答情況顯著相關。隨著腫瘤患者臨床治療中EGFR-TKI的利用率日益增高,耐藥問題成了亟需解決的難題。挖掘EGFR-TKI耐藥標志物和篩選適用EGFR-TKI治療的NSCLC患者,實現個體化治療,是改善臨床治療效果、延長患者生存期的關鍵。
糖蛋白非轉移性黑色素瘤蛋白B (glycoprotein non‐metastatic melanoma protein B,GPNMB)是一種高度糖基化的Ⅰ型跨膜糖蛋白,作為腫瘤細胞生長的調節基因而備受關注[8]。在不同的腫瘤中,GPNMB高表達都被證實能夠促進腫瘤的惡性進展,例如,GPNMB的表達水平越高,乳腺癌細胞的增殖遷移侵襲能力越強,神經膠質瘤和小細胞肺癌患者的生存時間越短,生存狀況越差[9-11]。最新研究[12]指出,GPNMB的表達水平可能和胃腸道惡性腫瘤患者EGFR-TKI治療后的耐藥有關。也有研究[13]表明,GPNMB在EGFR突變NSCLC細胞中表達水平的變化與NSCLC的進展相關,但系統性的研究尚未見報道。
本研究選擇將EGFR-TKI作為一線治療的EGFR基因擴增伴隨突變的NSCLC患者作為研究對象,檢測其血液中游離GPNMB的表達水平,探討其與患者耐藥及預后的相關性。
1 材料與方法
1.1 研究對象
選取2018年3月至2019年9月唐山市人民醫院收治的143例病理確診為NSCLC患者的臨床資料。利用ctDNA檢測和FISH法篩選EGFR擴增伴隨突變的NSCLC患者,排除資料不全和合并其他腫瘤者,最終納入55例患者作為觀察組。患者均以EGFR-TKI (奧希替尼) 作為一線治療,且未接受過局部治療。收集患者血液樣本和臨床資料。此外,隨機收集同期本院體檢中心的健康人群血液樣本作為對照組。所有研究對象均簽署了知情同意書,本研究獲得醫院倫理委員會批準。
1.2 血液中游離GPNMB檢測
2組血液樣本均置于EDTA管并于-80 ℃保存。使用人GPNMB的ELISA商品化試劑盒 (美國ELHOsteoactivin,RayBiotech公司)對血液樣本中游離的GPNMB進行定量分析,操作均按照試劑盒說明書進行。
1.3 隨訪
對觀察組患者進行隨訪。記錄患者應用EGFRTKI的療效。本研究通過療效評價患者的耐藥情況,根據實體瘤療效評價標準[14],EGFR-TKI臨床療效分為部分緩解 (partial response,PR)、疾病穩定 (stable disease,SD) 和疾病進展 (progressive disease,PD)。收集患者出院后的隨訪資料,記錄患者的無進展生存時間 (progression free survival,PFS),將患者的PFS作為本研究的主要終點事件。
1.4 統計學分析
采用SPSS 26.0和Graphpad Prism 8.4.2軟件進行統計分析。計數資料以例 (率) 表示,組間比較采用Fisher精確概率法或χ2檢驗。計量資料首先進行正態和方差齊性檢驗,所有正態分布的計量資料以±s表示,組間比較采用雙側t檢驗。患者PFS的生存分析采用Kaplan-Meier法和log-rank檢驗,采用多因素Cox回歸分析篩選影響患者生存的獨立危險因素。P< 0.05為差異有統計學意義。
2 結果
2.1 EGFR擴增伴隨突變NSCLC患者血液中游離的GPNMB的表達水平
血液中游離的GPNMB表達水平對照組為 (1.49±0.61) ng/mL,觀察組為 (3.09±0.88) ng/mL。根據觀察組中GPNMB表達水平的中位值 (3.13 ng/mL),將EGFR擴增伴隨突變的NSCLC患者分為高表達組 (n= 27) 和低表達組 (n= 28)。隨后,對GPNMB表達和EGFR擴增伴隨突變NSCLC患者臨床病理信息的相關性進行探究。結果顯示,在所有EGFR擴增伴隨突變NSCLC患者中,女性 (32例)居多,33例患者存在吸煙史,臨床分期均為Ⅲ期~Ⅳ期,組織分型以肺腺癌 (37例)為主。GPNMB高表達組和低表達組年齡、性別、體質量指數 (body mass index,BMI)、ECOG評分、臨床分期、組織分型以及吸煙史比較均無統計學差異(均P>0.05),見表1。

表1 觀察組GPNMB表達與各項臨床指標的相關性Tab.1 Correlation between GPNMB expression and the clinical data in the observation group
2.2 GPNMB表達水平和EGFR擴增伴隨突變NSCLC患者耐藥的相關性
高表達組中4例為PR,7例為SD,16例為PD;低表達組中7例為PR,15例為SD,6例為PD。2組療效比較有統計學差異 (P= 0.016),低表達組患者使用EGFR-TKI治療療效更優,見表1。2組患者的客觀反應率 (objective response rate,ORR) 比較,差異有統計學意義 (4/27 vs. 7/28,P< 0.01)。患者血液中游離GPNMB高表達可能提示耐藥程度更強,對于EGFRTKI治療的敏感性更差。
2.3 GPNMB表達水平和EGFR擴增伴隨突變NSCLC患者預后的相關性
觀察組隨訪時間為1.2~18.7個月,平均11.58個月。隨訪結果顯示,GPNMB高表達組患者的中位PFS為7.38個月 (95%CI:0.9~12.5),GPNMB低表達組患者的中位PFS為9.92個月 (95%CI:5.3~14.7)。Kaplan-Meier生存曲線結果顯示,GPNMB高表達組患者的PFS顯著短于低表達組 (P= 0.032),見圖1。加入GPNMB表達對患者進行分層生存分析,結果顯示,女性 (P= 0.009)、非腺癌 (P< 0.001)、從未吸煙 (P=0.006)、ECOG評分為1 (P< 0.001)、臨床分期為Ⅳ期(P= 0.009) 患者的PFS和GPNMB表達水平顯著相關。
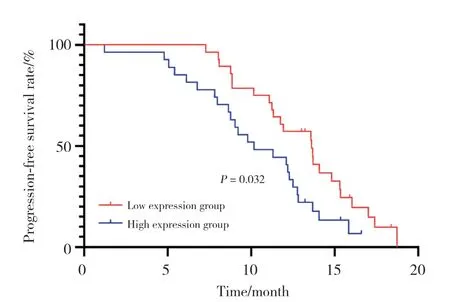
圖1 不同GPNMB表達NSCLC患者的PFS曲線Fig.1 PFS curve of NSCLC patients with different GPNMB expression
2.4 GPNMB表達水平是EGFR擴增伴隨突變NSCLC患者無進展生存的獨立危險因素
通過Kaplan-Meier法進行患者生存分析,采用log-rank檢驗所有自變量與因變量的關系,結果顯示,性別 (P= 0.008)、吸煙史 (P= 0.009)、ECOG評分(P= 0.002)、臨床分期 (P= 0.009)、組織類型 (P= 0.002)是患者生存可能的影響因素。隨后,將GPNMB表達分組和性別、組織類型、吸煙史、ECOG評分以及臨床分期等因素納入多因素Cox回歸分析。結果顯示,血液中游離的GPNMB高表達 (HR= 4.029,95%CI:1.942~8.358,P< 0.001) 是影響EGFR擴增伴隨突變NSCLC患者無進展生存的獨立危險因素。見表2。

表2 NSCLC患者無進展生存影響因素的多因素Cox回歸分析Tab.2 Multi-factor Cox regression analysis of progression-free survival in NSCLC patients
3 討論
NSCLC患者的血液樣本含有多種游離蛋白[15-16]。NAKASHIMA-NAKASUGA等[17]使用ELISA方法檢測結直腸癌患者血清樣本中LOX-1的蛋白表達,發現LOX-1與結直腸癌的預后顯著相關。本研究應用ELISA方法檢測了EGFR擴增伴隨突變NSCLC患者血清中的GPNMB蛋白表達,發現GPNMB表達與患者預后以及耐藥性顯著相關。
HAN等[13]研究發現GPNMB與腫瘤的EGFR突變呈正相關,且在EGFRL858R突變的NSCLC細胞中過表達。GPNMB糖基化可以激活突變的EGFR,開啟下游STAT3信號通路,促進NSCLC細胞轉移。本研究也發現EGFR擴增伴隨突變NSCLC患者血清GPNMB顯著高表達。根據GPNMB表達水平對EGFR擴增伴隨突變NSCLC患者進行分組,并評價GPNMB與耐藥性的關系。發現GPNMB高表達與EGFR-TKI的療效顯著相關。以上研究表明,GPNMB與腫瘤EGFR突變有關,且在EGFR擴增伴隨突變NSCLC患者中高表達,并增強其耐藥性。
GPNMB與腫瘤患者的預后密切相關[18]。FENG等[10]發現GPNMB與膠質瘤不良預后密切相關。MA等[16]研究證實GPNMB的過表達預示著上皮性卵巢癌的不良預后。本研究對EGFR擴增伴隨突變NSCLC患者進行生存分析,發現血液中游離GPNMB高表達患者的PFS顯著縮短。進一步分層生存分析和多因素Cox回歸分析發現,GPNMB高表達不利于患者無進展生存,且是影響EGFR擴增伴隨突變NSCLC患者無進展生存的獨立危險因素。以上結果表明,血液中游離GPNMB表達水平可作為EGFR擴增伴隨突變NSCLC患者預后標志物;GPNMB高表達與患者預后不良顯著相關,并對患者的生存狀況產生顯著影響。
綜上所述,EGFR擴增伴隨突變NSCLC患者血液中游離GPNMB高表達,其高表達與患者的耐藥程度增強密切相關,是潛在的耐藥標志物。與此同時,本研究也證實GPNMB高表達和患者的預后不良顯著相關,是影響患者生存的獨立危險因素。本研究樣本量較少,患者僅來自同一醫院,未來應納入更多樣本量進行多中心深入研究。

