二代基因測序技術聯合半乳甘露聚糖檢測對重癥肺炎合并真菌感染的診斷價值*
王美玉,王文博,李翠娟
[大慶龍南醫(yī)院(齊齊哈爾醫(yī)學院第五附屬醫(yī)院) 1.臨床藥學科,2.急診重癥監(jiān)護室,3.呼吸與危重癥醫(yī)學科,黑龍江 大慶 163458]
近年來,重癥肺炎一直是醫(yī)學界和公眾關注的焦點之一。重癥肺炎作為一種嚴重的呼吸系統(tǒng)感染,常見于重癥監(jiān)護病房患者,以呼吸困難、高熱、咳嗽及胸痛等臨床癥狀為主,伴隨病情遷延不愈,可導致多器官功能衰竭,病死率達20%~50%[1-2]。此外,部分重癥肺炎患者常合并真菌感染,加重肺部炎癥反應,誘導免疫系統(tǒng)失調及全身炎癥反應綜合征病情進展,增加死亡風險[3-4]。
目前,臨床上針對重癥肺炎合并真菌感染的診斷以臨床癥狀、影像學檢查及實驗室檢測為主。然而,臨床癥狀及影像學檢查在敏感性和特異性方面存在一定局限性,尤其對早期真菌感染的檢測,無法及時準確地確定感染的存在及病原菌種類[5-6]。病原微生物培養(yǎng)作為臨床診斷真菌感染的金標準,診斷效能高,但培養(yǎng)時間長,時效性差,加之患者病情多變,不利于患者的針對性治療及預后改善[7]。
半乳甘露聚糖(Galactomannan,GM)可通過檢測血液中GM抗原水平鑒別真菌感染,具有快速、非侵入性及定量化的優(yōu)勢[8]。二代基因測序技術(nextgeneration sequencing,NGS)是一種新型的高通量測序技術,可對樣本中的全部基因組進行廣泛測序,不僅能夠檢測真菌的存在及種類,還可檢測部分耐藥基因,確定相關致病機制,從而指導個體化治療決策[9]。目前,鮮有研究報道GM聯合NGS診斷重癥肺炎合并真菌感染的效能分析,因此本研究嘗試分析GM聯合NGS診斷重癥肺炎合并真菌感染的價值,為合并真菌感染患者的早期診斷、治療決策及預后改善提供參考。
1 資料與方法
1.1 研究對象
選取2020年3月—2023年3月大慶龍南醫(yī)院急診重癥監(jiān)護室收治的重癥肺炎患者148例。其中,女性72例,男性76例;年齡41~77歲,平均(63.01±6.08)歲。診斷標準:參考《美國胸科學會及感染病學會-成人社區(qū)獲得性肺炎診治標準2019》[1],符合下述≥1項主要診斷標準且≥ 3項次要診斷標準確診,主要標準:①氣管插管機械通氣,②膿毒癥患者液體復蘇后維持血管活性藥物治療;次要標準:①多肺葉受累或低血壓需液體復蘇或意識障礙,②氧合指數≤ 250,③呼吸頻率≥ 30次/min,④血尿素氮≥ 20 mg/dL,⑤血小板計數<100×109/L,⑥白細胞計數<4×109/L。本研究經醫(yī)院醫(yī)學倫理委員會批準,患者及家屬均簽署知情同意書。
1.2 納入與排除標準
1.2.1 納入標準 ①符合重癥肺炎的臨床診斷;②影像學檢查可見肺部存在病灶;③完成支氣管鏡檢及支氣管肺泡灌洗液收集。
1.2.2 排除標準 ①合并多器官衰竭綜合征;②合并紅斑狼瘡、類風濕等免疫性疾病;③精神病史;④肺癌;⑤妊娠或哺乳期女性。
1.3 研究方法
所有患者行支氣管鏡檢查并收集支氣管肺泡灌洗液,行病原微生物培養(yǎng)、血清GM及肺泡灌洗液NGS檢測。以病原微生物培養(yǎng)為金標準,分析血清GM及肺泡灌洗液NGS診斷重癥肺炎合并真菌感染的敏感性、特異性,評估血清GM檢測、肺泡灌洗液NGS檢測單獨及聯合診斷重癥肺炎合并真菌感染結果與病原微生物培養(yǎng)結果的一致性。
1.3.1 肺泡灌洗液收集 入院72 h內,咪達唑侖靜脈鎮(zhèn)靜,鼻腔進鏡,采用2%利多卡因行氣道黏膜表面局部麻醉,將支氣管鏡頂端嵌頓在病變相對嚴重段的支氣管分支,注入60~120 mL生理鹽水灌洗,100 mmHg負壓抽吸,回收率為40%~60%,灌洗液培養(yǎng)量≥ 10 mL。
1.3.2 病原微生物培養(yǎng) 灌洗液樣本常規(guī)富集培養(yǎng)、涂片,革蘭染色鏡檢剔除假陽性菌。使用全自動微生物檢測系統(tǒng)(美國Biolog公司,型號:GEN ⅢOmnilog型)檢測病原微生物種類。
1.3.3 血清GM檢測 入院72 h內,采集患者肘靜脈血4 mL,3 500 r/min離心10 min,離心半徑13 cm,取上清液用酶聯免疫吸附試驗檢測血清GM水平,檢測結果判定:I值≥ 1為陽性。
1.3.4 肺泡灌洗液NGS檢測 將肺泡灌洗液低溫4 ℃、4 000 r/min離心10 min、離心半徑13.5 cm,取上清液。采用DNA提取試劑盒提取上清液中游離DNA。DNA超聲破碎至150 bp的片段,插入200~300 bp的片段,使用DNA質控試劑(美國Thermo Fisher Scientific公司,商品名:Qubit dsDNA HS Assay Kit)將線性的DNA轉化為單鏈環(huán)形結構,后滾環(huán)復制生成DNA納米球。使用高通量測序平臺BGISEQ-5/MGISEQ-2000(深圳華大基因和MGISEQ公司)進行測序,篩除長度<35 bp的低質量片段。采用BEA測序軟件對比人參考基因組序列,剔除人基因組序列;剩余數據與細菌、真菌、病毒、寄生蟲數據庫進行自動對比,獲取匹配到病原體的序列數,判定病原體種類。
1.4 統(tǒng)計學方法
數據分析采用SPSS 19.0統(tǒng)計軟件。計數資料以構成比或率(%)表示,比較用χ2檢驗;計量資料以均數±標準差(±s)表示,比較用t檢驗;一致性檢驗用Kappa值,并進行χ2檢驗;繪制受試者工作特征(receiver operating characteristic,ROC)曲線。P<0.05為差異有統(tǒng)計學意義。
2 結果
2.1 病原學培養(yǎng)結果
148例重癥肺炎中合并真菌感染患者30例,其中肺孢子菌10例、白色念珠菌8例、曲霉菌7例、根霉菌1例、肺孢子菌感染合并白色念珠菌3例、肺孢子菌感染合并鮑曼不動桿菌1例。
2.2 兩組患者臨床資料比較
重癥肺炎合并真菌感染30例,未合并真菌感染患者118例。兩組年齡、氧合指數、氧分壓、中性粒細胞比例、急性生理與慢性健康評分比較,經t檢驗,差異均無統(tǒng)計學意義(P>0.05)。兩組性別構成、糖尿病、高血壓、慢性呼吸道疾病比較,經χ2檢驗,差異均無統(tǒng)計學意義(P>0.05)。見表1。
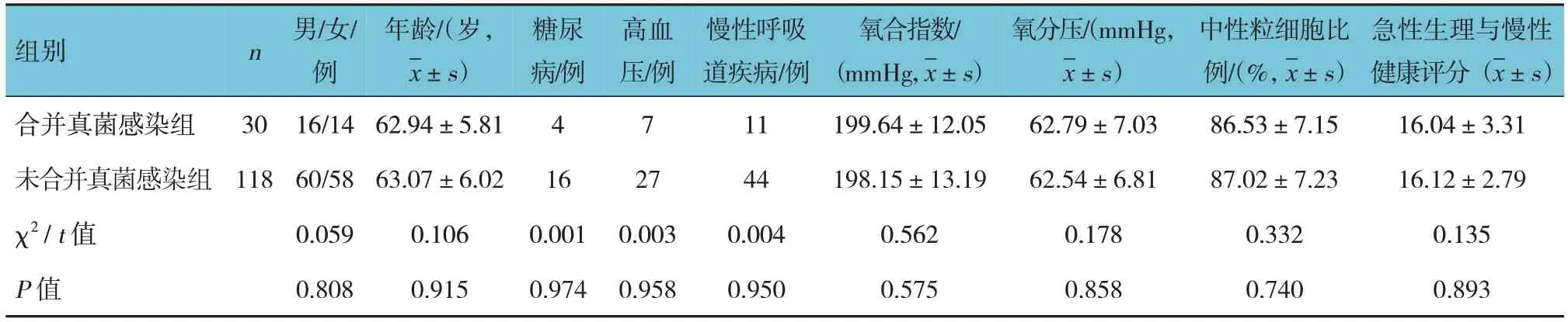
表1 兩組患者臨床資料比較
2.3 血清GM診斷重癥肺炎合并真菌感染
血清GM試驗結果顯示,陽性28例,陰性120例;病原學培養(yǎng),感染30例,非感染118例,Kappa值為0.700,經一致性檢驗,兩者具有一致性(χ2=39.981,P=0.001)。見表2。
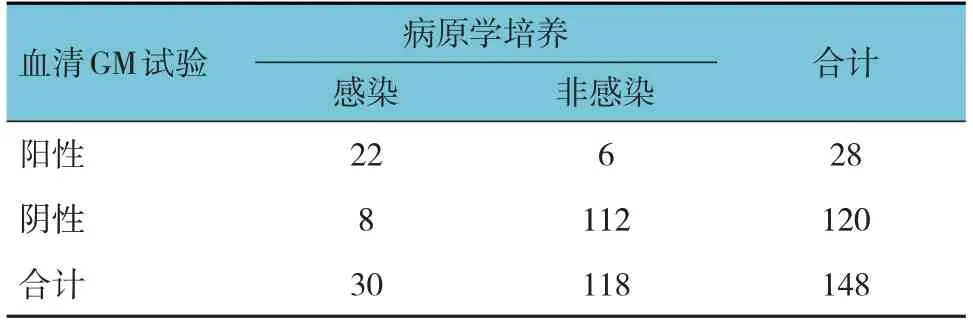
表2 血清診斷重癥肺炎合并真菌感染的結果 例
2.4 肺泡灌洗液NGS診斷重癥肺炎合并真菌感染
肺泡灌洗液NGS診斷結果顯示,陽性34例,陰性114例;病原學培養(yǎng),感染30例,非感染118例,Kappa值為0.841,經一致性檢驗,兩者具有一致性(χ2=54.716,P=0.001)。見表3。
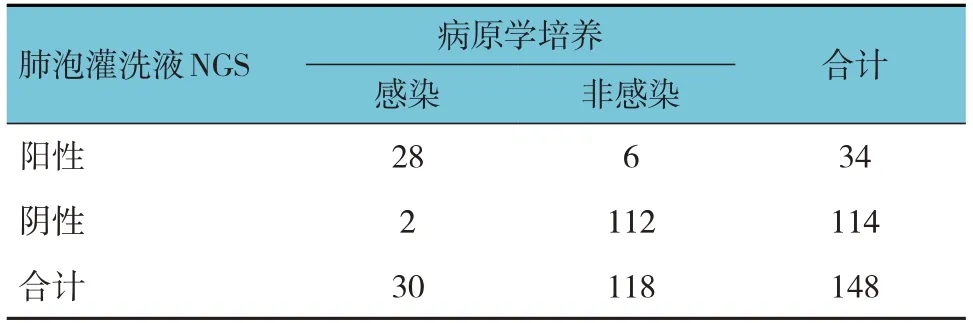
表3 泡灌洗液NGS診斷重癥肺炎合并真菌感染的結果 例
2.5 血清GM聯合肺泡灌洗液NGS診斷重癥肺炎合并真菌感染
血清GM聯合肺泡灌洗液NGS診斷結果顯示,陽性30例,陰性118例;病原學培養(yǎng),感染30例,非感染118例,Kappa值為0.916,經一致性檢驗,兩者具有一致性(χ2=66.293,P=0.001)。見表4。

表4 血清GM聯合肺泡灌洗液NGS診斷重癥肺炎合并真菌感染的結果 例
2.6 血清GM聯合肺泡灌洗液NGS診斷重癥肺炎合并真菌感染的價值
ROC曲線結果分析顯示,血清GM、肺泡灌洗液NGS單獨及聯合診斷重癥肺炎合并真菌感染的敏感性分別為73.3%(95% CI:0.538,0.870)、93.3%(95% CI:0.765,0.988)、93.3%(95% CI:0.765,0.988),特異性分別為94.9%(95% CI:0.888,0.979)、94.9%(95% CI:0.889,0.979)、98.3%(95% CI:0.934,0.997),曲線下面積(area under curve,AUC)分別為0.841、0.941和0.958。見表5。

表5 血清GM聯合肺泡灌洗液NGS診斷重癥肺炎合并真菌感染的效能分析
3 討論
近年來,抗菌藥物在臨床濫用現象增多,以及糖皮質激素應用增加,導致住院患者真菌感染率明顯升高,尤其是重癥肺炎患者,真菌感染可導致臨床癥狀加重,甚至危及生命[10-11]。抗生素的延遲使用是引起病原菌感染患者死亡的危險因素[12]。因此臨床上針對重癥肺炎疑似合并真菌感染的患者,在尋找病原學證據的同時,經驗性抗感染治療仍為現階段治療中的應急方案,但易增加藥物耐藥性,不利于抗生素的合理應用。目前,侵襲性肺曲霉是肺部真菌感染中檢出率偏高的一類病原菌,可導致肺泡壁的破裂及組織壞死,并形成炎癥灶及壞死區(qū)域,嚴重損傷患者肺功能[13-14]。此外,近些年研究報道,肺念珠菌、肺隱球菌等病原菌在肺部真菌感染中檢出率不斷升高,同樣是威脅肺部真菌感染患者預后的高危病原菌[15-16]。目前,病原菌培養(yǎng)作為臨床診斷真菌感染的金標準,診斷效能良好,然而因病原菌培養(yǎng)耗時較長,患者無法及時實施早期干預治療,導致病情進展,增加后期治療難度,不利于患者預后[17-18]。目前,G試驗和GM試驗是診斷肺炎患者合并真菌感染的常用方法,其中G試驗在識別免疫球蛋白G抗體中具有較高的特異性,但感染初期可能無法檢測到特異性的免疫球蛋白G抗體,往往需要進行免疫球蛋白M試驗或核酸檢測等補充測試,同時G檢驗無法區(qū)分活動感染和既往感染,只能檢測是否存在特定病原體的免疫球蛋白G抗體,臨床實踐中局限性明顯。GM試驗是篩查侵襲性曲霉菌感染的方法,在侵襲性曲霉菌感染中的輔助診斷價值良好,但血清GM試驗存在一定的局限性。有研究發(fā)現,血清GM試驗可能受時間窗口效應的影響,在病原菌感染早期,部分患者的抗原水平上升幅度并不顯著,局限性明顯[19-20]。因此,尋求更具特異性、敏感性及高效、快捷的輔助診斷方法,提高重癥肺炎合并真菌感染的診斷價值,成為近幾年臨床醫(yī)學者不斷探索的關鍵。
近年來,NGS技術不斷發(fā)展,已逐步從實驗室研究應用于臨床,早期實踐階段在腫瘤基因檢測、遺傳性疾病篩查等領域發(fā)揮作用,近年來已拓展至感染性疾病病原學診斷及監(jiān)測,并展現了巨大的臨床實用價值及應用前景。NGS是通過對宏基因組的樣本開展大規(guī)模測序,以獲得基因組核酸序列,進而借助生物信息工具進行定量分析,獲得詳細的病原基因信息,與基因庫基因型對比,從而獲得該病原微生物的分型、耐藥性及毒力等信息[21]。YANG等[22]研究表明,宏基因組學用于重癥肺炎合并診斷真菌感染的診斷中,與陽性微生物培養(yǎng)物及從培養(yǎng)物陰性樣本中測序獲得的臨床可操作信息一致,有潛力成為指導重癥肺癌抗菌決策的重要醫(yī)療技術。此外,肺泡灌洗液NGS技術具有高效、病原體覆蓋廣等優(yōu)點,彌補了傳統(tǒng)微生物檢測的耗時問題,可盡早地由經驗治療轉為目標治療,減輕患者痛苦,縮短治療時間,降低細菌耐藥率,節(jié)約醫(yī)療資源,為臨床疾病診治提供新的可靠依據。本研究結果顯示,30例重癥肺炎中合并真菌感染中肺孢子菌、白色念珠菌及曲霉菌的檢出率最高,表明重癥肺炎中合并真菌感染患者的真菌感染種類仍以肺孢子菌、白色念珠菌及曲霉菌為主,與張安兵等[23]報道結果一致。本研究結果顯示,血清GM診斷重癥肺炎合并真菌感染的敏感性、特異性、AUC及Kappa值分別為73.3%、94.9%、0.841及0.700,提示血清GM診斷重癥肺炎合并真菌感染的效能良好。與毛伍兵等[24]研究結果相近。但仍有8例合并真菌感染的患者未檢出,血清GM試驗鑒別真菌感染的效能取決于真菌細胞壁中的抗體成分GM,當重癥肺炎患者合并真菌感染時,活體或死亡的真菌細胞可分解釋放GM至體液中,從而顯示抗體陽性,但其含量及釋放同樣取決于菌種的種類,分析是導致血清GM試驗誤診、漏診的原因。此外,SADAQAT等[25]研究報道,部分細菌基因對半乳甘露聚糖及羧基同樣表現出生物活性,可能會通過釋放與血清GM結構或抗原性相似的活性物質或代謝產物,導致免疫系統(tǒng)對其產生交叉反應,導致血清GM試驗顯示為假陽性,增加誤診、漏診率。本研究結果顯示,肺泡灌洗液NGS診斷重癥肺炎合并真菌感染的敏感性、特異性、AUC及Kappa值分別為93.3%、94.9%、0.941及0.841,提示肺泡灌洗液NGS診斷重癥肺炎合并真菌感染的效能良好。但其中2例NGS診斷陰性患者經病原學培養(yǎng)后檢出霉菌菌絲,提示肺泡灌洗液NGS診斷重癥肺炎合并真菌感染同樣存在誤診、漏診風險。肺泡灌洗液NGS診斷通過DNA純化后與數據庫對比分析得出真菌感染種類,而對于低豐度感染的真菌,DNA或RNA可能被掩蓋,在早期感染、局部感染或低病原體負荷的情況下導致NGS無法準確檢測到真菌感染。
本研究樣本量有限,而重癥肺炎合并真菌感染的種類豐富。何德華等[26]研究認為,NGS對于罕見菌、不典型菌的檢出率低。因此,后續(xù)研究仍需完善多中心、大樣本研究,明確血清GM、NGS診斷重癥肺炎合并真菌感染的缺陷,不斷完善臨床診斷方案,改善患者預后。
綜上所述,血清GM聯合肺泡灌洗液NGS診斷重癥肺炎合并真菌感染,在肺孢子菌、白色念珠菌及曲霉菌等常見菌種中的診斷效能良好。

